剪切应力可以决定培养肉生产的成败。 为什么?因为所用的细胞缺乏保护性细胞壁,使其容易受到生物反应器中流体力的损害。本文深入探讨了剪切应力如何影响这些细胞、它们能承受的阈值以及设计保护它们的系统的方法。
关键要点:
- 剪切应力源于流体运动,可能会损害脆弱的动物细胞,导致膜损伤、脱落或死亡。
- 大多数哺乳动物细胞能耐受 0.3–1.7 帕斯卡, 但即使是更低的水平也能激活应激反应。
- 设计选择如搅拌器类型、曝气方法和生物反应器几何形状直接影响剪切力。
- 减少损害的策略包括使用更温和的生物反应器设计(e.g. 如气升式或摇摆系统)、优化搅拌速度,以及添加保护剂如 Pluronic F68.
对于培养肉来说,管理这种平衡至关重要,以确保细胞在不受损害的情况下生长和分化,尤其是在生产规模扩大时。让我们探讨这些阈值背后的科学以及生物反应器设计的实际解决方案。
110: 像地球一样旋转:与 Olivier De 设计低剪切生物反应器以改善细胞培养...
影响生物反应器中剪切应力的因素
了解影响生物反应器中剪切应力的因素对于优化条件至关重要,尤其是在涉及到脆弱细胞时。让我们深入探讨影响其强度和分布的主要因素。
生物反应器设计和操作条件
生物反应器的设计在决定剪切应力发生的位置和方式方面起着重要作用。一个关键因素是使用的叶轮类型。例如,Rushton涡轮可以产生高达容器平均能量耗散率280倍的能量耗散率,而高效轴流叶轮如HE3则产生接近180倍平均耗散率的能量。其他设计元素,如叶轮直径、速度和位置,也会影响能量分布。 有趣的是,曝气引入的力比搅拌更为剧烈。当小气泡(1–2 mm)破裂时,它们释放的能量水平在10⁷–10⁹ W/m³之间,这可能在一次事件中杀死超过1,000个细胞。这使得气泡行为成为一个关键考虑因素,特别是在培养肉生产中。 挡板是另一个关键设计元素。它们防止在培养液中形成漩涡,否则会将气泡拉入液体并增加表面破裂事件。此外,叶轮与容器直径的比率以及叶轮距底部的高度会影响能量在生物反应器中的传播。
剪切应力分布不均
剪切应力在生物反应器中分布不均。研究表明,能量耗散往往集中在特定区域,如叶轮排放区、尾涡和气泡破裂的液面。这些热点在放大过程中可能带来挑战。
来自Biogen Idec的胡伟伟强调了这一放大问题:
“剪切敏感性”的观念历来在生物反应器操作中对搅拌和曝气设定了任意的上限;然而,随着细胞密度和生产率的不断提高,传质需求可能会超过这些任意低限所施加的限制。[4].
例如,江南大学的张俊轩和李学良在2021年的一项研究中,使用计算流体动力学比较了250 mL旋转瓶和20 m³搅拌罐反应器。他们观察到,即使在最低搅拌速度下,大型反应器中的剪切力也足以使细胞从微载体上脱落,而曝气引入的应力甚至比搅拌更大 [3].
培养格式和剪切敏感性
培养格式也决定了细胞如何承受剪切应力。在微载体上生长的细胞特别脆弱。 如果剧烈混合或载体之间的碰撞导致细胞脱落,这些细胞实际上就会丢失 [4]. 另一方面,杂交瘤细胞的悬浮培养在无气液界面的挡板生物反应器中表现出韧性,在高达1,500 RPM的搅拌速度下仍能保持活力[4].
不同的培养系统以各种方式处理剪切力。固定床生物反应器通过将细胞固定在静止表面上来最小化剪切力,而流化床通过微载体的运动和向上的流体流动引入中到高的剪切力[2]. 一些微载体,尤其是多孔的,提供内部表面,可以保护细胞免受极端力量的影响,与实心微载体相比提供更好的保护[2]. 这些差异强调了在设计生物反应器时需要仔细平衡营养物质的输送与细胞损伤的风险。
不同细胞类型的剪切应力阈值
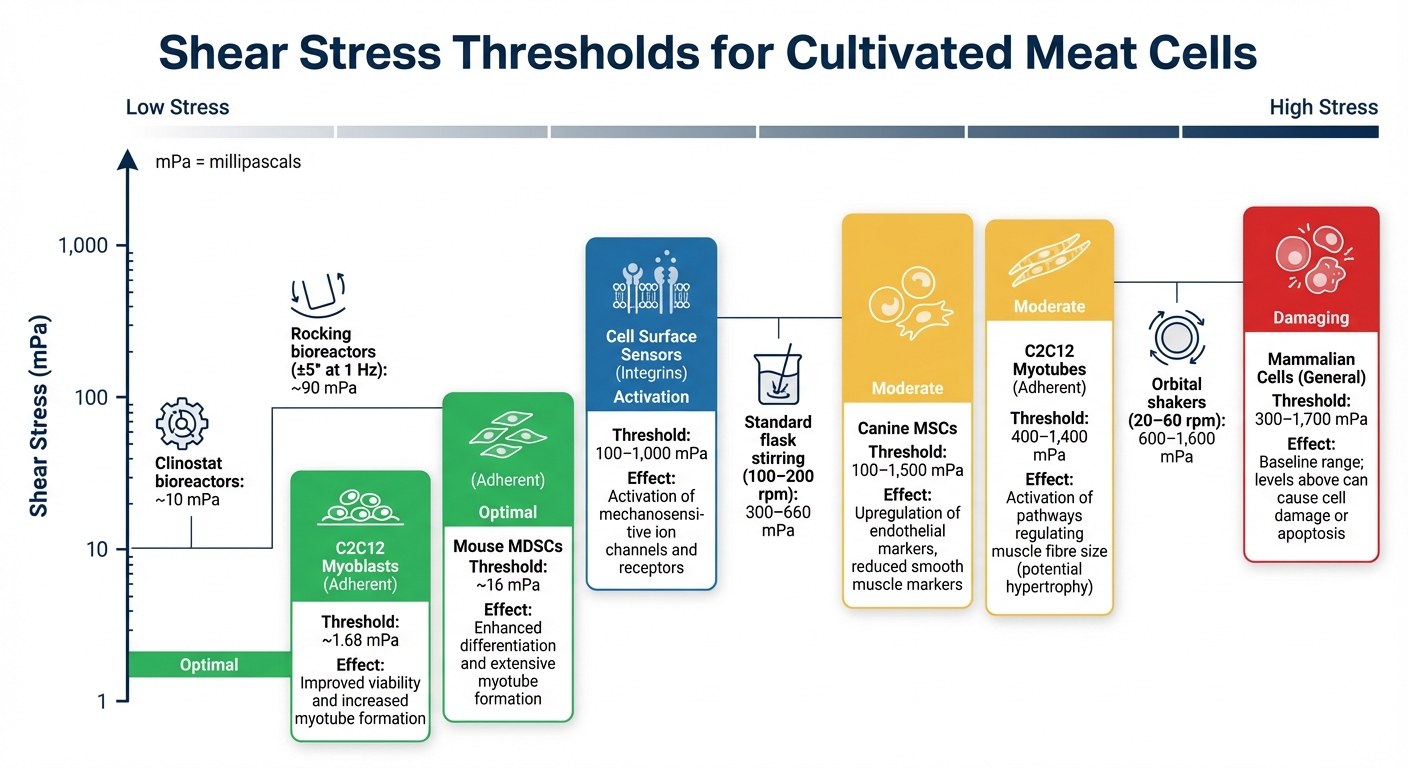
培养肉细胞类型的剪切应力耐受阈值
管理剪切应力对于培养肉生产至关重要,因为不均匀的应力会损害缺乏强细胞壁的细胞。了解每种细胞类型可以承受的特定应力水平有助于维持细胞健康、触发机械敏感反应或促进分化。
常见细胞类型的阈值
剪切应力耐受性在细胞类型之间差异显著,了解这些阈值是微调生物反应器设置的关键。
例如,培养肉成肌细胞如C2C12系在低剪切应力下表现良好。约1.68 mPa的循环应力改善了肌管的形成和融合[8]. 鼠肌肉来源的干细胞(MDSCs)在暴露于16 mPa时表现出更好的肌源性分化和更广泛的肌管形成[8]. 随着成肌细胞成熟为肌管,它们可以承受更高的应力水平;在400 mPa 和 1,400 mPa之间的脉冲应力激活调节肌纤维大小的通路,可能导致肥大[8].
间充质干细胞(MSCs)也有独特的反应。例如,暴露于100 mPa 和 1,500 mPa 之间的剪切应力的犬MSC上调内皮标志物如PECAM-1和VE-cadherin,同时下调平滑肌标志物[10].
剪切应力阈值比较表
以下是不同培养肉细胞类型的剪切应力阈值的快速比较:
| 细胞类型 | 剪切应力阈值 (mPa) | 观察到的效果 | 来源 |
|---|---|---|---|
| 哺乳动物细胞(一般) | 300–1,700 | 基线范围;高于此水平可能导致细胞损伤或凋亡 | [1] |
| C2C12 肌母细胞(贴壁) | ~1.68 | 改善的生存能力和增加的肌管形成 | [8] |
| 小鼠MDSCs(贴壁) | ~16 | 增强的分化和广泛的肌管形成 | [8] |
| C2C12肌管(贴壁) | 400–1,400 | 调节肌纤维大小的通路激活(潜在肥大) | [8] |
| 犬MSC | 100–1,500 | 内皮标志物上调,平滑肌标志物减少 | [10] |
| 细胞表面传感器(整合素) | 100–1,000 | 机械敏感离子通道和受体的激活 | [1] |
在标准烧瓶中以100–200 rpm的速度搅拌培养物会产生300–660 mPa, 的剪切应力,而以20–60 rpm运行的轨道摇床会产生更高的力,范围从600 mPa 到 1,600 mPa [1]. 温和的系统如摇动生物反应器(±5°,1 Hz)产生的应力约为90 mPa [9], ,而临床生物反应器的操作应力约为10 mPa, ,远低于机械敏感细胞表面传感器的激活阈值[1] .
这些阈值作为调整生物反应器条件的指南,有助于在放大和细胞生长阶段保持最佳环境。
sbb-itb-ffee270
如何减少剪切应力损伤
在培养肉生产中最小化剪切应力损伤就是要实现微妙的平衡。目标是确保有效的混合和氧气输送,同时保护敏感细胞免受机械损伤。这涉及到智能生物反应器设计和周到的操作策略的结合。
生物反应器设计修改
使用CFD(计算流体动力学)建模是优化生物反应器性能的关键步骤。现代CFD技术现在包括多相流模拟,这考虑了细胞和微载体之间的相互作用。这导致对剪切应力及其潜在损害的评估更加准确[5].
生物反应器的类型在确定剪切应力水平方面起着重要作用。虽然搅拌罐反应器仍然被广泛使用,但替代设计可以提供更温和的条件:
- 气升式生物反应器: 这些消除了机械搅拌器,改用气体诱导循环以减少机械剪切[5].
- 波动或摇摆式生物反应器: 通过依靠表面运动而不是叶轮,这些反应器非常适合需要温和混合的低至中密度培养物 [5] .
- 垂直轮式生物反应器: 特别适用于基于聚集体的培养,这些反应器在扩展人类iPSC聚集体期间已显示出维持细胞活力的成功 [11].
另一个重要因素是细胞悬浮液的非牛顿行为。例如,含有血清的悬浮液表现出剪切变稀特性,传统模型往往无法捕捉。使用先进的模型,如Sisko模型,可以更准确地预测剪切应力,有助于微调机械力并避免可能改变基因表达的阈值 [6].
细胞播种和搅拌方法
操作策略在减少剪切应力损伤方面也起着重要作用。例如,间歇搅拌 在细胞附着的早期阶段可以限制剪切暴露,同时仍能有效分配营养。调整搅拌需要仔细考虑血清含量、细胞密度和培养物的年龄等因素[6].
在确定搅拌速度时,CFD建模 可以帮助找到理想的平衡——足够的氧气传递而不造成机械损伤。分区模拟可以进一步优化剪切应力分布,使过程更高效[5].
对生物反应器设计和放大规模的影响
在扩大培养肉生产的生物反应器时,理解和应用剪切应力阈值至关重要。这些阈值会影响搅拌器速度、曝气器设计和其他参数的决策,以确保随着生产量的增加,细胞的存活率。
设置生物反应器操作参数
剪切应力阈值在定义操作限制方面起着关键作用。例如,造血干细胞(HSCs)的阈值约为0.092 Pa [12]. 保持在此水平以下 - 如以50 rpm运行,产生约0.068 Pa - 支持健康的细胞扩增,实现27.4倍增长. 然而,将搅拌提高到100 rpm会将剪切应力增加到约0.192 Pa,导致72%的凋亡率,并将扩增限制在 24。5‐fold[12].
"HSCs增殖和功能的临界剪切应力已被报道为0.092 Pa。" – Hosseinizand et al. [12]
当湍流涡流变得比细胞或聚集体直径的约三分之二还小时,会发生剪切损伤[12][13]. 在50 rpm时,涡流测量约280 µm,这对细胞是安全的。但在100 rpm时,涡流缩小到166 µm,增加了机械损伤的风险。
曝气引入了额外的流体动力学应力。小气泡(直径1 mm)在破裂时产生约6.4 m/s的局部流体速度,而较大的6 mm气泡产生较温和的峰值0.94 m/s[13]. 为了解决这个问题,使用了像Pluronic F68这样的添加剂来防止细胞粘附在气泡表面。然而,它们的有效性依赖于相对于气体表面积保持正确的浓度[13].
这些参数在过渡到更大的生物反应器系统时至关重要。
放大过程中保持条件
从250 mL旋转瓶放大到20 m³搅拌罐反应器会带来独特的挑战。小规模系统中的流体动力学条件不能直接转化为工业体积。即使在最低搅拌速度下操作大型反应器,也可能产生足够强的剪切力,使细胞从微载体上脱落[3].
“即使在接近Njs的搅拌速度下操作,单靠叶轮施加的剪切力也可能导致细胞从微载体上脱落,而通过曝气引入的流体动力学应力更大。” – 张等人。 [3]
为了在放大过程中保持一致的剪切条件,一种方法是保持叶轮尖端速度恒定。然而,这可能导致更长的混合时间以及营养和氧气梯度的形成,这可能对细胞生长和性能产生负面影响[3]. 计算流体动力学 (CFD) 建模在放大过程中识别应力区和优化反应器设计时变得至关重要[5].
对于对剪切高度敏感的细胞系,替代反应器设计通常更为合适。气升式反应器消除了机械搅拌器,已成功建模至高达 300,000 L 的体积,实现了理论细胞密度 2 × 10⁸ cells/mL[7]. 同样,摇摆式生物反应器使用轻柔的波动来最小化剪切,使其在种子培养链中有效,容量可达500 L[14][15]. 像
总结和建议
有效管理剪切应力对于维持培养肉生产中的细胞活力和生产力至关重要。研究表明,曝气过程中气泡破裂产生的破坏力比机械搅拌更大。例如,小气泡(1 mm)破裂时产生的流体速度为6.4 m/s,而较大的气泡(6 mm)则产生较温和的峰值速度为0.94 m/s [13]. 为了减少这些力,采购团队应专注于配备烧结微气泡发生器(15微米孔径)的生物反应器,这些反应器允许脉冲曝气并减少气液界面。这些考虑对于扩大生物反应器系统的规模至关重要。
另一个重要因素是涡流尺度与细胞直径的比率(η/d_c),这有助于减少搅拌造成的损害。生物过程工程与制药技术研究所在2017年8月进行的一项研究强调了这一点。使用3升Applikon玻璃生物反应器和Sf21昆虫细胞,他们展示了在205 rpm下使用六叶Rushton搅拌器,结合199微米气泡,产生了12.75 μg/mL的GFP蛋白产量。相比之下,171 rpm下的倾斜叶片搅拌器产生了更高的18.0 m²/m³的比气体表面积,仅产生了4.0 μg/mL的产量[13]. 这表明,总气体表面积比搅拌速度更具影响力。
保护剂如Pluronic F68(0.5–3 g/L)可以在气泡周围形成16–40 μm的保护层,防止细胞附着[13] . 然而,正如Tobias Weidner和同事观察到的:
如果[总气体]表面积超过某个阈值,Pluronic的浓度将不足以保护细胞[13].
这意味着工程师在放大过程中必须仔细监测气体表面积与Pluronic F68浓度的关系,以确保细胞保持受保护状态。
对于敏感的细胞系,替代反应器设计可以提供解决方案。例如,气升式反应器消除了机械搅拌器,创造了一个更温和的混合环境 [7]. 固定床生物反应器是另一种选择,能够维持超低壁面剪切应力,范围从10⁻³到10⁻² Pa [17]. 对于探索专业低剪切系统的团队,像
此外,将牛成肌细胞维持在25次群体倍增以下对于保持其分化能力至关重要[16]. 超过此阈值可能导致融合指数在每次传代时大约下降6.81%[16], 降低细胞形成肌纤维的能力。为了解决这个问题,工艺工程师应利用计算流体动力学(CFD)建模在从实验室到工业系统放大之前识别高剪切区域。这种方法确保在放大过程中更顺利的过渡和更好的结果。
常见问题
如何测量我的生物反应器中的剪切应力?
生物反应器中的剪切应力通常使用计算建模技术,如计算流体动力学(CFD)进行评估。这些方法可以分析流动模式并识别生物反应器内的剪切区域。此外,小规模剪切测试工具对于表征特定细胞系的敏感性和评估各种工艺条件非常有价值。对于连续监测,可以通过计算流体速度和粘度来确定剪切应力。这种方法在微流体系统中或通过使用在线剪切应力计算器特别有效。
哪种曝气方法能最大限度地减少气泡破裂损伤?
最大限度地减少气泡破裂损伤在很大程度上依赖于使用较小的气泡。这些气泡在体积对体积的比较中造成的细胞损伤较少。虽然没有详细说明具体技术,但管理气泡的大小和行为——如调节其大小——在减少破裂的有害影响方面起着关键作用。
在放大以减少剪切时,我应该保持什么不变?
在增加培养肉生物反应器的规模时,保持剪切应力在约 3 Pa 以下对于防止细胞受损至关重要。请密切注意 搅拌, 流动模式, 和 曝气 等因素,以确保整个操作过程中剪切水平保持一致。











