遗传稳定性对于培养肉生产至关重要。没有它,细胞系可能会发生突变,导致质量不一致、安全风险和生产失败。从数千个细胞扩展到数万亿个细胞会放大这些风险,因此强大的质量控制系统是必不可少的。像FDA和 EMA这样的监管机构要求在批准产品之前提供稳定性的证明,因为即使是轻微的遗传变化也可能引发过敏或有害的结果。
主要挑战包括遗传漂移、突变积累和癌基因激活。这些问题源于细胞长时间传代、选择压力和生产过程中的环境压力。高级测试方法,如核型分析、SNP阵列和下一代测序(NGS),有助于检测和解决这些风险。预防策略如结构化细胞库和靶向基因工程进一步防止不稳定性。
生产商必须在生产的每个阶段整合质量控制——从细胞库到大规模生物反应器。像STR分析、污染测试和功能测定这样的工具确保了一致性和安全性。像
加速从DNA到主细胞库的细胞系开发 - AGC Biologics
维持遗传稳定性的常见挑战
在培养肉的生产周期中确保遗传稳定性绝非易事。生产的巨大规模为遗传变化的发展和传播提供了许多机会。认识到这些挑战是建立有效质量控制系统的关键。
遗传漂变和突变积累
延长细胞传代是培养肉生产中基因组不稳定的主要来源。永生化细胞系本质上易于基因组变化,这可能导致长期培养期间的自发突变[6][5]. 随着细胞经历多次群体倍增,DNA复制中的错误积累,导致细胞群体多样化,并可能导致功能丧失。Christopher Frye 和 Luhong He 来自BioPharm International强调了这个问题:
克隆衍生的CHO细胞系经常被观察到在长时间的亚培养过程中发生分化,成为异质性群体[6].
在工业环境中,大约20%的生产细胞系在连续几代中表现出显著的转基因异质性 [6]. 这些突变可能在早期发生,在转染后的DNA复制过程中,或由于外源基因整合到宿主基因组时的错误 [5].
选择压力增加了复杂性。用于稳定细胞系的抗生素和代谢标记物(e.g. , MTX)等试剂实际上可以增加突变率 [6][5]. 在某些情况下,这些试剂的浓度越高,突变率越高 [6]. 环境压力 - 如营养短缺、放大过程中的亚最佳培养条件以及扩展带来的物理压力 - 可以进一步破坏遗传完整性 [6][5].
王帅,药明生物细胞系开发总监
指出:由于中国仓鼠卵巢(CHO)细胞的基因组可塑性,突变水平可能会在细胞传代过程中发生变化[5].
表观遗传变化也起到了一定作用。转基因在培养过程中可能会部分或完全丢失或沉默,影响长期稳定性。这些累积的突变不仅损害细胞功能,还增加了激活癌基因的风险。
癌基因激活风险
癌基因激活对培养肉生产商来说是一个关键的安全问题,因为它可能会影响整个生产批次。遗传不稳定性可以通过高甲基化等机制导致癌基因激活,从而导致肿瘤样特征[3][1]. 生产中所需的快速扩张进一步增加了积累这些有害突变的可能性 [5][6].
这是一个公认的挑战。根据国际创新联盟 & 制药开发质量 (IQ) 的数据,67% 的受访者认为基因突变在生产过程中比氨基酸误掺入构成更大的威胁 [5] . 2024年5月的一个案例说明了这一问题的严重性:WuXi Biologics 发现一个细胞系开发项目的 43% 的克隆携带相同的基因点突变。根本原因?在转染过程中使用的质粒 DNA 中存在 2.1%–2.2% 的变异水平,这一问题未被传统的 Sanger 测序检测到。为了解决这个问题,公司将下一代测序 (NGS) 纳入其质量控制流程,以便及早发现此类变异 [5].
早期检测遗传异常至关重要,因为致癌性变化可能会影响整个批次。标准的G带核型分析可以在二十个细胞中期中识别出仅14%嵌合体的异常亚群[1]. 更先进的技术如NGS可以以0.5%的灵敏度检测克隆细胞中的基因突变[5].
DNA甲基化分析是评估肿瘤发生潜力的另一个有价值的工具:
由于DNA甲基化水平和某些基因的过度甲基化发生在癌症的起始和进展过程中,DNA甲基化谱的分析可能提供关于细胞肿瘤发生潜力的补充信息[3].
真正的挑战在于实施能够在这些变化影响安全性之前识别它们的强大监测系统。对于培养肉生产商来说,在快速细胞扩增过程中保持遗传稳定性需要先进的质量控制措施。像
质量控制测试方法
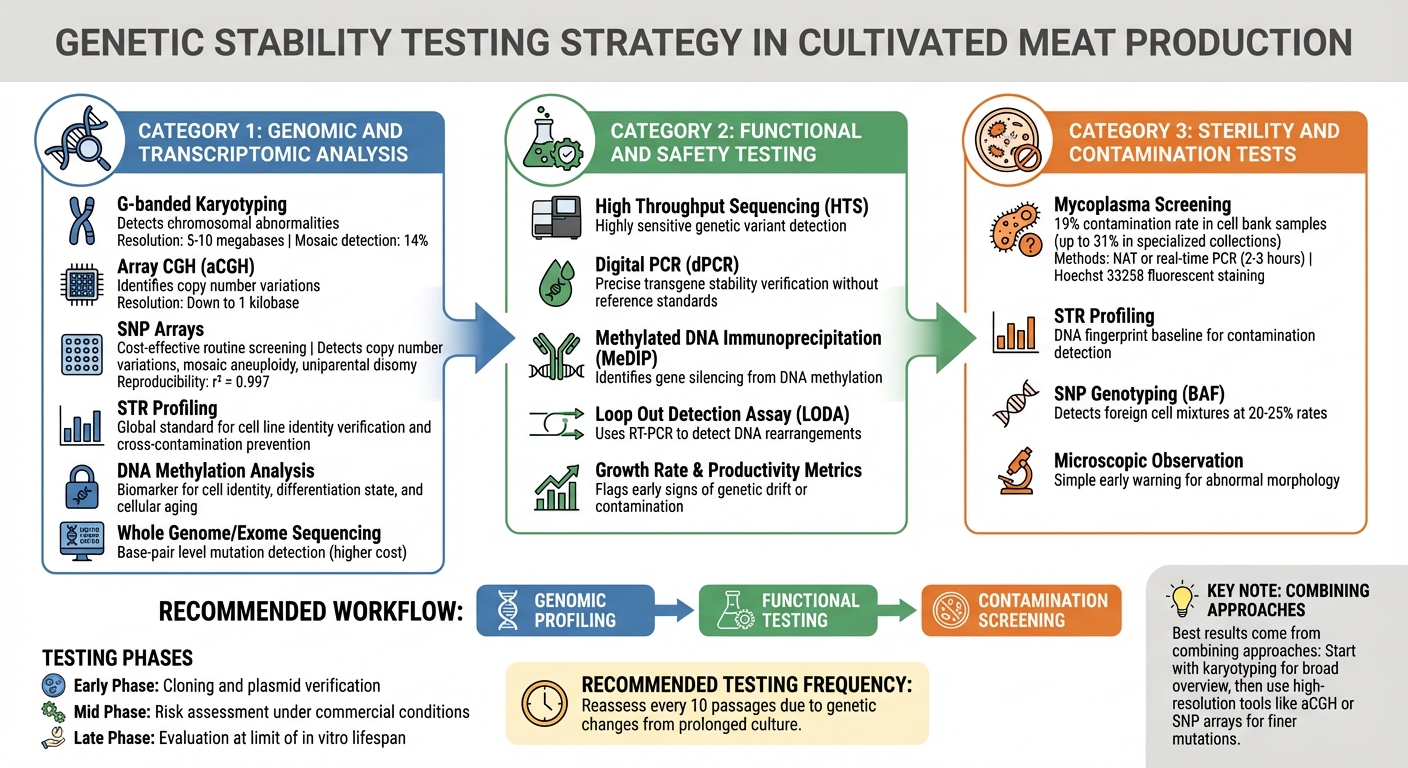
培养肉细胞系遗传稳定性的质量控制测试方法
在遗传不稳定性影响生产之前进行识别需要多层次的测试策略。培养肉生产商依赖于检测从大染色体变化到单碱基突变的各种方法。技术的选择取决于每个生产阶段存在的风险。这些基因组工具作为第一个检查点,随后是详细的功能和污染评估。
基因组和转录组分析
G带核型分析 是识别主要染色体问题(如数目异常和大型结构重排,如易位)的关键工具。虽然它可以检测到约14%的嵌合水平,但其分辨率仅限于5–10兆碱基的变化,这意味着较小的改变可能会被忽视[1].
阵列比较基因组杂交 (aCGH) 提供更高的分辨率,能够识别到1千碱基的拷贝数变异。同样,单核苷酸多态性 (SNP) 阵列 提供了一种具有成本效益的常规筛查选项,能够检测拷贝数变异、嵌合非整倍体和单亲二倍体。验证研究表明,SNP阵列具有高度的可重复性,B等位基因频率 (BAF) 测量达到令人印象深刻的r² = 0。997 [8] [1].
来自安达卢西亚公共卫生系统生物库的Rocio Aguilar-Quesada强调了结合方法的价值:
核型分析仍然是一种多功能的检测方法,特别是在与高分辨率测试结合时 [1].
短串联重复(STR)分析是验证细胞系身份和防止交叉污染的全球标准[1] [9]. 同时,DNA甲基化分析作为细胞身份、分化状态和细胞老化的生物标志物[1]. 对于碱基对水平的突变检测, 全基因组或外显子组测序是一个选择,尽管与基于阵列的方法相比成本更高[1].
最佳结果来自于结合这些方法。首先使用核型分析获得广泛的概览,然后使用高分辨率工具如aCGH或SNP阵列捕捉更细微的突变。定期重新评估——理想情况下每10次传代进行一次——是至关重要的,因为长期培养可能导致遗传变化[10]. 这些基因组见解随后通过功能测定进行补充,以确保在生产过程中细胞行为的一致性。
功能和安全测试
仅靠基因组分析是不够的。功能测试确认细胞在扩增过程中保持其预期特性。像生长速率和生产力这样的指标可以提前发现遗传漂移或污染的早期迹象[9].
高通量测序 (HTS) 对于检测遗传变异具有高度敏感性,而 数字PCR (dPCR) 在不需要参考标准的情况下精确验证转基因的稳定性 [11] . Christopher Frye 和 Luhong He 来自 BioPharm International 强调了这一步的重要性:
生产细胞系是任何生物工艺的基础,因此,生产细胞系的适当遗传特征化对于工艺开发的成功至关重要 [6].
表观遗传稳定性也至关重要。甲基化DNA免疫沉淀 (MeDIP) 有助于识别由DNA甲基化引起的基因沉默,这是生产力下降的常见原因 [7]. 工具如环外检测分析 (LODA) 使用RT-PCR检测DNA重排,例如当目标基因被删除而可选择标记仍然存在时[7].
测试应与生产阶段一致:早期阶段测试侧重于克隆和质粒验证,中期阶段测试在商业条件下评估风险,晚期阶段测试评估细胞在其体外寿命极限时的表现[6]. 从主细胞库开始使用新鲜、低传代细胞进行实验可降低遗传漂移的风险[9].
无菌和污染测试
污染测试对于避免可能破坏遗传稳定性的因素至关重要。支原体尤其令人担忧,因为它在不引起培养物可见变化的情况下改变细胞代谢和行为[1]. 研究显示,19%的细胞库样本存在支原体污染,一些专业收藏的污染率高达31% [1].
使用敏感的核酸扩增技术(NAT)或实时PCR进行常规支原体筛查,可以在2-3小时内提供半定量结果 [1]. Hoechst 33258荧光染色是另一种方法,揭示特征性的细胞外荧光模式 [9].
STR分析为细胞系建立DNA指纹,作为检测交叉污染的基线 [9]. 此外,使用B等位基因频率(BAF)分布的SNP基因分型可以识别来自其他细胞系的污染,以20-25%的比例检测外来细胞混合物 [8].
显微观察是一种简单而有效的早期预警工具,因为异常的细胞形态通常预示着培养问题[9]. 实施质量管理体系,如ISO 9001:2015, 以及良好的体外方法实践(GIVIMP),有助于保持标准化和可重复的培养条件,降低基因组不稳定的风险[10].
对于需要获取专业测试设备和材料的培养肉生产商,像
sbb-itb-ffee270
基因不稳定的预防策略
检测基因不稳定是一回事;预防它则是完全不同的挑战。为了保持遗传稳定性,培养肉生产商需要精心设计的系统,以防止细胞系在问题出现之前发生漂移。这里有两个关键策略:结构化细胞库和靶向基因工程. 这些方法共同直接应对遗传漂移和癌基因激活的风险。
细胞库和冷冻保存
突变积累是一个真实的担忧,因此可靠的细胞库系统是必需的。行业标准涉及一个两级系统:主细胞库 (MCB)和工作细胞库 (WCB). 这种设置确保了生产的一致起点。限制传代次数至关重要,因为每次传代都会增加突变的可能性。通过将细胞储存在液氮中,生物活性被有效暂停,从而减少储存期间遗传变化的风险。
细胞年龄不是通过时间来跟踪,而是通过倍增次数 . 例如,一个典型的5,000升生产生物反应器涉及大约30次倍增[6]. 为了保持遗传一致性,商业制造将此次数限制在45到60次倍增之间[6].
筛选方法如RT-PCR和单细胞qPCR可以及早发现问题,例如异常的mRNA剪接或转基因变异。显示出拷贝数广泛变异的细胞系应被丢弃以避免未来的问题。
质量控制是不可协商的。令人震惊的是,研究发现某些库中的细胞系多达31%被支原体污染 [3]. 为防止这种情况, STR分析用于在整个存储过程中确认细胞系的真实性。正如FSA研究和证据:
所强调的,稳定性的基因工程。 基因工程通过直接增强细胞系的稳定性提供了另一层防御。像靶向整合 (TI), 特别是重组酶介导的盒交换 (RMCE), 等技术允许将转基因精确插入特定的基因组位置。这种方法避免了随机整合的不确定性,因为位置效应和拷贝数不稳定性可能会造成严重影响。尽管CHO细胞中的RMCE效率低于0.1%[12], ,但由此产生的克隆更具可预测性和稳定性。由于储存的细胞是最终产品的起始材料,未来监管机构可能会要求高标准以确保高质量的安全肉制品 [2].
。
表达系统的选择也很重要。例如,谷氨酰胺合成酶 (GS)系统通常每个细胞大约有五个转基因拷贝,而二氢叶酸还原酶 (DHFR)系统可以将拷贝数放大到1000个[6]. 虽然更高的拷贝数听起来很有吸引力,但它们增加了DNA改变的可能性,使基于GS的系统成为长期稳定性的更明智选择。
为了进一步降低风险, 位点特异性诱变和 转染前NGS筛选至关重要。由于Sanger测序的检测限较高,NGS可以检测到低于0.5%的质粒突变,从而将克隆筛选成功率提高到90%以上[5].
来自WuXi Biologics的王帅及其同事强调了这种警惕性的重要性:
由于工艺优化无法纠正基因水平的突变,因此必须严格监测稳定克隆中的突变水平 [5].
对于需要专业工具的生产者 - 无论是用于冷冻保存、基因工程还是细胞系表征 -
将质量控制整合到生产中
在每个生产阶段中整合质量控制至关重要。没有结构化的系统,即使是维护良好的细胞系在扩展和放大过程中也可能发生变化。质量控制不应是事后的考虑 - 它必须是生产的核心部分。这始于扩展阶段,在此阶段,严格的管理系统和受控环境起着关键作用。
扩展和规模化过程中的质量控制
如前所述,基因组和污染测试至关重要,尤其是在规模化过程中。从小体积到数千升的转变引入了新的风险,每次细胞传代都会增加突变的可能性。 质量管理系统 (QMS)有助于有效管理这些风险。例如,在2017年至2022年期间,Josep M. Canals及其在巴塞罗那大学的团队实施了ISO 9001:2015 QMS,以标准化人类多能干细胞培养。他们对G带和aCGH数据的回顾性分析显示,与适应前条件相比,染色体畸变显著减少[10][13]. 运河强调了持续监测的重要性:
hPSCs在培养中的遗传不稳定性使得在计划将其用于实验时,频繁重新评估基因组完整性成为一项基本要求[10].
常规基因组筛查是必须的。像G带核型分析和aCGH这样的技术可以检测结构变化,而下一代测序(NGS)可以识别低于0.5%的突变[5]. 生长曲线分析也可以及早发现问题,例如污染或遗传漂移[9]. 环境监测增加了另一层安全保障,通过沉降板测试和每六个月一次的HEPA过滤器检查等做法,确保生产环境对细胞系保持稳定和无压力[4] .
培养基和试剂的一致性同样重要。使用无血清、定义明确的培养基如mTeSR1,以及具有分析证书的试剂,有助于减少批次间的差异,并限制病毒污染的风险[10][4]. 定期形态检查 - 在不同培养密度下进行简单的显微观察 - 可以捕捉到分化或压力的早期迹象[9]. 对于专业设备或试剂的采购,像
产品一致性的功能检测
虽然基因组监测可以保障过程安全,功能检测确保细胞按预期执行功能。仅有遗传稳定性是不够的;细胞还必须在生产批次中保持其正常功能。在培养肉中,这意味着要确认干细胞,如肌肉卫星细胞,在扩增后仍能分化为成熟的肌肉或脂肪组织。[2]. 分化分析对于验证这一点至关重要。
代谢分析如MTT、LDH和Resazurin提供了细胞健康和活力的见解[4][9]. 这些结合短串联重复(STR)分析, 有助于确认细胞系在整个生产过程中保持真实性并免受交叉污染[1][9].
转录分析是另一个关键步骤。Xiaoyue Chen 和 Sam Zhang 推荐:
推荐使用cDNA而不是基因组DNA测序进行突变检测,以评估转录水平的风险[5].
这种方法提供了更准确的最终产品图景,因为它反映了基因的表达方式,而不仅仅是它们的基因组位置。通过将基因组筛查与功能测定相结合,生产商可以确保每批产品在生产的每个阶段都符合严格的安全、质量和性能标准。
结论
保持遗传稳定性对于安全和一致地生产培养肉至关重要。Francisco J. Molina-Ruiz 和他在干细胞和再生医学实验室的同事们强调了风险:
hPSCs的遗传变化可能不仅危及基于hPSC的细胞产品的安全性...但也导致起始材料的异质性分化倾向、基因表达谱的改变以及最终细胞产品的低效 [10].
风险是显著的 - 超过531个错误识别的细胞系已被国际细胞系认证委员会记录 [1].
解决这些问题需要一个强有力的质量控制框架。这涉及结合STR分析、G带核型分析、aCGH和先进的NGS方法 [5], 以及ISO 9001:2015等系统,以标准化流程并最小化染色体异常 [13].
经济因素也推动了这些措施的需求。遗传漂变可能导致突变细胞获得生长优势,可能会破坏整个生产批次[10][11]. 随着对人类多能干细胞的关注日益增加,对稳定细胞系的需求从未如此之大。正如来自塔夫茨大学的David L. Kaplan教授所解释的:
永生化细胞系通常被认为是从稳定、强大的生物工艺中生成大量可食用组织的必要条件[14].
对于培养肉生产商来说,质量控制必须嵌入到每一个步骤中——从质粒筛选到大规模生产监控。通过结合全面测试和预防策略,生产商可以确保一致和可靠的结果。
常见问题
在扩大规模过程中,遗传稳定性测试应多久进行一次?
遗传稳定性测试是扩大规模过程中的关键步骤,应定期进行。测试的频率主要取决于特定的细胞系和相关过程。为了减少突变的可能性并保持细胞的干性,建议根据遗传分析设定传代限制。
哪些测试最能检测小突变和大染色体变化?
诸如SNP阵列分析和全基因组SNP基因分型等测试对于检测小突变、拷贝数变化和非整倍性非常有效。这些方法特别适用于识别细胞系中的大染色体改变。
防止生产批次间遗传漂移的最简单方法是什么?
为了最大限度地减少遗传漂移,定期进行细胞系的遗传和功能分析并限制其传代次数至关重要。实施建立主细胞库和定期检查遗传稳定性等做法,正如质量控制协议中所建议的。这些措施是保持一致性和确保不同生产批次间可靠结果的关键。











