生物安全检查对于确保英国及全球范围内的培养肉生产安全至关重要。这些检查侧重于防止污染、验证产品安全性和维护卫生标准。自2025年底以来,英国已将培养肉归类为“动物源性产品”,使其受到与传统肉类相同的严格安全法规的约束。挑战包括微生物污染(e.g. ,支原体影响5%-35%的细胞系)、化学残留和遗传稳定性。
关键措施包括:
- 设施设计: 使用HEPA过滤器、洁净室和CIP和SIP等灭菌协议。
- 员工培训: HACCP 四级认证和无菌技术。
- 材料处理: 可追溯的细胞库、遗传稳定性测试和残留监测。
英国食品标准局(FSA)和 苏格兰食品标准局(FSS)负责监督合规情况,并于2025年启动了 培养肉沙盒计划以指导企业。全球方法各异,美国和欧盟采用不同的框架,但都旨在维护安全。保持详细记录、迅速解决不合规问题以及利用第三方审计对于满足这些标准至关重要。
负责生物安全检查的监管机构
食品标准局(FSA)在英国的职责
在英国,食品标准局(FSA)负责英格兰和威尔士的食品安全,而 苏格兰食品标准局(FSS)在苏格兰承担类似职责。两家组织将培养肉产品(源自动物细胞的产品)根据法规 (EC) 853/2004 分类为 动物源性产品 (POAO)。这一分类意味着生产此类产品的设施必须遵循与传统肉类生产类似的卫生和安全标准 [5][7].
FSA 在这些产品进入市场之前确保安全方面发挥关键作用。它进行科学风险评估,并要求食品经营者应用危害分析和关键控制点 (HACCP)原则。这些措施旨在防止生物、化学和物理危害。此外,FSA 通过法规 (EC) 2017/625 下的 官方控制执行合规性 [5].
为了解决培养肉的特定挑战,FSA在2025年2月推出了其培养肉沙盒计划。该计划涉及八家公司参与每月的研讨会,使用真实的生产数据来解决细胞系身份、微生物学和毒理学等生物安全问题。该计划的目标是为行业创建详细的指导方针。到2026年初,FSA预计将收到大约15份来自培养肉企业的申请,并计划在两年内完成其中至少两份申请的安全评估 [6][7][8].
在北爱尔兰,欧盟法规仍然有效,确保与更广泛的欧洲标准保持一致。然而,根据北爱尔兰零售流动计划 (NIRMS) [7].
,在大不列颠授权的产品可以运输到北爱尔兰。这些量身定制的英国措施突显了与其他国家不同的监管方法,反映了全球在生物安全监督方面采用的多样化策略。
全球监管机构
全球范围内对培养肉的生物安全法规差异很大,这些法规受不同的理念和风险管理策略的影响。在美国,食品和药物管理局 (FDA) 和 美国农业部食品安全检验局 (USDA-FSIS) 根据2019年的协议共同承担责任。FDA负责初始阶段,如细胞采集和生长,而USDA-FSIS则负责收获、加工和标签阶段。值得注意的是,美国农业部食品安全检验局(USDA-FSIS)要求每班至少进行一次检查,这与传统肉类和家禽的流程相似 [9][10].
在欧盟,欧洲食品安全局(EFSA)负责领导培养肉产品的安全评估。同时, 粮食及农业组织(FAO)和 世界卫生组织(WHO)等组织提供更广泛的安全指导。他们在2023年4月发布的关于培养肉安全的联合报告影响了包括英国在内的多个国家的风险评估 [7]. 食品标准局(FSA)还与新加坡和澳大利亚的监管机构合作——这两个国家已经批准了培养肉产品——以促进全球一致的生物安全实践[6].
各国的监管框架差异显著。例如,美国农业部要求设施在生产开始前获得“检查许可”和设计批准。相比之下,英国食品标准局(FSA)使用其监管沙盒与企业合作制定行业特定指导方针[9] [7]. 进口规则也有所不同;美国要求进行“等效性”过程,以确保外国检查系统符合其公共卫生标准[9][10].
这些国际差异塑造了全球最佳实践,在需要监管一致性的同时尊重当地的生物安全方法。
培养肉类规模化和生物加工的趋势
生物安全标准和检查要求
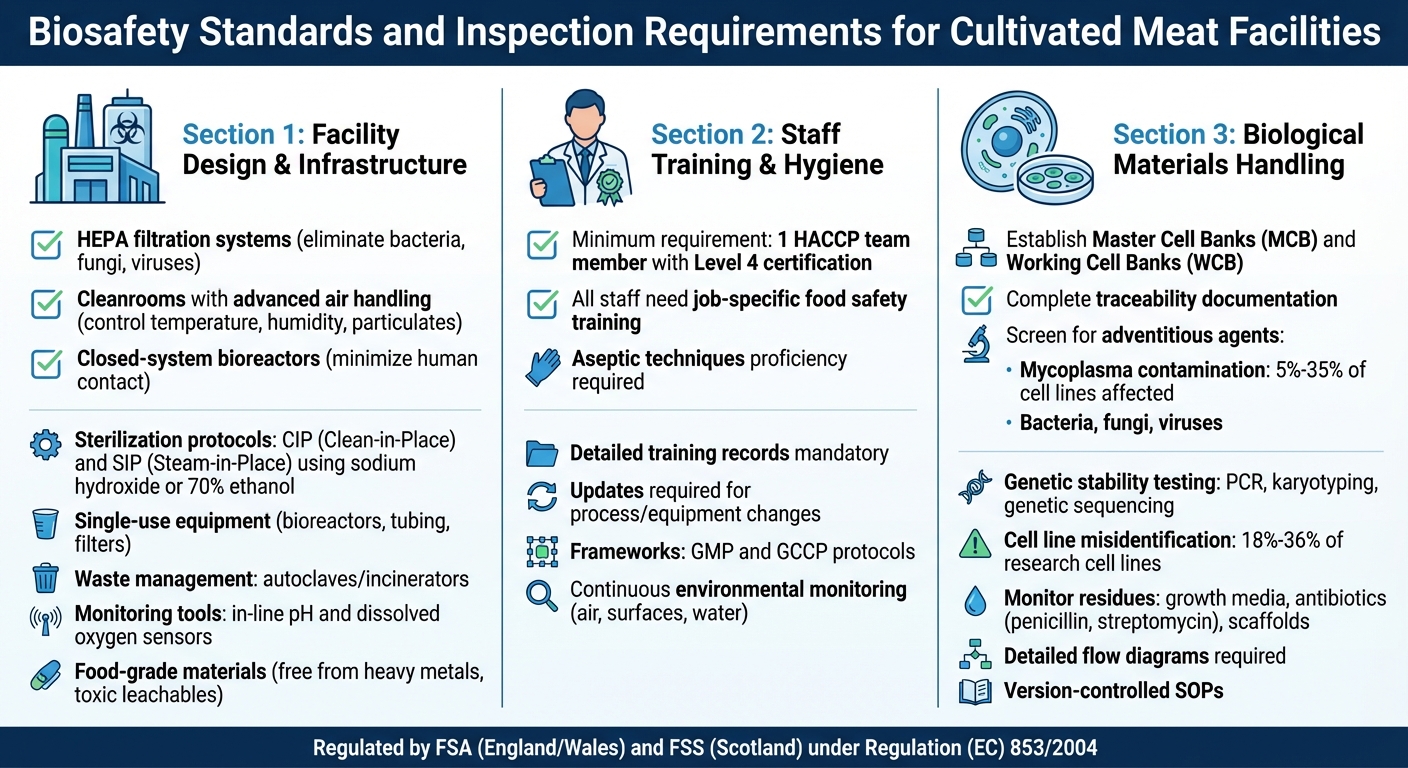
英国培养肉类设施的生物安全检查要求
设施设计和基础设施
设施的设计是符合生物安全检查标准的基础,如监管指南中所述。培养肉类设施必须实施严格的结构措施以防止污染。例如,HEPA过滤系统需要从空气中消除细菌、真菌和病毒[3] . 配备先进空气处理系统的洁净室调节温度、湿度和颗粒物,降低微生物风险[4].
为了减少人与细胞培养物的接触——这是污染的常见来源——设施通常依赖于封闭系统生物反应器和自动化设备[4] [3]. 此外,就地清洗 (CIP)和就地蒸汽灭菌 (SIP)协议对于在生产批次之间对设备进行灭菌至关重要,通常使用氢氧化钠或70%乙醇 [1] [3]. 使用一次性生物反应器、管道和过滤器进一步降低了批次间交叉污染的风险[4].
适当的废物管理和污染监测也至关重要。设施必须包括诸如高压灭菌器或焚化炉等系统,以处理用过的培养基和生物副产品。监测工具,如在线pH和溶解氧传感器,提供潜在污染的早期警告[1][4]. 此外,所有使用的材料——无论是在生物反应器表面还是管道中——都必须符合食品级标准,并且不含可能危害产品安全的有害物质,如重金属或有毒浸出物[1][3].
员工培训和卫生要求
虽然坚固的设施设计很重要,但训练有素的员工对于维持受控环境同样至关重要。根据英国卫生法规,HACCP团队中至少有一名成员必须具备HACCP原则的4级培训。此外,所有参与监测和纠正措施的员工都需要接受食品安全协议的岗位专门培训[5] .
从事生物材料工作的人员必须熟练掌握无菌技术,以避免将污染物引入细胞培养物中[4]. 设施需要保持详细的培训记录,并在生产过程、材料或设备发生变化时更新员工 [5]. 卫生标准还通过良好生产规范 (GMP) 和良好细胞培养规范 (GCCP) 等框架得到支持,这些框架为保持清洁设定了协议。对空气、表面和水的持续环境监测确保微生物污染能够早期检测到 [4].
生物材料的处理和储存
处理生物材料需要严格的协议以确保安全和合规。设施必须建立主细胞库 (MCB)和工作细胞库 (WCB), ,并为冷冻储存和细胞来源的完整可追溯性提供清晰的文档 [2]. 。必须筛查细菌、真菌、病毒和支原体等外来因子。研究结果表明,5%到35%的细胞系可能携带支原体感染,这些感染可以逃避标准过滤系统[1].
。为了监测在延长生产周期中可能发生的遗传漂移,设施会进行遗传稳定性测试,使用PCR、核型分析或基因测序等方法[1] [2]. 。研究表明,18%到36%的研究细胞系存在误识别或污染问题,这凸显了严格检查的必要性[1]. 。此外,设施必须确认生长培养基、抗生素(e.g. 、青霉素和链霉素)和支架材料的残留物保持在安全的食品级限度内[1][3].
详细的流程图对于跟踪从细胞来源到最终包装的每一步过程至关重要。版本控制系统确保标准操作程序(SOPs)保持最新,这是促进更顺利检查的要求[5]. 这些严格的处理协议构成了合规工作的基础,确保设施为彻底审计做好准备。
sbb-itb-ffee270
审计程序和合规验证
检查清单和文件记录
英国食品行业的审计围绕七个HACCP原则进行,所有食品经营者都必须依法遵循。检查员通常关注三个关键的文件领域:
- HACCP计划: 包括危害分析、工艺流程图和确定的关键控制点(CCPs)。
- 政策文件: 这些文件概述了卫生程序和相关协议。
- 操作记录: 这些记录包括监控日志、校准记录和其他日常合规证据。
为了证明持续合规,设施必须维护一个组织良好的安全文件夹。这应包括对关键限值的监测结果,如pH读数和温度记录,以及在这些限值被超出时采取的纠正措施记录。员工培训的证据也至关重要,HACCP团队中至少有一名成员需要持有四级认证。此外,所有标准操作程序(SOPs)必须是最新的,明确标注日期,并进行版本控制。
这些记录构成了验证审核的基础,确保持续遵守安全协议。设施应每年进行验证审核,或者如果危害性质、生产量或过去的问题需要的话,更频繁地进行。监管机构区分验证, 在实施前确认安全计划在理论上是有效的,以及验证, 涉及定期检查以确保计划在实践中有效。
管理不合规问题
未能达到生物安全标准会带来直接的法律后果。食品标准局 (FSA) 强调这一原则:
“如果食品不安全,则不得投放市场。这意味着它既不会对健康有害,也不适合人类食用。”
当发生不合规情况时,设施必须遵循三步响应流程:
- 恢复即时控制: 及时解决问题以尽量减少风险。
- 缓解受影响的产品: 采取措施管理并在必要时从市场上移除不安全的产品。
- 调查根本原因: 识别并纠正违规的根本原因。
每项纠正措施必须清楚记录,包括负责人员以及如何验证措施的有效性。
重复不合规可能导致严重后果。根据FSA指导:
“如果纠正措施需要反复采取,这意味着食品安全管理系统存在根本性错误。”
在这种情况下,监管机构可能会展开彻底调查,运营可能会被暂停,直到设施证明已解决系统性故障。详细记录所有纠正措施,包括根本原因分析,对于证明已实施长期解决方案至关重要。
满足生物安全标准的行业资源
确保生物安全合规通常需要的不仅仅是内部检查。外部资源通过提供符合检查期望的验证工具和材料,在帮助设施满足监管标准方面发挥关键作用。
Cellbase 在生物安全合规中的角色
对于培养肉生产商来说,管理细胞库——生产的基石——本身就有一系列挑战,尤其是因为没有标准化的指导方针[2]. 这使得采购合规设备和追踪细胞来源特别棘手。
与第三方审计员合作
第三方审计员通过验证HACCP计划并增强对食品安全管理系统的信心,提供了额外的保障层 [5]. 他们的专业知识包括进行微生物挑战研究,例如评估李斯特菌等病原体在培养肉中的生长潜力。这些研究提供了关键的安全数据,这一点尤为重要,因为该行业的平均微生物污染批次失败率为11。2% [11].
及早与第三方审计员合作也可以帮助设施为FDA的市场前审查和USDA的检查做好准备 [12][9]. 为了简化合规流程,审计报告应添加到永久的HACCP文件夹中,确保设施在官方检查期间准备好展示对安全标准的遵守情况 [5].
结论
生物安全检查在保护公众健康和维护培养肉行业的信任方面起着至关重要的作用。英国严格的卫生法规为设施设定了高标准,确保他们正面应对如支原体污染和细胞系误识别等风险 [5][1].
像CCP沙箱这样的项目有助于澄清监管期望,简化新兴食品技术的路径,同时不影响安全性。为了满足这些标准,生产商必须实施强有力的措施,包括认证的细胞库,确保至少有一名团队成员拥有4级HACCP培训,并进行年度安全计划审查[5][1][2]. 行业逐渐转向无血清培养基和采用实时监控技术,强调其致力于解决传统食品安全问题和与培养肉生产相关的独特风险。
外部支持也加强了合规努力。像
强有力的生物安全实践至关重要——不仅是为了获得市场批准,也是为了维护行业声誉并推动其未来增长。
常见问题
在培养肉设施中,是什么触发了生物安全检查?
培养肉设施中的生物安全检查在确保遵循重要标准方面起着关键作用,例如ISO 14644-1, EU GMP 附录 1, 和EN 17141. 这些检查通常在关键阶段进行,包括设计、施工和认证阶段。主要目标是防止微生物污染,并在整个过程中保持安全。
生产者如何确保其细胞系在时间上保持真实性和稳定性?
生产者通过实施严格的细胞库程序来维护其细胞系的完整性和可靠性。这些过程包括确认细胞系的身份,定期评估其稳定性,并遵循既定的行业标准和指南。通过遵循这些协议,他们确保在培养肉生产中获得一致和可靠的结果。
如果在生产过程中发现污染会发生什么?
生产过程中出现污染可能导致严重问题,例如未能达到安全标准、产品召回和增加的微生物风险。这突显了严格卫生实践和强有力认证过程的必要性,以保护产品的安全性和质量。











