ความเสถียรทางพันธุกรรมมีความสำคัญอย่างยิ่งต่อการผลิตเนื้อสัตว์ที่เพาะเลี้ยง หากไม่มีความเสถียรนี้ สายเซลล์อาจกลายพันธุ์ นำไปสู่คุณภาพที่ไม่สม่ำเสมอ ความเสี่ยงด้านความปลอดภัย และความล้มเหลวในการผลิต การขยายจากเซลล์นับพันไปจนถึงล้านล้านเซลล์จะเพิ่มความเสี่ยงเหล่านี้ ทำให้ระบบควบคุมคุณภาพที่แข็งแกร่งเป็นสิ่งจำเป็น หน่วยงานกำกับดูแลเช่น FDA และ EMA ต้องการหลักฐานความเสถียรก่อนที่จะอนุมัติผลิตภัณฑ์ เนื่องจากแม้แต่การเปลี่ยนแปลงทางพันธุกรรมเล็กน้อยก็สามารถกระตุ้นให้เกิดผลลัพธ์ที่ก่อให้เกิดภูมิแพ้หรือเป็นอันตรายได้
ความท้าทายหลัก ได้แก่ การล่องลอยทางพันธุกรรม การสะสมของการกลายพันธุ์ และการกระตุ้นยีนก่อมะเร็ง ปัญหาเหล่านี้เกิดจากการผ่านเซลล์เป็นเวลานาน แรงกดดันในการคัดเลือก และความเครียดจากสิ่งแวดล้อมระหว่างการผลิต วิธีการทดสอบขั้นสูง เช่น การทำคาริโอไทป์ อาร์เรย์ SNP และการหาลำดับเบสยุคใหม่ (NGS) ช่วยตรวจจับและแก้ไขความเสี่ยงเหล่านี้ กลยุทธ์การป้องกัน เช่น การจัดเก็บเซลล์อย่างมีโครงสร้างและการวิศวกรรมพันธุกรรมที่ตรงเป้าหมาย ช่วยป้องกันความไม่เสถียรเพิ่มเติม
ผู้ผลิตต้องบูรณาการการควบคุมคุณภาพในทุกขั้นตอนของการผลิต - ตั้งแต่การจัดเก็บเซลล์ไปจนถึงเครื่องปฏิกรณ์ชีวภาพขนาดใหญ่ เครื่องมือเช่นการตรวจสอบโปรไฟล์ STR, การทดสอบการปนเปื้อน, และการทดสอบการทำงานช่วยให้มั่นใจในความสม่ำเสมอและความปลอดภัย แพลตฟอร์มเช่น
เร่งการพัฒนาเซลล์ไลน์จาก DNA ไปยังธนาคารเซลล์หลัก - AGC Biologics
ความท้าทายทั่วไปในการรักษาความเสถียรทางพันธุกรรม
การรักษาความเสถียรทางพันธุกรรมตลอดวงจรการผลิตเนื้อสัตว์ที่เพาะเลี้ยงไม่ใช่เรื่องง่าย ขนาดการผลิตที่ใหญ่ทำให้มีโอกาสมากมายที่การเปลี่ยนแปลงทางพันธุกรรมจะพัฒนาและแพร่กระจาย การรับรู้ถึงความท้าทายเหล่านี้เป็นกุญแจสำคัญในการวางระบบควบคุมคุณภาพที่มีประสิทธิภาพ
การล่องลอยทางพันธุกรรมและการสะสมการกลายพันธุ์
การผ่านเซลล์หลายครั้งเป็นแหล่งสำคัญของความไม่เสถียรทางพันธุกรรมในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง เซลล์สายพันธุ์ที่เป็นอมตะมีแนวโน้มที่จะเกิดการเปลี่ยนแปลงทางพันธุกรรม ซึ่งอาจนำไปสู่การกลายพันธุ์ที่เกิดขึ้นเองในระหว่างการเพาะเลี้ยงระยะยาว [6][5]. เมื่อเซลล์ผ่านการเพิ่มจำนวนประชากรหลายครั้ง ข้อผิดพลาดในการจำลองดีเอ็นเอจะสะสมขึ้น ส่งผลให้เกิดประชากรเซลล์ที่หลากหลายและอาจสูญเสียหน้าที่ Christopher Frye และ Luhong He จาก BioPharm International เน้นย้ำปัญหานี้:
สายพันธุ์เซลล์ CHO ที่ได้จากการโคลนมักถูกสังเกตว่าเบี่ยงเบนกลายเป็นประชากรที่ไม่เหมือนกันในช่วงเวลาที่ยาวนานของการเพาะเลี้ยงย่อย [6].
ในสภาพแวดล้อมอุตสาหกรรม ประมาณ 20% ของสายการผลิตแสดงความหลากหลายของยีนที่ถ่ายโอนอย่างมากในรุ่นต่อๆ ไป [6]. การกลายพันธุ์เหล่านี้สามารถเกิดขึ้นได้ตั้งแต่ต้น ระหว่างการจำลองดีเอ็นเอหลังจากการถ่ายโอน หรือเนื่องจากข้อผิดพลาดเมื่อยีนต่างประเทศถูกรวมเข้ากับจีโนมของโฮสต์ [5].
แรงกดดันในการคัดเลือกเพิ่มความซับซ้อนอีกชั้นหนึ่ง ตัวแทนเช่นยาปฏิชีวนะและตัวบ่งชี้เมตาบอลิซึม (e.g. , MTX) ที่ใช้ในการทำให้สายเซลล์มีเสถียรภาพสามารถเพิ่มอัตราการกลายพันธุ์ได้จริง [6][5]. ในบางกรณี ยิ่งความเข้มข้นของตัวแทนเหล่านี้สูงขึ้น อัตราการกลายพันธุ์ก็ยิ่งสูงขึ้น [6]. ปัจจัยกดดันจากสิ่งแวดล้อม - เช่น การขาดแคลนสารอาหาร สภาพการเพาะเลี้ยงที่ไม่เหมาะสมระหว่างการขยายขนาด และความเครียดทางกายภาพจากการขยายตัว - สามารถทำให้ความสมบูรณ์ของพันธุกรรมไม่เสถียรยิ่งขึ้น [6][5].
Shuai Wang, ผู้อำนวยการฝ่ายพัฒนาสายเซลล์ที่ WuXi Biologics, กล่าวว่า:
ระดับการกลายพันธุ์มีแนวโน้มที่จะเปลี่ยนแปลงไปตามการผ่านเซลล์เนื่องจากความยืดหยุ่นทางพันธุกรรมของเซลล์รังไข่แฮมสเตอร์จีน (CHO) [5].
การเปลี่ยนแปลงทางอีพิเจเนติกส์ก็มีบทบาทเช่นกัน ยีนที่ถูกถ่ายโอนสามารถสูญหายหรือถูกปิดเสียงบางส่วนหรือทั้งหมดในระหว่างกระบวนการเพาะเลี้ยง ซึ่งส่งผลต่อความเสถียรในระยะยาว การกลายพันธุ์ที่สะสมเหล่านี้ไม่เพียงแต่ทำลายการทำงานของเซลล์ แต่ยังเพิ่มความเสี่ยงในการกระตุ้นยีนก่อมะเร็งอีกด้วย
ความเสี่ยงในการกระตุ้นยีนก่อมะเร็ง
การกระตุ้นยีนก่อมะเร็งเป็นข้อกังวลด้านความปลอดภัยที่สำคัญสำหรับผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยง เนื่องจากอาจทำให้ชุดการผลิตทั้งหมดเสียหาย ความไม่เสถียรทางพันธุกรรมสามารถนำไปสู่การกระตุ้นยีนก่อมะเร็งผ่านกลไกต่างๆ เช่น การเมทิลเลชันเกิน ซึ่งอาจส่งผลให้เกิดโปรไฟล์คล้ายเนื้องอก [3][1]. การขยายตัวอย่างรวดเร็วที่จำเป็นในการผลิตยิ่งเพิ่มความเป็นไปได้ในการสะสมการกลายพันธุ์ที่เป็นอันตรายเหล่านี้ [5][6].
นี่เป็นความท้าทายที่ได้รับการยอมรับอย่างดี ตามข้อมูลจาก International Consortium for Innovation & Quality in Pharmaceutical Development (IQ) พบว่า 67% ของผู้ตอบแบบสอบถามเชื่อว่าการกลายพันธุ์ทางพันธุกรรมเป็นภัยคุกคามที่มากกว่าการแทรกแซงกรดอะมิโนผิดพลาดระหว่างการผลิต [5] . กรณีจากเดือนพฤษภาคม 2024 แสดงให้เห็นถึงความรุนแรงของปัญหานี้: WuXi Biologics ค้นพบว่า 43% ของโคลนจากโปรแกรมพัฒนาสายเซลล์มีการกลายพันธุ์จุดพันธุกรรมเดียวกัน สาเหตุหลัก? ระดับความแปรปรวน 2.1%–2.2% ใน DNA พลาสมิดที่ใช้ระหว่างการถ่ายโอน ซึ่งไม่สามารถตรวจพบได้ด้วยการจัดลำดับ Sanger แบบดั้งเดิม เพื่อแก้ไขปัญหานี้ บริษัทได้รวมการจัดลำดับรุ่นถัดไป (NGS) เข้ากับกระบวนการควบคุมคุณภาพเพื่อจับความแปรปรวนดังกล่าวตั้งแต่เนิ่นๆ [5].
การตรวจพบความผิดปกติทางพันธุกรรมในระยะแรกเป็นสิ่งสำคัญ เนื่องจากการเปลี่ยนแปลงที่ก่อให้เกิดมะเร็งสามารถทำให้ชุดทั้งหมดเสียหายได้ การทำคาริโอไทป์แบบ G-band มาตรฐานสามารถระบุประชากรย่อยที่ผิดปกติได้ด้วยโมเสกเพียง 14% ในระยะเมตาเฟสของเซลล์ยี่สิบเซลล์ [1]. เทคนิคที่ก้าวหน้ากว่าเช่น NGS สามารถตรวจพบการกลายพันธุ์ทางพันธุกรรมในเซลล์โคลนด้วยความไว 0.5% [5].
การวิเคราะห์เมทิลเลชันของ DNA เป็นเครื่องมือที่มีคุณค่าอีกอย่างหนึ่งในการประเมินศักยภาพในการก่อมะเร็ง:
เนื่องจากระดับเมทิลเลชันของ DNA และการเกิดไฮเปอร์เมทิลเลชันของยีนบางตัวเกิดขึ้นในระยะเริ่มต้นและการพัฒนาของมะเร็ง การวิเคราะห์โปรไฟล์เมทิลเลชันของ DNA อาจให้ข้อมูลเสริมเกี่ยวกับศักยภาพในการก่อมะเร็งของเซลล์ [3].
ความท้าทายที่แท้จริงอยู่ที่การนำระบบการตรวจสอบที่แข็งแกร่งมาใช้ซึ่งสามารถระบุการเปลี่ยนแปลงเหล่านี้ได้ก่อนที่มันจะส่งผลกระทบต่อความปลอดภัยสำหรับผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยง การรักษาเสถียรภาพทางพันธุกรรมในระหว่างการขยายเซลล์อย่างรวดเร็วต้องการมาตรการควบคุมคุณภาพขั้นสูง แพลตฟอร์มเฉพาะทางเช่น
วิธีการทดสอบการควบคุมคุณภาพ
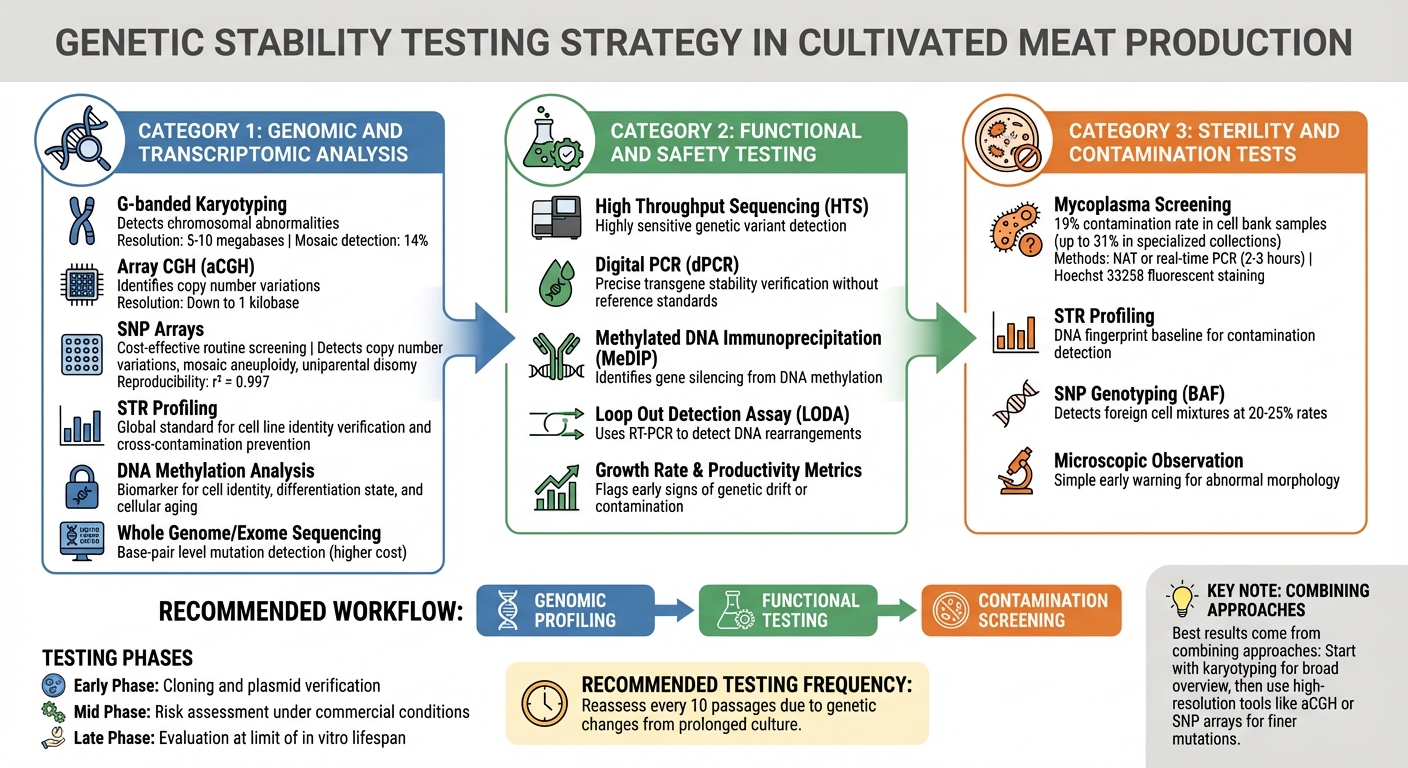
วิธีการทดสอบการควบคุมคุณภาพสำหรับเสถียรภาพทางพันธุกรรมในสายเซลล์เนื้อสัตว์ที่เพาะเลี้ยง
การระบุความไม่เสถียรทางพันธุกรรมก่อนที่จะส่งผลกระทบต่อการผลิตต้องใช้กลยุทธ์การทดสอบหลายชั้น ผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยงพึ่งพาวิธีการที่ตรวจจับทุกอย่างตั้งแต่การเปลี่ยนแปลงของโครโมโซมขนาดใหญ่ไปจนถึงการกลายพันธุ์ของเบสเดี่ยว การเลือกเทคนิคขึ้นอยู่กับความเสี่ยงที่มีอยู่ในแต่ละขั้นตอนการผลิต เครื่องมือทางจีโนมเหล่านี้ทำหน้าที่เป็นจุดตรวจสอบแรก ตามด้วยการประเมินการทำงานและการปนเปื้อนอย่างละเอียด
การวิเคราะห์จีโนมและทรานสคริปโตม
การทำแผนที่โครโมโซมแบบ G-banded เป็นเครื่องมือสำคัญในการระบุปัญหาโครโมโซมหลัก เช่น ความผิดปกติทางจำนวนและการจัดเรียงโครงสร้างขนาดใหญ่ เช่น การแลกเปลี่ยนตำแหน่ง แม้ว่าจะสามารถตรวจพบระดับโมเสกประมาณ 14% แต่ความละเอียดจำกัดอยู่ที่การเปลี่ยนแปลง 5–10 เมกะเบส หมายความว่าการเปลี่ยนแปลงขนาดเล็กอาจไม่ถูกสังเกตเห็น [1].
การไฮบริไดเซชันจีโนมเปรียบเทียบแบบอาร์เรย์ (aCGH) ให้ความละเอียดสูงกว่า โดยสามารถระบุการเปลี่ยนแปลงจำนวนสำเนาลงไปถึง 1 กิโลเบส ในทำนองเดียวกัน อาร์เรย์โพลีมอร์ฟิซึมของนิวคลีโอไทด์เดี่ยว (SNP) เป็นตัวเลือกที่คุ้มค่าสำหรับการตรวจคัดกรองตามปกติ โดยสามารถตรวจจับการเปลี่ยนแปลงจำนวนสำเนา โมเสกแอนยูพลอยดี และการไม่แยกจากพ่อแม่เดียว การศึกษาการตรวจสอบความถูกต้องแสดงให้เห็นว่าอาร์เรย์ SNP มีความสามารถในการทำซ้ำได้สูง โดยการวัดความถี่อัลลีล B (BAF) บรรลุค่า r² = 0997 [8] [1].
Rocio Aguilar-Quesada จาก Andalusian Public Health System Biobank เน้นย้ำถึงคุณค่าของการผสมผสานวิธีการ:
การทำคาริโอไทป์ยังคงเป็นการทดสอบที่หลากหลาย โดยเฉพาะเมื่อเสริมด้วยการทดสอบความละเอียดสูง [1].
การทำโปรไฟล์ Short Tandem Repeat (STR) เป็นมาตรฐานสากลสำหรับการตรวจสอบเอกลักษณ์ของเซลล์ไลน์และป้องกันการปนเปื้อนข้าม [1] [9]. ในขณะเดียวกัน, การวิเคราะห์เมทิลเลชั่นของ DNA ทำหน้าที่เป็นไบโอมาร์คเกอร์สำหรับเอกลักษณ์ของเซลล์, สถานะการแยกแยะ, และการเสื่อมสภาพของเซลล์ [1]. สำหรับการตรวจจับการกลายพันธุ์ในระดับคู่เบส, การหาลำดับจีโนมหรือเอ็กโซมทั้งหมด เป็นทางเลือก, แม้ว่าจะมีค่าใช้จ่ายสูงกว่าวิธีการที่ใช้แผง [1].
ผลลัพธ์ที่ดีที่สุดมาจากการผสมผสานวิธีการเหล่านี้ เริ่มต้นด้วยการทำคาริโอไทป์เพื่อให้ได้ภาพรวมกว้าง ๆ จากนั้นใช้เครื่องมือความละเอียดสูงเช่น aCGH หรือ SNP arrays เพื่อจับการกลายพันธุ์ที่ละเอียดขึ้น การประเมินซ้ำอย่างสม่ำเสมอ - โดยเฉพาะทุก ๆ 10 passages - เป็นสิ่งสำคัญ เนื่องจากการเพาะเลี้ยงที่ยาวนานอาจนำไปสู่การเปลี่ยนแปลงทางพันธุกรรม [10]. ข้อมูลเชิงลึกทางจีโนมเหล่านี้จะถูกเสริมด้วยการทดสอบการทำงานเพื่อให้แน่ใจว่าพฤติกรรมของเซลล์คงที่ตลอดการผลิต
การทดสอบการทำงานและความปลอดภัย
การทำโปรไฟล์จีโนมเพียงอย่างเดียวไม่เพียงพอ การทดสอบการทำงานยืนยันว่าเซลล์ยังคงรักษาลักษณะที่ตั้งใจไว้ในระหว่างการขยายตัว เมตริกเช่นอัตราการเติบโตและผลผลิตสามารถบ่งชี้สัญญาณเริ่มต้นของการล่องลอยทางพันธุกรรมหรือการปนเปื้อน [9].
การหาลำดับเบสที่มีความสามารถสูง (HTS) มีความไวสูงในการตรวจหาความแปรปรวนทางพันธุกรรม ในขณะที่ การตรวจวัดปริมาณ DNA แบบดิจิทัล (dPCR) ตรวจสอบความเสถียรของยีนที่ถูกแทรกได้อย่างแม่นยำโดยไม่ต้องใช้มาตรฐานอ้างอิง [11] . Christopher Frye และ Luhong He จาก BioPharm International เน้นย้ำถึงความสำคัญของขั้นตอนนี้:
สายเซลล์ที่ใช้ในการผลิตเป็นพื้นฐานของกระบวนการชีวภาพใด ๆ ดังนั้น การวิเคราะห์ลักษณะทางพันธุกรรมที่เหมาะสมของสายเซลล์ที่ใช้ในการผลิตจึงมีความสำคัญอย่างยิ่งต่อความสำเร็จของการพัฒนากระบวนการ [6].
ความเสถียรทางอีพิเจเนติกส์ก็มีความสำคัญเช่นกัน การตกตะกอนภูมิคุ้มกันของ DNA ที่มีเมทิล (MeDIP) ช่วยระบุการปิดเสียงของยีนที่เกิดจากการเมทิลเลชั่นของ DNA ซึ่งเป็นสาเหตุทั่วไปของการลดลงของประสิทธิภาพ [7]. เครื่องมือเช่น Loop Out Detection Assay (LODA) ใช้ RT-PCR เพื่อตรวจหาการจัดเรียง DNA ใหม่ เช่น เมื่อยีนที่สนใจถูกลบออกในขณะที่เครื่องหมายที่เลือกยังคงอยู่ [7].
การทดสอบควรสอดคล้องกับขั้นตอนการผลิต: การทดสอบในระยะแรกมุ่งเน้นไปที่การโคลนและการตรวจสอบพลาสมิด การทดสอบในระยะกลางประเมินความเสี่ยงภายใต้สภาวะเชิงพาณิชย์ และการทดสอบในระยะสุดท้ายประเมินเซลล์ที่ขีดจำกัดของอายุการใช้งานในหลอดทดลอง [6]. การเริ่มต้นการทดลองด้วยเซลล์ที่สดใหม่และผ่านการเพาะเลี้ยงน้อยจากธนาคารเซลล์หลักช่วยลดความเสี่ยงของการล่องลอยทางพันธุกรรม [9].
การทดสอบความปลอดเชื้อและการปนเปื้อน
การทดสอบการปนเปื้อนเป็นสิ่งสำคัญเพื่อหลีกเลี่ยงปัจจัยที่อาจทำให้พันธุกรรมไม่เสถียร Mycoplasma เป็นเรื่องที่น่ากังวลเป็นพิเศษ เนื่องจากมันเปลี่ยนแปลงการเผาผลาญและพฤติกรรมของเซลล์โดยไม่ทำให้เกิดการเปลี่ยนแปลงที่มองเห็นได้ในวัฒนธรรม [1]. การศึกษาพบว่ามีการปนเปื้อนของไมโคพลาสมาในตัวอย่างเซลล์แบงค์ 19% โดยบางคอลเลกชันเฉพาะมีอัตราสูงถึง 31% [1].
การตรวจคัดกรองไมโคพลาสมาเป็นประจำโดยใช้เทคนิคการขยายกรดนิวคลีอิกที่มีความไว (NAT) หรือ PCR แบบเรียลไทม์สามารถให้ผลลัพธ์กึ่งเชิงปริมาณภายใน 2–3 ชั่วโมง [1]. การย้อมสีฟลูออเรสเซนต์ Hoechst 33258 เป็นอีกวิธีหนึ่งที่เผยให้เห็นรูปแบบฟลูออเรสเซนต์ภายนอกที่มีลักษณะเฉพาะ [9].
การทำโปรไฟล์ STR สร้างลายนิ้วมือ DNA สำหรับสายเซลล์ ทำหน้าที่เป็นพื้นฐานในการตรวจหาการปนเปื้อนข้าม [9]. นอกจากนี้ การทำจีโนไทป์ SNP โดยใช้การกระจายความถี่อัลลีล B (BAF) สามารถระบุการปนเปื้อนจากสายเซลล์อื่น ๆ โดยตรวจพบส่วนผสมของเซลล์ต่างประเทศในอัตรา 20–25% [8].
การสังเกตด้วยกล้องจุลทรรศน์เป็นเครื่องมือเตือนภัยล่วงหน้าที่เรียบง่ายแต่มีประสิทธิภาพ เนื่องจากลักษณะเซลล์ที่ผิดปกติมักบ่งบอกถึงปัญหาการเพาะเลี้ยง [9]. การนำระบบการจัดการคุณภาพมาใช้ เช่น ISO 9001:2015, พร้อมกับแนวปฏิบัติที่ดีในการเพาะเลี้ยงในหลอดทดลอง (GIVIMP) ช่วยรักษาสภาพการเพาะเลี้ยงที่ได้มาตรฐานและสามารถทำซ้ำได้ ลดความเสี่ยงของความไม่เสถียรทางพันธุกรรม [10].
สำหรับผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยงที่ต้องการเข้าถึงอุปกรณ์และวัสดุทดสอบเฉพาะทาง แพลตฟอร์มเช่น
sbb-itb-ffee270
กลยุทธ์การป้องกันความไม่เสถียรทางพันธุกรรม
การตรวจจับความไม่เสถียรทางพันธุกรรมเป็นเรื่องหนึ่ง การป้องกันเป็นอีกความท้าทายหนึ่งโดยสิ้นเชิงเพื่อรักษาเสถียรภาพทางพันธุกรรมให้คงอยู่ ผู้ผลิตเนื้อสัตว์เพาะเลี้ยงจำเป็นต้องมีระบบที่คิดมาอย่างดีเพื่อหยุดสายเซลล์ไม่ให้ล่องลอยก่อนที่ปัญหาจะเกิดขึ้น สองกลยุทธ์หลักที่นำทางในที่นี้คือ การจัดเก็บเซลล์อย่างมีโครงสร้าง และ การดัดแปลงพันธุกรรมที่มีเป้าหมาย. ร่วมกัน วิธีการเหล่านี้จัดการกับความเสี่ยงของการล่องลอยทางพันธุกรรมและการกระตุ้นยีนมะเร็งโดยตรง
การจัดเก็บเซลล์และการแช่แข็ง
การสะสมการกลายพันธุ์เป็นเรื่องที่น่ากังวลจริง ๆ ดังนั้นระบบการจัดเก็บเซลล์ที่เชื่อถือได้จึงเป็นสิ่งจำเป็น มาตรฐานอุตสาหกรรมเกี่ยวข้องกับระบบสองระดับ: ธนาคารเซลล์หลัก (MCB) และ ธนาคารเซลล์ทำงาน (WCB). การตั้งค่านี้ทำให้มั่นใจได้ถึงจุดเริ่มต้นที่สม่ำเสมอสำหรับการผลิต การจำกัดจำนวนการผ่านเป็นสิ่งสำคัญ เนื่องจากการผ่านแต่ละครั้งจะเพิ่มโอกาสในการกลายพันธุ์ การเก็บเซลล์ในไนโตรเจนเหลวจะหยุดกิจกรรมทางชีวภาพอย่างมีประสิทธิภาพ ลดความเสี่ยงของการเปลี่ยนแปลงทางพันธุกรรมระหว่างการจัดเก็บ
แทนที่จะติดตามเวลา อายุของเซลล์ถูกวัดโดย การเพิ่มจำนวนประชากร . ตัวอย่างเช่น เครื่องปฏิกรณ์ชีวภาพการผลิตขนาด 5,000 ลิตรทั่วไปเกี่ยวข้องกับการเพิ่มจำนวนประชากรประมาณ 30 ครั้ง[6]. เพื่อรักษาความสม่ำเสมอทางพันธุกรรม การผลิตเชิงพาณิชย์จำกัดจำนวนนี้ไว้ระหว่าง 45 ถึง 60 ครั้ง[6].
วิธีการคัดกรองเช่น RT-PCR และ single-cell qPCR สามารถจับปัญหาได้ตั้งแต่เนิ่นๆ เช่น การแยก mRNA ที่ผิดปกติหรือความแปรปรวนของทรานส์ยีน สายเซลล์ที่แสดงความแปรปรวนในจำนวนสำเนาควรถูกทิ้งเพื่อหลีกเลี่ยงปัญหาในอนาคต
การควบคุมคุณภาพเป็นสิ่งที่ไม่สามารถต่อรองได้ น่าตกใจที่การศึกษาพบว่าสายเซลล์ถึง 31% ในบางธนาคารถูกปนเปื้อนด้วยไมโคพลาสมา [3]. เพื่อป้องกันสิ่งนี้ การทำโปรไฟล์ STR ถูกใช้เพื่อยืนยันความถูกต้องของสายเซลล์ตลอดกระบวนการธนาคารตามที่เน้นโดย FSA Research and Evidence:
เนื่องจากเซลล์ที่ถูกเก็บไว้เป็นวัสดุตั้งต้นสำหรับผลิตภัณฑ์สุดท้าย มาตรฐานสูงอาจถูกกำหนดโดยหน่วยงานกำกับดูแลในอนาคตเพื่อให้มั่นใจในผลิตภัณฑ์เนื้อที่ปลอดภัยและมีคุณภาพสูง [2].
วิศวกรรมพันธุกรรมเพื่อความเสถียร
วิศวกรรมพันธุกรรมให้การป้องกันอีกชั้นหนึ่งโดยการเพิ่มความเสถียรของสายเซลล์โดยตรง เทคนิคเช่น การบูรณาการเป้าหมาย (TI), โดยเฉพาะ การแลกเปลี่ยนแคสเซ็ตต์ที่ควบคุมโดยรีคอมบิเนส (RMCE), อนุญาตให้แทรกทรานส์ยีนอย่างแม่นยำในตำแหน่งจีโนมเฉพาะ วิธีนี้หลีกเลี่ยงความไม่แน่นอนของการบูรณาการแบบสุ่ม ซึ่งผลกระทบของตำแหน่งและความไม่เสถียรของจำนวนสำเนาสามารถสร้างความเสียหายได้ แม้ว่า RMCE ในเซลล์ CHO จะมีอัตราประสิทธิภาพต่ำกว่า 0.1%[12], โคลนที่ได้จะมีความคาดเดาได้และเสถียรมากขึ้น
การเลือกระบบการแสดงออกก็มีความสำคัญเช่นกัน ตัวอย่างเช่น ระบบ Glutamine Synthetase (GS) มักจะส่งผลให้มีสำเนายีนแทรกประมาณห้าสำเนาต่อเซลล์ ในขณะที่ระบบ Dihydrofolate Reductase (DHFR) สามารถเพิ่มจำนวนสำเนาได้ถึง 1,000[6]. แม้ว่าจำนวนสำเนาที่สูงขึ้นอาจฟังดูน่าสนใจ แต่ก็เพิ่มความเป็นไปได้ของการเปลี่ยนแปลงของ DNA ทำให้ระบบที่ใช้ GS เป็นตัวเลือกที่ชาญฉลาดกว่าสำหรับความเสถียรในระยะยาว
เพื่อให้ลดความเสี่ยงลงไปอีก การกลายพันธุ์เฉพาะจุด และ การคัดกรอง NGS ก่อนการถ่ายโอน มีความสำคัญ เนื่องจากการหาลำดับ Sanger มีขีดจำกัดการตรวจจับที่สูงกว่า NGS สามารถจับการกลายพันธุ์ของพลาสมิดที่ต่ำกว่า 0.5% ได้ ทำให้การคัดกรองโคลนประสบความสำเร็จมากกว่า 90%[5].
Shuai Wang และเพื่อนร่วมงานจาก WuXi Biologics เน้นย้ำถึงความสำคัญของการเฝ้าระวังนี้:
เนื่องจากการปรับปรุงกระบวนการไม่สามารถแก้ไขการกลายพันธุ์ในระดับยีนได้ ควรตรวจสอบระดับการกลายพันธุ์ในโคลนที่เสถียรอย่างเข้มงวด[5].
สำหรับผู้ผลิตที่ต้องการเครื่องมือเฉพาะทาง - ไม่ว่าจะเป็นการแช่แข็ง การดัดแปลงพันธุกรรม หรือการวิเคราะห์สายเซลล์ -
การบูรณาการการควบคุมคุณภาพในการผลิต
การรวมการควบคุมคุณภาพในทุกขั้นตอนการผลิตเป็นสิ่งสำคัญ หากไม่มีระบบที่มีโครงสร้าง แม้แต่สายเซลล์ที่ได้รับการดูแลอย่างดีก็อาจเกิดการเปลี่ยนแปลงระหว่างการขยายและการเพิ่มขนาด การควบคุมคุณภาพไม่ควรเป็นเรื่องที่คิดภายหลัง - ต้องเป็นส่วนสำคัญของการผลิต This begins at the scale-up stage, where strict management systems and controlled environments play a key role.
การควบคุมคุณภาพในระหว่างการขยายและการเพิ่มขนาด
ตามที่ได้กล่าวถึงก่อนหน้านี้ การทดสอบจีโนมและการปนเปื้อนมีความสำคัญอย่างยิ่ง โดยเฉพาะในระหว่างการเพิ่มขนาด การย้ายจากปริมาณน้อยไปสู่หลายพันลิตรนำมาซึ่งความเสี่ยงใหม่ ๆ โดยการผ่านเซลล์แต่ละครั้งจะเพิ่มโอกาสในการกลายพันธุ์ ระบบการจัดการคุณภาพ (QMS) ช่วยจัดการความเสี่ยงเหล่านี้ได้อย่างมีประสิทธิภาพ ตัวอย่างเช่น ระหว่างปี 2017 ถึง 2022 Josep M. Canals และทีมของเขาที่มหาวิทยาลัยบาร์เซโลนาได้ดำเนินการใช้ ISO 9001:2015 QMS เพื่อมาตรฐานการเพาะเลี้ยงเซลล์ต้นกำเนิดพลูริโพเทนต์ของมนุษย์ การวิเคราะห์ย้อนหลังของข้อมูล G-banding และ aCGH ของพวกเขาเผยให้เห็นการลดลงอย่างมีนัยสำคัญของความผิดปกติของโครโมโซมเมื่อเทียบกับสภาพก่อนการปรับตัว[10][13]. Canals highlighted the importance of ongoing monitoring:
ความไม่เสถียรทางพันธุกรรมที่แสดงโดย hPSCs ในการเพาะเลี้ยงทำให้การประเมินความสมบูรณ์ของจีโนมบ่อยครั้งเป็นข้อกำหนดที่จำเป็นเมื่อวางแผนที่จะใช้พวกมันในการทดลอง[10] .
การตรวจคัดกรองจีโนมเป็นประจำเป็นสิ่งจำเป็น เทคนิคเช่น G-banding karyotyping และ aCGH ตรวจจับการเปลี่ยนแปลงโครงสร้าง ในขณะที่ Next-Generation Sequencing (NGS) ระบุการกลายพันธุ์ในระดับต่ำกว่า 0.5%[5]. การวิเคราะห์เส้นโค้งการเจริญเติบโตยังสามารถระบุปัญหาได้ตั้งแต่เนิ่นๆ เช่น การปนเปื้อนหรือการล่องลอยทางพันธุกรรม[9]. การตรวจสอบสิ่งแวดล้อมเพิ่มชั้นความปลอดภัยอีกชั้นหนึ่ง ด้วยการปฏิบัติเช่นการทดสอบแผ่นตกตะกอนและการตรวจสอบแผ่นกรอง HEPA ทุกหกเดือนเพื่อให้แน่ใจว่าสภาพแวดล้อมการผลิตยังคงเสถียรและปราศจากความเครียดสำหรับสายเซลล์[4].
ความสม่ำเสมอในสื่อและสารเคมีมีความสำคัญเท่าเทียมกัน การใช้สื่อที่ปราศจากเซรั่มและกำหนดไว้เช่น mTeSR1 ร่วมกับสารเคมีที่มีใบรับรองการวิเคราะห์ ช่วยลดความแปรปรวนระหว่างชุดและจำกัดความเสี่ยงของการปนเปื้อนของไวรัส[10][4]. การตรวจสอบลักษณะทางสัณฐานวิทยาเป็นประจำ - การสังเกตด้วยกล้องจุลทรรศน์อย่างง่ายที่ความหนาแน่นของวัฒนธรรมที่แตกต่างกัน - สามารถจับสัญญาณเริ่มต้นของการแยกแยะหรือความเครียดได้[9]. สำหรับการจัดหาอุปกรณ์หรือสารเคมีเฉพาะทาง แพลตฟอร์มเช่น
การทดสอบการทำงานเพื่อความสม่ำเสมอของผลิตภัณฑ์
ในขณะที่การตรวจสอบจีโนมปกป้องกระบวนการ การทดสอบการทำงานช่วยให้มั่นใจได้ว่าเซลล์ทำงานตามที่ตั้งใจไว้ความเสถียรทางพันธุกรรมเพียงอย่างเดียวไม่เพียงพอ; เซลล์ต้องรักษาความสามารถในการทำงานอย่างถูกต้องในแต่ละชุดการผลิตด้วย ในเนื้อสัตว์ที่เพาะเลี้ยง หมายถึงการยืนยันว่าเซลล์ต้นกำเนิด เช่น เซลล์ดาวเทียมของกล้ามเนื้อ ยังคงสามารถแยกแยะเป็นเนื้อเยื่อกล้ามเนื้อหรือไขมันที่โตเต็มที่หลังจากการขยายตัว[2]. การทดสอบการแยกแยะเป็นสิ่งจำเป็นเพื่อยืนยันสิ่งนี้
การทดสอบเมตาบอลิซึม เช่น MTT, LDH, และ Resazurin ให้ข้อมูลเชิงลึกเกี่ยวกับสุขภาพและความมีชีวิตของเซลล์[4] [9]. สิ่งเหล่านี้เมื่อรวมกับ การวิเคราะห์ Short Tandem Repeat (STR), ช่วยยืนยันว่าเซลล์ไลน์ยังคงเป็นของแท้และปราศจากการปนเปื้อนข้ามตลอดกระบวนการผลิต[1][9].
การวิเคราะห์การถอดรหัสเป็นอีกขั้นตอนที่สำคัญXiaoyue Chen และ Sam Zhang แนะนำ:
แนะนำให้ใช้การจัดลำดับ cDNA แทนการจัดลำดับ DNA ของจีโนมสำหรับการตรวจจับการกลายพันธุ์เพื่อประเมินความเสี่ยงในระดับการถอดรหัส[5].
วิธีนี้ให้ภาพที่แม่นยำยิ่งขึ้นของผลิตภัณฑ์สุดท้าย เนื่องจากสะท้อนถึงการแสดงออกของยีนมากกว่าตำแหน่งของจีโนมเท่านั้น โดยการจับคู่การคัดกรองจีโนมกับการทดสอบการทำงาน ผู้ผลิตสามารถมั่นใจได้ว่าทุกชุดเป็นไปตามมาตรฐานที่เข้มงวดสำหรับความปลอดภัย คุณภาพ และประสิทธิภาพในทุกขั้นตอนของการผลิต
บทสรุป
การรักษาเสถียรภาพทางพันธุกรรมเป็นสิ่งสำคัญสำหรับการผลิตเนื้อสัตว์ที่เพาะเลี้ยงอย่างปลอดภัยและสม่ำเสมอ Francisco J. Molina-Ruiz และเพื่อนร่วมงานของเขาจากห้องปฏิบัติการเซลล์ต้นกำเนิดและการแพทย์ฟื้นฟูเน้นถึงความเสี่ยง:
การเปลี่ยนแปลงทางพันธุกรรมใน hPSCs อาจเป็นอันตรายต่อความปลอดภัยของผลิตภัณฑ์เซลล์ที่ใช้ hPSC...แต่ยังนำไปสู่ความแตกต่างที่หลากหลายของวัสดุตั้งต้น, โปรไฟล์การแสดงออกของยีนที่เปลี่ยนแปลงและความไม่มีประสิทธิภาพของผลิตภัณฑ์เซลล์สุดท้าย [10].
ความเสี่ยงมีความสำคัญ - มีการบันทึกสายเซลล์ที่ระบุผิดพลาดมากกว่า 531 สายโดย คณะกรรมการรับรองสายเซลล์นานาชาติ [1].
การแก้ไขปัญหาเหล่านี้ต้องการกรอบการควบคุมคุณภาพที่แข็งแกร่ง ซึ่งรวมถึงการใช้วิธีการต่างๆ เช่น การทำโปรไฟล์ STR, การทำคาริโอไทป์ G-banding, aCGH, และ NGS ขั้นสูง [5], ควบคู่ไปกับระบบเช่น ISO 9001:2015 เพื่อมาตรฐานกระบวนการและลดความผิดปกติของโครโมโซม [13] .
ปัจจัยทางเศรษฐกิจก็เป็นแรงผลักดันให้ต้องมีมาตรการเหล่านี้เช่นกันการล่องลอยทางพันธุกรรมสามารถทำให้เซลล์ที่กลายพันธุ์มีความได้เปรียบในการเจริญเติบโต ซึ่งอาจทำให้ชุดการผลิตทั้งหมดเสียหายได้ [10][11]. ด้วยความสนใจที่เพิ่มขึ้นในเซลล์ต้นกำเนิดพลูริโพเทนต์ของมนุษย์ ความต้องการสำหรับสายเซลล์ที่มีเสถียรภาพจึงไม่เคยมีมาก่อน ดังที่ศาสตราจารย์ David L. Kaplan จาก มหาวิทยาลัยทัฟส์ อธิบายว่า:
สายเซลล์ที่เป็นอมตะมักถูกพิจารณาว่าเป็นข้อกำหนดสำหรับการสร้างเนื้อเยื่อที่กินได้ในปริมาณมากจากกระบวนการชีวภาพที่มีเสถียรภาพและแข็งแรง [14].
สำหรับผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยง การควบคุมคุณภาพต้องฝังอยู่ในทุกขั้นตอน - ตั้งแต่การคัดกรองพลาสมิดไปจนถึงการตรวจสอบการผลิตขนาดใหญ่ โดยการรวมการทดสอบอย่างละเอียดเข้ากับกลยุทธ์ป้องกัน ผู้ผลิตสามารถมั่นใจได้ถึงผลลัพธ์ที่สม่ำเสมอและเชื่อถือได้
คำถามที่พบบ่อย
ควรทำการทดสอบเสถียรภาพทางพันธุกรรมบ่อยแค่ไหนในระหว่างการขยายขนาด?
การทดสอบเสถียรภาพทางพันธุกรรมเป็นขั้นตอนสำคัญในระหว่างการขยายขนาดและควรดำเนินการเป็นประจำ ความถี่ของการทดสอบนี้ขึ้นอยู่กับสายเซลล์เฉพาะและกระบวนการที่เกี่ยวข้อง เพื่อลดโอกาสของการกลายพันธุ์และรักษาความเป็นสเต็มของเซลล์ ควรกำหนดขีดจำกัดการผ่านที่ได้รับข้อมูลจากการวิเคราะห์ทางพันธุกรรม
การทดสอบใดที่ดีที่สุดในการตรวจจับการกลายพันธุ์ขนาดเล็กและการเปลี่ยนแปลงของโครโมโซมขนาดใหญ่?
การทดสอบเช่น การวิเคราะห์ SNP array และ การทำ SNP genotyping ทั่วทั้งจีโนม มีประสิทธิภาพในการตรวจจับการกลายพันธุ์ขนาดเล็ก การเปลี่ยนแปลงจำนวนสำเนา และ aneuploidy วิธีการเหล่านี้มีประโยชน์อย่างยิ่งในการระบุการเปลี่ยนแปลงของโครโมโซมขนาดใหญ่ในสายเซลล์
วิธีที่ง่ายที่สุดในการป้องกันการล่องลอยทางพันธุกรรมระหว่างชุดการผลิตคืออะไร?
เพื่อให้การล่องลอยทางพันธุกรรมลดลง สิ่งสำคัญคือต้องดำเนินการวิเคราะห์ทางพันธุกรรมและการทำงานของสายเซลล์อย่างสม่ำเสมอและจำกัดจำนวนครั้งที่พวกมันผ่านการแบ่งเซลล์ ดำเนินการตามแนวทางปฏิบัติเช่นการจัดตั้งธนาคารเซลล์หลักและตรวจสอบความเสถียรทางพันธุกรรมเป็นประจำตามที่แนะนำในโปรโตคอลการควบคุมคุณภาพ มาตรการเหล่านี้เป็นกุญแจสำคัญในการรักษาความสม่ำเสมอและรับรองผลลัพธ์ที่เชื่อถือได้ในชุดการผลิตที่แตกต่างกัน











