Xác nhận môi trường nuôi cấy là bước bắt buộc đối với các công ty thịt nuôi cấy muốn được chấp thuận tại thị trường Vương quốc Anh. Quá trình này đảm bảo an toàn, chất lượng và tuân thủ các sản phẩm theo các khung quy định nghiêm ngặt như Quy định Thực phẩm Mới của Vương quốc Anh (EU 2015/2283). Đây là những điều bạn cần biết:
- Yêu Cầu Chính: Môi trường nuôi cấy phải đáp ứng các tiêu chuẩn về độc chất học, kiểm soát ô nhiễm, chất lượng dinh dưỡng và khả năng gây dị ứng.
- Quy Định Vương Quốc Anh: Cơ Quan Tiêu Chuẩn Thực Phẩm (FSA) yêu cầu tuân thủ các nguyên tắc HACCP và phân loại theo Sản phẩm có nguồn gốc động vật (POAO).
- Tiêu Chuẩn Toàn Cầu: Trong khi Vương quốc Anh và EU có các khung tương tự, Mỹ tuân theo các quy định CGMP theo Đạo luật FD&C.
- Quy Trình Xác Thực: Bao gồm kiểm tra kỹ lưỡng về thành phần, độ tinh khiết, chức năng và sự tuân thủ của nhà cung cấp, cùng với tài liệu đầy đủ.
- Các Sáng Kiến Hỗ Trợ: Hộp cát quy định trị giá 1,6 triệu bảng Anh của Vương quốc Anh, ra mắt vào năm 2025, hỗ trợ các công ty đáp ứng các tiêu chuẩn này.
Xác thực đúng cách đảm bảo an toàn, xây dựng niềm tin và phù hợp với các yêu cầu pháp lý. Bài viết đi sâu vào quy trình từng bước, bao gồm các phương pháp thử nghiệm, tiêu chuẩn nhà cung cấp và mẹo nộp hồ sơ quy định.
Tiêu Chuẩn Quy Định cho Môi Trường Tăng Trưởng
Tiêu Chuẩn và Hướng Dẫn
Môi trường tăng trưởng, một thành phần quan trọng trong sản xuất thịt nuôi cấy, phải đáp ứng các tiêu chuẩn quy định quốc tế nghiêm ngặt. Các tiêu chuẩn này khác nhau giữa các khu vực, mỗi khu vực có các yêu cầu cụ thể về thành phần, an toàn và độ tinh khiết.
Tại Vương quốc Anh, môi trường tăng trưởng được điều chỉnh theo Quy định Thực phẩm Mới (Quy định (EU) 2015/2283 đã được đồng hóa). Trước khi được phê duyệt cho thị trường, cần có một đánh giá an toàn kỹ lưỡng [1]. Cơ quan Tiêu chuẩn Thực phẩm (FSA) phân loại các sản phẩm nuôi cấy tế bào là Sản phẩm có nguồn gốc động vật (POAO) theo Quy định (EC) 853/2004. Phân loại này yêu cầu các nhà sản xuất thực hiện các hệ thống quản lý an toàn thực phẩm dựa trên các nguyên tắc Phân tích Mối nguy và Điểm kiểm soát tới hạn (HACCP) [3]. FSA cũng đang trong quá trình phát triển hướng dẫn kỹ thuật chi tiết về thành phần môi trường tăng trưởng, với các cập nhật tiếp theo dự kiến [1]. Các khung này cung cấp nền tảng cho các yêu cầu quy định cụ thể hơn.
Tại Hoa Kỳ, cách tiếp cận khác nhau.Các thành phần môi trường tăng trưởng phải đáp ứng các yêu cầu Thực hành Sản xuất Tốt Hiện hành (CGMP) được nêu trong Mục 501(a)(4)(B) của Đạo luật Thực phẩm, Dược phẩm và Mỹ phẩm Liên bang (FD&C Act) [4]. FDA phân loại các thành phần môi trường là "vật tư và thuốc thử", được quản lý bởi 21 CFR phần 210 và 211. Các thành phần này phải trải qua xác minh chất lượng để ngăn ngừa ô nhiễm [4]. Thú vị là, các thành phần tổng hợp của môi trường thịt nuôi - như axit amin, vitamin và muối - thường được phân loại là thiết bị y tế Loại I theo 21 CFR 864.2220, miễn trừ chúng khỏi yêu cầu thông báo trước khi đưa ra thị trường [6][7].
Tại Liên minh Châu Âu, khung pháp lý tương đồng chặt chẽ với Vương quốc Anh, vì nó cũng tuân theo Quy định (EU) 2015/2283.Cơ quan An toàn Thực phẩm Châu Âu (EFSA) giám sát quy trình cấp phép. Theo hướng dẫn ICH Q6B, các thành phần môi trường nuôi cấy, bao gồm kháng sinh, chất cảm ứng và các thành phần khác, được coi là tạp chất liên quan đến quy trình. Những tạp chất này phải được kiểm soát và giảm xuống mức chấp nhận được. Nếu có thể, tá dược và thuốc thử nên tuân thủ các tiêu chuẩn dược điển.
| Thẩm quyền | Quy định chính | Phân loại | Hệ thống an toàn | Giám sát truyền thông |
|---|---|---|---|---|
| Vương quốc Anh (GB) | Quy định đồng hóa (EU) 2015/2283 [1] | Sản phẩm có nguồn gốc động vật (POAO) [3] | HACCP (Quy định 852/2004) [3] | Hướng dẫn Sandbox FSA/FSS [1] |
| Liên minh Châu Âu / NI | Quy định (EU) 2015/2283 [1] | Sản phẩm có nguồn gốc động vật (POAO) [3] | HACCP (Quy định 852/2004) [3] | Quy trình phê duyệt của EFSA [1] |
| Hoa Kỳ | FD&C Act Section 501(a)(4)(B) [4] | Thuốc thú y mới / Thực phẩm [4] | CGMP (21 CFR 210/211) [4] | FDA CVM / USDA-FSIS [4] |
Yêu cầu pháp lý đối với thịt nuôi cấy
Các nhà sản xuất thịt nuôi cấy phải đảm bảo rằng mỗi lô môi trường tăng trưởng tuân thủ các tiêu chuẩn an toàn và chất lượng nghiêm ngặt.Việc xác nhận môi trường nuôi cấy là một khía cạnh quan trọng của khung pháp lý rộng hơn cho các sản phẩm này. Theo các nguyên tắc HACCP (Quy định (EC) 852/2004), môi trường nuôi cấy được xác định là một đầu vào chính và là nguồn tiềm năng gây ô nhiễm - hóa học, vi sinh hoặc các loại khác [3]. FSA nhấn mạnh mối quan ngại này:
"Các mối nguy chính trong sản xuất sản phẩm nuôi cấy tế bào liên quan đến nhận dạng dòng tế bào (và tính nhất quán), các mối nguy được đưa vào trong quá trình sản xuất (ô nhiễm vi sinh, môi trường nuôi cấy và các thành phần còn lại trong sản phẩm cuối cùng), và các chất gây dị ứng." [3]
Nếu có thay đổi trong công thức môi trường nuôi cấy, cần phải thực hiện ngay việc xem xét lại HACCP [3].Tại Vương quốc Anh, việc xác nhận phải diễn ra trước khi thực hiện để đảm bảo độ chính xác của sơ đồ luồng và hiệu quả của các biện pháp kiểm soát [3].
Tại Hoa Kỳ, FDA yêu cầu tất cả các thuốc thử và thành phần môi trường phải đáp ứng các tiêu chuẩn chất lượng nghiêm ngặt để tránh đưa vào các tác nhân có hại [4]. Các nhà cung cấp và phòng thí nghiệm hợp đồng phải tuân thủ các quy định CGMP, và bất kỳ nhà cung cấp nào không tuân thủ sẽ bị loại bỏ để ngăn chặn sản phẩm bị phân loại là "bị làm giả" [4]. FDA nhấn mạnh tầm quan trọng của điều này:
"Tất cả các loại thuốc mới cho động vật, bao gồm ACTP, phải được sản xuất theo CGMP để đảm bảo rằng các loại thuốc này đáp ứng các yêu cầu của Đạo luật Thực phẩm, Dược phẩm và Mỹ phẩm Liên bang (FD&C Act) về an toàn." [4]
Hiện tại, một số công ty tham gia vào hộp cát quy định của Vương quốc Anh - chẳng hạn như BlueNalu, Gourmey, Hoxton Farms, Mosa Meat, Roslin Technologies, Vital Meat, và Vow - đang hợp tác với FSA để tinh chỉnh các tiêu chuẩn kỹ thuật này [1]. Theo quy định của Vương quốc Anh, các doanh nghiệp có thể yêu cầu bảo vệ dữ liệu lên đến năm năm cho thông tin bảo mật được nộp trong quá trình cấp phép [1].
Các bước để Xác nhận Phương tiện Tăng trưởng
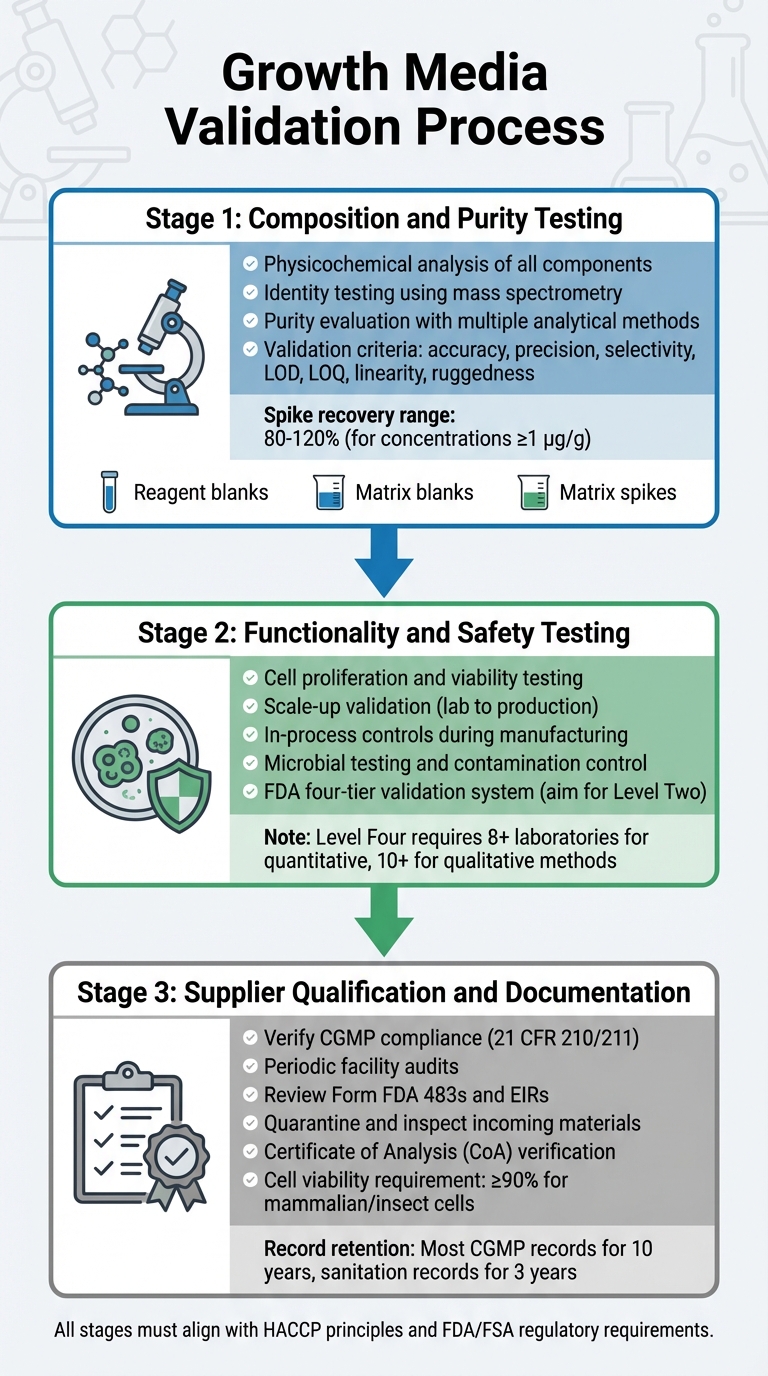
Quy trình Xác nhận Phương tiện Tăng trưởng cho Sự Chấp thuận Quy định Thịt Nuôi Cấy
Xác nhận phương tiện tăng trưởng bao gồm một quy trình chi tiết kiểm tra thành phần, chức năng, an toàn và sự tuân thủ của nhà cung cấp. Mỗi bước xây dựng dựa trên bước trước đó, đảm bảo một quy trình xác nhận mạnh mẽ phù hợp với yêu cầu quy định. Điều này bao gồm kiểm tra thành phần, chức năng và sự tuân thủ của nhà cung cấp.
Kiểm tra Thành phần và Độ tinh khiết
Giai đoạn đầu tiên tập trung vào phân tích lý hóa kỹ lưỡng của từng thành phần. Điều này bao gồm việc xác định thành phần chính xác, tính chất vật lý và cấu trúc phân tử của các thành phần như axit amin, vitamin và muối vô cơ [5].Để xác nhận cấu trúc phân tử, kiểm tra nhận dạng sử dụng các phương pháp đặc hiệu cao, bao gồm các kỹ thuật lý hóa, sinh học và miễn dịch hóa. Các công cụ như khối phổ được sử dụng để xác minh danh tính phân tử thông qua các mẫu phân mảnh của chúng [8].
Đánh giá độ tinh khiết yêu cầu nhiều phương pháp phân tích để tách các thành phần mong muốn khỏi tạp chất. Các thử nghiệm này phải giải quyết cả tạp chất liên quan đến quy trình và sản phẩm [5]. Các kỹ thuật phân tích nên đáp ứng các tiêu chí xác nhận nghiêm ngặt, bao gồm độ chính xác, độ chính xác, tính chọn lọc, giới hạn phát hiện (LOD), giới hạn định lượng (LOQ), tính tuyến tính và độ bền [8]. Các giao thức xác nhận cũng nên bao gồm:
- Mẫu trắng thuốc thử để đảm bảo thuốc thử không có chất phân tích.
- Ma trận trống để xác nhận môi trường mẫu không gây nhiễu.
- Ma trận tăng cường để ước tính độ thu hồi và độ chính xác.
Đối với các phương pháp định lượng ở nồng độ 1 µg/g (ppm), độ thu hồi tăng cường chấp nhận được thường nằm trong khoảng từ 80% đến 120% [8].
Để duy trì tính nhất quán, các nhà sản xuất nên thiết lập các tài liệu tham khảo chính nội bộ được lấy từ các lô đại diện cho sản xuất. Những tài liệu này phục vụ như các tiêu chuẩn có thể truy xuất để hiệu chuẩn các tài liệu tham khảo làm việc [5]. Khi thử nghiệm độ tinh khiết hoàn tất, môi trường phải chứng minh khả năng hỗ trợ sự phát triển tế bào hiệu quả và đáp ứng các tiêu chuẩn an toàn.
Kiểm tra chức năng và an toàn
Sau khi xác nhận thành phần, phương tiện phải chứng minh hiệu quả của nó trong việc hỗ trợ sản xuất thịt nuôi cấy. Điều này bao gồm việc chứng minh rằng các tế bào có thể sinh sôi, duy trì khả năng sống và mở rộng từ điều kiện phòng thí nghiệm đến khối lượng sản xuất. FDA yêu cầu kiểm soát trong quá trình sản xuất, bắt đầu từ các giai đoạn đầu như chuyển giao tế bào và thu hoạch, để đảm bảo tính nhất quán và an toàn của sản phẩm [4].
Xác nhận an toàn bao gồm kiểm tra vi sinh nghiêm ngặt và kiểm soát ô nhiễm, như được nêu trong các đánh giá trước thị trường của FDA [9].
FDA sử dụng hệ thống bốn cấp cho việc xác nhận phương pháp hóa học, từ Cấp Một (sử dụng khẩn cấp hoặc hạn chế) đến Cấp Bốn (nghiên cứu hợp tác đầy đủ đáp ứng tiêu chuẩn AOAC/ISO) [8].Đối với thử nghiệm quy định định kỳ, hãy nhắm đến Xác nhận đơn phòng thí nghiệm Cấp Hai, bao gồm đánh giá hiệu suất toàn diện [8]. Các nghiên cứu hợp tác đầy đủ cho các phương pháp định lượng yêu cầu sự tham gia từ ít nhất tám phòng thí nghiệm, trong khi các phương pháp định tính cần mười [8]. Khi hiệu suất của phương tiện đã được xác nhận, điều quan trọng là đảm bảo rằng tất cả nguyên liệu thô đến từ các nhà cung cấp tuân thủ.
Đánh giá và Tài liệu Nhà cung cấp
Các nhà sản xuất phải làm việc với các nhà cung cấp đã được xác minh, tuân thủ CGMP. Các nhà cung cấp nên đáp ứng các tiêu chuẩn được nêu trong 21 CFR 210/211 [4]. Việc xác minh bao gồm các cuộc kiểm tra định kỳ các cơ sở của nhà cung cấp để đánh giá sự tuân thủ các chương trình chất lượng, quy trình và tuân thủ CGMP tổng thể [4].
Trước khi ký kết hợp đồng, hãy xem xét lịch sử tuân thủ của nhà cung cấp, bao gồm các Biên bản FDA 483 và Báo cáo Kiểm tra Cơ sở (EIRs) [4]. FDA nhấn mạnh nghĩa vụ này:
"Trước khi ký kết bất kỳ hợp đồng, thỏa thuận, hoặc sắp xếp nào với một cơ sở khác để thực hiện bất kỳ bước sản xuất nào cho bạn, bạn nên xác minh rằng cơ sở đó tuân thủ các quy định CGMP áp dụng." [4]
Tất cả các nguyên liệu đầu vào phải được cách ly và kiểm tra trước khi phát hành, đảm bảo chúng đáp ứng các thông số kỹ thuật chính [10]. Các nhà cung cấp được yêu cầu cung cấp Chứng nhận Phân tích (CoA) hoặc kết quả kiểm tra tuân thủ CGMP/GLP có thể truy xuất [10].Đối với các dòng tế bào ổn định, tài liệu phải bao gồm lịch sử nhân bản có thể truy xuất [10]. Tế bào động vật có vú hoặc côn trùng thường yêu cầu ít nhất 90% khả năng sống sót để được chấp nhận trong các dự án CGMP [10]. Hồ sơ nên được lưu giữ theo hướng dẫn quy định [4].
Hợp đồng phải nêu rõ trách nhiệm CGMP và yêu cầu nhà cung cấp thông báo cho nhà sản xuất về bất kỳ thay đổi đề xuất nào đối với bộ dụng cụ thử nghiệm hoặc phương pháp luận [4]. Nếu thử nghiệm được thuê ngoài, đảm bảo rằng các phòng thí nghiệm hợp đồng sử dụng các phương pháp phân tích đã được xác nhận và đã đăng ký với FDA [4].
Chuẩn bị Tài liệu Nộp Hồ sơ Quy định
Khi môi trường tăng trưởng của bạn đã được xác nhận, bước tiếp theo là biên soạn một hồ sơ chứng minh sự tuân thủ với tất cả các tiêu chuẩn an toàn và chất lượng do FDA và USDA-FSIS yêu cầu. Hồ sơ này đóng vai trò là một liên kết quan trọng giữa xác nhận và tuân thủ quy định, cung cấp cho các cơ quan chức năng cái nhìn rõ ràng về sự an toàn và quy trình sản xuất của môi trường của bạn.
Các Yếu tố Cần Thiết của Hồ sơ Nộp
Hồ sơ của bạn nên bao gồm một phân tích chi tiết về thành phần của môi trường, liệt kê tất cả các axit amin, vitamin, muối vô cơ và các yếu tố tăng trưởng. Hướng dẫn của FDA nhấn mạnh rằng quá trình xem xét không chỉ đánh giá môi trường mà còn toàn bộ quy trình sản xuất. Điều này bao gồm việc thiết lập các dòng tế bào và ngân hàng, thực hiện các kiểm soát sản xuất, và xác minh tất cả các thành phần và đầu vào [11].
Ngoài ra, hồ sơ phải có đánh giá an toàn và độc tính kỹ lưỡng, chứng minh an toàn thực phẩm của vật liệu nuôi cấy và tất cả các đầu vào của nó. Bao gồm hồ sơ kiểm soát sản xuất, dữ liệu xác nhận quy trình và tài liệu chương trình chất lượng để chứng minh rằng sản xuất của bạn nhất quán và không có chất gây ô nhiễm.
Bạn cũng nên cung cấp hồ sơ xác minh cung ứng và thuốc thử, cho thấy sự xác nhận cho tất cả các vật liệu được sử dụng trong môi trường, bao gồm cả những vật liệu được chuẩn bị nội bộ. Đối với các sản phẩm được quy định bởi USDA-FSIS, bao gồm các kế hoạch HACCP và các giao thức vệ sinh. FDA khuyến nghị giữ lại hầu hết các hồ sơ CGMP ít nhất 10 năm, trong khi hồ sơ vệ sinh và làm sạch cơ sở nên được giữ ít nhất 3 năm [4]. Điều này phù hợp với nỗ lực đủ điều kiện của nhà cung cấp, đảm bảo tất cả các đầu vào đáp ứng yêu cầu CGMP và quy định.
Tài liệu về Tuân thủ Cơ sở
Trước khi sản xuất, chế biến hoặc lưu trữ thịt nuôi cấy để tiêu thụ cho con người, các cơ sở phải đăng ký với FDA [12]. Tài liệu của bạn nên bao gồm một kế hoạch an toàn thực phẩm toàn diện, giải quyết phân tích mối nguy (sinh học, hóa học và vật lý), các biện pháp kiểm soát phòng ngừa (như vệ sinh, quản lý dị ứng và các biện pháp chuỗi cung ứng), và các thủ tục giám sát [12].
Các mô phỏng điền môi trường cũng là một yêu cầu quan trọng. Chúng bao gồm thử nghiệm ủ và thúc đẩy tăng trưởng trong 14 ngày để xác nhận các thực hành vô trùng.Như FDA giải thích:
"Quy trình điền môi trường nên đánh giá việc lắp ráp và vận hành vô trùng của thiết bị quan trọng (vô trùng), xác nhận trình độ của các nhân viên vận hành và đánh giá kỹ thuật của họ, và chứng minh rằng các kiểm soát môi trường là đủ" [2].
Đảm bảo hồ sơ của bạn bao gồm dữ liệu xác nhận nhà cung cấp, chẳng hạn như các thử nghiệm được thực hiện trên ba lô đầu tiên của môi trường từ một nhà cung cấp để xác nhận chúng phù hợp với Chứng nhận Phân tích. Các hồ sơ quan trọng khác bao gồm nhật ký kiểm soát môi trường, lịch trình hiệu chuẩn thiết bị, và dữ liệu giám sát nhiệt độ. Đối với các quy trình được USDA điều chỉnh, chuẩn bị các kế hoạch HACCP, các quy trình vận hành tiêu chuẩn vệ sinh bằng văn bản (SSOPs), và các quy trình thu hồi [12][13].
sbb-itb-ffee270
Sử dụng Cellbase cho Mua Sắm Môi Trường Tăng Trưởng Tuân Thủ Quy Định
Nhà Cung Cấp Đã Được Xác Minh cho Thịt Nuôi Cấy
Khi bạn đã xác nhận công thức môi trường tăng trưởng của mình, bước tiếp theo là tìm nguồn cung cấp các thành phần đáp ứng tiêu chuẩn quy định. Điều này không đơn giản như đặt hàng từ các nhà cung cấp thông thường. Đối với các sản phẩm nuôi cấy tế bào, các quy định vệ sinh nghiêm ngặt được áp dụng, và mỗi thành phần của môi trường tăng trưởng phải đi kèm với tài liệu cụ thể để được phê duyệt theo quy định [3]. Đó là lúc
Các Tính Năng Mua Sắm
Nền tảng cũng cung cấp giá cả minh bạch và tính năng nhắn tin trực tiếp, cho phép các nhóm nhanh chóng yêu cầu báo giá, chứng chỉ phân tích và các tài liệu quy định khác.Bằng cách hợp nhất các chức năng mua sắm quan trọng này vào một hệ thống được thiết kế riêng cho sản xuất thịt nuôi cấy,
Kết luận
Xác nhận phương tiện tăng trưởng để được phê duyệt theo quy định không chỉ là một hộp để đánh dấu - đó là một yêu cầu pháp lý để giới thiệu các sản phẩm thịt nuôi cấy vào thị trường Vương quốc Anh. Điều này bao gồm thử nghiệm kỹ lưỡng về thành phần và độ tinh khiết, thực hiện một kế hoạch HACCP mạnh mẽ và giữ tài liệu chi tiết trong suốt quá trình.
"Thực phẩm không được đưa ra thị trường nếu không an toàn. Điều này có nghĩa là nó không gây hại cho sức khỏe hoặc không phù hợp cho tiêu thụ của con người." - Cơ quan Tiêu chuẩn Thực phẩm [3]
Cơ quan Tiêu chuẩn Thực phẩm Vương quốc Anh £1.6 triệu Regulatory Sandbox nhấn mạnh cam kết của mình trong việc hợp tác với các đối tác trong ngành để thiết lập hướng dẫn kỹ thuật rõ ràng về thành phần môi trường tăng trưởng [1]. Các công ty ưu tiên xác thực đúng cách ngay bây giờ sẽ có vị thế mạnh hơn khi các hướng dẫn này được xác định đầy đủ.
Đáp ứng các tiêu chuẩn tuân thủ không chỉ là việc đánh dấu các ô quy định - đó là việc xây dựng niềm tin của người tiêu dùng và đảm bảo an toàn sản phẩm. Kiểm tra chất lượng nghiêm ngặt là cốt lõi của cả việc phê duyệt quy định và đạt được sự chấp nhận của thị trường. Để đơn giản hóa quy trình cấp phép, hãy tập trung vào việc xây dựng các giao thức xác thực mạnh mẽ, duy trì hồ sơ chính xác và hợp tác với các nhà cung cấp đáng tin cậy. Những bước này không chỉ đơn giản hóa việc phê duyệt mà còn mở đường cho sự tin tưởng lớn hơn từ người tiêu dùng.
Câu hỏi thường gặp
Các bước chính để xác nhận phương tiện tăng trưởng cho sự chấp thuận của cơ quan quản lý là gì?
Xác nhận phương tiện tăng trưởng cho sự chấp thuận của cơ quan quản lý là chứng minh rằng công thức an toàn, đáng tin cậy và phù hợp để sản xuất thịt nuôi cấy. Đây là quy trình thường diễn ra như sau:
- Đánh giá rủi ro: Bắt đầu bằng cách xác định dòng tế bào bạn sẽ sử dụng, mục tiêu của sản phẩm và các thuộc tính chất lượng quan trọng của nó (như pH hoặc thành phần dinh dưỡng). Xác định bất kỳ mối nguy tiềm ẩn nào, chẳng hạn như ô nhiễm vi sinh vật, và đưa ra các biện pháp để kiểm soát những rủi ro này.
- Kiểm tra và thông số kỹ thuật: Đặt ra các tiêu chí chấp nhận rõ ràng cho các yếu tố như vô trùng, độ tinh khiết và hiệu lực. Sử dụng các phương pháp kiểm tra đã được thiết lập để đảm bảo các tiêu chuẩn này luôn được đáp ứng.
- Nghiên cứu xác nhận: Thực hiện xác nhận quy trình kỹ lưỡng, bao gồm việc đủ điều kiện thiết bị và thử nghiệm nhiều lô, để xác nhận rằng kết quả có thể tái tạo và nhất quán.
- Kiểm tra độ ổn định: Kiểm tra cách mà môi trường duy trì theo thời gian bằng cách đánh giá chất lượng của nó trong suốt thời hạn sử dụng dự kiến dưới điều kiện bảo quản thích hợp (thường là 2–8 °C).
- Tài liệu: Tập hợp mọi thứ lại thành một hồ sơ xác nhận toàn diện. Điều này nên bao gồm tất cả các kết quả thử nghiệm và phân tích để đáp ứng yêu cầu quy định.
Bằng cách cẩn thận giải quyết từng bước này, bạn sẽ thu thập được bằng chứng cần thiết để chứng minh rằng môi trường đáp ứng các tiêu chuẩn an toàn và chất lượng cần thiết cho sản xuất thịt nuôi cấy.
Những điểm khác biệt chính giữa quy định của Vương quốc Anh và Hoa Kỳ đối với môi trường tăng trưởng được sử dụng trong thịt nuôi cấy là gì?
Tại Vương quốc Anh, quy định về môi trường tăng trưởng cho thịt nuôi cấy thuộc Quy định Thực phẩm Mới (Quy định EU 2015/2283), đã được giữ lại trong luật pháp của Vương quốc Anh. Bất kỳ môi trường tăng trưởng nào được sử dụng trong các sản phẩm không được tiêu thụ phổ biến trước ngày 15 tháng 5 năm 1997 phải trải qua đánh giá thực phẩm mới chính thức bởi Cơ quan Tiêu chuẩn Thực phẩm (FSA). Quá trình này yêu cầu nộp tài liệu chi tiết, bao gồm thông tin về thành phần, nguồn gốc và độ tinh khiết của môi trường. Ngoài ra, cần có một đánh giá rủi ro dựa trên HACCP để chứng minh cách kiểm soát các chất gây ô nhiễm trong quá trình nuôi cấy tế bào.
Kể từ tháng 12 năm 2025, FSA đã triển khai một hộp cát Sản phẩm Nuôi cấy Tế bào. Sáng kiến này cung cấp hướng dẫn và hỗ trợ thu thập dữ liệu nhanh hơn cho các ứng dụng thực phẩm mới.Để đạt được sự phê duyệt cuối cùng, các công ty phải nộp một hồ sơ toàn diện giải quyết các vấn đề về an toàn phương tiện, tính nhất quán và xác nhận sản xuất. Chỉ sau khi được phê duyệt này, sản phẩm mới có thể được bán tại Vương quốc Anh.
Ngược lại, Hoa Kỳ không có khung thực phẩm mới cụ thể dành cho phương tiện tăng trưởng, khiến việc so sánh quy định trực tiếp trở nên khó khăn. Đối với các công ty có trụ sở tại Vương quốc Anh, việc tìm nguồn cung cấp các thành phần phương tiện đã tuân thủ các tiêu chuẩn nghiêm ngặt này có thể đơn giản hóa quy trình phê duyệt.Cách thức sandbox quy định của Vương quốc Anh hỗ trợ xác nhận phương tiện tăng trưởng?
Sandbox quy định của Vương quốc Anh cho các sản phẩm nuôi cấy cung cấp một môi trường được tổ chức tốt, nơi các công ty có thể thử nghiệm và tinh chỉnh các công thức phương tiện tăng trưởng của họ. Được giám sát bởi Cơ quan Tiêu chuẩn Thực phẩm (FSA) và Tiêu chuẩn Thực phẩm Scotland (FSS), chương trình này diễn ra trong các giai đoạn sáu tháng. Trong thời gian này, các doanh nghiệp có thể thực hiện các thử nghiệm an toàn, thực hiện đánh giá rủi ro và xem xét tài liệu trong khi nhận được phản hồi có giá trị từ các cơ quan quản lý.
Cách tiếp cận thực hành này cho phép thử nghiệm thực tế và cải tiến từng bước, đẩy nhanh việc thu thập dữ liệu an toàn và giúp các công ty tuân thủ các yêu cầu quy định. Đối với những người làm việc về thịt nuôi cấy, việc tìm nguồn cung cấp phương tiện tăng trưởng đã được phê duyệt trước thông qua











