Các sửa đổi histone là những thay đổi hóa học đối với protein ảnh hưởng đến hoạt động của gen mà không làm thay đổi DNA. Những sửa đổi này rất quan trọng cho việc phát triển các dòng tế bào được sử dụng trong sản xuất thịt nuôi cấy, giúp tế bào phát triển, duy trì bản sắc của chúng và phân hóa thành mô cơ. Bài viết khám phá cách các dấu hiệu histone cụ thể như H3K4me3 (kích hoạt gen), H3K27ac (hoạt động tăng cường), và H3K27me3 (ức chế gen) điều chỉnh hành vi của tế bào.
Các điểm chính được đề cập:
- H3K4me3 hỗ trợ các gen hoạt động và phân hóa nhanh chóng.
- H3K27ac kiểm soát các yếu tố tăng cường cho biểu hiện gen trong các giai đoạn phát triển.
- H3K27me3 đảm bảo các chương trình gen không mong muốn vẫn không hoạt động.
- Trạng thái chromatin, được hình thành bởi các dấu hiệu này, khác nhau giữa các loài và loại tế bào, ảnh hưởng đến chất lượng sản xuất.
Bài báo cũng nêu bật nghiên cứu gần đây, bao gồm cách biểu hiện gen vị trí trong tế bào lợn ảnh hưởng đến chất lượng thịt và cách chỉnh sửa epigenetic có mục tiêu có thể cải thiện hiệu suất dòng tế bào. Hướng đi trong tương lai bao gồm tinh chỉnh công cụ epigenetic và nghiên cứu trạng thái chromatin để tối ưu hóa hiệu quả sản xuất và quy mô.
Giải thích về Sửa đổi Histone | Acetyl hóa, Methyl hóa & Điều chỉnh Gen
sbb-itb-ffee270
Các loại Sửa đổi Histone và Chức năng của chúng
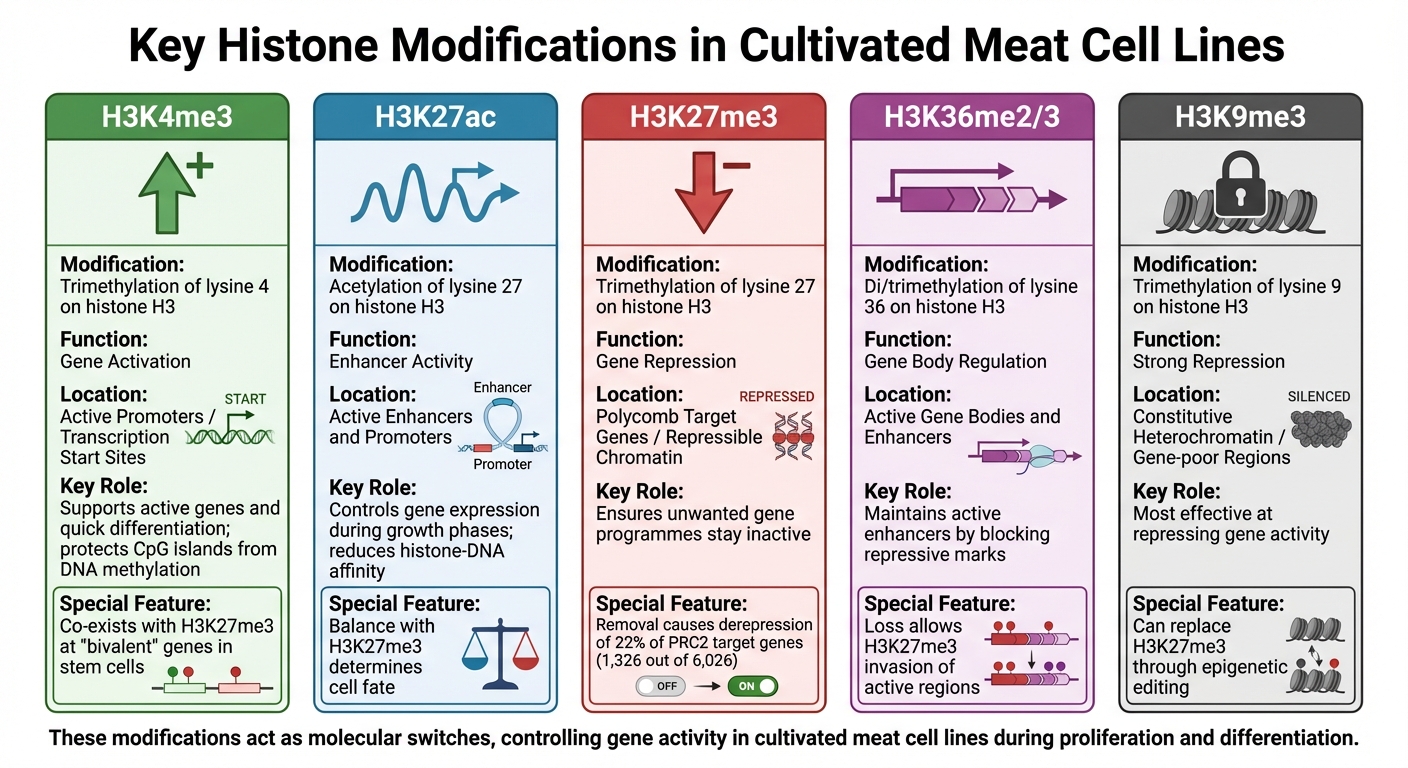
Các Sửa đổi Histone Chính trong Dòng Tế bào Thịt Nuôi: Chức năng và Bối cảnh Genomic
Sửa đổi histone đóng vai trò quan trọng trong việc điều chỉnh hoạt động của gen, hoạt động như các công tắc phân tử để kiểm soát liệu các gen có được bật hay tắt trong các dòng tế bào thịt nuôi.Các thẻ hóa học này - chủ yếu là methyl hóa và acetyl hóa - gắn vào các dư lượng cụ thể trên histone, tạo ra các mẫu gen đặc biệt. Mỗi sự sửa đổi có một chức năng cụ thể, và bằng cách hiểu những vai trò này, các nhà nghiên cứu có thể dự đoán và ảnh hưởng tốt hơn đến hành vi của tế bào trong quá trình sản xuất. Kiến thức này là cần thiết để tối ưu hóa các quy trình trong quy trình sinh học thịt nuôi cấy.
Dưới đây là phân tích các sửa đổi histone chính ảnh hưởng đến điều hòa gen trong các dòng tế bào thịt nuôi cấy.
H3K4me3 và Kích hoạt Gen
H3K4me3 (trimethyl hóa lysine 4 trên histone H3) liên quan đến các promoter gen hoạt động và tạo điều kiện cho phiên mã tại các vị trí bắt đầu của gen, đặc biệt là đối với các gen liên quan đến sự phát triển và trao đổi chất của tế bào. Sự sửa đổi này cũng bảo vệ các promoter đảo CpG khỏi sự methyl hóa DNA mới, đảm bảo các gen thiết yếu luôn có thể truy cập để phiên mã [4].
Trong dòng tế bào sơ cấp hoặc bất tử hóa được sử dụng cho thịt nuôi cấy, H3K4me3 thường tồn tại cùng với các dấu hiệu ức chế như H3K27me3 tại các gen "hai trạng thái". Những gen này vẫn sẵn sàng để kích hoạt, cho phép phân hóa nhanh chóng thành mô cơ khi cần thiết [4].
Thú vị là, H3K4me3 tương tác với các sửa đổi khác. Ví dụ, sự lắng đọng của H3K36me3 có thể ức chế các methyltransferase H3K4, giảm mức độ H3K4me3 tại các promoter và thay đổi các mẫu biểu hiện gen [4].
H3K27ac và Hoạt động của Enhancer
H3K27ac (acetyl hóa lysine 27 trên histone H3) là một dấu hiệu của các enhancer và promoter hoạt động. Bằng cách giảm ái lực giữa histone và DNA, H3K27ac tạo ra một môi trường thúc đẩy phiên mã [5]. Trong các dòng tế bào thịt nuôi cấy, sự thay đổi mức độ H3K27ac trong các giai đoạn phát triển khác nhau quyết định những gen nào được biểu hiện khi tế bào chuyển từ giai đoạn tăng sinh sang phân hóa.
Sự cân bằng giữa H3K27ac và các sửa đổi ức chế như H3K27me3 là chìa khóa để xác định số phận của tế bào. Ví dụ, sự mất H3K36me2, hỗ trợ hoạt động của enhancer, có thể cho phép H3K27me3 xâm nhập vào các vùng trước đây hoạt động, giảm mức độ H3K27ac và làm im lặng các gen mục tiêu [5].
H3K27me3 và Sự Ức Chế Gen
H3K27me3 (trimethyl hóa lysine 27 trên histone H3) là một dấu hiệu ức chế thúc đẩy cấu trúc chromatin đóng, hiệu quả làm im lặng các gen. Sự sửa đổi này, được xúc tác bởi Polycomb Repressive Complex 2 (PRC2), rất quan trọng để duy trì sự ức chế của hàng ngàn gen phát triển [4].
Trong các dòng tế bào thịt nuôi cấy, H3K27me3 đảm bảo rằng các chương trình gen không mong muốn vẫn không hoạt động trong các giai đoạn phát triển cụ thể, bảo tồn danh tính dự định của tế bào.
"H3K27me3, cùng với H2AK119ub1, là cần thiết để duy trì sự ức chế phiên mã của hàng nghìn gen mục tiêu Polycomb." - Nature Communications [4]
Nghiên cứu đã chỉ ra rằng việc loại bỏ H3K27me3 trong các tế bào gốc phôi chuột dẫn đến việc giải ức chế khoảng 22% (1,326 trong số 6,026) gen mục tiêu PRC2 [4]. Đối với thịt nuôi cấy, kiểm soát sự biến đổi này có thể giúp ngăn chặn các số phận tế bào thay thế, chẳng hạn như hình thành mô mỡ hoặc mô liên kết, trong khi tập trung vào phát triển cơ bắp.
| Sửa đổi Histone | Chức năng Điều tiết | Bối cảnh Genomic |
|---|---|---|
| H3K4me3 | Kích hoạt Gen | Promoter Hoạt động / Vị trí Bắt đầu Phiên mã |
| H3K27ac | Hoạt động Tăng cường | Tăng cường và Promoter Hoạt động |
| H3K27me3 | Đàn áp Gen | Gen Mục tiêu Polycomb / Chromatin có thể Đàn áp |
| H3K36me2/3 | Điều tiết Thân Gen | Thân Gen Hoạt động và Tăng cường |
| H3K9me3 | Đàn áp Mạnh mẽ | Heterochromatin Liên tục / Khu vực Nghèo Gen |
Trạng thái Chromatin trong Dòng Tế bào Thịt Nuôi Cấy
Các sửa đổi histone không hoạt động một mình - chúng kết hợp để tạo thành trạng thái chromatin, là những môi trường gen độc đáo kiểm soát khả năng tiếp cận gen.Các trạng thái này đóng vai trò quan trọng trong việc định hình hành vi của các dòng tế bào thịt nuôi cấy trong cả quá trình mở rộng và phân hóa, làm cho chúng trở thành yếu tố then chốt để tối ưu hóa quy trình sinh học.
Xác định Trạng thái Chromatin Thông qua Dấu Ấn Histone
Các nhà nghiên cứu lập bản đồ trạng thái chromatin bằng cách nghiên cứu các tổ hợp dấu ấn histone như H3K4me3, H3K27ac, và H3K27me3. Ví dụ, trong các tế bào nguyên bào sợi bào thai lợn (PFF) và tế bào ngoại bì nuôi dưỡng (PTr2), 10 trạng thái chromatin khác nhau đã được xác định, bao gồm các vị trí bắt đầu phiên mã hoạt động, các promoter lưỡng tính, và các enhancer giả định [6] . Các trạng thái này giúp dự đoán hoạt động của gen.
Các trạng thái enhancer, được đánh dấu chủ yếu bởi H3K27ac trong các vùng liên gen và nội gen, thường được làm giàu đồng thời với protein tái cấu trúc chromatin BRG1 [6].
Một đặc điểm đáng chú ý là sự hiện diện của các miền H3K4me3 rộng, bao phủ các vùng từ 4 kb trở lên. Các miền này chỉ chiếm 1,7% đến 1,8% của tất cả các vị trí bắt đầu phiên mã dự đoán trong dòng tế bào lợn nhưng rất quan trọng trong việc đánh dấu các gen phát triển và đặc hiệu mô [6]. Thú vị là, trong nguyên bào sợi bào thai lợn, 52% gen được đánh dấu bởi các miền rộng này là đặc hiệu mô, so với chỉ 25% trong tế bào PTr2 [6].
"Những phát hiện này nâng cao hiểu biết của chúng ta về cảnh quan biểu sinh hiện diện trong sự phát triển sớm của lợn và cung cấp cái nhìn sâu sắc về cách các biến đổi trong trạng thái chromatin liên kết với danh tính tế bào." - BMC Epigenetics & Chromatin [6]
Các hồ sơ trạng thái chromatin không chỉ khác nhau trong một loài mà còn thay đổi giữa các dòng tế bào động vật khác nhau được sử dụng trong sản xuất thịt nuôi cấy.
Sự khác biệt về Chromatin giữa các dòng tế bào động vật
Mẫu trạng thái chromatin thay đổi đáng kể tùy thuộc vào loài và loại tế bào được sử dụng trong sản xuất thịt nuôi cấy. Ví dụ, trong các dòng tế bào gà, H3K4me3 chiếm 30% đến 55% sự hiện diện trong bộ gen tại các promoter gene [7]. Tuy nhiên, trong các tế bào mầm nguyên thủy của gà (PGCs), mức độ H3K4me3 giảm đáng kể so với các tế bào đa năng. Sự giảm này hỗ trợ sự chuyển đổi của các trạng thái bivalent thành các trạng thái ức chế trong quá trình xác định dòng mầm [7].
Tế bào trophectoderm lợn (PTr2) cho thấy mức độ H3K27ac cao hơn trong các vùng promoter (57,36%) so với nguyên bào sợi thai (41,58%), trong khi sự làm giàu H3K27me3 thấp hơn ở tế bào PTr2 (7,77%) so với tế bào PFF (22%) [6]. Những biến thể này phản ánh nhu cầu epigenetic khác biệt của mỗi giai đoạn phát triển và ảnh hưởng đến cách các tế bào này phản ứng với điều kiện nuôi cấy.
Trong tế bào vệ tinh bò, phân hóa thành số phận "tế bào dự trữ" (Pax7+/Ki-67-) được điều khiển bởi trạng thái chromatin yên tĩnh được điều chỉnh bởi tín hiệu NOTCH và MAPK/ERK. Tuy nhiên, quá trình này làm giảm sản lượng protein [3]. Sự biến đổi như vậy nhấn mạnh cách trạng thái chromatin ảnh hưởng trực tiếp đến hiệu quả sản xuất. Hiểu sâu hơn về những khác biệt này là rất quan trọng để điều chỉnh hiệu suất dòng tế bào trong sản xuất thịt nuôi cấy.
Sử dụng Sửa Đổi Histone để Cải Thiện Dòng Tế Bào
Dựa trên những gì chúng ta biết về trạng thái chromatin, hãy đi sâu vào cách các sửa đổi histone có mục tiêu có thể cải thiện trực tiếp hiệu suất của các dòng tế bào thịt nuôi cấy.
Tăng Cường Sự Sinh Sôi và Thích Ứng với Sự Phát Triển Treo
Điều chỉnh các dấu histone có thể tăng đáng kể sự sinh sôi của tế bào và giúp tế bào chuyển từ phát triển bám dính sang phát triển treo. Sự chuyển đổi này rất quan trọng cho hệ thống bioreactor cho thịt nuôi cấy. Ví dụ, giảm methyl hóa H3K36 làm cho nguyên bào sợi ít phản ứng với TGFβ hơn, dẫn đến trạng thái tế bào linh hoạt hơn [1].
Vào tháng 12 năm 2022, các nhà nghiên cứu tại Believer Meats đã đạt được một bước đột phá với nguyên bào sợi gà (HUN-CF-2 và HUN-CF-4).Họ đã chứng minh sự bất tử tự phát trong các nền văn hóa huyền phù không có huyết thanh, đạt tới 100 triệu tế bào mỗi ml (10⁸ tế bào/ml) và đạt được năng suất 36% w/v. Nhóm nghiên cứu, do Yaakov Nahmias dẫn đầu, đã sử dụng lecithin - một phân tử nhỏ an toàn thực phẩm - để kích hoạt con đường PPARγ và thúc đẩy sự hình thành chất béo mà không cần dựa vào biến đổi gen. Nguyên mẫu gà nuôi cấy của họ đã đạt được đánh giá cảm quan là 4.5 trên 5.0 [2].
"Sự bất tử mà không cần biến đổi gen và sản xuất năng suất cao là rất quan trọng cho việc hiện thực hóa thị trường của thịt nuôi cấy." - Yaakov Nahmias, Giám đốc Khoa học, Believer Meats [2]
Những phát hiện này nhấn mạnh tiềm năng của các công cụ biểu sinh chính xác để tinh chỉnh hơn nữa sự phát triển của dòng tế bào.
Độ chính xác trong Chỉnh sửa Biểu sinh
Để bổ sung cho những thay đổi tế bào này, các phương pháp chỉnh sửa biểu sinh chính xác cho phép thao tác có mục tiêu đối với các dấu histone. Một nghiên cứu năm 2025 trên tế bào gốc phôi chuột cho thấy rằng một chất tuyển dụng lai (S12N) kết hợp với các miền xúc tác từ SUV39H2 hoặc SETD2 có thể thay thế H3K27me3 bằng H3K9me3 hoặc H3K36me3 tại hàng ngàn gen. Trong số này, H3K9me3 tỏ ra hiệu quả hơn trong việc ức chế hoạt động gen [8].
Tuy nhiên, sự thành công của những sửa đổi này phụ thuộc nhiều vào môi trường chromatin hiện có. Ví dụ, H3K4me3 còn sót lại tại các promoter gen có thể chặn máy móc methyl hóa DNA, làm cho việc đạt được sự im lặng gen mong muốn trở nên khó khăn hơn [8]. Điều này cho thấy rằng tối ưu hóa hiệu suất tế bào thường đòi hỏi điều chỉnh nhiều dấu histone cùng một lúc thay vì tập trung vào một sửa đổi duy nhất.
Kết luận và Hướng đi Tương lai
Những Điểm Chính
Biến đổi histone đóng vai trò quan trọng như công tắc phân tử, kiểm soát hoạt động gen trong các dòng tế bào thịt nuôi cấy. Cụ thể, H3K36me2 và H3K36me3 giúp duy trì các enhancer hoạt động bằng cách ngăn chặn các dấu ức chế như H3K27me2/3 xâm nhập vào thân gen [9][10]. Khi methyl hóa H3K36 bị mất, cấu trúc chromatin bị gián đoạn, cho phép các dấu ức chế như H3K9me3 xâm nhập vào các vùng hoạt động [9].
"Methyl hóa H3K36 [là] một điều chỉnh quan trọng của trạng thái chromatin và cấu trúc gen." - Nature Communications [9]
Tương tác giữa các dấu histone là cần thiết để cải thiện hiệu suất dòng tế bào.Nghiên cứu cho thấy rằng nhắm mục tiêu nhiều sửa đổi histone cùng lúc thường đạt được kết quả tốt hơn so với chỉ tập trung vào một [4].
Với những phát hiện này, các nghiên cứu trong tương lai phải tận dụng các công cụ epigenetic chính xác để đảm bảo cải tiến liên tục trong hiệu suất dòng tế bào thịt nuôi cấy.
Cơ hội Nghiên cứu Tương lai
Nâng cao hiệu suất dòng tế bào đòi hỏi các phương pháp tiếp cận sáng tạo, chẳng hạn như giải trình tự RNA đơn nhân, để lập bản đồ cảnh quan epigenetic trong các tiểu quần thể tế bào khác nhau. Điều này đặc biệt quan trọng để xác định và hiểu các "tế bào dự trữ" yên tĩnh chống lại sự phân hóa. Những tế bào này, biểu hiện các dấu hiệu như PAX7 và NOTCH2 thay vì cam kết hợp nhất myogenic, đặt ra một thách thức đáng kể trong sản xuất thịt nuôi cấy [3].
Một hướng đi đầy hứa hẹn khác liên quan đến việc phát triển các phức hợp epigenetic chimeric để kiểm soát chính xác, không di truyền. Ví dụ, vào năm 2025, các nhà nghiên cứu đã chứng minh rằng việc kết hợp N-terminal của SUZ12 với các miền xúc tác từ SUV39H2 hoặc SETD2 có thể thay thế hiệu quả H3K27me3 bằng H3K9me3 hoặc H3K36me3 tại nhiều gen [4]. Thêm vào đó, việc giám sát H3K36me2 tại các enhancer có thể hoạt động như một dấu hiệu kiểm soát chất lượng để đảm bảo sự ổn định của dòng tế bào [9].
Các nỗ lực trong tương lai nên tập trung vào việc duy trì methyl hóa H3K36 qua các thế hệ tế bào. Điều này sẽ giúp ngăn chặn sự trôi dạt epigenetic, cho phép các nhà nghiên cứu và các công ty như
Câu hỏi thường gặp
Các dấu hiệu histone ảnh hưởng như thế nào đến sự phân hóa cơ trong các dòng tế bào thịt nuôi cấy?
Các dấu hiệu histone là những yếu tố quan trọng trong sự phân hóa cơ, đặc biệt đối với các dòng tế bào thịt nuôi cấy. Ví dụ, sự giảm H3K27me3 trong quá trình phân hóa kích hoạt các chương trình phiên mã myogenic, cho phép kích hoạt các gen cần thiết cho sự phát triển cơ. Việc điều chỉnh tinh tế các sửa đổi histone như H3K27me3 hỗ trợ quá trình chuyển đổi của các dòng tế bào từ sự sinh sôi đến việc hình thành mô cơ với các đặc điểm cụ thể. Những điều chỉnh biểu sinh này là cần thiết để thúc đẩy sản xuất thịt nuôi cấy.
Những sửa đổi histone nào dự đoán tốt nhất sự tăng trưởng tế bào ổn định, năng suất cao trong các bioreactor?
Methyl hóa H3K36 nổi bật như một dấu hiệu đáng tin cậy cho sự tăng trưởng tế bào ổn định, năng suất cao trong các bioreactor.Sự sửa đổi này đóng vai trò quan trọng trong việc bảo tồn danh tính tế bào và quản lý các chương trình dòng dõi - cả hai đều cần thiết để đảm bảo sự phát triển tế bào nhất quán, đặc biệt là trong sản xuất thịt nuôi cấy.
Chỉnh sửa biểu sinh có thể cải thiện các dòng tế bào mà không thay đổi trình tự DNA của chúng không?
Chỉnh sửa biểu sinh cung cấp một cách để cải thiện các dòng tế bào mà không thay đổi trình tự DNA của chúng. Bằng cách điều chỉnh các dấu histone và cấu trúc chromatin, nó kiểm soát sự biểu hiện gen. Nghiên cứu về các sửa đổi histone làm nổi bật cách những thay đổi này có thể ảnh hưởng đến danh tính và chức năng của tế bào. Cách tiếp cận này đặc biệt hứa hẹn trong việc tinh chỉnh các dòng tế bào thịt nuôi cấy.











