يوفر التحليل الطيفي طريقة سريعة ودقيقة لمراقبة وسائط النمو في إنتاج اللحوم المزروعة. من خلال تتبع العناصر الغذائية مثل الجلوكوز والجلوتامين في الوقت الفعلي، يساعد في تحسين نمو الخلايا والحفاظ على الجودة. تبرز طريقتان رئيسيتان:
- التحليل الطيفي بالأشعة تحت الحمراء القريبة: يعمل في نطاق 780-2500 نانومتر، وهو مثالي لتتبع العناصر الغذائية والمواد الأيضية مثل الجلوكوز واللاكتات. إنه فعال من حيث التكلفة ويتكامل بسهولة مع المفاعلات الحيوية ولكنه قد يواجه تداخلًا من إشارات الماء.
- التحليل الطيفي رامان: يستخدم تشتت الضوء غير المرن لتوفير بيانات جزيئية محددة للغاية. يعمل بشكل جيد في البيئات التي يهيمن عليها الماء، مما يوفر دقة للمواد الأيضية مثل اللاكتات والجلوكوز ولكنه يأتي بتكاليف أعلى.
تدعم كلتا الطريقتين الأنظمة الآلية لتوصيل العناصر الغذائية واكتشاف التلوث، مما يحسن الكفاءة ويقلل من مخاطر أخذ العينات اليدوية.منصات مثل
تحليل وسط النمو باستخدام التحليل الطيفي بالأشعة تحت الحمراء القريبة
كيف يعمل التحليل الطيفي بالأشعة تحت الحمراء القريبة
يعمل التحليل الطيفي بالأشعة تحت الحمراء القريبة (NIR) ضمن نطاق الطول الموجي من 780 نانومتر إلى 2,500 نانومتر، مع التركيز على اكتشاف الأوتار وأشرطة التركيب للذبذبات الجزيئية الأساسية [7]. وهذا يجعله فعالاً بشكل خاص في تحديد الروابط مثل C-H, O-H, و N-H، والتي توجد عادة في جزيئات مثل الجلوكوز، الأحماض الأمينية، والبروتينات.
تشمل العملية تسليط ضوء NIR عبر وسط النمو وقياس كمية الضوء الممتصة عند أطوال موجية مختلفة. كل جزيء ينتج نمط طيفي فريد، أو "بصمة"، يوفر رؤى حول تكوين الوسط.ومع ذلك، نظرًا لأن نطاقات الطيف غالبًا ما تتداخل، فإن تقنيات الكيمياء المتقدمة مثل الانحدار الجزئي للمربعات الصغرى مطلوبة لاستخراج بيانات كمية دقيقة [1].
واحدة من الفوائد البارزة لتحليل الطيف بالأشعة تحت الحمراء القريبة (NIR) هي أنه غير جراحي. يمكن دمج المجسات مباشرة في المفاعلات الحيوية باستخدام منافذ إنغولد القياسية، وهي مصممة لتحمل دورات التعقيم (SIP/CIP)، مما يضمن توافقها مع معايير النظافة الصناعية [10]. هذه القدرة على القياس دون تعطيل العملية تجعل NIR أداة قيمة لمراقبة وسائط النمو.
تطبيقات NIR في مراقبة وسائط النمو
يستخدم تحليل الطيف بالأشعة تحت الحمراء القريبة (NIR) على نطاق واسع لتتبع العناصر الغذائية والمواد الأيضية الحرجة، مثل الجلوكوز، الجلوتامين، الأحماض الأمينية، اللاكتات، الأمونيا، وإجمالي عدد الخلايا (TCC) [6][8].من خلال توفير البيانات في الوقت الفعلي، يساعد المنتجين على اكتشاف استنفاد المغذيات مبكرًا، مما يمنع التأثيرات على حيوية الخلايا، أو تحديد المنتجات الثانوية السامة قبل تراكمها.
أظهرت الدراسات الفوائد العملية لـ NIR. على سبيل المثال، استخدمت إحدى التحقيقات NIR للمراقبة عبر الإنترنت في مفاعل حيوي بخزان محرك، محققة أخطاء تنبؤ 1.54 mM للجلوكوز و0.83 mM لللاكتيت [8]. بالنسبة لعمليات اللحوم المزروعة، حيث تنمو الخلايا على ناقلات دقيقة، فإن المعايرة الخاصة بالنظام ضرورية بسبب تأثيرات تشتت الضوء الناتجة عن الخرز. نجح البحث في سانوفي باستور في تطبيق NIR لمراقبة خلايا Vero المزروعة على ناقلات دقيقة Cytodex 1، محققة دقة تنبؤ 0.36 g/l للجلوكوز و0.29 g/l لللاكتيت [9]. تبرز هذه النتائج أهمية المعايرة المخصصة للأنظمة المختلفة.
"تعد تقنية التحليل الطيفي بالأشعة تحت الحمراء القريبة (NIRS) أداة واعدة بديلة في الموقع لتحليل العمليات (PAT)... حيث توفر طيفًا يمثل 'التوقيع' لجميع المكونات الموجودة في المحلول المحلل."
- آني مارك، كيمياء العمليات الحيوية [9]
استخدام آخر متزايد لتقنية NIR هو في إنشاء ملفات تعريف "الدفعة الذهبية" - وهي معايير تمثل الأداء الأمثل للعملية. يمكن للمشغلين مقارنة العمليات الحالية مع هذه الملفات في الوقت الفعلي. على سبيل المثال، استخدم الباحثون في جامعة ليبنيز هانوفر تقنية NIR لمراقبة زراعة خلايا CHO-K01 في مفاعل حيوي بسعة 7.5 لتر. اكتشف نظامهم تلوثًا بكتيريًا في "الدفعة 3" بعد 30 ساعة فقط من بدء العملية، حيث تجاوزت قراءات NIR الحدود المحددة للعملية [4].
أساسيات التحليل الطيفي بالأشعة تحت الحمراء القريبة – كيف يعمل التحليل الطيفي بالأشعة تحت الحمراء القريبة؟
التحليل الطيفي رامان لتحليل وسائط النمو
بينما يعتبر التحليل الطيفي بالأشعة تحت الحمراء القريبة رائعًا لفك تشفير نطاقات الامتصاص المتداخلة، يتخذ التحليل الطيفي رامان مسارًا مختلفًا. فهو يستخدم تشتت الضوء غير المرن للتعمق في البنية الجزيئية، مما يوفر طريقة تحليل مكملة.
كيف يعمل التحليل الطيفي رامان
يعمل التحليل الطيفي رامان عن طريق تسليط ليزر بطول موجي 785 نانومتر على عينة والتقاط الفوتونات التي تتشتت بشكل غير مرن. عندما تتفاعل هذه الفوتونات مع الجزيئات، تحدث تحولات في الطاقة بسبب الحركات الاهتزازية. تخلق هذه التحولات "بصمة" طيفية فريدة، تكشف عن البنية الجزيئية لمكونات مثل البروتينات والدهون والأحماض النووية والسكريات [12][5].
يكمن الاختلاف الرئيسي عن التحليل الطيفي بالأشعة تحت الحمراء القريبة في ما يقيسه رامان.بدلاً من اكتشاف تغييرات في لحظة ثنائية القطب، يركز رامان على تغييرات في الاستقطابية للروابط الجزيئية أثناء الاهتزاز [5]. هذا الاختلاف يجعله مفيدًا بشكل خاص لتطبيقات اللحوم المزروعة. لماذا؟ لأن الماء، الذي يهيمن على وسائط النمو، يكاد يكون غير مرئي لاكتشاف رامان. هذا يعني أن رامان يمكنه "الرؤية من خلال" الماء لاكتشاف كميات صغيرة من المغذيات والمواد الأيضية، متجنبًا التداخل الذي غالبًا ما يعقد الطرق تحت الحمراء [11][12][5].
تولّد مطيافية رامان إشارات خاصة بالمحلل لا تتداخل مع إشارات الماء... مما يجعلها مفيدة بشكل خاص للتطبيقات في زراعة الخلايا، حيث تكون المصفوفة مائية في الغالب.
ومع ذلك، نظرًا لأن نطاقات الطيف يمكن أن تتداخل، تُستخدم النماذج الرياضية المتقدمة مثل الانحدار الجزئي للمربعات أو تحليل المكونات الرئيسية لاستخراج بيانات كمية دقيقة من الأطياف الحادة والمحددة [12][13][14].
تطبيقات رامان في مراقبة وسائط النمو
بفضل قدرتها على إنتاج بصمات جزيئية مفصلة، أصبحت مطيافية رامان أداة قوية للمراقبة في الوقت الفعلي في بيئات الإنتاج. تعمل كجهاز استشعار بصري، حيث تتبع استهلاك المغذيات - مثل الجلوكوز والجلوتامين - وإنتاج المنتجات الأيضية الثانوية، مثل اللاكتات والأمونيا [14]. يتيح هذا التغذية الراجعة في الوقت الفعلي إجراء تعديلات تلقائية، مثل تحسين جداول تغذية المغذيات لتحسين الكفاءة.
على سبيل المثال، في أبريل 2025، استخدم الباحثون جهاز Viserion مطياف رامان في خمسة مزارع خلايا CHO بسعة 10 لترات، وحققوا تنبؤات دقيقة للغاية (e.g، RMSEP بقيمة 0.51 جم/لتر للجلوكوز) [12]. وبالمثل، في مارس 2018، استخدم فريق في Cell and Gene Therapy Catapult في لندن نظام رامان مدمج (محلل Kaiser Optical Systems RamanRxn2™) لمراقبة إنتاج الخلايا التائية الذاتية. قاموا بتتبع مستويات الجلوكوز (R = 0.987) واللاكتات (R = 0.986) بدقة، مما سمح بتحديد التغيرات الأيضية الخاصة بالمتبرع ومعدلات التكاثر دون الحاجة إلى أخذ عينات يدوية [14] .
إلى جانب العناصر الغذائية والمنتجات الثانوية، يراقب التحليل الطيفي رامان أيضًا تركيز الخلايا، ويقيم حيوية الخلايا، ويكتشف المخاطر المحتملة مثل السالمونيلا أو الإشريكية القولونية. يضمن ذلك التناسق عبر الدفعات ويوفر طريقة موثوقة لتوصيف مكونات الوسائط [11][1][14][15].
NIR مقابل رامان: أي طريقة يجب استخدامها
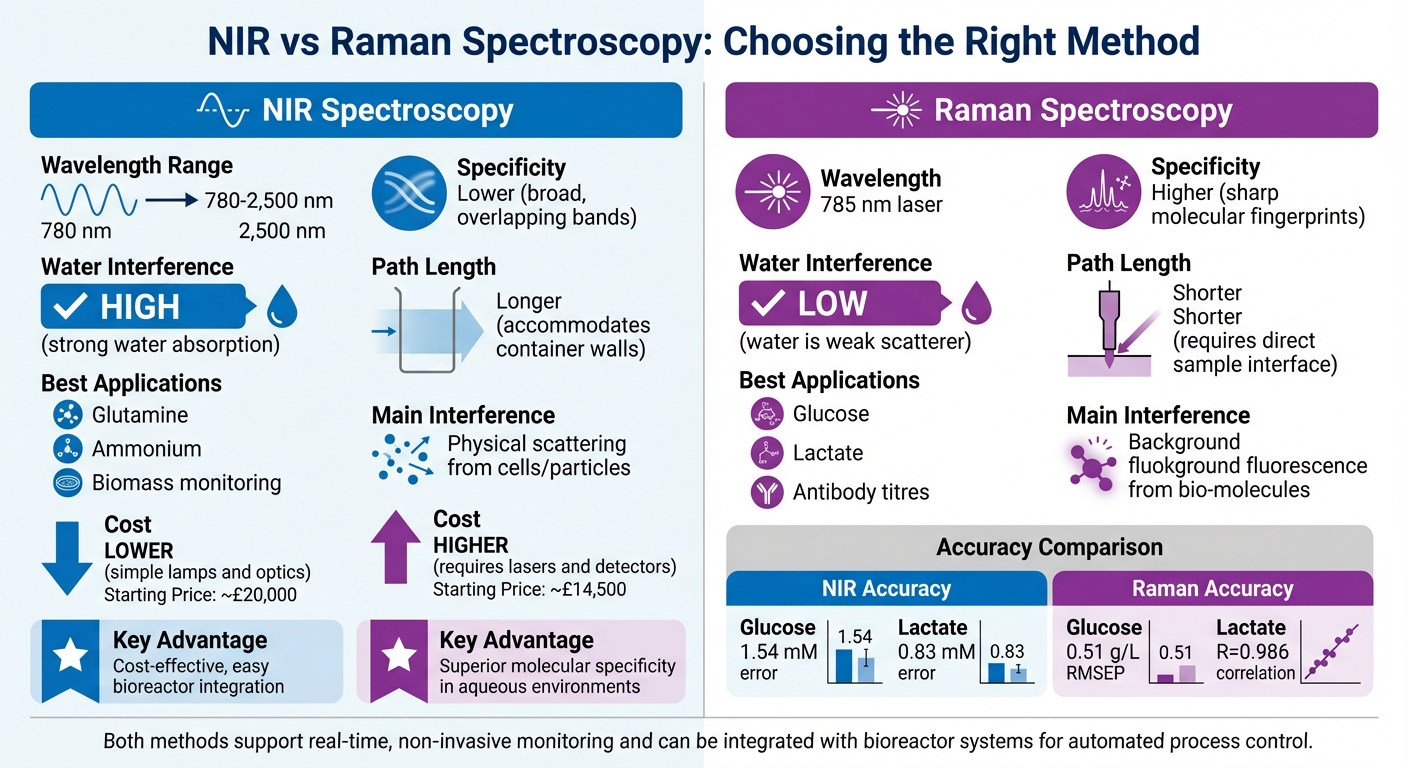
مقارنة بين التحليل الطيفي NIR ورامان لتحليل وسائط النمو
يعتمد القرار بين التحليل الطيفي NIR ورامان على المواد المحددة التي تحللها، والميزانية، وإعداد نظامك.
عوامل المقارنة
يتميز التحليل الطيفي رامان بقدرته على تقديم معلومات جزيئية محددة للغاية.إنه يولد "بصمات" طيفية حادة ومميزة، مما يسهل تحديد المركبات الفردية. من ناحية أخرى، ينتج التحليل الطيفي بالأشعة تحت الحمراء القريبة نطاقات واسعة ومتداخلة تتطلب أدوات كيميائية متقدمة للتحليل [1]. هذا يجعل رامان مفيدًا بشكل خاص لتتبع المستقلبات المحددة بدقة.
يمكن لامتصاص الماء في الأشعة تحت الحمراء القريبة أن يحجب إشارات المغذيات، بينما يضمن الحساسية المنخفضة لرامان للماء اكتشافًا أوضح. ومع ذلك، فإن رامان ليس بدون تحدياته - يمكن أن يواجه تداخلًا من الفلورة الخلفية التي تسببها المركبات البيولوجية مثل التحلل البروتيني [1].
أظهرت الأبحاث التي تتضمن مفاعلات حيوية لخلايا CHO أن رامان يتفوق على الأشعة تحت الحمراء القريبة في التنبؤ بالجلوكوز واللاكتات والأجسام المضادة، بينما تكون الأشعة تحت الحمراء القريبة أكثر فعالية للجلوتامين وأيونات الأمونيوم [2]. دراسة أجريت في مارس 2017 بواسطة R.C.Rowland-Jones في جامعة ليدز دعم بشكل إضافي نقاط قوة رامان، موضحًا أنه كان أكثر موثوقية في قياس اللاكتات (RMSECV 1.11 g/L) والجلوكوز (RMSECV 0.92 g/L) في المفاعلات الحيوية المصغرة بسعة 15 مل [16] .
من منظور التكلفة، فإن أنظمة NIR عادة ما تكون أكثر تكلفة بسبب مصادر الضوء الأبسط. ومع ذلك، تتطلب أنظمة رامان ليزرات وكاشفات متقدمة، مما يجعلها أكثر تكلفة [1].الجدول أدناه يبرز هذه الاختلافات الرئيسية:
| العامل | مطيافية NIR | مطيافية رامان |
|---|---|---|
| التخصصية | أقل؛ نطاقات واسعة ومتداخلة [1] | أعلى؛ "بصمات" جزيئية حادة [1] |
| تداخل الماء | عالي؛ امتصاص قوي للماء [2] | منخفض؛ الماء مشتت ضعيف [2] |
| الأفضل لـ | مراقبة الجلوتامين، الأمونيوم، والكتلة الحيوية [2] | الجلوكوز، اللاكتات، عيارات الأجسام المضادة [2, 19] |
| التكلفة | بشكل عام أقل؛ مصابيح بسيطة وبصريات [1] | بشكل عام أعلى؛ يتطلب ليزر وكاشفات [1] |
| طول المسار | أطول؛ يستوعب جدران الحاوية [6] | أقصر؛ يتطلب واجهة عينة مباشرة [6] |
| التداخل الرئيسي | التشتت الفيزيائي من الخلايا/الجسيمات [6] | الفلورة الخلفية من الجزيئات الحيوية [2] |
التالي، سنستكشف كيفية تطبيق بيانات التحليل الطيفي لتحسين الوسائط في الوقت الحقيقي في الإنتاج.
sbb-itb-ffee270
استخدام بيانات التحليل الطيفي في الإنتاج
تحسين الوسائط في الوقت الفعلي
يحول التحليل الطيفي البيانات الخام إلى رؤى قابلة للتنفيذ، مما يسهل توصيل المغذيات في عمليات الإنتاج. من خلال تمكين المراقبة المتزامنة وغير الغازية للمعايير الرئيسية مثل الجلوكوز واللاكتات والجلوتامين والأمونيوم، يضمن التحسين المستمر للثقافات. على سبيل المثال، عندما تنخفض مستويات الجلوكوز عن النطاق المثالي، يقوم النظام تلقائيًا بتشغيل تغذية المغذيات. هذا يمنع تجويع الخلايا ويقلل من خطر تراكم المنتجات الثانوية السامة [2].
إنشاء مسارات "الدفعة الذهبية" من عمليات الإنتاج المثلى يسمح بالتعرف المبكر على المشكلات، مثل التلوث أو مشاكل التهوية [4].تأخذ الأنظمة الحديثة هذا الأمر إلى أبعد من ذلك - يمكن لقياس الطيف بالأشعة تحت الحمراء القريبة، على سبيل المثال، تقدير تركيزات المغذيات بدقة تصل إلى 15% من الطرق المرجعية التقليدية. في المفاعلات الحيوية الكبيرة التي تصل سعتها إلى 12,500 لتر، تمكن تحليل المكونات الرئيسية لبيانات NIR من حساب 96% من تباين العملية [17].
يتكامل هذا التدفق المستمر للبيانات بسلاسة مع أنظمة المفاعلات الحيوية، مما يتيح التحكم الآلي في العمليات للحفاظ على الاتساق والكفاءة.
ربط قياس الطيف بأنظمة المفاعلات الحيوية
يأخذ تكامل قياس الطيف مع أنظمة المفاعلات الحيوية البيانات في الوقت الحقيقي إلى المستوى التالي، مما يتيح التحكم التلقائي الكامل في التغذية الراجعة. تقوم المجسات المغمورة، القادرة على تحمل دورات التعقيم والضغط العالي، بنقل البيانات في الوقت الحقيقي مباشرة إلى وحدات التحكم في المفاعلات الحيوية [6].
أجريت دراسة في سبتمبر 2018 في جامعة لورين حيث تم مقارنة مجسات رامان وNIR في الموقع تعمل بالتوازي داخل مفاعل حيوي لخلايا CHO بسعة 2 لتر. أظهرت النتائج أن مطيافية رامان كانت متفوقة في الكشف عن الجلوكوز واللاكتات، بينما كانت NIR أكثر فعالية في مراقبة الجلوتامين والأمونيوم. إن الجمع بين نقاط القوة في كلا الطريقتين يوفر المراقبة الأكثر شمولاً في الوقت الحقيقي لإنتاج اللحوم المزروعة [2].
تغذي بيانات المطيافية أيضًا أنظمة التحكم الإحصائي متعدد المتغيرات (MSPC)، والتي تقارن باستمرار الدفعات الجارية بمعايير الدفعة الذهبية المعتمدة. يتيح هذا النهج للمشغلين اكتشاف الانحرافات - سواء كانت ناتجة عن التلوث أو نقص المغذيات أو فشل المعدات - في غضون ساعات بدلاً من أيام. والنتيجة هي تحسين الكفاءة وزيادة الاتساق في الإنتاج [4].
توفير معدات التحليل الطيفي عبر Cellbase
لماذا تستخدم Cellbase لمعدات التحليل الطيفي
اختيار المعدات المناسبة للتحليل الطيفي لإنتاج اللحوم المزروعة يمكن أن يبدو كالتنقل في متاهة من التفاصيل التقنية. مع وجود أجهزة التحليل الطيفي العامة التي تقدم آلاف التكوينات [18]، من السهل أن تشعر بالإرهاق دون الخبرة المناسبة.
هنا يأتي دور
الميزات الرئيسية لـ Cellbase لشراء المعدات
يقوم
بالإضافة إلى ذلك، تساعد خبرة
الخاتمة
تلعب تقنيات التحليل الطيفي NIR وRaman دورًا حيويًا في تحسين وسائط النمو للحوم المزروعة. تُمكّن هذه التقنيات المتقدمة من المراقبة في الوقت الحقيقي وغير الغازية للمحللات الرئيسية مثل الجلوكوز واللاكتات والأمونيا.هذا يعني أن فرق الإنتاج يمكنها إجراء تعديلات سريعة دون مقاطعة العملية - ميزة حيوية نظرًا لأن تصميم الوسائط يظل أحد أكبر التحديات في توسيع إنتاج اللحوم المزروعة [16][19] .
كل طريقة تجلب نقاط قوتها الخاصة إلى الطاولة. تتفوق تقنية التحليل الطيفي بالأشعة تحت الحمراء القريبة في تقييم الكتلة الحيوية والتركيب العام، بينما يوفر التحليل الطيفي رامان رؤى مفصلة حول المستقلبات المحددة في المحاليل المائية [1]. خلال دراسات المفاعلات الحيوية المصغرة، أظهر التحليل الطيفي رامان دقة تنبؤية مثيرة للإعجاب، مما يجعله خيارًا موثوقًا للقياسات الدقيقة [16] . كما تدعم كلتا التقنيتين تطوير ملف تعريف "الدفعة الذهبية"، مما يمكن المشغلين من اكتشاف المشكلات مثل التلوث البكتيري أو مشاكل التهوية بمجرد ظهورها [4].
عندما يتعلق الأمر باختيار المعدات الصحيحة للتحليل الطيفي، يمكن أن تكون العملية مرهقة. هنا يأتي دور
يسلط البروفيسور آلان جي. رايدر الضوء على أهمية هذه الأساليب:
يمكن استخدام الأساليب الطيفية السريعة إذا تم تطبيقها بشكل صحيح للفحص السريع والفعال لوسائط زراعة الخلايا لتحديد التباين الجزيئي والمشكلات المحتملة في تصنيع الوسائط [1].
الأسئلة الشائعة
ما هي فوائد استخدام التحليل الطيفي في إنتاج اللحوم المزروعة؟
تقدم تقنيات التحليل الطيفي مثل الأشعة تحت الحمراء القريبة (NIR) ورامان أدوات قيمة لصناعة اللحوم المزروعة. فهي تتيح المراقبة في الوقت الحقيقي وبدون تدخل لوسائط النمو، مما يجعل من الممكن تتبع العناصر الغذائية والمواد الأيضية وكثافة الخلايا بشكل مستمر - دون الحاجة إلى أخذ عينات أو استخدام كواشف إضافية. يساعد هذا المستوى من المراقبة في الحفاظ على تحكم أكثر دقة في العملية ويسرع من التعديلات في تكوين الوسائط، وهو أمر ضروري لضمان جودة متسقة عند توسيع الإنتاج.
كما أن هذه الأساليب فعالة وتوفر التكاليف. من خلال قياس واحد، يمكنها تحليل مكونات متعددة في وقت واحد - مثل الأحماض الأمينية والسكريات والدهون - مما يلغي الحاجة إلى اختبارات كيميائية منفصلة.هذا يقلل من تكاليف العمالة والمواد بينما يوفر بيانات يمكن أن تحسن النماذج التنبؤية، مما يساعد على توحيد الجودة وتقليل التباين بين الدفعات.
ميزة أخرى هي مدى سهولة دمج التحليل الطيفي مع الأنظمة الآلية. على سبيل المثال، يمكن تركيب مجسات NIR مباشرة في المفاعلات الحيوية لتوفير بيانات مستمرة، مما يتيح التعديلات الآلية للمعايير الحرجة مثل معدلات التغذية أو درجة الحرارة. لأولئك الذين يحتاجون إلى معدات متخصصة،
ما هي الفروقات الرئيسية بين التحليل الطيفي NIR وRaman لتحليل وسائط النمو في إنتاج اللحوم المزروعة؟
التحليل الطيفي بالأشعة تحت الحمراء القريبة (NIR) مثالي لـ المراقبة السريعة وغير الجراحية للتكوين العام لوسائط النمو.قدرته على توفير التحكم عبر الإنترنت أو في الخط يعني أنه يمكنه تقديم بيانات في الوقت الحقيقي، مما يساعد المنتجين على إجراء تعديلات فورية أثناء عملية الإنتاج.
من ناحية أخرى، يوفر التحليل الطيفي رامان بصمة جزيئية دقيقة، مما يجعله خيارًا ممتازًا لتحديد وقياس المستقلبات المحددة مثل الجلوكوز واللاكتات. هذا المستوى من الدقة مفيد بشكل خاص لضبط تكوين الوسائط لتلبية الاحتياجات المحددة لإنتاج اللحوم المزروعة.
لماذا يعتبر المراقبة في الوقت الحقيقي لوسائط النمو مهمة لإنتاج اللحوم المزروعة؟
تلعب المراقبة في الوقت الحقيقي دورًا رئيسيًا في الحفاظ على وسائط النمو بشكل مثالي لإنتاج اللحوم المزروعة. من خلال مراقبة دقيقة للمغذيات والمستقلبات وصحة الخلايا، يمكن للمنتجين تعديل الظروف بسرعة للحفاظ على نمو الخلايا المستقر وتحسين جودة المنتج النهائي.
تعمل هذه الطريقة العملية على تقليل وقت الانتظار المرتبط بالاختبارات التقليدية غير المتصلة بالإنترنت، مما يؤدي إلى تحسين الإنتاج وتقليل الهدر. كما تضمن استخدام الموارد بشكل أكثر فعالية، مما يسهل عملية الإنتاج ويعزز الموثوقية.











