Chuyển từ huyết thanh bò thai (FBS) sang môi trường không huyết thanh (SFM) là rất quan trọng để mở rộng sản xuất thịt nuôi cấy. Sự phụ thuộc vào FBS tạo ra những thách thức như chi phí cao, nguồn cung hạn chế và chất lượng không đồng nhất. SFM cung cấp một giải pháp thay thế an toàn hơn, được kiểm soát tốt hơn, nhưng đi kèm với những trở ngại:
- Vấn Đề Bám Dính Tế Bào: Myoblasts gặp khó khăn trong việc bám dính mà không có huyết thanh, thường cần các lớp phủ đắt tiền như laminin hoặc Matrigel. Môi trường điều kiện hoặc các chất bổ sung cụ thể có thể cải thiện sự bám dính.
- Tốc Độ Tăng Trưởng Chậm Hơn: Hệ thống không huyết thanh thiếu các chất dinh dưỡng quan trọng, dẫn đến sự giảm sinh sản và tích tụ amoniac. Thêm các yếu tố tăng trưởng và thay thế glutamine bằng các lựa chọn khác có thể giúp ích.
- Hiệu Suất Môi Trường Không Đồng Nhất: Nhiều SFM thương mại, được tối ưu hóa cho tế bào người, không hỗ trợ hiệu quả sự phát triển của myoblasts gia súc. Kiểm tra trên nhiều loài và trong thời gian dài hơn với bộ kit khám phá tối ưu hóa môi trường là rất quan trọng.
Các giải pháp bao gồm công thức tùy chỉnh, thay thế một phần môi trường, và hệ thống đồng nuôi cấy để mô phỏng điều kiện giống huyết thanh. Trong khi SFM có thể đạt hiệu suất của hệ thống FBS, việc mở rộng quy mô lên các lò phản ứng sinh học 3D giới thiệu các phức tạp như kết dính và quản lý chất thải. Giám sát cẩn thận chất lượng tế bào đảm bảo thành công trong sản xuất quy mô lớn.
Chuyển sang SFM không chỉ là về khoa học tốt hơn - nó đang trở thành một nhu cầu khi giá FBS tiếp tục tăng. Các nhà nghiên cứu và nhà sản xuất phải tập trung vào tối ưu hóa môi trường và tìm nguồn nguyên liệu đáng tin cậy để làm cho sản xuất thịt nuôi cấy khả thi và hiệu quả về chi phí.
Giàn giáo từ thực vật thúc đẩy sự bám dính tế bào không cần huyết thanh cho thịt nuôi cấy - Indi Geurs - ISCCM9
sbb-itb-ffee270
Vấn Đề Thường Gặp Trong Môi Trường Không Huyết Thanh Cho Tế Bào Cơ
Chuyển từ công thức có huyết thanh sang không huyết thanh có thể gặp nhiều thách thức kỹ thuật làm gián đoạn quy trình và tăng chi phí. Những vấn đề này thường xuất hiện theo những cách cụ thể, bắt đầu từ sự bám dính của tế bào.
Giảm Sự Bám Dính và Sống Sót Của Tế Bào
Một trong những trở ngại lớn nhất là tế bào cơ không bám dính tốt trong môi trường không huyết thanh. Huyết thanh tự nhiên cung cấp một hỗn hợp protein, yếu tố tăng trưởng và lipid giúp tế bào bám vào bề mặt. Thiếu những thành phần này, tế bào cơ gặp khó khăn trong việc bám dính, thường dẫn đến chết tế bào sớm.
Để giải quyết vấn đề này, nhiều hệ thống không huyết thanh dựa vào các tác nhân phủ đắt tiền như laminin 511 hoặc Matrigel. Nhưng ngay cả với những lớp phủ này, mức độ bám dính thường không đạt được như trong các nền văn hóa dựa trên huyết thanh. Ví dụ, một nghiên cứu năm 2024 phát hiện rằng môi trường không có huyết thanh tiêu chuẩn chỉ hỗ trợ 2.210 ± 319 tế bào/cm² trên các đĩa không phủ. Ngược lại, môi trường không có huyết thanh được điều kiện - bổ sung với các yếu tố tiết ra từ các dòng tế bào khác - gần như tăng gấp ba con số đó lên 5.985 ± 1.558 tế bào/cm² [2].
Một vấn đề khác là tăng độ nhạy cảm với kháng sinh. Trong các thiết lập không có huyết thanh, các kháng sinh như Penicillin, Streptomycin và Amphotericin B có thể giảm sự phát triển lên đến 62%, so với mức giảm 20–26% trong các hệ thống dựa trên huyết thanh [1]. Không có các yếu tố bảo vệ của huyết thanh, các tế bào dễ bị tổn thương hơn trước căng thẳng, điều này càng cản trở sự sống sót và phát triển của chúng.
Tăng trưởng tế bào chậm hơn
Ngay cả khi các tế bào có thể bám dính, tốc độ tăng trưởng thường chậm hơn.Serum cung cấp các chất dinh dưỡng thiết yếu như yếu tố tăng trưởng, cytokine, cholesterol và axit béo - nhiều trong số đó thiếu hoặc không đủ trong hầu hết các công thức không có serum thương mại. Khoảng cách dinh dưỡng này dẫn đến sản lượng tế bào thấp hơn và thời gian sản xuất dài hơn.
Một vấn đề phức tạp khác là sự tích tụ amoniac từ quá trình chuyển hóa glutamine. Amoniac ức chế sự phát triển và, trong điều kiện không có serum, nơi mà các tế bào đã chịu áp lực chuyển hóa, độc tính này có thể cản trở nghiêm trọng sự mở rộng. Nhiều môi trường thương mại ban đầu được thiết kế cho tế bào người, vì vậy chúng có thể không đáp ứng nhu cầu dinh dưỡng cụ thể của myoblast bò hoặc lợn [1][3].
Thay thế một phần môi trường, chẳng hạn như thay thế 75% môi trường trong quá trình cho ăn, có thể giúp giữ lại một số yếu tố tăng trưởng nội sinh.Mặc dù điều này cải thiện tốc độ tăng trưởng một cách khiêm tốn, nhưng nó không hoàn toàn lấp đầy khoảng cách giữa các hệ thống không có huyết thanh và có huyết thanh [1].
Hiệu Suất Biến Đổi Giữa Các Sản Phẩm Thương Mại
Không phải tất cả các môi trường không có huyết thanh thương mại đều hoạt động như nhau. Trong một nghiên cứu so sánh bảy công thức, chỉ có ba - FBM™, Essential 8™, và TeSR™-E8™ - hỗ trợ sự phát triển nhất quán của tế bào cơ bò trong sáu ngày. Những sản phẩm khác, như StemPro™ và mTeSR1™, chỉ hỗ trợ sự phát triển trong bốn ngày trước khi ngừng lại, trong khi STEMmacs™ hoàn toàn không duy trì được sự phát triển [1].
Vấn đề nằm ở chỗ hầu hết các môi trường thương mại được tối ưu hóa cho tế bào gốc hoặc nguyên bào sợi của con người, không phải cho tế bào cơ của gia súc. Những gì hoạt động tốt trong nghiên cứu y sinh thường không đáp ứng được cho sản xuất thịt nuôi cấy. Sự không nhất quán này nhấn mạnh nhu cầu về các công thức được thiết kế đặc biệt cho tế bào cơ của gia súc.Dữ liệu từ nhà sản xuất cho tế bào người không thể dự đoán một cách đáng tin cậy về hiệu suất của môi trường với tế bào bò hoặc lợn.
Để tìm môi trường không có huyết thanh phù hợp, điều quan trọng là phải tiến hành thử nghiệm kéo dài - lý tưởng là từ sáu đến mười ngày - để đảm bảo nó hỗ trợ sự mở rộng tế bào bền vững thay vì chỉ tăng trưởng ngắn hạn.
So sánh Các Tùy Chọn Môi Trường Không Huyết Thanh Thương Mại
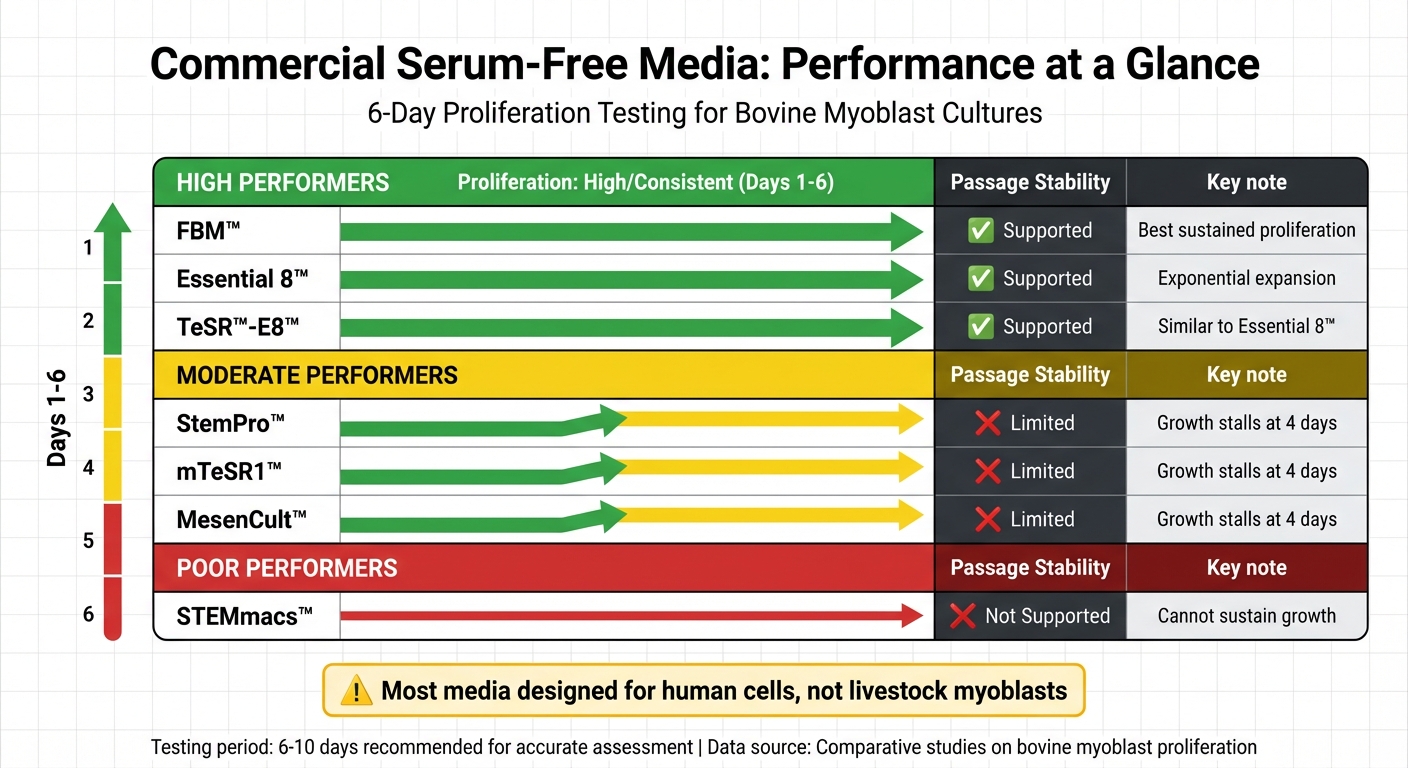
So Sánh Hiệu Suất của Các Môi Trường Không Huyết Thanh Thương Mại cho Nuôi Cấy Myoblast Bò
Dữ Liệu Hiệu Suất cho Các Môi Trường Thông Thường
Khi nói đến môi trường không huyết thanh cho nuôi cấy myoblast, hiệu suất có thể thay đổi rất nhiều. Một số sản phẩm, như FBM™, Essential 8™, và TeSR™-E8™, liên tục hỗ trợ sự phát triển của myoblast bò trong sáu ngày. Ngược lại, những sản phẩm khác, như StemPro™, mTeSR1™, và MesenCult™, thường bị đình trệ sau chỉ bốn ngày.Trong khi đó, STEMmacs™ không thể duy trì sự phát triển hoàn toàn [1].
Đây là so sánh nhanh về các chỉ số hiệu suất cho các phương tiện này:
| Phương tiện | Sự phát triển (Ngày 1–6) | Ổn định khi truyền qua | Quan sát chính |
|---|---|---|---|
| FBM™ | Cao/Ổn định | Được hỗ trợ | Cung cấp tiềm năng tốt nhất cho sự phát triển bền vững [1] |
| Essential 8™ | Cao/Ổn định | Được hỗ trợ | Hỗ trợ mở rộng theo cấp số nhân, mặc dù ít hơn so với dựa trên huyết thanh [1] |
| TeSR™-E8™ | Cao/Ổn định | Được hỗ trợ | Tương tự như Essential 8™ cho myoblasts bò [1] |
| StemPro™ | Trung bình | Hạn chế | Tăng trưởng ngừng lại sau bốn ngày [1] |
| mTeSR1™ | Trung bình | Hạn chế | Tăng trưởng ngừng lại sau bốn ngày [1] |
| MesenCult™ | Trung bình | Hạn chế | Tăng trưởng ngừng lại sau bốn ngày [1] |
| STEMmacs™ | Thấp/Không có | Không hỗ trợ | Không thể duy trì sự phát triển của tế bào cơ bò [1] |
Thú vị là, hầu hết các môi trường - ngoại trừ FBM™ - cho thấy số lượng tế bào giảm đáng kể trong vòng 24 giờ sau khi gieo so với các đối chứng dựa trên huyết thanh.Điều này nhấn mạnh tầm quan trọng của việc đánh giá các chỉ số này khi lựa chọn một môi trường, đặc biệt là xem xét các xu hướng quy định trong môi trường tăng trưởng về an toàn thực phẩm.
Cách Chọn Môi Trường Không Huyết Thanh Phù Hợp
Việc chọn môi trường không huyết thanh tốt nhất không chỉ là về tốc độ tăng trưởng; nó đòi hỏi sự cân bằng của nhiều yếu tố như sự phát triển, sự bám dính và hiệu quả chi phí. Việc thử nghiệm môi trường trong khoảng thời gian sáu ngày là rất quan trọng, vì các thử nghiệm ngắn hơn có thể cung cấp kết quả sai lệch [1].
Tính đặc thù của loài là một yếu tố quan trọng khác cần xem xét. Nhiều lựa chọn không huyết thanh được thiết kế với các tế bào người trong tâm trí, điều này có nghĩa là chúng có thể không đáp ứng được nhu cầu dinh dưỡng của các tế bào cơ của gia súc như tế bào bò hoặc lợn. Nhu cầu dinh dưỡng của các loài và trạng thái tế bào khác nhau có thể khác nhau đáng kể, vì vậy việc thử nghiệm là cần thiết [3] .
Yêu cầu về lớp phủ cũng đóng một vai trò lớn. Một số môi trường cần lớp phủ đắt tiền như laminin hoặc Matrigel để đảm bảo sự bám dính của tế bào. Nếu quy trình của bạn liên quan đến bề mặt không phủ hoặc vật liệu cấp thực phẩm, đáng để thử nghiệm xem liệu môi trường có thể hỗ trợ sự bám dính mà không cần các chất phụ gia này hay không. Môi trường điều kiện hoặc công thức được điều chỉnh cho các đĩa không phủ có thể là một lựa chọn thay thế tiết kiệm chi phí [2] .
Một yếu tố quan trọng khác là việc sử dụng kháng sinh. Cocktail kháng sinh tiêu chuẩn, chẳng hạn như Penicillin/Streptomycin, có thể giảm sự phát triển của myoblast từ 20–26% trong môi trường chứa huyết thanh và lên đến 62% trong hệ thống không có huyết thanh. Loại bỏ kháng sinh có thể dẫn đến sản lượng tế bào cao hơn đáng kể [1].
Cuối cùng, đừng bỏ qua quản lý chất thải trao đổi chất. Sự tích tụ amoniac có thể gây độc cho các nền văn hóa, vì vậy việc bổ sung môi trường với các hợp chất không sinh amoniac như α-ketoglutarate hoặc pyruvate là một ý tưởng tốt. Những chất phụ gia này giúp giảm độc tính của amoniac và kéo dài tuổi thọ của các nền văn hóa [3].
Phương pháp cải thiện nuôi cấy tế bào cơ không huyết thanh
Giải quyết các thách thức của nuôi cấy tế bào cơ không huyết thanh đòi hỏi các chiến lược nhắm mục tiêu. Dưới đây là một số phương pháp thực tế để nâng cao hiệu suất của chúng.
Thêm các chất bổ sung quan trọng
Kết hợp các chất bổ sung cụ thể có thể cải thiện đáng kể sự phát triển của tế bào cơ. Một hỗn hợp FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), và insulin (10 μg/ml) đã được chứng minh là tăng cường sự mở rộng tế bào trong môi trường cơ bản như FBM [1] . Các yếu tố tăng trưởng này hoạt động cùng nhau để thúc đẩy sự tăng sinh tế bào trong khi duy trì trạng thái chưa phân hóa cần thiết cho sản xuất.
Amino acids và vitamin cũng rất quan trọng. Các hợp chất như pyridoxamine (Vitamin B6), asparagine, và glutamic acid đóng vai trò quan trọng trong việc khuyến khích sự bám dính và tăng sinh tế bào, đặc biệt trên các bề mặt không phủ [2] . Các chất bổ sung này giúp thay thế sự hỗ trợ chuyển hóa thường được cung cấp bởi huyết thanh, giải quyết các thách thức liên quan đến bám dính.
"Phân tích thành phần và các thí nghiệm xác nhận cho thấy pyridoxamine, asparagine và glutamic acid đã đóng góp vào việc đạt được chức năng nuôi cấy của môi trường phát triển." - npj Science of Food [2]
Tuy nhiên, cần thận trọng với các chất bổ sung dựa trên lipid như LipoGro. Mặc dù chúng có thể kích thích tăng trưởng, chúng cũng có thể gây ra sự phân hóa mỡ, khiến các tế bào cơ phát triển không bào mỡ và mất đi đặc tính của tế bào cơ [1].
Điều chỉnh Công thức Môi trường
Tùy chỉnh công thức môi trường có thể tối ưu hóa các nền văn hóa không có huyết thanh bằng cách sử dụng bộ phát hiện yếu tố tăng trưởng. Một phương pháp hiệu quả là sử dụng môi trường điều kiện. Môi trường điều kiện bằng cách đồng nuôi cấy HepG2 (ung thư gan người) và NIH/3T3 (nguyên bào sợi chuột) tái tạo hồ sơ chuyển hóa của gan thai nhi. Phương pháp này đạt được mật độ tế bào 5,985 ± 1,558 tế bào/cm² trên đĩa không phủ, tương đương với 6,722 ± 1,500 tế bào/cm² đạt được với môi trường có chứa huyết thanh [2] . Tương tác giữa các loại tế bào này thúc đẩy sự tiết ra các thành phần giống huyết thanh, tăng cường sự phát triển.
Một chiến lược tiết kiệm chi phí khác là thay thế một phần môi trường nuôi cấy. Bằng cách chỉ thay thế 75% môi trường thay vì thay đổi hoàn toàn, các yếu tố tăng trưởng nội sinh do tế bào sản xuất được bảo tồn, cải thiện tốc độ tăng trưởng mà không cần bổ sung thêm [1].
Ngăn chặn sự phân hóa sớm bằng chất ức chế
Duy trì trạng thái tăng sinh đòi hỏi kiểm soát cẩn thận các tín hiệu phân hóa. Ví dụ, môi trường điều kiện từ tế bào HepG2 có thể ức chế biểu hiện của dấu hiệu phân hóa cơ Desmin, giữ cho tế bào không phân hóa và sẵn sàng cho sự mở rộng [2].
Thêm vào đó, theo dõi các dấu hiệu như CD29 (integrin beta-1) và Ki67 giúp đảm bảo công thức hiệu quả trong việc duy trì sự tăng sinh của tế bào, giảm nguy cơ phân hóa sớm.Các dấu hiệu này cung cấp một cách đáng tin cậy để giám sát và điều chỉnh điều kiện nuôi cấy nhằm đạt kết quả tối ưu.
Quy mô nuôi cấy Myoblast không huyết thanh để sản xuất
Chuyển sang Hệ thống Nuôi cấy 3D
Chuyển đổi nuôi cấy myoblast không huyết thanh từ đĩa phẳng 2D sang hệ thống bioreactor 3D đi kèm với những thách thức riêng, đặc biệt là khi nói đến sự bám dính của tế bào. Việc phủ các thành phần bioreactor bằng các tác nhân đắt tiền như laminin không thực tế cho sản xuất quy mô lớn. Tuy nhiên, sử dụng môi trường điều kiện từ đồng nuôi cấy HepG2 và NIH/3T3 hoặc làm giàu môi trường cơ bản với các hợp chất như pyridoxamine, asparagine và axit glutamic đã chứng minh hiệu quả. Những phương pháp này cho phép myoblast bám vào các giàn giáo 3D không phủ và microcarriers, giải quyết các vấn đề bám dính mà không cần sử dụng lớp phủ đắt tiền [2].
Một yếu tố quan trọng khác trong việc mở rộng quy mô là quản lý chất thải chuyển hóa.Các nền văn hóa bioreactor dày đặc có thể gặp phải sự tích tụ amoniac độc hại, điều này có thể tránh được bằng cách thay thế glutamine bằng các lựa chọn thay thế không sinh amoniac như α-ketoglutarate, glutamate hoặc pyruvate [3]. Những điều chỉnh này là cần thiết khi chuyển sang các hệ thống quy mô lớn hơn và yêu cầu kiểm soát chất lượng và giám sát cảm biến cẩn thận để duy trì tính toàn vẹn của myoblasts trong quá trình sản xuất.
Xác nhận Chất lượng Tế bào trong Các Nền Văn hóa Đã Thích nghi
Khi các nền văn hóa được thích nghi cho sản xuất quy mô lớn hơn, đảm bảo chất lượng của các tế bào là rất quan trọng. Các kỹ thuật như phân tích transcriptomic, metabolomic và chức năng được sử dụng để xác minh rằng các tế bào duy trì mức độ cao của CD29 và Ki67 trong khi ức chế biểu hiện Desmin. Những dấu hiệu này chỉ ra rằng các tế bào vẫn ở trạng thái tăng sinh, chưa phân biệt trong quá trình mở rộng quy mô [2]. Việc giám sát các chỉ số này đặc biệt quan trọng khi các biện pháp tiết kiệm chi phí, chẳng hạn như chuyển sang sử dụng các thành phần đạt tiêu chuẩn thực phẩm hoặc sử dụng thay đổi môi trường một phần, được áp dụng. Bước này đảm bảo rằng việc chuyển đổi từ hệ thống đạt tiêu chuẩn nghiên cứu sang hệ thống đạt tiêu chuẩn sản xuất không làm giảm chất lượng tế bào. Việc điều chỉnh các thông số này là một bước quan trọng để làm cho sản xuất thịt nuôi cấy có thể mở rộng và tiết kiệm chi phí.
Hiệu Suất Nuôi Cấy Không Huyết Thanh So Với Có Huyết Thanh
Khi được tối ưu hóa, các hệ thống không huyết thanh có thể đạt được kết quả gần với các nuôi cấy truyền thống có huyết thanh.Bảng dưới đây nêu bật các chỉ số chính từ các nền văn hóa myoblast bò được nuôi trên bề mặt không phủ:
| Chỉ số | Dựa trên huyết thanh (20% FBS + 10% HS) | Không huyết thanh có điều kiện |
|---|---|---|
| Bám dính tế bào (24h) | ~6,722 tế bào/cm² | ~5,985 tế bào/cm² |
| Sinh sản tế bào (72h) | ~10,050 tế bào/cm² | ~8,998 tế bào/cm² |
| Biểu hiện CD29 | Cao | Cao |
| Biểu hiện Ki67 | Cao | Cao |
| Biểu hiện Desmin | Bị ức chế | Bị ức chế |
Dữ liệu được lấy từ npj Science of Food [2]
Trong khi các hệ thống dựa trên huyết thanh vẫn có lợi thế nhẹ về mật độ tế bào, môi trường không có huyết thanh mang lại kết quả tương đương trong việc biểu hiện dấu hiệu bám dính và giữ cho tế bào không phân hóa - những yếu tố quan trọng cho sản xuất.Khoảng cách thu hẹp hơn nữa khi các chất bổ sung cụ thể được thêm vào để tối ưu hóa công thức, làm cho hệ thống không có huyết thanh trở thành một lựa chọn ngày càng thực tế cho sản xuất thịt nuôi cấy quy mô lớn.
Kết luận
Chuyển đổi các nền văn hóa myoblast sang môi trường không có huyết thanh đi kèm với những trở ngại nhất định: vấn đề gắn kết sớm, tăng trưởng tế bào chậm hơn và kết quả không nhất quán từ các sản phẩm thương mại. Tuy nhiên, những thay đổi đơn giản - như loại bỏ kháng sinh và chọn thay thế một phần môi trường - có thể cải thiện đáng kể tỷ lệ sinh sản [1]. Bằng cách lựa chọn cẩn thận môi trường và thêm các yếu tố tăng trưởng cụ thể, các nhà nghiên cứu có thể thu hẹp khoảng cách giữa hệ thống không có huyết thanh và có huyết thanh về mặt hiệu suất. Những tiến bộ này mở đường cho việc mở rộng quy mô sản xuất.
Tuy nhiên, việc mở rộng các nền văn hóa không có huyết thanh giới thiệu các lớp phức tạp mới.Chuyển đổi tế bào sang hệ thống bioreactor 3D trong khi đảm bảo chúng duy trì được kiểu hình đòi hỏi kiểm soát chất lượng nghiêm ngặt. Tuy nhiên, bằng chứng cho thấy rằng các hệ thống không có huyết thanh được tối ưu hóa tốt có thể đạt được mật độ tế bào tương đương với những tế bào được nuôi trong môi trường có huyết thanh. Điều này làm cho các phương pháp không có huyết thanh ngày càng thực tế hơn cho sản xuất thịt nuôi cấy thương mại.
Lập luận kinh tế cho môi trường không có huyết thanh là khó có thể bỏ qua. Với giá FBS tiếp tục tăng, các phương pháp dựa trên huyết thanh đang trở nên không khả thi về mặt tài chính [1] . Sự chuyển đổi này không chỉ là về cải tiến kỹ thuật - mà còn là về sự sống còn kinh tế cho ngành công nghiệp thịt nuôi cấy.
Đối với các nhà nghiên cứu và đội ngũ sản xuất đang thực hiện chuyển đổi này, việc tìm nguồn cung cấp vật liệu phù hợp là điều cần thiết. Từ môi trường hóa học xác định đến yếu tố tăng trưởng tái tổ hợp, việc có quyền truy cập vào nguồn cung cấp đáng tin cậy là chìa khóa. Đây là nơi
Câu hỏi thường gặp
Làm thế nào để cải thiện sự bám dính của myoblast trong môi trường không có huyết thanh mà không cần laminin hoặc Matrigel?
Để cải thiện sự bám dính của myoblast trong môi trường không có huyết thanh mà không sử dụng laminin hoặc Matrigel, hãy cân nhắc sử dụng môi trường không có huyết thanh điều kiện. Cách tiếp cận này có thể thúc đẩy sự bám dính và phát triển ngay cả trên các đĩa không phủ. Một lựa chọn khác là tối ưu hóa môi trường bằng cách thêm các thành phần như FGF2, fetuin, và BSA. Những điều chỉnh này có thể tạo ra sự khác biệt đáng kể trong việc tăng cường sự bám dính và phát triển của tế bào, loại bỏ nhu cầu cho các lớp phủ ma trận ngoại bào.
Cách nhanh nhất để giảm tích tụ amoniac trong nuôi cấy myoblast không có huyết thanh là gì?
Để giảm tích tụ amoniac trong nuôi cấy myoblast không có huyết thanh, hãy tập trung vào cải thiện công thức môi trường. Một cách tiếp cận là sử dụng môi trường điều kiện hóa thúc đẩy cả sự bám dính và phát triển của tế bào trong khi giữ mức amoniac thấp. Ngoài ra, tinh chỉnh điều kiện nuôi cấy có thể giúp giảm thiểu sản xuất amoniac. Điều này có thể bao gồm điều chỉnh các yếu tố như pH, nhiệt độ hoặc nồng độ dinh dưỡng để phù hợp hơn với nhu cầu trao đổi chất của tế bào.
Làm thế nào để xác nhận rằng myoblast vẫn không phân hóa sau khi chuyển sang môi trường không có huyết thanh?
Để đảm bảo myoblast vẫn ở trạng thái không phân hóa khi nuôi cấy trong môi trường không có huyết thanh, điều quan trọng là theo dõi các dấu hiệu cụ thể. Pax7 là một chỉ số đáng tin cậy của các tế bào cơ chưa phân hóa, trong khi sự vắng mặt của các dấu hiệu phân hóa như chuỗi nặng myosin (MHC) xác nhận rằng chúng chưa bắt đầu phân hóa.
Bạn có thể sử dụng các kỹ thuật như:
- Hóa mô miễn dịch: Để quan sát sự biểu hiện protein trong tế bào.
- Đo tế bào dòng chảy: Để phân tích sự biểu hiện của dấu hiệu trong một quần thể tế bào lớn.
- qPCR: Để đo mức độ mRNA của các dấu hiệu chính.
Thêm vào đó, quan sát tế bào dưới kính hiển vi là rất cần thiết. Tế bào cơ nên duy trì hình dạng đặc trưng của chúng, tránh hình thành các ống cơ đa nhân, đây là dấu hiệu rõ ràng của sự phân hóa. Bằng cách kết hợp các phương pháp này và theo dõi thường xuyên, bạn có thể đảm bảo rằng các tế bào vẫn chưa phân hóa.











