- 目的: 确保生物反应器符合监管和生产标准,保持无菌、精确的环境控制和食品安全。
- 关键特性: 搅拌罐式生物反应器因其适合牛肌肉细胞而被选中,提供可控的剪切力和可扩展性。
- 挑战: 为了实现高细胞密度的生物反应器扩展并降低成本,需要重新考虑材料、灭菌方法和工艺设计。
- 解决方案: 改用食品级材料,采用具有成本效益的灭菌方法,并整合机器学习进行工艺优化,显著降低了成本。
- 结果: 生产成本从£437,000/公斤降至£1.95/公斤,生产率提高了15倍,并在使用可再生能源时减少了高达92%的温室气体排放。
本研究概述了验证协议和智能设计选择如何推动培养肉接近与传统肉类的价格平价。
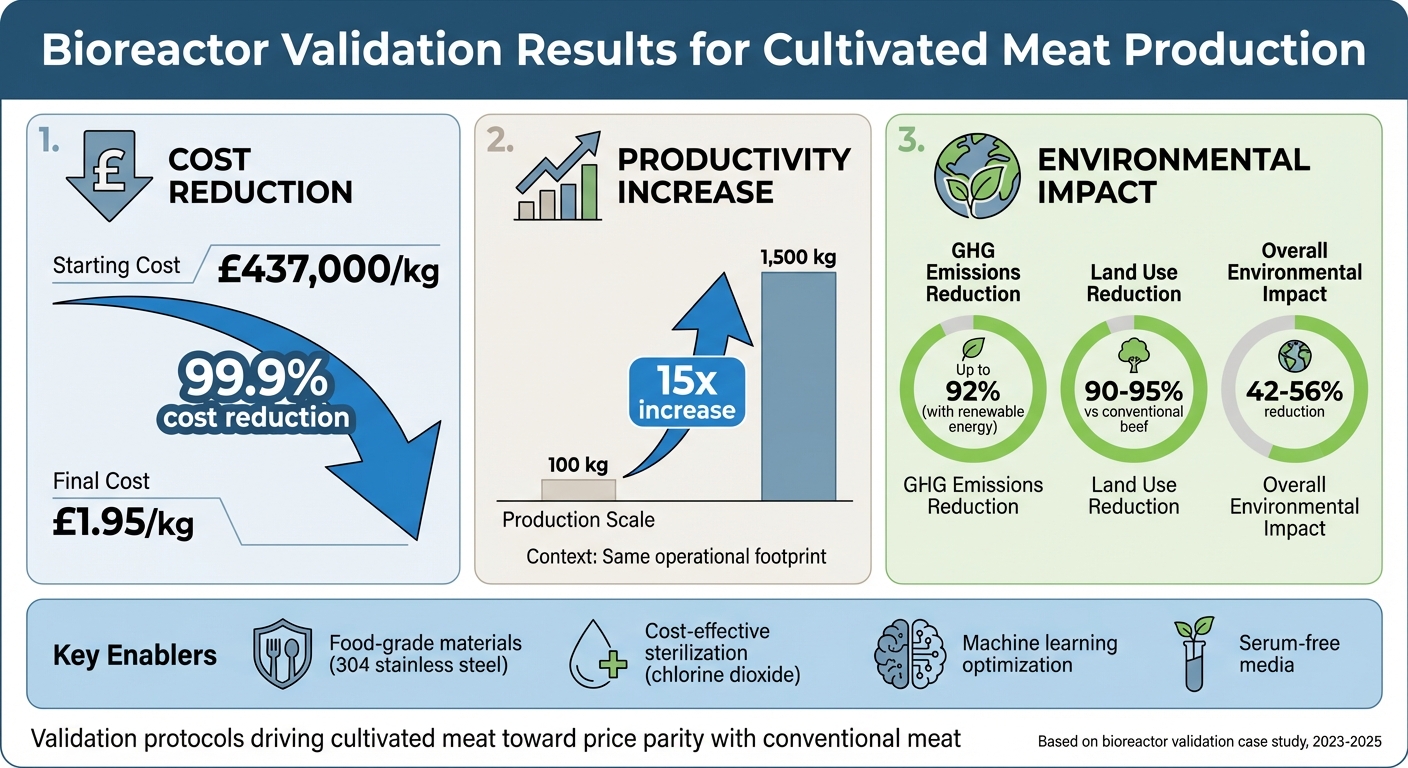
生物反应器验证影响:培养肉生产中的成本降低和环境效益
生物反应器验证的监管要求
适用的监管标准
在培养肉行业中,满足严格的监管标准是生物反应器验证过程中的关键部分。在英国,食品标准局(FSA)和苏格兰食品标准局(FSS)将培养肉归类为“动物源性产品”(POAO)。这一分类确保食品安全和卫生法规适用于所有生产阶段,包括生物反应器操作。然而,根据英国指导(2025年12月),虽然这些产品属于POAO类别,但它们在法律上不被视为“肉类”。这一区别意味着某些传统的动物福利和微生物要求被排除在外,从而影响了英国所需的特定验证协议。
在全球范围内,安全评估的持续时间各不相同。新加坡和美国通常在12个月内完成审查,而欧盟平均约为18个月。英国通过CCP Sandbox计划开辟了自己的道路,该计划资助至2027年2月。此举使监管机构能够与Gourmey, Hoxton Farms, 和Mosa Meat, 等公司直接合作,简化数据要求并加快安全评估。
"沙盒计划使我们能够快速获取监管知识,以减少新兴食品技术的障碍,同时不影响安全标准。"
– Dr. Thomas Vincent, 创新副主任, FSA [3]
无论管辖权如何,公司在进入市场之前必须提交详细的安全档案。这些档案概述了生产过程、产品成分和安全数据。它们还必须确认培养肉在营养上与传统肉类相当,包括宏观和微观营养素以及氨基酸和脂肪酸谱的分析。
验证协议要求
监管标准要求严格的生物反应器验证协议,以确保安全和可控的操作。一个关键组成部分是实施危害分析和关键控制点 (HACCP) 计划。这个框架在生产的每个阶段识别和减轻风险,从最初的细胞活检到细胞团的最终收获。鉴于培养肉生产的新颖性,安全评估必须在整个过程中解决潜在的危害。
验证协议必须证明生物反应器系统在生产周期内保持无菌条件,有效防止微生物污染。此外,这些协议需要评估培养肉中的蛋白质是否会引发消费者的过敏反应。
“我们的新指南为企业提供了清晰的指引,帮助他们理解并正确向英国食品监管机构展示其产品的安全性。具体来说,该指南确保公司在产品被授权销售之前,已经评估了潜在的过敏风险,并且它们在营养上是适当的。”
– Dr.托马斯·文森特,创新副主任,FSA [2]
在英国,验证的重点是为科学风险评估提供足够的数据,而不是授予市场授权。GOURMEY的联合创始人兼首席执行官尼古拉斯·莫林-福雷斯特强调了这一区别:
“大不列颠的验证标志着我们新型食品监管旅程中的关键一步,并确认我们现在正在推进全面风险评估,使我们离将产品提供给消费者更近了一步。”[4]
生物反应器选择和系统规格
选择的生物反应器技术
该设施选择了搅拌罐式生物反应器, 这一选择是由于其在牛肌肉祖细胞. 方面的可靠性能驱动的。影响这一决策的关键因素包括细胞的具体需求、所需的生产规模和整体成本考虑。
牛肌肉细胞是依赖附着的,需要低于0.1 N/m²的低剪切力,以避免在培养过程中受到损害。搅拌罐设计满足了这一要求,同时证明其适用于试验规模实验和商业生产。成本是另一个主要因素,试验规模的设备价格在£50,000到£100,000之间,使其在培养肉行业的预算中更为可及,而不是制药行业[5][7].
生产规模目标在100到1,000升之间,以确保商业可行性。模块化搅拌罐系统被选择而不是填充床替代方案,因为它们能够在不超过传质限制的情况下放大10倍,保持kLa值在50 h⁻¹以上。这些系统旨在每批生产1–10公斤的培养肉,资本投资约为每升容量£200[7] [8].
系统设计特点
一旦选择了搅拌罐生物反应器,其设计就结合了先进的功能以促进最佳细胞生长。气体交换系统采用微型曝气器技术,提供20–100 µm的气泡。此设置在37°C下实现100–200 h⁻¹的kLa值,保持溶解氧水平在30–50%饱和度。为了管理CO₂剥离,顶空曝气与膜接触器和消泡传感器相结合[5][6].
为了高效混合,生物反应器使用双Rushton搅拌器, 以50–150 rpm的速度运行。这确保了均匀混合,剪切速率低于5,000 s⁻¹, 保护细胞免受损伤,同时保持营养梯度低于10%。搅拌采用PID控制,实时反馈pH值和溶解氧水平,支持1–5容器体积/天的灌流速率[5][7].
可扩展性是设计的关键重点。生物反应器在不同规模上保持几何相似性,遵循2:1的高径比。CFD优化的搅拌器确保线性放大,试验显示从10升到200升的放大过程中细胞活力保持95%。模块化设计允许集成到更大的生产系统中,同时满足GxP合规标准 [7] [8].
过程分析技术也被集成,具有拉曼光谱,用于实时监测关键参数,如pH值(6.8–7.2)和乳酸(保持在2 g/L以下)。预测模型从单克隆抗体生产中改编而来,跟踪葡萄糖水平,R²值高于0.95,确保精确的过程控制[5] [6][7].
这些功能不仅增强了细胞培养,还满足英国监管机构要求的严格验证标准。
验证协议执行
核心验证程序
为了确保操作完整性,进行了彻底的验证协议,结合了先进的设计功能。实时监控发挥了关键作用,过程分析技术 (PAT) 传感器在每次培养运行期间持续跟踪溶解氧、pH 和 CO₂ 水平等关键参数[6]. 该过程始于以 1×10⁵ 个细胞/mL 的密度接种的细胞,在含有 3 g/L 葡萄糖的培养基中培养一周。拉曼光谱用于监测整个过程中的乳酸和葡萄糖水平 [5].
剪切应力分析确认搅拌力保持在 0.1 Pa 以下,这是牛肌肉细胞的临界限度。应力测试后显示细胞活力保持在 90% 以上[6].
对所有原材料进行无菌测试,特别关注培养基。供应商需提供经第三方测试验证的分析证书,符合英国设施标准。该协议包括ELISA免疫测定以检测革兰氏阴性菌的内毒素,并通过流式细胞术根据细胞大小、形状和荧光特性识别污染物[9] .
工艺优化方法
一旦系统稳定性得到确认,工作重点转向使用高级分析技术优化工艺。机器学习算法根据连续的PAT数据动态调整培养基流速和搅拌速度。这些模型在实验设计 (DoE)数据集上训练,通过将电导率测量与生物质质量相关联,识别出成本效益高的饲养策略[6]. 这种方法在增殖阶段特别有效,在该阶段,稳定的生长率对于商业生产至关重要。
拉曼光谱最初为单克隆抗体生产而开发,成功地适用于培养肉应用。其分析物特异性使设施能够采用既定的验证协议,同时保持在整个培养周期中进行实时监测所需的精度[5].
技术挑战和解决方案
放大和生产力问题
将生物反应器从实验室环境扩展到商业生产绝非易事。该设施旨在生产10–100公斤的培养肉,需要大量的10¹²–10¹³个细胞来实现这一目标[11]. 然而,实现高细胞密度被证明是一个重大障碍。虽然中空纤维生物反应器理论上可以实现10⁸到10⁹个细胞/mL的密度[13], 但传统的生物反应器设计在培养肉生产方面未能达到要求。
GFI研究员Matt McNulty解释了问题的根源:“用于培养肉的生物反应器仍然主要是从传统食品和制药设计中改造而来的。这些设计并未专门针对培养肉生产的需求进行定制,因此由于这种不匹配而导致效率低下,从而推高了成本”[12]. 这种设计与用途之间的不匹配需要对设备和工艺进行彻底的重新思考。
实施的解决方案和性能数据
为了解决这些挑战,该设施重新调整了其设备和协议,以更好地符合培养肉生产的特定需求。一个关键的变化是从制药级标准转向食品级标准。例如,团队用304不锈钢替代了316不锈钢容器,这满足了食品安全要求,同时显著降低了资本成本[12]. 此外,传统的就地蒸汽灭菌工艺被氯二氧化物气体处理所取代。这一调整允许使用由替代材料制成的薄壁容器,进一步降低了成本[12].
另一项节省成本的措施是将用于培养基制备的药用级水更换为被分类为“普遍认为安全”(GRAS)的食品级水 [12]. 团队还引入了可食用的微载体和支架,这不仅解决了细胞脱落问题,还符合食品安全法规 [11].
为了进一步优化操作,设施实施了多路传感器系统。这些传感器提供了实时性能数据,可用于机器学习应用以微调流程 [12]. 总体而言,这些变化对生产成本产生了显著影响,将其从£437,000/公斤削减到仅£1.95/公斤 [10]. 这种显著的成本降低突显了如何通过将生产协议与监管标准对齐来实现商业规模化,而不牺牲安全性或质量。
sbb-itb-ffee270
验证结果和行业影响
测量的性能结果
通过严格的测试,该系统展示了生产力的显著提升。使用无气泡连续生物反应器技术,细胞生长生产力提高了15倍, 将产量从100公斤提升到1,500公斤——全部在相同的操作空间内完成[16]. 在分化阶段,优化细胞生物量的调整导致了128%的增长, 显著减少了整体环境影响42–56%. 从C2C12到CHO细胞代谢的转变在减少环境影响方面也发挥了重要作用,在使用可再生能源时实现了高达67%的减排[14]. 更为显著的是,可再生能源的使用将温室气体排放量减少了高达92% ,并将土地使用减少了90–95%,与传统牛肉生产方法相比[15] [16] . 这些结果为整个行业的更广泛采用铺平了道路。
对行业实践的贡献
验证结果重新定义了培养肉生产中生物反应器设计和法规合规的标准。通过证明食品级标准可以有效替代药品级标准而不影响安全性,该过程为行业引入了一条节约成本的路线图。例如,从316不锈钢切换到304不锈钢,结合二氧化氯消毒和使用GRAS分类的水,大大降低了资本成本,同时保持合规性。
除了证明技术可行性,这些进步正在改变行业基准。经济模型表明,集成连续加工在十年内可节省55%的资本和运营成本[1]. 对于采购团队,像
结论
主要发现
本分析强调了通过明智的设备选择和优化操作协议,培养肉类生产如何走向商业成功。选择食品级材料如304不锈钢而不是更昂贵的316不锈钢,确保安全和合规的同时降低成本。转向无血清培养基,正如新加坡食品局在2023年初批准GOOD Meat的配方所验证的那样,消除了与动物衍生投入相关的伦理和财务挑战[15].
使用气升式反应器扩大生产规模,特别是在260,000升时,已显示出将成本降低到约£10.50/公斤的潜力。与较小的42,000升搅拌罐反应器相关的£24.50/公斤成本相比,这是一个显著的改进[17]. 然而,实现高细胞密度 - 高达 2 × 10⁸ 个细胞/mL - 需要先进的灌流系统来处理代谢废物,如氨和乳酸。工艺优化已被证明在解决这些挑战中至关重要[11]. 对于采购团队,像
未来发展
随着成本效益和工艺控制的验证,重点现在转向巨型生物反应器,这有望重新定义生产经济学。GOOD Meat在2022年5月宣布了一座设施,配备十个250,000升的生物反应器——每年可生产13,700公吨的培养鸡肉和牛肉——标志着从试点项目到工业规模生产的重大转变 [11][15]. 这与加州大学戴维斯分校Patrick G. Negulescu等人设定的经济基准一致:
“为了直接与牛肉竞争,CM产品,或至少生产成本,必须降到每公斤肉低于9美元的水平”[17]
预测表明,这一目标是可以实现的,尤其是随着培养基成本的持续下降,目标设定为每升低于0.20英镑。
像可食用微载体和混合系统这样的创新,将细胞扩增和分化结合在一个容器中,预计将简化验证过程并降低污染风险。本案例研究中概述的协议为公司扩大运营规模提供了一个可复制的模型,证明严格的测试可以与成本降低共存。随着更多设施采用这些验证的方法,培养肉行业正逐步接近与传统肉类的价格平价。与此同时,该行业带来了显著的环境效益,包括在使用可再生能源时温室气体排放量减少高达92%[15].
生物反应器回顾:传感器、建模、放大和替代反应器设计
常见问题
监管机构在培养肉的生物反应器验证档案中期望看到哪些证据?
监管机构要求生物反应器验证档案以确认系统在定义的参数内运行。这涉及确保一致的过程性能和关键因素的实时监控,如pH值, 溶解氧, 和 温度. 此外,灭菌测试在防止污染中起着至关重要的作用。遵循 ISO 14644-1和EU GMP 附录1等标准是维持微生物控制和保持无菌生产实践的强制要求。
如何在不损害牛肌肉细胞的情况下扩大搅拌罐式生物反应器的规模?
扩大用于培养肉生产的搅拌罐式生物反应器的规模涉及管理剪切应力, ,这可能会损害牛肌肉细胞。为了解决这个问题,使用计算流体动力学(CFD)和缩小模型等工具来预测流动模式。这些见解指导了对搅拌器设计和搅拌速度的调整,有助于减少细胞损伤。
同样重要的是确保营养和氧气的均匀分布。先进的监测系统结合有效的混合技术,是创造一致条件的关键。这种方法有助于最大限度地减少局部应力,并在大规模生产过程中支持细胞健康。
哪些成本削减验证变更对£/kg的影响最大?
采用一次性生物反应器对降低以£/kg计的成本有显著影响。虽然这些系统减少了初始资本投资和劳动力费用,但它们确实伴随着更高的消耗品成本。此外,引入实时监控和培养基回收技术提高了运营效率。这些进步不仅简化了流程,还带来了长期的成本节约。











