Pensijilan bilik bersih adalah penting untuk pengeluaran daging yang diternak, memastikan keselamatan dan pematuhan dengan peraturan UK seperti Peraturan (EC) 853/2004. Tanpa pensijilan, kemudahan berisiko pencemaran, ketidakpatuhan, dan isu kualiti produk. Berikut adalah gambaran ringkas tentang proses ini:
- Kepentingan Pensijilan: Mencegah pencemaran mikroba, selaras dengan prinsip HACCP, dan memastikan pengeluaran yang konsisten.
- Piawaian Utama: ISO 14644-1 (kebersihan udara), EU GMP Annex 1 (pembuatan steril), dan EN 17141 (kawalan mikroba).
-
Langkah-langkah untuk Pensijilan:
- Reka Bentuk dan Pembinaan: Pasang penapis HEPA, sistem aliran udara, dan kekalkan perbezaan tekanan yang betul.
- Kelayakan Pemasangan (IQ): Sahkan bilik bersih sepadan dengan spesifikasi reka bentuk.
- Kelayakan Operasi (OQ): Uji prestasi di bawah keadaan terkawal.
- Kelayakan Prestasi (PQ): Mengesahkan fungsi semasa operasi sebenar.
- Pemantauan Berterusan: Pemeriksaan berkala untuk zarah, tekanan, suhu, dan kelembapan.
- Pematuhan Berterusan: Kelayakan semula setiap 6–12 bulan atau selepas perubahan besar.
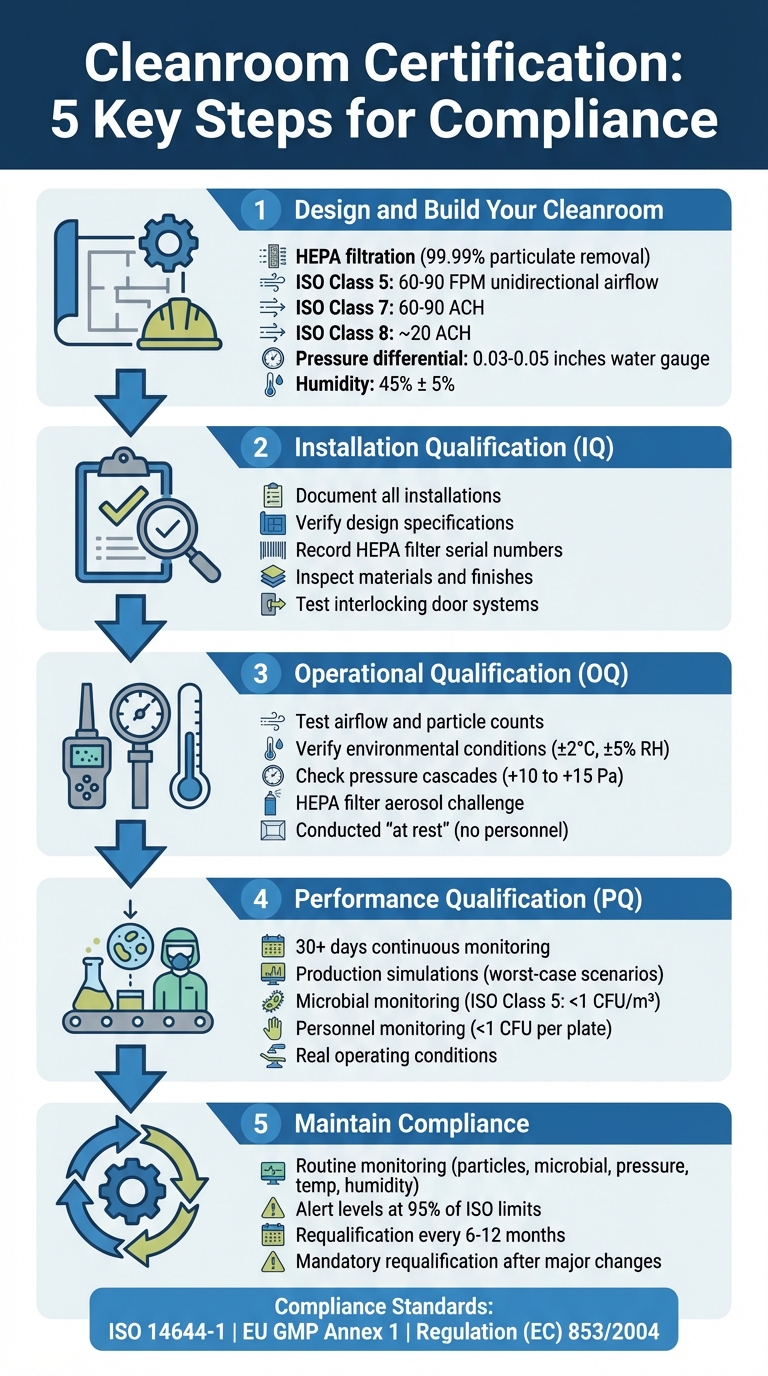
Proses Pensijilan Bilik Bersih 5 Langkah untuk Kemudahan Daging Ternakan
Reka Bentuk dan Pensijilan Bilik Bersih
Langkah 1: Reka Bentuk dan Bina Bilik Bersih Anda
Membina bilik bersih untuk pengeluaran daging ternakan memerlukan perancangan teliti terhadap tiga sistem utama: penapisan HEPA, kawalan persekitaran, dan pemisahan aliran kerja. Elemen-elemen ini memastikan keadaan steril dan membantu anda mengelakkan pengubahsuaian yang mahal kemudian.Setelah sistem ini dipasang, fokus pada mengoptimumkan prestasi mereka semasa pemasangan.
Keperluan Penapisan HEPA dan Aliran Udara
Sistem pengendalian udara adalah tulang belakang bilik bersih anda dan menentukan sama ada ia memenuhi klasifikasi ISO yang diperlukan. Penapis HEPA mengeluarkan 99.99% zarah[5], tetapi keberkesanannya bergantung pada penghantaran udara pada kadar dan corak tertentu yang disesuaikan untuk setiap zon pengeluaran.
Untuk kawasan ISO Kelas 5 - di mana proses aseptik seperti penuaian daging berlaku - anda memerlukan aliran udara sehala (laminar) pada 60 hingga 90 kaki per minit (FPM) [5]. Ini melibatkan unit penapis kipas yang dipasang di siling (FFU) mengarahkan aliran udara melalui ventilasi dinding rendah dengan sudut pelepasan yang sempit.
Di zon ISO Kelas 7 dan 8, reka bentuk aliran udara campuran digunakan. Di sini, udara bekalan segar bercampur dengan udara dalaman, memerlukan perubahan udara yang lebih sedikit setiap jam (ACH). Zon ISO Kelas 7 memerlukan 60–90 ACH, manakala zon ISO Kelas 8 memerlukan sekitar 20 ACH[1][6]. Untuk mengira ACH, bahagikan jumlah udara bekalan (setiap jam) dengan jumlah bilik. Ingat bahawa siling yang lebih tinggi meningkatkan kedua-dua keperluan aliran udara dan kos[3].
Diferensial tekanan adalah kunci untuk menghalang pencemaran. Kekalkan diferensial tekanan positif sebanyak 0.03–0.05 inci tolok air antara bilik bersih dan kawasan bersebelahan [7]. Walau bagaimanapun, jangan melebihi 0.1 inci tolok air merentasi pintu, kerana ini boleh menyukarkan untuk dibuka - memerlukan sehingga 11 paun daya pada pintu standard 3×7 kaki[7].
Selepas pemasangan, uji sistem penapisan untuk integriti menggunakan ujian cabaran aerosol seperti ujian DOP atau PAO untuk mengesahkan tiada kebocoran atau pengedap lemah dalam perumahan penapis HEPA[1]. Kajian visualisasi asap juga boleh membantu mengesahkan aliran udara laminar dan memastikan tiada pergolakan atau aliran balik di zon sensitif.
Dengan penapisan yang ada, langkah seterusnya adalah memastikan keadaan persekitaran yang konsisten.
Kawalan Persekitaran untuk Pengeluaran
Menjaga suhu, kelembapan, dan tekanan yang stabil adalah penting untuk meminimumkan risiko mikrob[9]. Sistem HVAC anda mesti sentiasa mengekalkan parameter ini sambil menyokong kadar pertukaran udara yang tinggi yang diperlukan untuk klasifikasi ISO bilik bersih anda.
Kawalan suhu adalah sangat penting. Sistem mesti mengatasi haba dari bioreaktor, pencahayaan, dan kakitangan tanpa mengganggu corak aliran udara. Kelembapan relatif harus kekal pada 45% ± 5%, yang membantu mencegah cas elektrostatik yang menarik partikel dan mengelakkan masalah pemeluwapan. Julat ini juga memastikan persekitaran kerja yang selesa untuk kakitangan yang memakai gaun[7].
Pengawasan masa nyata terhadap parameter persekitaran seperti pH dan oksigen terlarut boleh membantu mengesan tanda awal pertumbuhan mikrob[9]. Pemantauan berterusan terhadap udara, permukaan, dan air adalah amalan penting lain untuk menangkap pencemaran sebelum ia meningkat. Selain itu, reka bentuk sistem HVAC anda untuk masa pemulihan yang singkat - ini memastikan bilik bersih cepat kembali ke tahap kebersihan yang ditetapkan selepas kejadian pencemaran, mengurangkan masa henti[1].
Setelah kawalan persekitaran dilaksanakan, fokus pada pengurusan bagaimana bahan dan orang bergerak melalui ruang untuk meminimumkan risiko pencemaran.
Menguruskan Aliran Bahan dan Personel
"Pekerja bilik bersih adalah sumber pencemaran terbesar bilik bersih dan semua proses kritikal harus diasingkan dari pintu akses personel dan laluan." - Vincent A. Sakraida, Jurutera[7]
Personel adalah risiko pencemaran terbesar dalam bilik bersih, melepaskan zarah kulit, rambut, dan serpihan lain[7][6]. Untuk menangani ini, susun atur bilik bersih anda harus memisahkan secara fizikal proses kritikal dari kawasan lalu lintas tinggi dan titik akses.
Bahan harus bergerak dalam satu arah - dari zon gred rendah ke zon gred tinggi - menggunakan proses pembasmian kuman atau pensterilan yang disahkan sepanjang perjalanan[8].Steriliser dua hujung, seperti autoklaf pintu dua atau terowong depirogenasi, adalah ideal untuk memindahkan barang ke dalam kawasan pemprosesan aseptik tanpa menjejaskan kualiti udara[8].
Ruang udara bertindak sebagai penampan antara kawasan dengan tahap kebersihan yang berbeza. Zon ISO Kelas 7 atau lebih bersih harus termasuk bilik persalinan untuk berpakaian, yang menghalang pencemaran luar daripada memasuki kawasan pengeluaran[6]. Untuk zon Gred A dan B, sistem pintu berkunci memastikan hanya satu pintu boleh dibuka pada satu masa[8]. Jika ruang udara berasingan untuk kakitangan dan bahan tidak dapat dilaksanakan, pemisahan berdasarkan masa prosedur boleh membantu mengelakkan pergerakan serentak antara zon[8].
Hadkan ruang kritikal kepada satu titik akses untuk mengurangkan risiko pencemaran silang[7].Tingkap pemerhatian atau kamera jauh boleh membolehkan penyelia memantau aktiviti tanpa memasuki bilik bersih, mengurangkan akses yang tidak perlu[8].
Setiap langkah ini memainkan peranan penting dalam mencapai pensijilan bilik bersih dan memastikan kemudahan anda memenuhi piawaian ketat yang diperlukan untuk pengeluaran daging yang ditanam dengan selamat dan mematuhi peraturan.
Langkah 2: Lengkapkan Kelayakan Pemasangan (IQ)
Sebaik sahaja pembinaan selesai, langkah seterusnya adalah Kelayakan Pemasangan (IQ). Proses ini memastikan bahawa setiap komponen bilik bersih telah dipasang dengan betul sebelum beralih kepada ujian operasi. Pada dasarnya, IQ bertindak sebagai jambatan antara menyelesaikan pembinaan fizikal dan memulakan pengimbangan HVAC, mengesahkan bahawa semuanya sedia untuk fasa seterusnya.
"Pemeriksaan Kelayakan Pemasangan (IQ) memastikan bahawa peralatan, komponen, dan susunan bilik bersih mematuhi spesifikasi pengeluar dan bahawa semuanya telah dipasang dengan betul." - Kjeld Lund, Pakar Bilik Bersih [11]
IQ memberi tumpuan kepada keadaan "seperti dibina" - apabila struktur bilik bersih telah siap tetapi peralatan pengeluaran belum dipasang. Tujuan utama di sini adalah untuk memastikan bahawa apa yang telah dibina sepadan dengan reka bentuk asal, dengan sebarang penyimpangan didokumentasikan dan ditangani dengan betul.
Dokumentasikan Semua Langkah Pemasangan
Dokumentasi yang teliti adalah kunci semasa fasa ini. Anda memerlukan rekod terperinci seperti dibina, yang termasuk lukisan seni bina yang dikemas kini, senarai peralatan HVAC, urutan kawalan, dan diagram pendawaian elektrik. Rekod ini harus mencerminkan bagaimana bilik bersih sebenarnya dibina, bukan hanya bagaimana ia dirancang.
Untuk setiap penapis HEPA atau ULPA, catat nombor siri, lokasi tepat, dan tarikh pemasangan. Adalah penting untuk memeriksa penapis bagi kerosakan semasa transit sebaik sahaja dipasang - kerana walaupun kebocoran kecil boleh menjejaskan integriti bilik bersih. Tag setiap peralatan dan sensor dengan ID unik yang sepadan dengan senarai peralatan anda, memudahkan audit dan penyelenggaraan masa depan.
Sijil penentukuran untuk semua instrumen pemantauan juga mesti difailkan. Ini termasuk kaunter zarah, sensor tekanan berbeza, probe suhu dan kelembapan, dan peranti aliran udara. Seperti yang dijelaskan oleh Toni Horsfield dari ISO Cleanroom, "Sijil penentukuran [untuk kaunter zarah] disertakan dalam laporan pengesahan bilik bersih anda." [10]
Pemeriksaan bahan dan kemasan adalah sama penting. Sahkan bahawa panel dinding, lantai, pintu, laluan masuk, dan sealant memenuhi piawaian GMP. Permukaan harus tidak mudah mengelupas, rendah VOC, dan ditutup dengan betul. Pintu dan tingkap mesti rata dengan dinding untuk mengekalkan integriti tekanan.
Simpan log penyimpangan untuk sebarang variasi reka bentuk, mencatat penilaian dan tindakan pembetulan yang diambil. Log ini akan menjadi sebahagian daripada laporan pengesahan akhir anda, menyatukan semua penemuan dari fasa pemasangan.
Sahkan Spesifikasi Reka Bentuk
Setelah rekod pemasangan anda lengkap, langkah seterusnya adalah memastikan setiap sistem selaras dengan reka bentuk yang diluluskan. Rujuk silang Spesifikasi Keperluan Pengguna (URS) dengan pemasangan fizikal untuk mengesahkan bahawa tiada apa yang terlepas pandang semasa penghantaran atau pemasangan.
Untuk sistem HVAC dan penapisan, periksa bahawa unit pengendalian udara, sambungan saluran, dan kedudukan penyebar sepadan dengan lukisan reka bentuk. Sahkan bahawa penapis HEPA dipasang dengan betul dalam perumahannya dan semua ujian tekanan saluran udara telah berjaya diselesaikan. Rekodkan spesifikasi dan helaian data untuk setiap unit penapis kipas.
Pengesahan struktur termasuk memeriksa kunci antara, kunci udara, dan laluan untuk memastikan ia berfungsi seperti yang diinginkan. Uji sistem pintu berkunci antara untuk memastikan kedua-dua pintu tidak boleh dibuka pada masa yang sama. Periksa bahawa semua pengedap adalah utuh dan bilik bersih dapat mengekalkan perbezaan tekanan yang diperlukan.
Jalankan sistem HVAC untuk mencapai keadaan mantap sebelum beralih ke peringkat ujian seterusnya.
Menjalankan IQ dengan ketepatan adalah penting, kerana ia meletakkan asas untuk semua peringkat kelayakan seterusnya. Melangkau langkah atau tergesa-gesa melalui dokumentasi boleh menyebabkan komplikasi semasa ujian operasi dan audit pengawalseliaan. Dengan melengkapkan pemeriksaan ini dengan teliti, anda memastikan peralihan yang lancar ke kelayakan operasi.
Langkah 3: Laksanakan Kelayakan Operasi (OQ)
Setelah Kelayakan Pemasangan mengesahkan bahawa semuanya dipasang dengan betul, langkah seterusnya adalah Kelayakan Operasi (OQ). Fasa ini memastikan bilik bersih anda beroperasi seperti yang dimaksudkan di bawah keadaan yang ditetapkan. Biasanya, ujian ini dijalankan "dalam keadaan rehat", bermakna sistem HVAC berfungsi, tetapi tiada aktiviti kakitangan atau pengeluaran berlaku.
"Pengesahan menyediakan bukti objektif bahawa bilik bersih melakukan apa yang direka untuk dilakukan: mengekalkan suasana yang stabil dan bebas pencemaran di bawah kedua-dua keadaan statik (dalam keadaan rehat) dan operasi." - Standard Tech [12]
Ujian OQ adalah penting untuk menunjukkan pematuhan dengan piawaian ISO 14644-1 dan GMP. Untuk kemudahan daging yang ditanam, langkah ini amat penting kerana proses biologi bergantung pada kawalan partikel dan mikrob yang ketat.Untuk memastikan hasil yang tepat, stabilkan bilik bersih sekurang-kurangnya 30 minit sebelum memulakan ujian untuk mengelakkan kiraan zarah yang menyimpang [12]. Pemeriksaan ini membina fasa pemasangan, meletakkan asas untuk penalaan halus kawalan persekitaran anda.
Uji Aliran Udara dan Kiraan Zarah
Kiraan zarah udara adalah asas kepada pengelasan ISO. Menggunakan kaunter zarah laser yang telah dikalibrasi, ukur kepekatan zarah di udara untuk mengesahkan pematuhan dengan kelas ISO yang diperlukan. Untuk ISO Kelas 5, rujuk had zarah yang dinyatakan dalam jadual piawaian.
Bilangan lokasi pensampelan bergantung pada saiz bilik bersih. ISO 14644-1 menyediakan garis panduan yang jelas: bilik yang lebih besar memerlukan lebih banyak titik pensampelan, disusun dalam corak grid [16]. Jika anda menguji dua hingga sembilan lokasi, anda perlu mengira Had Keyakinan Atas 95% (UCL) untuk menentukan pematuhan.Untuk sepuluh atau lebih titik pensampelan, pengiraan ini tidak diperlukan [15].
Pengukuran halaju dan volum aliran udara memastikan kadar pertukaran udara anda memenuhi spesifikasi reka bentuk. Gunakan anemometer untuk mengukur halaju di pelbagai titik, terutamanya berhampiran kawasan proses kritikal, dan sahkan bahawa nilai-nilai ini sepadan dengan sasaran reka bentuk anda.
Kajian asap menawarkan cara visual untuk memeriksa arah aliran udara, memastikan ia bergerak dari zon yang lebih bersih ke zon yang kurang bersih. Hasilkan asap berhampiran pintu, laluan, dan kawasan terdedah lain untuk mengesan kebocoran atau pergolakan yang boleh mengganggu aliran udara [12]. Walaupun kaunter zarah adalah tepat, kajian asap boleh mendedahkan isu seperti zon pegun yang mungkin tidak disedari.
Penapis HEPA dan ULPA juga mesti disahkan semula semasa OQ. Gunakan cabaran aerosol untuk memeriksa kebocoran dalam penapis atau pengedapnya. Walaupun kesilapan pemasangan kecil boleh menjejaskan prestasi, jadi sentiasa uji semula selepas sebarang penyelenggaraan atau penggantian penapis [12].
Sebaik sahaja prestasi aliran udara disahkan, tumpuan beralih kepada keadaan persekitaran yang mempengaruhi kualiti produk dan keselesaan pengendali.
Sahkan Keadaan Persekitaran
Suhu dan kelembapan memainkan peranan penting dalam mengekalkan kualiti produk dan memastikan persekitaran kerja yang selesa. Untuk kemudahan daging yang ditanam, sasaran pengesahan biasanya ±2°C untuk suhu dan ±5% untuk kelembapan relatif [12]. Pemantauan berterusan sekurang-kurangnya 24 jam adalah disyorkan, kerana pemeriksaan tempat mungkin terlepas turun naik yang boleh menjejaskan pengesahan [12].
Bilik bersih untuk daging yang ditanam biasanya mengekalkan julat suhu 18–22°C dan kelembapan relatif antara 30–60% [14].Keadaan ini menyokong proses kultur sel sambil menghalang pemeluwapan, yang boleh menggalakkan pertumbuhan mikrob. Gunakan sensor haba yang ditentukur dan probe RH yang diletakkan di seluruh bilik bersih untuk mengenal pasti sebarang variasi dalam keadaan.
Kaskade tekanan adalah faktor kritikal lain. Ini memastikan bahawa aliran udara bergerak dari kawasan yang lebih bersih ke kawasan yang kurang bersih, mengurangkan risiko pencemaran. Sahkan perbezaan tekanan - biasanya +10 hingga +15 Pa antara bilik yang dikelaskan bersebelahan - menggunakan tolok yang ditentukur. Ambil ukuran di pintu dan laluan di bawah keadaan mantap untuk mengesahkan hubungan tekanan yang betul [12].
Ujian masa pemulihan mengukur seberapa cepat bilik bersih kembali mematuhi selepas kejadian pencemaran. Perkenalkan sumber zarah terkawal, kemudian pantau berapa lama masa yang diambil untuk kiraan zarah kembali ke asas.Masa pemulihan yang lebih cepat menunjukkan reka bentuk aliran udara yang lebih baik dan kawalan pencemaran yang lebih berkesan [1].
Untuk mengelakkan kelewatan atau ujian semula yang mahal, kalibrasi semua instrumen dengan segera sebelum ujian OQ. Rekod semua butiran yang berkaitan, termasuk tarikh, masa, lokasi, ID instrumen, dan keadaan persekitaran untuk setiap ujian. Dokumentasi ini penting untuk laporan pengesahan anda dan akan diperlukan semasa audit pengawalseliaan [12].
sbb-itb-ffee270
Langkah 4: Laksanakan Kelayakan Prestasi (PQ)
Kelayakan Prestasi (PQ) menilai prestasi bilik bersih anda di bawah keadaan pengeluaran sebenar, dengan peralatan beroperasi dan kakitangan bekerja secara aktif [1][12].Membina atas Kelayakan Pemasangan dan Operasi, PQ memberikan pengesahan bahawa bilik bersih berfungsi secara konsisten dan boleh dipercayai semasa operasi sebenar.
"PQ mengesahkan prestasi bilik bersih di bawah keadaan operasi sebenar, termasuk operasi peralatan dan aktiviti kakitangan." - G-CON [1]
Untuk memastikan ujian yang menyeluruh, fasa PQ harus merangkumi sekurang-kurangnya 30 hari pemantauan berterusan. Jangka masa yang dilanjutkan ini membantu mengenal pasti variasi, seperti turun naik suhu semasa kitaran pengeluaran atau perubahan dalam pencemaran mikrob disebabkan oleh pergerakan kakitangan, yang mungkin terlepas dalam ujian yang lebih pendek. Untuk kemudahan daging yang ditanam, di mana kawalan pencemaran yang ketat adalah kritikal, PQ menawarkan bukti yang didokumentasikan bahawa bilik bersih kekal mematuhi semasa operasi rutin.
Jalankan Simulasi Pengeluaran
Simulasi pengeluaran harus meniru senario terburuk.Ini mungkin termasuk kapasiti maksimum, operasi serentak semua peralatan, dan risiko pencemaran sementara seperti pembukaan pintu yang kerap atau pergerakan yang intens [1][13]. Pendekatan berasaskan risiko, seperti menggunakan Analisis Kegagalan dan Kesan (FMEA), boleh membantu mengenal pasti lokasi pensampelan berdasarkan risiko pencemaran, aliran bahan, dan kawasan trafik tinggi [16].
Pemantauan mikrob semasa simulasi ini adalah penting. Unit pembentuk koloni (CFU) harus dipantau menggunakan kedua-dua kaedah pensampelan aktif dan pasif [14][17]. Untuk bilik bersih ISO Kelas 5, had tindakan untuk pencemaran mikrob biasanya adalah 1 CFU/m³ [14].
Oleh kerana manusia adalah sumber zarah terbesar dalam bilik bersih, pemantauan kakitangan adalah sama penting.Pensampelan hujung jari bersarung boleh mengesahkan teknik aseptik yang betul, dengan had yang boleh diterima kurang daripada 1 CFU setiap plat [17]. Pengendali harus diberi taklimat mengenai protokol pemakaian pakaian dan pergerakan terlebih dahulu untuk mengelakkan lonjakan buatan dalam tahap pencemaran [12].
Selain itu, uji seberapa cepat bilik bersih pulih selepas cabaran zarah terkawal. Perkenalkan sumber zarah dan ukur masa yang diambil untuk keadaan kembali ke garis dasar. Proses ini menilai aliran udara dan keberkesanan sistem kawalan pencemaran [1][12].
Menetapkan Pemantauan Persekitaran
Selepas ujian simulasi, pemantauan persekitaran berterusan memastikan prestasi yang konsisten.Sistem-sistem ini menyediakan data masa nyata mengenai parameter kritikal seperti zarah udara, pencemaran mikrob, suhu, kelembapan, dan perbezaan tekanan. Ini penting untuk mengesan perubahan prestasi sebelum ia membawa kepada isu pematuhan [1]. Untuk pengeluaran daging yang diternak, pemantauan berterusan adalah sangat diperlukan.
Semasa fasa kelayakan, jalankan pensampelan udara mikrob setiap 1–2 jam di zon kritikal untuk mengesahkan kawalan pencemaran yang berkesan [14]. Gunakan Tryptic Soy Agar (TSA) untuk mengesan bakteria, inkubasi sampel pada suhu 30–35°C sekurang-kurangnya tiga hari, dan Sabouraud Dextrose Agar (SAB) untuk kulat dan acuan, inkubasi pada suhu 20–25°C sekurang-kurangnya tujuh hari [17]. Elakkan menggunakan semburan aerosol atau pembasmi kuman berhampiran pengambil sampel udara semasa ujian.Jika pembasmi kuman berputar atau alkohol isopropil 70% telah digunakan, tunggu sekurang-kurangnya lima minit sebelum memulakan pensampelan udara [17].
Tetapkan had amaran dan tindakan yang jelas untuk semua parameter yang dipantau. Tahap amaran menandakan keperluan untuk penyiasatan apabila nilai mula menyimpang, manakala had tindakan memerlukan tindakan pembetulan segera jika parameter melebihi julat yang boleh diterima [14]. Simpan rekod terperinci bagi setiap pengukuran, termasuk tarikh, masa, lokasi, butiran instrumen, dan keadaan persekitaran. Ini memastikan anda sentiasa bersedia untuk audit dan boleh menunjukkan pematuhan dengan piawaian ISO 14644 dan GMP.
Langkah 5: Mengekalkan Pematuhan Melalui Pemantauan
Sebaik sahaja anda melengkapkan Kelayakan Prestasi, kerja tidak berhenti di situ. Mengekalkan pematuhan memerlukan pemantauan berterusan dan pengkelasan semula berkala.Pensijilan bilik bersih bukanlah satu pencapaian sekali sahaja - ia memerlukan usaha berterusan untuk memastikan kemudahan anda dalam "keadaan terkawal." Untuk kemudahan daging yang ditanam, proses berterusan ini memastikan anda memenuhi kedua-dua piawaian peraturan dan operasi, melanjutkan amalan teliti fasa kelayakan ke dalam operasi harian.
Laksanakan Pemantauan Rutin
Untuk memastikan bilik bersih anda kekal mematuhi piawaian ISO 14644 dan GMP, anda perlu memantau pencemaran mikrob dan partikel secara berkala. Parameter utama yang perlu diperhatikan termasuk:
- Kiraan partikel
- Tahap mikrob
- Tekanan
- Suhu
- Kelembapan
- Aliran udara
Kekerapan pemantauan harus selaras dengan klasifikasi bilik bersih anda dan penilaian risiko yang menyeluruh.Sebagai contoh, zon ISO Kelas 5 sering memerlukan pemantauan zarah secara berterusan atau setiap jam semasa pengeluaran, manakala kawasan yang kurang kritikal mungkin hanya memerlukan pemeriksaan harian atau mingguan.
Tetapkan tahap amaran pada 95% daripada had ISO untuk mengesan isu berpotensi lebih awal. Tahap ini bertindak sebagai amaran apabila parameter mula menyimpang, mendorong siasatan sebelum ia meningkat. Sebaliknya, had tindakan memerlukan tindakan pembetulan segera jika parameter melebihi julat yang boleh diterima [14] .
Satu lagi bahagian penting dalam pemantauan ialah pensampelan hujung jari bersarung tangan (GFS). Kaedah ini memastikan kakitangan mengekalkan teknik aseptik yang betul. Kriteria standard biasanya kurang daripada 1 CFU setiap plat [17]. Melakukan GFS selepas tugas aseptik kritikal atau pada akhir setiap syif membantu mengenal pasti dan menangani kelemahan dalam teknik lebih awal.
Walaupun pemantauan rutin membantu mengekalkan kawalan harian, pengesahan semula memastikan sistem bilik bersih anda kekal berkesan dalam jangka masa panjang.
Jadualkan Pengesahan Semula
Pengesahan semula harus dijalankan setiap 6 hingga 12 bulan. Walau bagaimanapun, acara tertentu menjadikan pengesahan semula wajib, seperti pengubahsuaian struktur, pemasangan peralatan baru, penggantian penapis HEPA, atau perubahan ketara pada sistem HVAC [1][14].
Semasa pengesahan semula, banyak ujian dari fasa Kelayakan Operasi perlu diulang. Ini termasuk:
- Pemantauan zarah udara
- Ujian integriti penapis HEPA (membuktikan kecekapan 99.99% untuk zarah ≥0.3 mikron)
- Pengukuran kelajuan aliran udara
- Pemeriksaan perbezaan tekanan
Satu ujian yang sangat kritikal ialah ujian masa pemulihan, yang mengukur seberapa cepat bilik bersih kembali ke tahap kebersihan sasarannya selepas kejadian pencemaran. Ujian ini mengesahkan keupayaan sistem HVAC anda untuk menangani tekanan dengan berkesan [1].
Simpan Pelan Induk Pengesahan (VMP) untuk mendokumentasikan semua peringkat kelayakan (IQ, OQ, PQ) dan jadual pengesahan semula anda. Pastikan semua instrumen yang digunakan untuk ujian - seperti kaunter zarah dan anemometer - dikalibrasi dan mempunyai sijil yang boleh dikesan kepada piawaian kebangsaan [1] [14]. Ini memastikan ketepatan dan kebolehpercayaan dalam usaha pematuhan anda.
Peralatan Cleanroom Sumber untuk Pematuhan
Cari Pembekal yang Disahkan di Cellbase
Setelah standard operasi dan prestasi cleanroom anda ditetapkan dan disahkan, langkah seterusnya adalah mendapatkan peralatan yang betul untuk mengekalkan pematuhan. Untuk pengeluaran daging yang ditanam, ini bermakna bekerja dengan pembekal yang memahami keperluan unik industri ini.
Pastikan Perolehan Mematuhi GMP
Selepas mengesahkan peralatan, proses perolehan juga mesti memenuhi piawaian GMP yang ketat.
Selain itu, platform ini mengutamakan bahan yang memenuhi keperluan GMP. Sebagai contoh, bahan pembinaan seperti keluli tahan karat 316L dengan permukaan yang digilap dan tidak mengelupas ditonjolkan. Bahan-bahan ini tahan terhadap pembasmian kuman kimia berulang dan menyokong protokol Pembersihan di Tempat (CIP) dan Pensterilan di Tempat (SIP) yang disahkan [4]. Dengan mengesahkan keserasian bahan pada awalnya, anda boleh mengelakkan pengubahsuaian mahal atau kitaran kelayakan semula di kemudian hari. Pendekatan proaktif ini membantu mengekalkan pematuhan sambil menjimatkan masa dan sumber.
Kesimpulan
Pengajaran Utama
Mencapai pensijilan bilik bersih adalah penting untuk mengekalkan kualiti produk dan memenuhi piawaian peraturan. Ia bermula dengan mereka bentuk bilik bersih yang dilengkapi dengan penapisan HEPA, aliran udara terkawal, dan aliran bahan yang cekap. Proses ini diteruskan dengan pendekatan kelayakan tiga peringkat: Kelayakan Pemasangan (IQ), Kelayakan Operasi (OQ), dan Kelayakan Prestasi (PQ). Peringkat ini memastikan semua sistem beroperasi dengan berkesan di bawah keadaan kerja sebenar.
Pensijilan tidak berakhir di situ. Pemantauan berterusan terhadap faktor seperti suhu, kelembapan, tekanan, dan kiraan zarah adalah penting untuk mengenal pasti sebarang isu prestasi. Penilaian semula secara berkala memastikan pematuhan dengan ISO 14644-1 dan piawaian GMP, mewujudkan rangka kerja kukuh untuk penambahbaikan masa depan.
Langkah Seterusnya untuk Kemudahan Anda
Untuk menyelaraskan kemudahan anda dengan piawaian ini, pertimbangkan untuk membangunkan Pelan Induk Pengesahan (VMP). Pelan ini mengintegrasikan proses kelayakan dengan keperluan operasi harian, membantu anda kekal di hadapan tuntutan peraturan [1]. Selain itu, melaksanakan sistem pengurusan keselamatan makanan berasaskan HACCP adalah penting. Sekurang-kurangnya seorang ahli pasukan harus dilatih ke Tahap 4 dalam prinsip HACCP untuk memastikan pematuhan [2].
Untuk keperluan peralatan, beralih kepada
Soalan Lazim
Apakah faedah pensijilan bilik bersih untuk pengeluaran daging yang diternak?
Pensijilan bilik bersih memainkan peranan penting dalam pengeluaran daging yang diternak dengan memastikan pematuhan kepada piawaian keselamatan dan alam sekitar yang ketat. Bilik bersih yang disahkan direka untuk meminimumkan risiko pencemaran daripada mikrob dan zarah, mengekalkan keadaan steril yang penting untuk penanaman sel. Ini bukan sahaja melindungi kualiti dan keselamatan produk akhir tetapi juga memastikan pematuhan kepada piawaian yang diiktiraf di peringkat antarabangsa seperti klasifikasi ISO dan gred GMP - keperluan utama untuk kelulusan pengawalseliaan dan penerimaan pasaran.
Di luar pematuhan, pensijilan meningkatkan kebolehpercayaan operasi dengan mengesahkan sistem kritikal seperti aliran udara, penapisan, dan pemantauan alam sekitar. Sistem-sistem ini bekerjasama untuk mengurangkan risiko pencemaran, membolehkan pengeluaran yang konsisten dan meningkatkan kecekapan proses keseluruhan.Sebuah bilik bersih yang diperakui juga menanam keyakinan di kalangan pihak berkepentingan, memudahkan pemeriksaan peraturan, dan menyokong usaha pengembangan dengan mempamerkan pematuhan kepada amalan terbaik dalam menguruskan persekitaran terkawal.
Berapa kerap bilik bersih perlu dikualifikasi semula untuk memastikan pematuhan?
Bilik bersih perlu dikualifikasi semula secara berkala untuk memastikan ia memenuhi piawaian industri. Kekerapan ini bergantung kepada beberapa faktor, termasuk klasifikasi bilik bersih, cara ia digunakan, dan penemuan daripada penilaian risiko atau pelan pemantauan persekitaran.
Biasanya, pengkualifikasian semula dilakukan sekali setahun. Walau bagaimanapun, persekitaran berisiko tinggi atau situasi yang melibatkan perubahan besar - seperti peningkatan peralatan atau pelarasan susun atur - mungkin memerlukan pemeriksaan yang lebih kerap. Pemantauan prestasi yang berterusan juga penting untuk mengesahkan bahawa aliran udara, penapisan, dan kawalan persekitaran terus memenuhi piawaian yang diperlukan.
Apakah faktor persekitaran yang perlu dipantau dalam bilik bersih untuk pengeluaran daging yang diternak?
Untuk memastikan pematuhan dan mengurangkan risiko pencemaran di kemudahan daging yang diternak, adalah penting untuk memantau beberapa faktor persekitaran dengan teliti. Ini termasuk kiraan zarah, pencemaran mikrob, pola aliran udara, perbezaan tekanan udara, suhu, dan tahap kelembapan. Pemantauan berkala elemen-elemen ini membantu mengekalkan piawaian GMP dan mewujudkan persekitaran terkawal yang penting untuk pengeluaran.
Dengan menguruskan keadaan ini dengan teliti, kemudahan dapat melindungi kualiti produk sambil memenuhi kriteria ketat yang diperlukan untuk pensijilan bilik bersih.











