การทดสอบความปลอดเชื้อเป็นสิ่งสำคัญสำหรับการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ซึ่งแม้แต่การปนเปื้อนเล็กน้อยก็อาจนำไปสู่ความล้มเหลวของชุดการผลิตที่มีค่าใช้จ่ายสูง กระบวนการนี้ช่วยให้มั่นใจได้ว่าไม่มีจุลินทรีย์ที่เป็นอันตรายรบกวนการทำงานของเครื่องปฏิกรณ์ชีวภาพ ปกป้องทั้งคุณภาพของผลิตภัณฑ์และความสามารถในการทำกำไร ด้วยอัตราการปนเปื้อนเฉลี่ย 11.2% - และเพิ่มขึ้นเป็น 19.5% สำหรับการผลิตขนาดใหญ่ ผู้ผลิตต้องเผชิญกับความท้าทายที่สำคัญในการรักษาสภาพแวดล้อมที่ปลอดเชื้อ
ประเด็นสำคัญได้แก่:
- แหล่งที่มาของการปนเปื้อนหลัก: บุคลากร วัตถุดิบ และการดำเนินงานของเครื่องปฏิกรณ์ชีวภาพเป็นจุดเริ่มต้นทั่วไปสำหรับจุลินทรีย์
- วิธีการทดสอบ: การกรองผ่านเยื่อสำหรับปริมาณมาก การฉีดตรงสำหรับตัวอย่างขนาดเล็ก และการทดสอบปริมาณจุลินทรีย์ระหว่างการผลิตเป็นที่นิยมใช้กันอย่างแพร่หลาย
- การตรวจสอบแบบเรียลไทม์: เครื่องมือเช่นเซ็นเซอร์ออกซิเจนละลายและการวิเคราะห์ก๊าซที่ปล่อยออกมาช่วยให้สามารถตรวจจับกิจกรรมของจุลินทรีย์ได้ตั้งแต่เนิ่นๆ
- เทคโนโลยีที่เกิดขึ้นใหม่: การตรวจสอบด้วย AI, การฆ่าเชื้อด้วยพลาสมาเย็น, และระบบการถ่ายภาพอัตโนมัติ ช่วยให้การจัดการการปนเปื้อนรวดเร็วและแม่นยำยิ่งขึ้น
สำหรับผู้ผลิตเนื้อสัตว์ที่เพาะเลี้ยง การผสมผสานการทดสอบความปลอดเชื้อแบบดั้งเดิมกับโซลูชันการตรวจสอบขั้นสูงเป็นสิ่งสำคัญเพื่อลดความเสี่ยงและปรับปรุงประสิทธิภาพการผลิต
Rocker Discover - วิธีการทดสอบความปลอดเชื้อ?
sbb-itb-ffee270
แหล่งที่มาของการปนเปื้อนในระบบไบโอรีแอคเตอร์
เพื่อป้องกันความล้มเหลวของชุดการผลิตในระบบไบโอรีแอคเตอร์ การระบุแหล่งที่มาของการปนเปื้อนเป็นสิ่งสำคัญ โดยทั่วไปแล้วสารปนเปื้อนจะแบ่งออกเป็นสามประเภทหลัก: จุลินทรีย์, อนุภาค, และเอนโดท็อกซิน แต่ละประเภทมีความท้าทายเฉพาะสำหรับการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ทำให้จำเป็นต้องพัฒนากลยุทธ์การป้องกันเฉพาะเจาะจง
บุคลากรเป็นแหล่งปนเปื้อนหลัก มักนำสารปนเปื้อนเข้ามาผ่านการหลุดลอกของผิวหนัง การสวมใส่ชุดที่ไม่ถูกต้อง หรือการล้างมือที่ไม่ดี [4][7]. แม้จะมีมาตรการที่เข้มงวด การเคลื่อนไหวง่ายๆ ก็สามารถรบกวนการไหลของอากาศ ทำให้เกิดความปั่นป่วนหรือพื้นที่นิ่งที่สารปนเปื้อนสามารถสะสมได้ [4][9]. U.S. องค์การอาหารและยาเน้นย้ำถึงความเสี่ยงที่เกี่ยวข้อง โดยระบุว่า "การจัดการด้วยมือหรือเครื่องจักรใดๆ ของยาที่ผ่านการฆ่าเชื้อแล้ว ส่วนประกอบ ภาชนะ หรือฝาปิดก่อนหรือระหว่างการประกอบแบบปลอดเชื้อมีความเสี่ยงต่อการปนเปื้อนและจึงจำเป็นต้องมีการควบคุมอย่างระมัดระวัง" [4].
ปัจจัยด้านสิ่งแวดล้อมก็มีบทบาทสำคัญเช่นกัน.ตัวอย่างเช่น การไม่สามารถรักษาความดันบวกที่ 10–15 ปาสคาล อาจทำให้อากาศที่ไม่ได้กรองเข้าสู่เขตปลอดเชื้อได้ [3][4] นอกจากนี้ ปัญหาต่างๆ เช่น ประสิทธิภาพของแผ่นกรอง HEPA ที่ลดลง - ซึ่งการกักเก็บอนุภาคต่ำกว่า 99.97% - หรือแผ่นกรองก๊าซอัดที่เสียหาย สามารถทำให้ความปลอดเชื้อถูกทำลายได้อย่างรวดเร็ว [4].
การปนเปื้อนของวัตถุดิบและสายเซลล์
วัตถุดิบที่เข้าสู่ระบบเครื่องปฏิกรณ์ชีวภาพเป็นความเสี่ยงหลักของการปนเปื้อน ส่วนประกอบของวัตถุดิบที่ไม่ได้รับการตรวจสอบ ส่วนประกอบของสื่อการเจริญเติบโต และสายเซลล์ (ที่มีอยู่ผ่าน ตลาด B2B เฉพาะทาง) สามารถนำเชื้อโรคที่ฉวยโอกาสเข้ามาได้ [2] สภาพแวดล้อมที่อุดมด้วยสารอาหารของสื่อการเพาะเลี้ยงเซลล์มีความเสี่ยงต่อการปนเปื้อนเป็นพิเศษ ทำให้กระบวนการผลิตเนื้อสัตว์ที่เพาะเลี้ยงมีความเสี่ยงมากกว่ากระบวนการชีวภาพของจุลินทรีย์ [8]
ส่วนผสมที่ไวต่อความร้อนที่ไม่สามารถผ่านการฆ่าเชื้อด้วยเครื่องอบไอน้ำได้มีความเสี่ยงเป็นพิเศษ เนื่องจากต้องใช้วิธีการ ฆ่าเชื้อทางเลือกเช่นการกรอง [1] [8]. นอกจากนี้ กระบวนการฉีดเชื้อเองก็มีความเสี่ยงในตัว แม้ว่าเมมเบรนจะถูกฆ่าเชื้อด้วยแอลกอฮอล์หรือกระบวนการจะดำเนินการใกล้เปลวไฟเปิด ก็ไม่มีการรับประกันอย่างแน่นอนว่าจะไม่เกิดการปนเปื้อนในระหว่างการแนะนำสายเซลล์ [8]. ความเสี่ยงเหล่านี้เน้นย้ำถึงความสำคัญของการตรวจสอบวัตถุดิบอย่างละเอียดก่อนที่จะนำเข้าสู่ระบบ.
ความเสี่ยงในการดำเนินงานของเครื่องปฏิกรณ์ชีวภาพ
การดำเนินงานประจำวันภายในเครื่องปฏิกรณ์ชีวภาพมีโอกาสเกิดการปนเปื้อนมากมาย การสุ่มตัวอย่างด้วยมือมีความเสี่ยงสูงเป็นพิเศษ เนื่องจากทุกจุดเข้าถึงเพิ่มโอกาสในการนำสิ่งปนเปื้อนเข้าไป [1].ปัญหาต่างๆ เช่น ซีลที่ถูกทำลาย, โอริงที่เสียหาย, หรือการปิดที่ไม่ได้ผ่านการฆ่าเชื้อ ยิ่งเพิ่มความเสี่ยงมากขึ้น [4][8]. นอกจากนี้ การย้ายวัสดุจากพื้นที่ที่มีการจัดระดับต่ำกว่าไปยังพื้นที่ที่มีการจัดระดับสูงกว่าโดยไม่ผ่านการฆ่าเชื้ออย่างถูกต้องเป็นอีกหนึ่งช่องโหว่ที่สำคัญ [7].
การรักษาการควบคุมสิ่งแวดล้อมอย่างเข้มงวดเป็นสิ่งที่ไม่สามารถต่อรองได้ ความแตกต่างของความดันระหว่างพื้นที่ห้องสะอาดควรถูกตรวจสอบอย่างต่อเนื่อง และการเปลี่ยนแปลงที่ผิดปกติใดๆ ต้องถูกตรวจสอบทันที [4]. ในพื้นที่วิกฤต Class 100 (ISO 5) จำนวนอนุภาคที่มีขนาด ≥0.5 μm ต้องคงอยู่ต่ำกว่า 3,520 อนุภาคต่อหนึ่งลูกบาศก์เมตรในระหว่างการดำเนินงาน [4].นอกจากนี้ การพ่นละอองน้ำยาฆ่าเชื้อหรือแอลกอฮอล์ไอโซโพรพิล 70% ใกล้กับเครื่องเก็บตัวอย่างอากาศสามารถเพิ่มการอ่านค่าฝุ่นละอองได้ ในขณะที่การควบแน่นบนตัวกรองก๊าซอาจทำให้เกิดการอุดตันหรือส่งเสริมการเจริญเติบโตของจุลินทรีย์ [4][7].
ความเสี่ยงในการดำเนินงานเหล่านี้เน้นย้ำถึงความสำคัญของการใช้วิธีการทดสอบความปลอดเชื้อที่เข้มงวดเพื่อปกป้องกระบวนการของเครื่องปฏิกรณ์ชีวภาพ
วิธีการทดสอบความปลอดเชื้อสำหรับเครื่องปฏิกรณ์ชีวภาพ
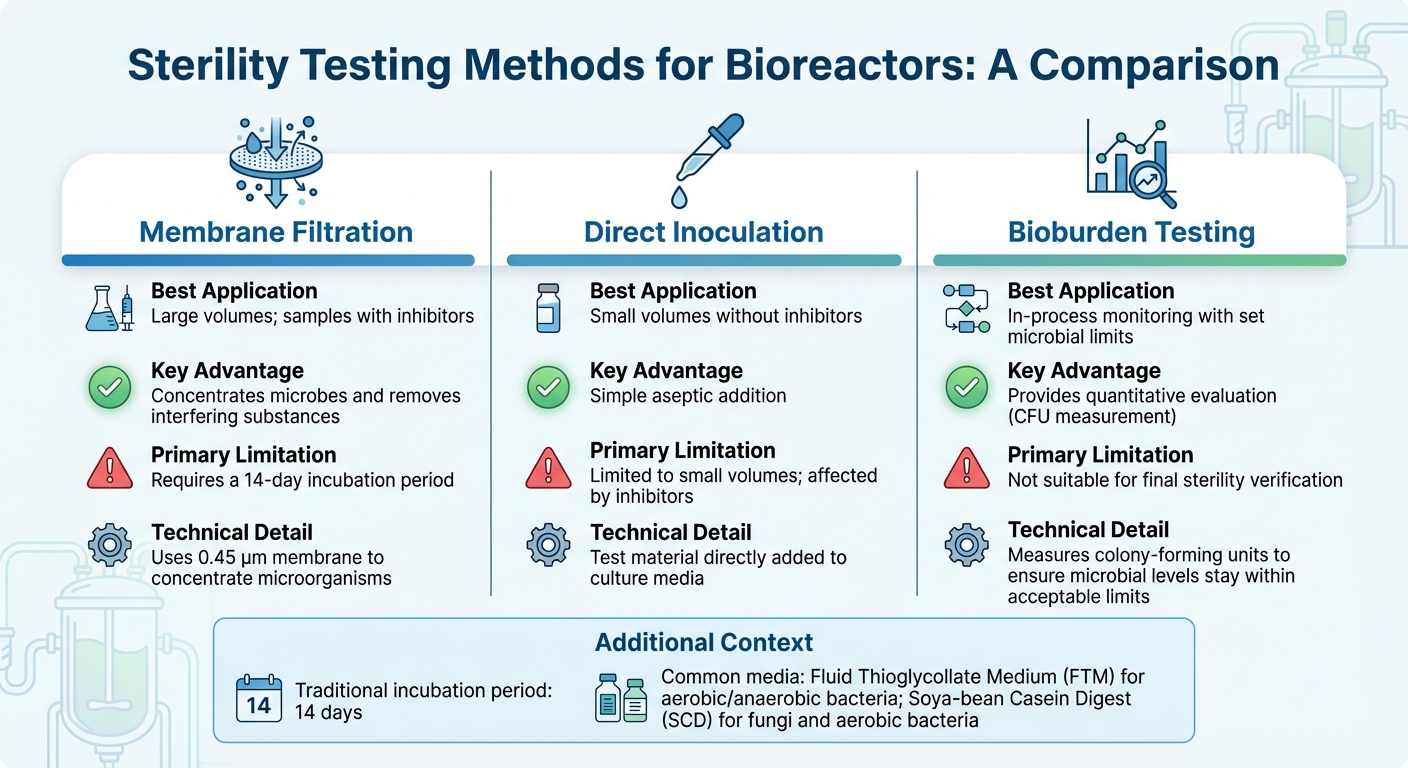
การเปรียบเทียบวิธีการทดสอบความปลอดเชื้อสำหรับเครื่องปฏิกรณ์ชีวภาพ
การเลือกวิธีทดสอบความปลอดเชื้อที่เหมาะสมสำหรับเครื่องปฏิกรณ์ชีวภาพขึ้นอยู่กับปัจจัยต่างๆ เช่น ขนาดของเครื่องปฏิกรณ์ชีวภาพ ขั้นตอนการผลิตและความท้าทายในการขยายขนาด และองค์ประกอบของตัวอย่าง - โดยเฉพาะเมื่อมีสารยับยั้งอยู่ สำหรับการใช้งานในอุตสาหกรรมส่วนใหญ่ การกรองผ่านเยื่อเมมเบรน เป็นวิธีที่นิยมใช้ [3] .ในขณะเดียวกัน เทคนิคทางโมเลกุลเช่น PCR เสนอการตรวจจับที่รวดเร็วขึ้นสำหรับสารปนเปื้อนเฉพาะ ด้านล่างนี้ เราจะสำรวจวิธีการที่ปรับให้เหมาะสมกับการผลิตเนื้อสัตว์ที่เพาะเลี้ยง โดยจัดการกับความท้าทายที่ไม่เหมือนใครของการทดสอบตัวอย่างทั้งขนาดใหญ่และขนาดเล็ก
สำหรับตัวอย่างปริมาณมาก ซึ่งพบได้ทั่วไปในเครื่องปฏิกรณ์ชีวภาพขนาดอุตสาหกรรม การกรองผ่านเยื่อเมมเบรน ใช้เยื่อเมมเบรนขนาด 0.45 µm เพื่อรวมจุลินทรีย์ เพิ่มความไวในการตรวจจับ [10] วิธีนี้มีประสิทธิภาพเป็นพิเศษสำหรับตัวอย่างที่มีสารปฏิชีวนะ เนื่องจากการล้างสามารถกำจัดสารยับยั้งก่อนการบ่ม ในทางกลับกัน การฉีดตรง ซึ่งวัสดุทดสอบถูกเพิ่มลงในสื่อเพาะเลี้ยงโดยตรง ทำงานได้ดีกว่าสำหรับปริมาณตัวอย่างที่เล็กกว่า แต่มีปัญหาในการจัดการกับสารยับยั้ง หลังจากรวมตัวอย่างและกำจัดสารยับยั้งแล้ว การบ่มและการตรวจสอบความถูกต้องจะช่วยให้มั่นใจในความถูกต้องของผลลัพธ์
การทดสอบความปลอดเชื้อแบบดั้งเดิมอาศัยระยะเวลาการบ่ม 14 วันเพื่อยืนยันการเจริญเติบโตของจุลินทรีย์ด้วยการมองเห็น [3]. สื่อที่ใช้กันทั่วไปได้แก่ Fluid Thioglycollate Medium (FTM) สำหรับแบคทีเรียที่ใช้ออกซิเจนและไม่ใช้ออกซิเจน และ Soya-bean Casein Digest (SCD) สำหรับเชื้อราและแบคทีเรียที่ใช้ออกซิเจน ก่อนทำการทดสอบความปลอดเชื้อใด ๆ จำเป็นต้องตรวจสอบให้แน่ใจว่าผลิตภัณฑ์ไม่ยับยั้งการเจริญเติบโตของจุลินทรีย์ผ่านการทดสอบการยับยั้งแบคทีเรียและเชื้อรา
สำหรับการตรวจสอบกระบวนการอย่างต่อเนื่อง การทดสอบปริมาณจุลินทรีย์ (quantitative bioburden testing) เสนอวิธีแก้ปัญหาที่ใช้งานได้จริงมากกว่าการทดสอบความปลอดเชื้อแบบไบนารี โดยเฉพาะในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง แตกต่างจากการทดสอบความปลอดเชื้อที่ให้ผลลัพธ์แบบผ่าน/ไม่ผ่าน การทดสอบปริมาณจุลินทรีย์วัดหน่วยสร้างอาณานิคม (CFU) เพื่อให้แน่ใจว่าระดับจุลินทรีย์อยู่ในขอบเขตที่ยอมรับได้วิธีการนี้สอดคล้องกับมาตรฐานอาหารที่เกิดขึ้นใหม่ โดยสร้างสมดุลระหว่างการควบคุมทางเภสัชกรรมที่เข้มงวดและความเป็นจริงทางเศรษฐกิจของการผลิตอาหารขนาดใหญ่
สำหรับอุปกรณ์ทดสอบความปลอดเชื้อและโซลูชันไบโอรีแอคเตอร์ ผู้เชี่ยวชาญด้านเนื้อสัตว์เพาะเลี้ยงสามารถหันไปหาผู้ให้บริการที่เชื่อถือได้ เช่น
| วิธีการ | การใช้งานที่ดีที่สุด | ข้อได้เปรียบหลัก | ข้อจำกัดหลัก |
|---|---|---|---|
| การกรองด้วยเมมเบรน | ปริมาณมาก; ตัวอย่างที่มีสารยับยั้ง | เข้มข้นจุลินทรีย์และกำจัดสารรบกวน[3] | ต้องใช้ระยะเวลาบ่ม 14 วัน[3] |
| การฉีดโดยตรง | ปริมาณน้อยที่ไม่มีสารยับยั้ง | การเติมแบบปลอดเชื้อที่ง่าย | จำกัดเฉพาะปริมาณน้อย; ได้รับผลกระทบจากสารยับยั้ง[3] |
| การทดสอบปริมาณจุลินทรีย์ | การตรวจสอบระหว่างกระบวนการด้วยขีดจำกัดจุลินทรีย์ที่กำหนด | ให้การประเมินเชิงปริมาณ | ไม่เหมาะสำหรับการตรวจสอบความปลอดเชื้อขั้นสุดท้าย [3] |
การตรวจสอบแบบเรียลไทม์และการรับรองความปลอดเชื้อ
การพึ่งพาการทดสอบความปลอดเชื้อแบบดั้งเดิมที่ใช้เวลา 14 วันมาพร้อมกับความเสี่ยงที่จะสูญเสียทั้งชุดหากพบการปนเปื้อนช้าเกินไปการตรวจสอบแบบเรียลไทม์นำเสนอวิธีการแก้ปัญหาเชิงรุกโดยการเฝ้าดูพารามิเตอร์กระบวนการที่สำคัญในขณะที่เกิดขึ้น ซึ่งช่วยให้สามารถดำเนินการได้ทันทีหากมีสิ่งผิดปกติเกิดขึ้น ในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ซึ่งการทำงานของเครื่องปฏิกรณ์ชีวภาพใช้เวลาหลายสัปดาห์และใช้สื่อการเจริญเติบโตที่มีค่าใช้จ่ายสูง การตรวจพบการปนเปื้อนในระยะแรกสามารถประหยัดเงินได้หลายพันปอนด์และหลีกเลี่ยงความล่าช้าในการผลิต โดยการรวมข้อมูลแบบเรียลไทม์กับการทดสอบความปลอดเชื้อแบบดั้งเดิม ผู้ผลิตสามารถเชื่อมช่องว่างระหว่างการยืนยันที่ล่าช้าและการแทรกแซงอย่างรวดเร็ว
การตรวจสอบด้วยเซ็นเซอร์
ตัวบ่งชี้สำคัญเช่นระดับออกซิเจนละลาย (DO) และระดับ pH สามารถส่งสัญญาณการปนเปื้อนได้ในระยะแรก เมื่อแบคทีเรียหรือเชื้อราบุกเข้าไปในเครื่องปฏิกรณ์ชีวภาพ พวกมันจะบริโภคออกซิเจนอย่างรวดเร็ว - ทำให้ระดับ DO ลดลง - และปล่อยกรดเมตาบอลิกที่ลด pH ลงอย่างมาก [12] การเปลี่ยนแปลงเหล่านี้สามารถตรวจพบได้หลายชั่วโมงก่อนที่การปนเปื้อนจะปรากฏให้เห็นได้ชัดเจนในขณะที่การทดสอบความปลอดเชื้อแบบดั้งเดิมยืนยันผลลัพธ์หลังจากกระบวนการเสร็จสิ้น การตรวจสอบแบบเรียลไทม์ทำหน้าที่เป็นการป้องกัน เพื่อให้แน่ใจว่ากระบวนการดำเนินไปตามแผนและจัดการความเสี่ยงจากการปนเปื้อนล่วงหน้า
การวิเคราะห์ก๊าซที่ปล่อยออกมา โดยใช้แมสสเปกโตรเมตรีแบบเซกเตอร์แม่เหล็ก วัดระดับออกซิเจนและคาร์บอนไดออกไซด์ในก๊าซไอเสียของไบโอรีแอคเตอร์อย่างต่อเนื่อง ในการศึกษาการปนเปื้อนที่ควบคุมได้ วิธีนี้สามารถระบุการเจริญเติบโตของจุลินทรีย์ภายใน 22.4 ชั่วโมงผ่านการเปลี่ยนแปลงของออกซิเจน ในขณะที่การตรวจจับด้วยค่า pH ล่าช้ากว่าอยู่ที่ 25.8 ชั่วโมง [13] ระบบเซกเตอร์แม่เหล็กให้การวัดออกซิเจนที่แม่นยำด้วยความแม่นยำสูงถึง 0.003% (v/v) ในระยะเวลาเจ็ดวัน ซึ่งดีกว่าตัวตรวจจับพาราแมกเนติกแบบดั้งเดิมที่มีความแม่นยำเพียง ±0.2% (v/v) [13].
เซ็นเซอร์สเปกโตรสโกปี ให้การตรวจสอบแบบไม่รุกล้ำผ่านผนังของไบโอรีแอคเตอร์แบบใช้ครั้งเดียว ซึ่งมีความสำคัญต่อการรักษาความปลอดเชื้อสามารถตรวจจับความเสียหายของเยื่อหุ้มเซลล์ได้โดยการวัดการดูดซับแสงที่ 350–400 นาโนเมตร ในขณะที่วัสดุภายในเซลล์ที่รั่วไหลจะปรากฏที่ 800–900 นาโนเมตร [14]. โพรบวัดความจุไฟฟ้า ซึ่งเป็นเซ็นเซอร์ที่มีจำหน่ายในเชิงพาณิชย์เพียงชนิดเดียวที่ออกแบบมาเพื่อวัดความหนาแน่นของเซลล์ที่มีชีวิต ทำได้โดยการตรวจจับการเปลี่ยนแปลงของการมีขั้วของเยื่อหุ้มเซลล์ [14]. สำหรับสถานที่ที่จัดการเครื่องปฏิกรณ์ชีวภาพหลายเครื่อง เครื่องมือเช่น Rapid Multi-Stream Sampler สามารถตรวจสอบกระแสก๊าซได้ถึง 16 สายพร้อมกัน [13].
ระบบที่ใช้เซ็นเซอร์เหล่านี้ เมื่อรวมกับการควบคุมสิ่งแวดล้อม เช่น การป้องกันการปนเปื้อนของ HVAC สร้างการป้องกันที่แข็งแกร่งต่อการปนเปื้อน.
การควบคุมสิ่งแวดล้อมและความดัน
การรักษาความดันบวกระหว่างโซนห้องสะอาดเป็นสิ่งสำคัญในการป้องกันไม่ให้สารปนเปื้อนเข้ามา [3].ระบบแรงดันบวก เมื่อจับคู่กับการกรอง HEPA จะทำหน้าที่เป็นเกราะป้องกันทางกายภาพต่อการบุกรุกของจุลินทรีย์ สัญญาณเตือนที่ได้ยินหรือมองเห็นบนตัวกรอง HEPA สามารถแจ้งเตือนพนักงานได้ทันทีหากแรงดันลดลงต่ำกว่าระดับที่ยอมรับได้ [3].
การนับอนุภาคที่ไม่สามารถมีชีวิตได้ เป็นอีกชั้นหนึ่งของการป้องกัน เครื่องนับอนุภาคเลเซอร์ตรวจสอบอย่างต่อเนื่องว่าสภาพแวดล้อมเป็นไปตามมาตรฐานความสะอาดของอากาศ ISO ระหว่างการดำเนินงาน โดยการตรวจสอบอนุภาคขนาด 0.5 µm และ 5.0 µm อุปกรณ์เหล่านี้จะรับรองว่าคุณภาพอากาศยังคงอยู่ในขอบเขตที่กำหนด [7] หากเกิดการเบี่ยงเบนที่ไม่คาดคิด เช่น การลดลงของ DO อย่างกะทันหันหรือความผันผวนของ pH การแยกตัวของไบโอรีแอคเตอร์ที่ได้รับผลกระทบและการหยุดการเติมอาหารทันทีสามารถป้องกันการแพร่กระจายของการปนเปื้อนได้ [12].
สำหรับการจัดหาตัวเซ็นเซอร์และอุปกรณ์เฉพาะทางที่ปรับให้เหมาะสมกับการดำเนินงานเนื้อสัตว์ที่เพาะเลี้ยง บริษัทต่างๆ เช่น
เทคโนโลยีใหม่ในการทดสอบความปลอดเชื้อ
วิธีการทดสอบความปลอดเชื้อแบบดั้งเดิมมักจะไม่เพียงพอเนื่องจากระยะเวลาการบ่ม 14 วันที่ยาวนานและการพึ่งพาการสุ่มตัวอย่างด้วยตนเอง ซึ่งอาจทำให้เกิดช่องว่างในการตรวจจับได้ เทคโนโลยีใหม่กำลังเข้ามาแก้ไขปัญหาเหล่านี้ โดยเสนอการตรวจจับการปนเปื้อนที่รวดเร็วและแม่นยำยิ่งขึ้น ซึ่งมีความสำคัญอย่างยิ่งในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ซึ่งต้นทุนสูงของสื่อการเจริญเติบโตและระยะเวลาการเพาะเลี้ยงที่ยาวนานทำให้การปนเปื้อนในระยะสุดท้ายเป็นฝันร้ายทางการเงิน
ระบบการตรวจสอบที่ขับเคลื่อนด้วย AI
ปัญญาประดิษฐ์กำลังเปลี่ยนแปลงการตรวจจับการปนเปื้อนโดยการวิเคราะห์ข้อมูลแบบเรียลไทม์เพื่อระบุการบุกรุกของจุลินทรีย์เมื่อแบคทีเรียบุกรุกไบโอรีแอคเตอร์ พวกมันจะบริโภคออกซิเจนและผลิตกรดเมตาบอลิก ทำให้ระดับออกซิเจนละลายและค่า pH ลดลงอย่างเห็นได้ชัด ระบบ AI สามารถตรวจจับ การเบี่ยงเบนในการบริโภคออกซิเจนและสารอาหาร โดยระบุการปนเปื้อนที่อาจเกิดขึ้นได้เร็วกว่าการทดสอบ การปนเปื้อนทางชีวภาพและโปรโตคอลความปลอดเชื้อ แบบดั้งเดิม [12].
แพลตฟอร์ม AI เหล่านี้ยังรวมโมเดลทางคณิตศาสตร์เพื่อ ระบุเวลาที่เกิดการปนเปื้อน และจำลองการเติบโตของประชากรจุลินทรีย์เมื่อเวลาผ่านไป ซึ่งช่วยให้ผู้ปฏิบัติงานสามารถติดตามการปนเปื้อนไปยังแหล่งที่มา ไม่ว่าจะเป็นแหล่งอาหารที่มีปัญหา ความผิดพลาดในการดำเนินงาน หรือปัญหาอุปกรณ์ เทคนิคเช่นการวิเคราะห์ความน่าจะเป็นของปัวซองยังช่วยเพิ่มความแม่นยำในการทดสอบการปนเปื้อนทางชีวภาพ ลดโอกาสของผลลบเท็จ [12].
"แบบจำลองทางคณิตศาสตร์ช่วยในการประมาณเวลาการปนเปื้อนและการเจริญเติบโตของจุลินทรีย์ ทำให้การติดตามการปนเปื้อนมีประสิทธิภาพมากขึ้น" - Naveenganesh Muralidharan, ผู้จัดการอาวุโส, MSAT, AGC Biologics [12]
เมื่อมีการแจ้งเตือนความผิดปกติ การดำเนินการทันที - เช่น การแยกไบโอรีแอคเตอร์และหยุดการเติมอาหารทั้งหมด - สามารถป้องกันปัญหาจากการแพร่กระจาย [12]. การใช้วิธีการอย่างเป็นระบบที่รวมถึงการทดสอบการปนเปื้อน, การระบุโมเลกุล, และการวิเคราะห์อัตราการเจริญเติบโตเป็นสิ่งจำเป็นสำหรับการระบุสาเหตุที่แท้จริงและการดำเนินการแก้ไข เครื่องมือ AI เหล่านี้เชื่อมช่องว่างระหว่างวิธีการแบบดั้งเดิมและการจัดการการปนเปื้อนเชิงรุก.
การฆ่าเชื้อด้วยพลาสมาเย็น
เทคโนโลยีพลาสมาเย็นเสนอทางเลือกการฆ่าเชื้อที่ไม่ใช้ความร้อนซึ่งเหมาะสมอย่างยิ่งสำหรับการผลิตเนื้อสัตว์ที่เพาะเลี้ยง.ทำงานที่หรือใกล้เคียงกับอุณหภูมิห้อง มันเหมาะสำหรับการฆ่าเชื้อ ชิ้นส่วนที่ไวต่อความร้อน เช่น ชิ้นส่วนของไบโอรีแอคเตอร์, เซ็นเซอร์, และพลาสติก ที่ไม่สามารถทนต่อความร้อนของการฆ่าเชื้อด้วยออโตเคลฟแบบดั้งเดิม [15][16] [17]. วิธีนี้ใช้อนุพันธ์ออกซิเจนและไนโตรเจนที่มีปฏิกิริยา พร้อมกับแสงยูวี เพื่อทำลายเยื่อหุ้มเซลล์และดีเอ็นเอของจุลชีพ มันมีประสิทธิภาพต่อสารปนเปื้อนหลากหลายชนิด รวมถึงสปอร์ของแบคทีเรีย (Bacillus, Clostridium), เชื้อรา, ไวรัส, และแม้กระทั่งพรีออน [15][17].
หนึ่งในคุณสมบัติเด่นของพลาสมาเย็นคือมันไม่ทิ้ง สารตกค้างที่เป็นพิษ. เมื่อปิดเครื่องแล้ว อนุพันธ์ที่มีปฏิกิริยาจะกลับคืนสู่สภาพออกซิเจนอย่างรวดเร็ว ทำให้ไม่จำเป็นต้องมีขั้นตอนการดูดซับ [16][18].นอกจากนี้ยังประหยัดพลังงาน โดยต้องการเพียงเต้าเสียบไฟฟ้ามาตรฐานแทนแหล่งความร้อนที่ใช้เชื้อเพลิงฟอสซิล [15][16]. ตัวอย่างเช่น การศึกษาพบว่า พลาสมาเย็นสามารถลด >5 log ของสปอร์ Bacillus cereus ภายใน 25 นาที ที่กำลังไฟ 300W [15].
อย่างไรก็ตาม เทคโนโลยีนี้ไม่ได้ปราศจากข้อจำกัด ผลของการฆ่าเชื้อส่วนใหญ่จะอยู่ที่ ระดับผิวหน้า ซึ่งหมายความว่ามันมีปัญหาในการเจาะเข้าไปในรูปทรงที่ซับซ้อนที่จุลินทรีย์อาจซ่อนตัวอยู่ในรอยแตกหรือร่อง [15][16]. ปริมาณโปรตีนหรือไขมันสูงในสภาพแวดล้อมของเครื่องปฏิกรณ์ชีวภาพยังสามารถป้องกันจุลินทรีย์โดยการเก็บกวาดชนิดที่ทำปฏิกิริยา ลดประสิทธิภาพของการฆ่าเชื้อ [15][18].
| คุณสมบัติ | พลาสมาเย็น |
|---|---|
| ข้อดี | ไม่ใช้ความร้อน, ไม่เป็นพิษ, ประหยัดพลังงาน, ไม่มีสารตกค้าง, รวดเร็ว[16] |
| ข้อจำกัด | การแทรกซึมจำกัด, ประสิทธิภาพลดลงในรูปทรงที่ซับซ้อน[15][16] |
ระบบตรวจจับภาพอัตโนมัติ
การเพิ่มระบบภาพอัตโนมัติเป็นเครื่องมือที่ทรงพลังสำหรับการตรวจจับการปนเปื้อนแบบเรียลไทม์ ระบบเหล่านี้ให้ข้อมูลเชิงลึกทางสัณฐานวิทยาอย่างละเอียดเกี่ยวกับการเจริญเติบโตของเซลล์ซึ่งมีความสำคัญต่อการระบุรูปแบบการปนเปื้อนขณะที่เกิดขึ้น[19].ไม่เหมือนกับกล้องจุลทรรศน์แบบออฟไลน์แบบดั้งเดิม - ซึ่งต้องการการเก็บตัวอย่างและการย้อมสีด้วยมือ - การถ่ายภาพอัตโนมัติสามารถผสานเข้ากับการตั้งค่าการตรวจสอบออนไลน์หรือที่สายได้อย่างราบรื่น สิ่งนี้ช่วยให้ผู้ปฏิบัติงานสามารถตรวจสอบชีวมวลและสุขภาพของเซลล์โดยไม่กระทบต่อความปลอดเชื้อ [19].
โดยการลดการแทรกแซงด้วยมือ ระบบเหล่านี้ช่วยลดข้อผิดพลาดของมนุษย์และปรับปรุงความสามารถในการทำซ้ำในกระบวนการเพาะเลี้ยง [19]. อัลกอริธึมการประมวลผลภาพขั้นสูงสามารถติดตามความก้าวหน้าของการหมัก ปรับปรุงการผลิตเมตาโบไลต์ และรับประกันความสม่ำเสมอ - ซึ่งเป็นปัจจัยสำคัญเมื่อขยายกระบวนการชีวภาพ [19].
"การมีอยู่ของเทคนิคการเก็บตัวอย่างขั้นสูงที่รวมกับเครื่องมือวัดอัตโนมัติ...อาจลดเวลาที่จำเป็นสำหรับการเลือกสายพันธุ์ การพัฒนากระบวนการ และการควบคุมกระบวนการได้อย่างมากโดยลดจำนวนขั้นตอนในกระบวนการผลิต/การเพาะเลี้ยง โดยเฉพาะขั้นตอนที่ทำด้วยมือ และลดการแพร่กระจายของข้อผิดพลาด" - A.C. Veloso และ E.C. Ferreira, มหาวิทยาลัย Minho [19]
แม้จะมีข้อดีของพวกเขา การรวมระบบเหล่านี้ไม่ใช่เรื่องง่ายเสมอไป การเพาะเลี้ยงเซลล์มีความซับซ้อน วัตถุดิบมีความหลากหลาย และเซ็นเซอร์ต้องทนต่อวิธีการฆ่าเชื้อที่รุนแรงเช่นการอบไอน้ำหรือการฉายรังสีแกมมา [19]. สำหรับบริษัทที่ต้องการนำเทคโนโลยีเหล่านี้มาใช้ แพลตฟอร์มเช่น
บทสรุป
การรับรองความปลอดเชื้อของเครื่องปฏิกรณ์ชีวภาพในการผลิตเนื้อสัตว์เพาะเลี้ยงไม่ใช่เรื่องง่าย แต่กลยุทธ์การทดสอบความปลอดเชื้อแบบบูรณาการสามารถทำให้เป็นไปได้This strategy blends traditional methods, like membrane filtration for larger sample volumes and direct inoculation for smaller ones, with modern molecular tools such as PCR and qPCR for quick pathogen screening. Additionally, environmental monitoring - via air sampling and surface swabbing - adds an extra safeguard, addressing contamination risks in HVAC systems, catching potential contamination before it can impact production vessels [11].
The choice of testing approach hinges on factors like sample size, the presence of substances that might interfere with results, and whether the focus is on full sterility validation or simply monitoring bioburden. Sampling from multiple points in the bioreactor - top, middle, and bottom - helps create a thorough microbial profile and reduces the chance of missing localised contamination [1].สิ่งนี้มีความสำคัญอย่างยิ่งเนื่องจากความเสี่ยงของการปนเปื้อนในการผลิตเนื้อสัตว์เพาะเลี้ยงสูงกว่าการผลิตยาชีวภาพอย่างเห็นได้ชัด ซึ่งเน้นย้ำถึงความจำเป็นในการใช้โปรโตคอลความปลอดเชื้อที่เข้มงวด [6].
กุญแจสำคัญในการรักษา ความปลอดเชื้อของสื่อในเครื่องปฏิกรณ์ชีวภาพ คือการจัดหาอุปกรณ์ที่เหมาะสม เครื่องมือเช่นระบบสุ่มตัวอย่างปลอดเชื้อที่มีฝาปิดที่ผ่านการฆ่าเชื้อล่วงหน้าและตัวกรอง HEPA ที่สามารถดักจับอนุภาคขนาดใหญ่กว่า 0.3 μm ได้ถึง 99.97% เป็นสิ่งจำเป็น [4]. แพลตฟอร์มเช่น
เมื่ออุตสาหกรรมเติบโตขึ้น แนวทางความปลอดเชื้อแบบผสมผสานจึงมีความสำคัญมากขึ้นเรื่อยๆ การใช้การควบคุมระดับเภสัชกรรมในช่วงเริ่มต้นของการเพาะเลี้ยงเมล็ดพันธุ์ ในขณะที่ใช้มาตรฐานระดับอาหารสำหรับการผลิตขนาดใหญ่ เป็นการสร้างสมดุลระหว่างความปลอดภัยและความคุ้มค่า [5] [6] มาตรการแบบบูรณาการเหล่านี้จะเป็นรากฐานของการผลิตเนื้อสัตว์เพาะเลี้ยงที่ปลอดภัยและมีประสิทธิภาพเมื่อสาขานี้ยังคงก้าวหน้า
คำถามที่พบบ่อย
สาเหตุหลักของการปนเปื้อนในระบบเครื่องปฏิกรณ์ชีวภาพที่ใช้ในการผลิตเนื้อสัตว์เพาะเลี้ยงคืออะไร
การปนเปื้อนในระบบเครื่องปฏิกรณ์ชีวภาพเกิดขึ้นเมื่อสภาพแวดล้อมที่ปลอดเชื้อถูกทำลายหรือเมื่อสื่อที่อุดมด้วยสารอาหารให้สภาพแวดล้อมที่เหมาะสมสำหรับจุลินทรีย์ในการเจริญเติบโต สิ่งนี้อาจเกิดจากหลายปัจจัย เช่น การรั่วไหลระหว่างการสุ่มตัวอย่าง การบำรุงรักษา หรือการเก็บเกี่ยวเซลล์; ตัวกรองก๊าซที่เสียหายหรืออุดตัน; การปนเปื้อนที่มีอยู่แล้วในสื่อการเจริญเติบโต; หรือการเปิดชั่วคราวที่เกิดขึ้นเมื่อทำการติดตั้งหรือบำรุงรักษาเซ็นเซอร์นอกจากนี้ อุปกรณ์ที่สึกหรอสามารถปล่อยอนุภาคไมโครพลาสติก ซึ่งอาจเป็นที่อยู่อาศัยของจุลินทรีย์ได้
ในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง แม้แต่การปนเปื้อนที่เล็กที่สุดก็สามารถทำลายทั้งความปลอดภัยและผลผลิตของชุดการผลิตได้ เพื่อลดความเสี่ยงเหล่านี้ จำเป็นต้องลงทุนในอุปกรณ์คุณภาพสูง เช่น ตัวกรองปลอดเชื้อ เครื่องปฏิกรณ์ชีวภาพ และชุดเซ็นเซอร์ที่เป็นไปตามมาตรฐานปลอดเชื้อที่เข้มงวด แพลตฟอร์มเช่น
ปัญญาประดิษฐ์ช่วยเพิ่มประสิทธิภาพการทดสอบความปลอดเชื้อในเครื่องปฏิกรณ์ชีวภาพได้อย่างไร
ระบบที่ขับเคลื่อนด้วย AI กำลังเปลี่ยนแปลงการทดสอบความปลอดเชื้อในเครื่องปฏิกรณ์ชีวภาพสำหรับเนื้อสัตว์ที่เพาะเลี้ยง โดยให้ข้อมูลเชิงลึกแบบเรียลไทม์ผ่านการตรวจสอบอย่างต่อเนื่องการใช้เซ็นเซอร์ชีวภาพขั้นสูง ระบบเหล่านี้ติดตามปัจจัยสำคัญเช่น pH , ออกซิเจนละลาย, และเมตาบอไลต์ที่จำเป็นเช่นกลูโคสและกรดอะมิโน ทั้งหมดนี้เกิดขึ้นโดยไม่ต้องตรวจสอบด้วยตนเอง ซึ่งช่วยลดความเสี่ยงของการปนเปื้อนอย่างมาก
สิ่งที่ทำให้ระบบเหล่านี้แตกต่างคือความสามารถในการวิเคราะห์ข้อมูลโดยใช้อัลกอริทึมที่เปรียบเทียบการอ่านค่ากับมาตรฐานความปลอดเชื้อที่กำหนดไว้ ซึ่งหมายความว่าพวกเขาสามารถตรวจจับสัญญาณการเจริญเติบโตของจุลินทรีย์ที่เล็กที่สุดได้เร็วกว่าวิธีการแบบดั้งเดิม นอกเหนือจากการตรวจจับแล้ว การวิเคราะห์เชิงคาดการณ์ยังมีบทบาทในการระบุความเสี่ยงที่อาจเกิดขึ้น เช่น ปัญหาระหว่างการติดตั้งเซ็นเซอร์หรือการเข้าออกผ่านพอร์ต ระบบเหล่านี้ยังแนะนำมาตรการแก้ไขเพื่อช่วยให้ผู้ผลิตหลีกเลี่ยงการสูญเสียแบทช์ที่มีค่าใช้จ่ายสูง
การใช้กล้องจุลทรรศน์ที่ขับเคลื่อนด้วย AI เพิ่มประสิทธิภาพอีกชั้นหนึ่งโดยการแยกแยะระหว่างเซลล์ที่แข็งแรงและสารปนเปื้อนได้ทันที เร่งกระบวนการตรวจสอบความปลอดเชื้อสำหรับผู้ผลิต แพลตฟอร์มเช่น
ความท้าทายใดที่จำกัดการใช้การฆ่าเชื้อด้วยพลาสมาเย็นในเครื่องปฏิกรณ์ชีวภาพสำหรับการผลิตเนื้อสัตว์ที่เพาะเลี้ยง?
การฆ่าเชื้อด้วยพลาสมาเย็นมีประสิทธิภาพในการทำลายจุลินทรีย์ แต่มีความท้าทายเมื่อใช้กับเครื่องปฏิกรณ์ชีวภาพในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ปัญหาหลักคือความลึกของการแทรกซึมที่จำกัดของสารที่เกิดจากพลาสมา ซึ่งทำให้ยากต่อการฆ่าเชื้อในปริมาณมากหรือสื่อที่มีความหนาแน่นสูงอย่างทั่วถึง นอกจากนี้ การทำให้ครอบคลุมพลาสมาอย่างสม่ำเสมอทั่วทั้งเครื่องปฏิกรณ์จะยากขึ้นเมื่อขนาดของระบบเพิ่มขึ้น
การขยายระบบพลาสมาเย็นจากการตั้งค่าในห้องปฏิบัติการไปยังเครื่องปฏิกรณ์ชีวภาพในระดับการค้าเพิ่มอุปสรรคเพิ่มเติมเครื่องปฏิกรณ์ขนาดใหญ่ต้องการอัตราส่วนพลังงานต่อปริมาตรที่สูงขึ้น ซึ่งอาจส่งผลให้เวลาการฆ่าเชื้อไม่เป็นไปตามที่คาดหวัง ระบบพลาสมาเย็นหลายระบบยังทำงานภายใต้สภาวะสุญญากาศหรือพึ่งพาแก๊สที่มีปฏิกิริยา ซึ่งเพิ่มความซับซ้อนในแง่ของความปลอดภัย การปฏิบัติตามกฎระเบียบ และการออกแบบอุปกรณ์ ปัจจัยเหล่านี้ทำให้วิธีการนี้ไม่เหมาะสำหรับเครื่องปฏิกรณ์ชีวภาพขนาดใหญ่ที่จำเป็นในกระบวนการผลิตเนื้อสัตว์เพาะเลี้ยงเชิงพาณิชย์ อีกหนึ่งข้อกังวลคือความเสียหายที่อาจเกิดจากอนุพันธ์ออกซิเจนและไนโตรเจนที่มีปฏิกิริยา (RONS) ซึ่งเป็นกุญแจสำคัญในการทำลายจุลินทรีย์ อนุพันธ์ที่มีปฏิกิริยาเหล่านี้สามารถทำลายเซลล์สัตว์เลี้ยงลูกด้วยนมที่ไวต่อการกระทบหรือทำให้ส่วนประกอบของสื่อเสื่อมสภาพ จำเป็นต้องมีการปรับแต่งอย่างระมัดระวังเพื่อรักษาความมีชีวิตของเซลล์ ดังนั้น พลาสมาเย็นมักถูกใช้ร่วมกับเทคนิคการฆ่าเชื้ออื่น ๆ แทนที่จะใช้เป็นวิธีการเดียว











