الانتقال بالخلايا إلى وسط خالٍ من المصل (SFM) أمر حيوي لإنتاج اللحوم المزروعة بشكل أخلاقي وقابل للتوسع. هذه العملية تقضي على المصل المشتق من الحيوانات، مما يقلل من مخاطر التلوث ويضمن بيئة متسقة لنمو الخلايا. ومع ذلك، فإنها تأتي مع تحديات مثل استنفاد المغذيات، التحولات الأيضية، والحفاظ على حيوية الخلايا. تلعب أدوات المراقبة مثل قياس التدفق الخلوي، علم الأيض، وعلم النسخ دورًا رئيسيًا في التغلب على هذه التحديات من خلال تتبع صحة الخلايا، واستخدام المغذيات، وتغيرات التعبير الجيني.
النقاط الرئيسية:
- لماذا يهم: يضمن SFM التناسق، يقلل من مخاطر التلوث, ويتوافق مع المعايير الأخلاقية.
- التحديات: الخلايا في SFM حساسة للضغوط مثل تغيرات الأس الهيدروجيني، استنفاد المغذيات، والقوى الميكانيكية.
-
أدوات المراقبة:
- قياس التدفق الخلوي: يتتبع حيوية الخلايا وعلامات الاستماتة.
- علم الأيض: يحلل استهلاك المغذيات والتحولات الأيضية.
- علم النسخ: يفحص تغييرات التعبير الجيني في المسارات الرئيسية.
- التطبيقات: تساعد البيانات من هذه الأدوات في تحسين تركيبات الوسائط, تقليل التكاليف وتحسين نمو الخلايا.
نظرة سريعة:
توفر أدوات مثل HPLC، مطياف الكتلة، وأجهزة الاستشعار الفورية بيانات قابلة للتنفيذ لتحسين الانتقالات الخالية من المصل. تسهل المنصات مثل
الثقافات الخالية من المصل: لماذا وكيف؟ (فبراير 2022)
sbb-itb-ffee270
الأدوات التحليلية للتكيف الخالي من المصل
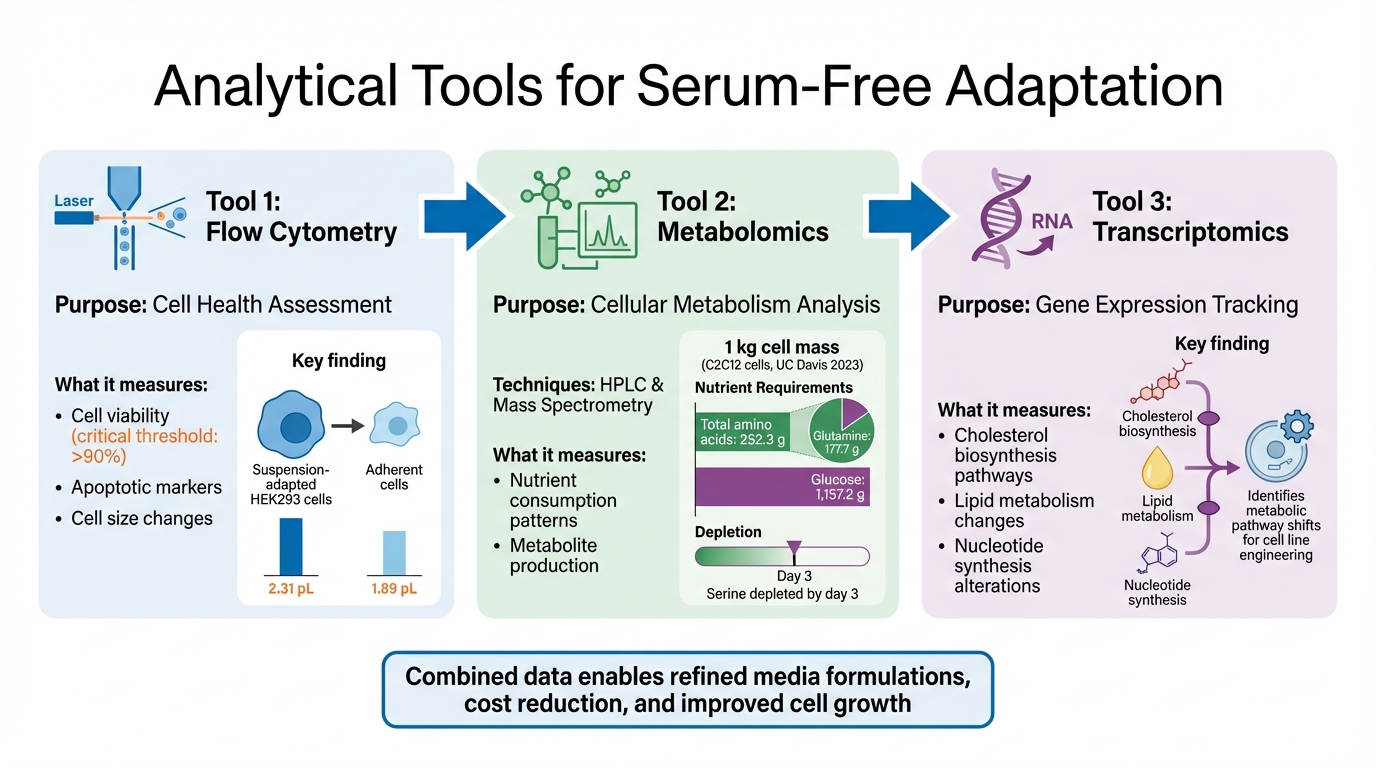
ثلاثة أدوات تحليلية رئيسية لمراقبة تكيف الخلايا الخالية من المصل
قياس التدفق الخلوي لتقييم صحة الخلايا
يعد قياس التدفق الخلوي أداة قوية لتقييم حيوية الخلايا والصحة العامة بسرعة أثناء التكيف الخالي من المصل. الحفاظ على حيوية الخلايا العالية أمر حاسم لنجاح عملية التكيف[1]. تكتشف هذه الطريقة أيضًا علامات الاستماتة وتتابع التغيرات في حجم الخلايا. على سبيل المثال، تظهر الأبحاث أن خلايا HEK293 المعلقة المتكيفة تميل إلى أن تكون ذات أحجام أكبر، بمتوسط حوالي 2.31 بيكولتر مقارنة بـ 1.89 بيكولتر في نظيراتها الملتصقة[1]. توفر هذه الرؤى صورة أوضح لسلوك الخلايا أثناء التكيف.ما وراء ذلك، يوفر علم الميتابولوميات نظرة أعمق في التحولات الأيضية التي تكمن وراء هذه التغييرات.
الميتابولوميات لتحليل الأيض الخلوي
يركز علم الميتابولوميات على تحليل استخدام المغذيات وإنتاج المستقلبات، مما يوفر رؤية مفصلة للأيض الخلوي خلال التكيف بدون مصل. تعتبر تقنيات مثل HPLC وقياس الطيف الكتلي ذات قيمة كبيرة في تحديد أنماط استهلاك المغذيات ومخرجات المستقلبات. هذه النتائج ضرورية لـ ضبط تركيبات الوسائط لتعزيز الكفاءة وتقليل التكاليف [2].
دراسة بارزة أجريت في يونيو 2023 من قبل باحثين في جامعة كاليفورنيا، ديفيس, استكشفت خلايا العضلات C2C12 المزروعة في وسائط Essential 8 الخالية من المصل. وجدوا أنه بينما كانت معدلات النمو متطابقة مع تلك في الوسائط المعتمدة على المصل على مدى سبعة أيام، كانت مستويات السيرين قد استنفدت تقريبًا بحلول اليوم الثالث، مما يشير إلى نهاية النمو الأسي.حسبت الدراسة أن إنتاج 1 كجم من الكتلة الخلوية الرطبة يتطلب حوالي 252.3 جرام من الأحماض الأمينية الكلية (بما في ذلك 177.7 جرام من الجلوتامين) و1,157.2 جرام من الجلوكوز [2]. تعتبر هذه البيانات محورية لتحسين تركيبات الوسائط، خاصة لإنتاج اللحوم المزروعة.
بالإضافة إلى ذلك، كشف تحليل الأيض الخلوي الداخلي عن تغييرات كبيرة في أيض الكربون المركزي. في سبتمبر 2022، اكتشف الباحثون في جامعة العلوم والتكنولوجيا النرويجية أن الخلايا المعلقة أظهرت مستويات أعلى بشكل ملحوظ من الإيتاكونات داخل الخلايا مقارنة بالخلايا الملتصقة. يبرز هذا كيف يمكن لطرق الزراعة أن تؤثر بشكل عميق على الأيض الخلوي [1].
علم النسخ لتتبع التعبير الجيني
لتكملة الدراسات الأيضية، يسلط علم النسخ الضوء على التغيرات في تنظيم الجينات التي تحدث أثناء التكيف مع البيئة الخالية من المصل.هذه التقنية فعالة بشكل خاص في تحديد التغيرات في المسارات مثل تخليق الكوليسترول، استقلاب الدهون، وتخليق النوكليوتيدات - العمليات التي تتأثر بشكل متكرر خلال الانتقال إلى الظروف الخالية من المصل[1]. من خلال رسم خرائط لتغيرات التعبير الجيني هذه، يمكن للباحثين فهم كيفية تصرف الخلايا في البيئات الخالية من المصل وتطوير استراتيجيات لتصميم خطوط الخلايا لتحسين التكيف.
أكد مي جانغ من NTNU على أهمية هذه النتائج:
"تمت ملاحظة أكبر الفروقات في الملفات الأيضية بين أوضاع الزراعة (الملتصقة مقابل التعليق)، تليها حالة وسط الزراعة (وسط النمو القياسي مقابل الوسط الخالي من المصل)" [1].
يقدم دمج علم النسخ مع البيانات الأيضية وبيانات الحيوية صورة أكثر اكتمالاً عن كيفية تكيف الخلايا، مما يمهد الطريق لأنظمة زراعة خالية من المصل أكثر كفاءة.
استخدام البيانات لتحسين التكيف الخالي من المصل
العثور على مشاكل في تكيف خطوط الخلايا
تلعب البيانات دورًا حيويًا في تحديد ومعالجة القضايا أثناء تكيف خطوط الخلايا. مراقبة الحيوية تعمل كنظام إنذار مبكر. عندما تنخفض حيوية الخلايا إلى ما دون المستوى المقبول، يعود الباحثون إلى خطوة التكيف السابقة لتجنب فقدان الثقافة بأكملها. يتيح هذا النهج إجراء التعديلات قبل المضي قدمًا[1] [5].
تحليل الوسائط المستهلكة هو أداة قوية أخرى للكشف عن قيود المغذيات التي تعيق التكيف. على سبيل المثال، غالبًا ما تكشف مطيافية الكتلة أن الخلايا في الوسائط الخالية من المصل تستنفد المغذيات مثل الجلوتامين والجليسين بشكل أسرع مما كان متوقعًا، مما يمكن أن يشير إلى نهاية النمو الأسي[2] . بالإضافة إلى ذلك، فإن تتبع تراكم اللاكتات أمر ضروري، حيث يمكن أن تؤدي مستويات اللاكتات المرتفعة إلى قمع النمو والنشاط العضلي، خاصة في الثقافات ذات الكثافة العالية[2].
توفر حركيات النمو مؤشرات قابلة للقياس على الأداء. يشير الزيادة الملحوظة في وقت التضاعف أو الانخفاض في معدل النمو المحدد إلى أن صيغة الوسائط قد لا تدعم خط الخلايا بشكل فعال[1][4]. تشير الانحرافات عن معايير النمو المحددة إلى مناطق تتطلب اهتمامًا فوريًا.
توفر التغيرات المورفولوجية أيضًا أدلة قيمة. على سبيل المثال، التكتل الشديد أو الاستدارة المصحوبة بأوقات تضاعف أبطأ تشير إلى فشل التكيف[5] . ومع ذلك، إذا ظلت أوقات التضاعف مستقرة على الرغم من التحولات المورفولوجية، فإن ذلك يشير إلى أن التكيف يتقدم بنجاح.هذه الملاحظات تمكن الباحثين من تحسين الوسائط الخالية من المصل بناءً على رؤى مستندة إلى البيانات.
تطوير وسائط خالية من المصل مخصصة
باستخدام هذه المقاييس التشخيصية، يمكن للباحثين ضبط تركيبات خالية من المصل لتناسب خطوط الخلايا المحددة. تحليل التعبير الجيني يسلط الضوء على المسارات الأيضية التي تواجه صعوبة أثناء التكيف، مثل تخليق الكوليسترول، تخليق النيوكليوتيدات، وأيض الدهون[1] . توجه هذه المعلومات اختيار مكملات الوسائط الخالية من المصل لتعزيز التركيبات.
يأتي مثال من Menarini Biotech srl، حيث نجح فريق بقيادة ليوناردو سيبيليو في تكييف خط خلايا CHO-DG44 في سبتمبر 2019. قاموا بفحص 20 تركيبة محددة كيميائيًا باستخدام لوحة تقييم الوسائط وقرروا أن الوسيط رقم 27 كان الأنسب.هذا الوسط دعم نموًا متسقًا وقابلية فوق 90% لأكثر من 10 تمريرات[7].
وبالمثل، يمكن أن تؤدي بيانات النسخ ووسائط الإنفاق إلى رؤى قابلة للتنفيذ. في يوليو 2025، استخدم باحثو Merck Healthcare KGaA البروتيوميات المقارنة لدراسة خلايا HepG2 التي تنتقل إلى ظروف خالية من المصل. وجدوا تعبيرًا زائدًا كبيرًا للإنزيمات المضادة للأكسدة مثل الجلوتاثيون بيروكسيداز. من خلال ربط هذه النتائج باختبارات نشاط الإنزيم، اكتشفوا أن "التغذية الفائقة بالسيلينيوم" كانت ضرورية لحماية الخلايا من الإجهاد التأكسدي. أدى تعديل مستويات السيلينيوم في وسائطهم المخصصة إلى معالجة هذه المشكلة مباشرة[6].
يساعد التحليل الأيضي أيضًا في تحسين التكاليف مع الحفاظ على الأداء.على سبيل المثال، كشفت الأبحاث على خلايا C2C12 أن إنتاج 1 كجم من الكتلة الخلوية الرطبة يتطلب حوالي 250-275 جرام من الأحماض الأمينية و1,100-1,500 جرام من الجلوكوز[2]. تسمح هذه المقاييس الدقيقة للباحثين بإزالة العناصر الغذائية غير الضرورية، مما يقلل التكاليف دون التأثير على صحة الخلايا. كما أن تحليل الوسائط المستهلكة يحدد المكونات المكلفة غير المستخدمة، مما يمكن من إعادة صياغة الوسائط بشكل فعال من حيث التكلفة.
كيف Cellbase يدعم التكيف مع الوسائط الخالية من المصل
توفير أدوات تحليلية من خلال Cellbase
للمراقبة المستمرة، تتوفر تقنيات مثل أجهزة الاستشعار الطيفية Raman وNIR، وأجهزة الاستشعار اللينة، وأدوات PAT، مما يتيح التعديلات في الوقت الحقيقي أثناء الزراعة[8]. يتم دعم تقييم صحة الخلايا بواسطة أنظمة الفحص عالية المحتوى مثل مجهر ImageXpress Pico، الذي يقوم بأتمتة العمليات مثل عد الخلايا وتقسيم صور صبغة النواة[2] . تتوافق هذه الأدوات مع مبادئ الجودة حسب التصميم (QbD) وتلتزم بممارسات التصنيع الجيدة الحالية (cGMP)، مما يحول التركيز من اختبار ما بعد الدفعة إلى مراقبة الجودة في الوقت الحقيقي[8].
بالإضافة إلى الأدوات التحليلية،
الوصول إلى التكنولوجيا للتكيف الخالي من المصل
إلى جانب المعدات،
هذا التركيز مهم بشكل خاص نظرًا للضغوط المالية التي تواجه صناعة اللحوم المزروعة. كما يشير ديفيد إي. بلوك من جامعة كاليفورنيا، ديفيس:
"سيحتاج وسط زراعة الخلايا المزروعة إلى أن يكون أرخص بكثير من جميع وسائل زراعة الخلايا الحيوانية التجارية الحالية للسماح بتحقيق التكافؤ السعري لمنتجات اللحوم المزروعة مع اللحوم التقليدية"[2].
الخاتمة
يلعب الرصد الدقيق دورًا رئيسيًا في تحقيق التكيف الناجح الخالي من المصل.أدوات مثل HPLC، مطياف الكتلة، وتدفق الخلايا السيتومتري لا غنى عنها لتتبع التغيرات الأيضية، وتحديد الاختناقات، والحفاظ على حيوية الخلايا فوق العتبة الحرجة 90%[3][9]. بدون هذه التقنيات، يصبح من الصعب تحديد ما إذا كانت الخلايا تتكيف حقًا أو ببساطة تبقى على قيد الحياة تحت الضغط. هذه النتائج تسلط الضوء على الحاجة إلى معالجة الحواجز اللوجستية والتقنية المرتبطة بالحصول على المعدات اللازمة.
الحصول على المعدات المتخصصة لا يزال عقبة كبيرة. التكيف بدون مصل هو عملية معقدة، وغالبًا ما تستغرق أكثر من شهر لإكمالها[9]. هذه التعقيدات تتطلب الوصول إلى أدوات متقدمة، والتي ليست دائمًا سهلة المصدر. لذلك، تعتبر المنصات التي تبسط عملية شراء هذه المعدات ضرورية.كما يشير سيباستيان خوان رييس من بوليتكنيك مونتريال:
"يتم تشجيع صناعة تاريخياً محافظة على الابتكار وتحسين منصات الإنتاج من خلال تبني تقنيات جديدة عند ظهورها لتعزيز مراقبة العمليات دون عبء تنظيمي إضافي"[8] .
لقد جعل إدخال أنظمة التحكم في الجودة في الوقت الحقيقي من الممكن تعديل العمليات فوراً، باستخدام البيانات المستمرة لتوجيه القرارات[8].
بناءً على هذه الأساليب التحليلية،
الأسئلة الشائعة
ما هي المقاييس التي تثبت بشكل أفضل أن الخلايا قد تكيفت حقًا مع الوسائط الخالية من المصل؟
تشمل المؤشرات الرئيسية للانتقال الناجح إلى الوسائط الخالية من المصل حركيات النمو, ملفات تعريف المستقلبات داخل الخلايا, معدلات استخدام المغذيات (مثل الجلوكوز، الجلوتامين، الجلايسين، والسيستين)، وحيوية الخلايا. توفر هذه المقاييس صورة واضحة عن مدى تكيف الخلايا مع الحفاظ على وظائفها الطبيعية.
كيف يمكنني اكتشاف اختناقات المغذيات مبكرًا أثناء التكيف الخالي من المصل؟
لاكتشاف قيود المغذيات مبكرًا، من الضروري مراقبة النشاط الأيضي واستخدام المغذيات. تقنيات مثل تحليل الوسائط المستهلكة يمكن أن تحدد التغيرات في استهلاك المغذيات الأساسية مثل الجلوكوز، الجلوتامين، الجليسين، والسيستين. بالإضافة إلى ذلك، يمكن أن يكشف التوصيف الأيضي عن التغيرات في المسارات الجليكوليتيكية والأكسدة. من خلال تتبع مستويات المستقلبات ومعدلات امتصاص المغذيات بشكل روتيني، يمكنك إجراء تعديلات في الوقت المناسب على الوسائط أو طرق التغذية، مما يعزز فرص التكيف السلس الخالي من المصل.
متى يجب أن أستخدم قياس التدفق الخلوي، أو الميتابولوميات، أو النسخ الجيني؟
يقدم كل من قياس التدفق الخلوي، والميتابولوميات، والنسخ الجيني رؤى فريدة عند دراسة كيفية تكيف خطوط الخلايا مع الوسائط الخالية من المصل.قياس التدفق الخلوي مثالي لتقييم خصائص الخلايا مثل الحيوية والعلامات السطحية. الميتابولوميات تتعمق في تحليل المستقلبات الخلوية، مما يسلط الضوء على استهلاك المغذيات والتغيرات الأيضية. في الوقت نفسه، التعبير الجيني يركز على التعبير الجيني، مما يساعد في تحديد الاستجابات الجزيئية والمسارات التنظيمية. يعتمد الاختيار بين هذه الأساليب على ما إذا كنت تستهدف النمط الظاهري للخلايا أو الأيض أو تنظيم الجينات.











