Genetische Stabilität ist entscheidend für die Produktion von kultiviertem Fleisch. Ohne sie können Zelllinien mutieren, was zu inkonsistenter Qualität, Sicherheitsrisiken und Produktionsausfällen führen kann. Die Skalierung von Tausenden zu Billionen von Zellen verstärkt diese Risiken, was robuste Qualitätskontrollsysteme unerlässlich macht. Regulierungsbehörden wie die FDA und EMA verlangen den Nachweis der Stabilität, bevor Produkte zugelassen werden, da selbst geringfügige genetische Veränderungen allergene oder schädliche Auswirkungen auslösen können.
Zu den wichtigsten Herausforderungen gehören genetische Drift, Akkumulation von Mutationen und Aktivierung von Onkogenen. Diese Probleme entstehen durch verlängerte Zellpassagen, selektiven Druck und Umweltstressoren während der Produktion. Fortschrittliche Testmethoden wie Karyotypisierung, SNP-Arrays und Next-Generation-Sequencing (NGS) helfen, diese Risiken zu erkennen und zu adressieren. Präventive Strategien wie strukturiertes Zellbanking und gezielte genetische Manipulation bieten zusätzlichen Schutz gegen Instabilität.
Produzenten müssen die Qualitätskontrolle in jede Phase der Produktion integrieren - von der Zellbank bis zu großtechnischen Bioreaktoren. Werkzeuge wie STR-Profiling, Kontaminationstests und funktionelle Assays gewährleisten Konsistenz und Sicherheit. Plattformen wie
Beschleunigung der Zelllinienentwicklung von DNA zur Masterzellbank - AGC Biologics
Häufige Herausforderungen bei der Aufrechterhaltung der genetischen Stabilität
Die Sicherstellung der genetischen Stabilität während des gesamten Produktionszyklus von kultiviertem Fleisch ist keine leichte Aufgabe. Der schiere Umfang der Produktion bietet viele Gelegenheiten für genetische Veränderungen, sich zu entwickeln und zu verbreiten. Diese Herausforderungen zu erkennen, ist der Schlüssel zur Implementierung effektiver Qualitätskontrollsysteme.
Genetische Drift und Mutationsakkumulation
Erweiterte Zellpassagen sind eine Hauptquelle für genomische Instabilität in der Produktion von kultiviertem Fleisch. Unsterbliche Zelllinien sind von Natur aus anfällig für genomische Veränderungen, die während der Langzeitkultur zu spontanen Mutationen führen können [6][5]. Wenn Zellen mehrere Populationsverdopplungen durchlaufen, häufen sich Fehler in der DNA-Replikation an, was zu unterschiedlichen Zellpopulationen und möglicherweise zu einem Funktionsverlust führt. Christopher Frye und Luhong He von BioPharm International heben dieses Problem hervor:
Klondal abgeleitete CHO-Zelllinien wurden oft beobachtet, dass sie divergieren und über lange Zeiträume der Subkultivierung zu einer heterogenen Population werden [6].
In industriellen Umgebungen zeigen etwa 20% der Produktionszelllinien über aufeinanderfolgende Generationen eine erhebliche Transgen-Heterogenität [6]. Diese Mutationen können früh auftreten, während der DNA-Replikation nach der Transfektion oder aufgrund von Fehlern bei der Integration fremder Gene in das Wirtsgenom [5].
Selektionsdrücke fügen eine weitere Komplexitätsebene hinzu. Mittel wie Antibiotika und Stoffwechselmarker (e.g. , MTX), die zur Stabilisierung von Zelllinien verwendet werden, können tatsächlich die Mutationsraten erhöhen [6][5]. In einigen Fällen gilt: Je höher die Konzentration dieser Mittel, desto höher die Mutationsrate [6]. Umweltstressoren - wie Nährstoffmangel, suboptimale Kulturbedingungen während des Scale-ups und physischer Stress durch Expansion - können die genetische Integrität weiter destabilisieren [6][5].
Shuai Wang, Direktor der Zelllinienentwicklung bei WuXi Biologics, merkt an:
Mutationsniveaus ändern sich wahrscheinlich über die Zellpassage hinweg aufgrund der genomischen Plastizität von CHO-Zellen (Chinese Hamster Ovary) [5].
Epigenetische Veränderungen spielen ebenfalls eine Rolle. Transgene können während des Kulturprozesses teilweise oder vollständig verloren gehen oder stillgelegt werden, was die Langzeitstabilität beeinträchtigt. Diese angesammelten Mutationen schaden nicht nur der Zellfunktion, sondern erhöhen auch das Risiko der Aktivierung von Onkogenen.
Risiken der Onkogenaktivierung
Die Aktivierung von Onkogenen stellt ein kritisches Sicherheitsproblem für Produzenten von kultiviertem Fleisch dar, da sie ganze Produktionschargen gefährden kann. Genetische Instabilität kann zur Aktivierung von Onkogenen durch Mechanismen wie Hypermethylierung führen, was zu tumorähnlichen Profilen führen kann [3][1]. Die rasche Expansion, die in der Produktion erforderlich ist, erhöht die Wahrscheinlichkeit, diese schädlichen Mutationen anzusammeln [5][6].
Dies ist eine wohlbekannte Herausforderung. Laut dem International Consortium for Innovation & Quality in Pharmaceutical Development (IQ) glauben 67% der Befragten, dass genetische Mutationen eine größere Bedrohung darstellen als die Fehlinkorporation von Aminosäuren während der Produktion [5] . Ein Fall aus dem Mai 2024 veranschaulicht die Schwere dieses Problems: WuXi Biologics entdeckte, dass 43% der Klone aus einem Zelllinienentwicklungsprogramm die gleiche genetische Punktmutation trugen. Die Ursache? Ein Variantenlevel von 2,1%–2,2% in der Plasmid-DNA, die während der Transfektion verwendet wurde und von der traditionellen Sanger-Sequenzierung nicht erkannt wurde. Um dies zu beheben, integrierte das Unternehmen Next-Generation Sequencing (NGS) in seine Qualitätskontrollprozesse, um solche Varianten frühzeitig zu erkennen [5].
Die frühzeitige Erkennung genetischer Anomalien ist entscheidend, da onkogene Veränderungen ganze Chargen beeinträchtigen können. Standard-G-Band-Karyotypisierung kann abnormale Subpopulationen mit nur 14% Mosaik in zwanzig Zellmetaphasen identifizieren [1]. Fortschrittlichere Techniken wie NGS können genetische Mutationen in klonalen Zellen mit einer Sensitivität von 0,5% nachweisen [5].
Die DNA-Methylierungsanalyse ist ein weiteres wertvolles Werkzeug zur Bewertung des tumorigene Potentials:
Da DNA-Methylierungsniveaus und Hypermethylierung bestimmter Gene bei der Krebsentstehung und -progression auftreten, könnte die Analyse von DNA-Methylierungsprofilen ergänzende Informationen über das tumorigene Potential von Zellen liefern [3].
Die eigentliche Herausforderung besteht darin, robuste Überwachungssysteme zu implementieren, die in der Lage sind, diese Veränderungen zu identifizieren, bevor sie die Sicherheit beeinträchtigen.Für Produzenten von kultiviertem Fleisch erfordert die Aufrechterhaltung der genetischen Stabilität während der schnellen Zellvermehrung fortschrittliche Qualitätskontrollmaßnahmen. Spezialisierte Plattformen wie
Methoden der Qualitätskontrolle
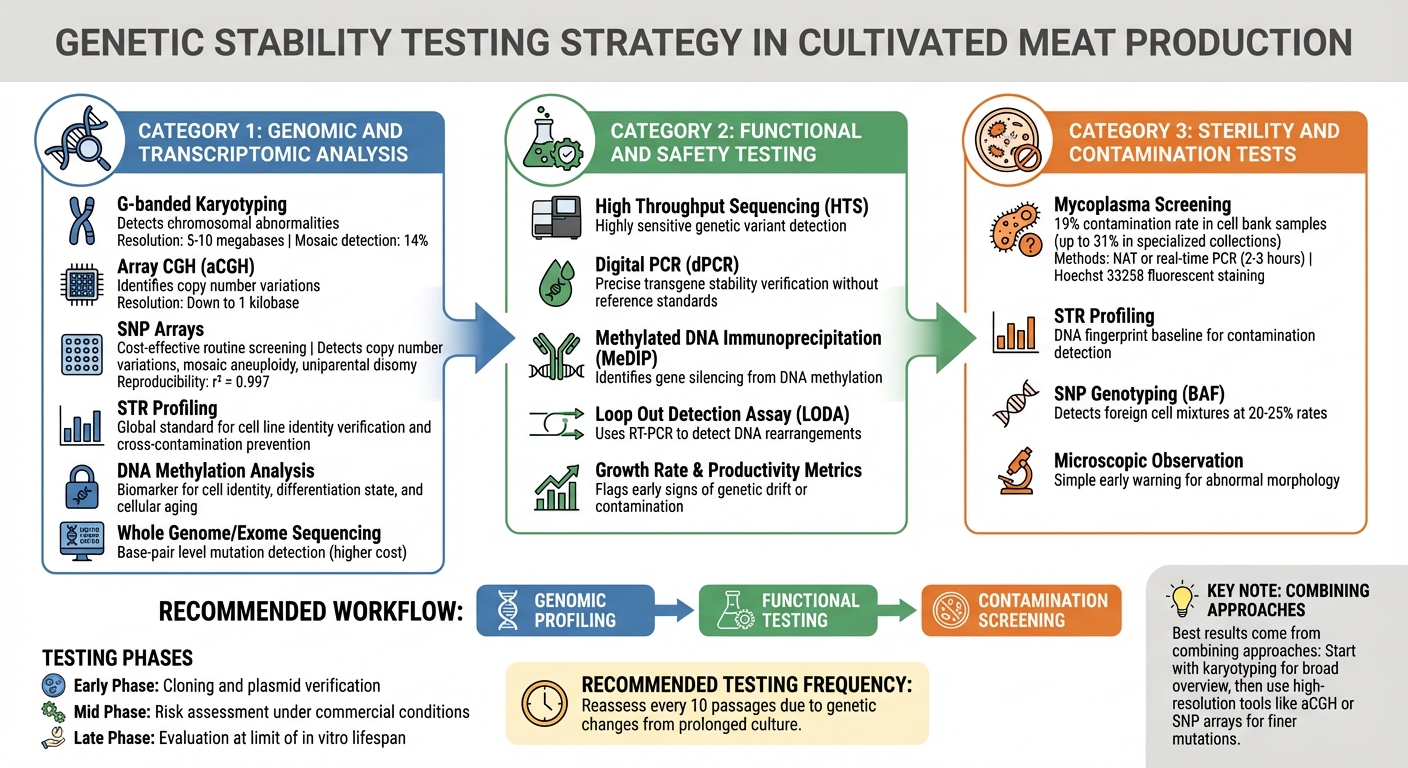
Methoden der Qualitätskontrolle für genetische Stabilität in kultivierten Fleischzelllinien
Die Identifizierung genetischer Instabilität, bevor sie die Produktion beeinträchtigt, erfordert eine mehrschichtige Teststrategie. Produzenten von kultiviertem Fleisch verlassen sich auf Methoden, die alles von großen chromosomalen Veränderungen bis hin zu Einzelbasenmutationen erkennen. Die Wahl der Techniken hängt von den Risiken ab, die in jeder Produktionsstufe vorhanden sind. Diese genomischen Werkzeuge fungieren als erste Kontrollstelle, gefolgt von detaillierten funktionalen und Kontaminationsbewertungen.
Genomische und Transkriptomische Analyse
G-bändiges Karyotypisieren ist ein wichtiges Werkzeug zur Identifizierung von größeren chromosomalen Problemen wie numerischen Anomalien und großen strukturellen Umlagerungen, wie Translokationen. Während es Mosaikniveaus von etwa 14% erkennen kann, ist seine Auflösung auf Änderungen von 5–10 Megabasen begrenzt, was bedeutet, dass kleinere Veränderungen unbemerkt bleiben könnten [1].
Array-Komparative Genomische Hybridisierung (aCGH) bietet eine höhere Auflösung und identifiziert Kopienzahlvariationen bis zu 1 Kilobase. Ebenso bieten Einzelnukleotid-Polymorphismus (SNP) Arrays eine kostengünstige Option für das routinemäßige Screening, indem sie Kopienzahlvariationen, Mosaikaneuploidie und uniparentale Disomie erkennen. Validierungsstudien haben gezeigt, dass SNP-Arrays hoch reproduzierbar sind, wobei B-Allelfrequenz (BAF)-Messungen einen beeindruckenden r² = 0 erreichen.997 [8] [1].
Rocio Aguilar-Quesada vom Andalusian Public Health System Biobank hebt den Wert der Kombination von Methoden hervor:
Karyotypisierung bleibt ein vielseitiger Test, insbesondere wenn er mit hochauflösenden Tests ergänzt wird [1].
Short Tandem Repeat (STR) Profiling ist der globale Standard zur Überprüfung der Zelllinienidentität und zur Vermeidung von Kreuzkontaminationen [1] [9]. In der Zwischenzeit dient DNA-Methylierungsanalyse als Biomarker für Zellidentität, Differenzierungszustand und zelluläres Altern [1]. Für die Erkennung von Mutationen auf Basenpaarebene ist Whole Genome oder Exome Sequencing eine Option, obwohl es mit höheren Kosten im Vergleich zu array-basierten Methoden verbunden ist [1].
Die besten Ergebnisse erzielt man durch die Kombination dieser Ansätze. Beginnen Sie mit der Karyotypisierung für einen umfassenden Überblick und verwenden Sie dann hochauflösende Werkzeuge wie aCGH oder SNP-Arrays, um feinere Mutationen zu erfassen. Eine regelmäßige Neubewertung - idealerweise alle 10 Passagen - ist entscheidend, da eine längere Kultur zu genetischen Veränderungen führen kann [10]. Diese genomischen Erkenntnisse werden dann durch funktionelle Tests ergänzt, um ein konsistentes Zellverhalten während der Produktion sicherzustellen.
Funktionelle und Sicherheitstests
Genomisches Profiling allein reicht nicht aus. Funktionelle Tests bestätigen, dass die Zellen während der Expansion ihre beabsichtigten Eigenschaften beibehalten. Kennzahlen wie Wachstumsraten und Produktivität können frühe Anzeichen von genetischer Drift oder Kontamination aufzeigen [9].
Hochdurchsatz-Sequenzierung (HTS) ist hochsensitiv für die Erkennung genetischer Varianten, während digitale PCR (dPCR) die Transgenstabilität präzise ohne Referenzstandards überprüft [11] . Christopher Frye und Luhong He von BioPharm International betonen die Bedeutung dieses Schrittes:
Die Produktionszelllinie ist die Grundlage jedes Bioprozesses, und daher ist eine angemessene genetische Charakterisierung der Produktionszelllinie absolut entscheidend für den Erfolg der Prozessentwicklung [6].
Epigenetische Stabilität ist ebenfalls entscheidend. Methylierte DNA-Immunpräzipitation (MeDIP) hilft, die durch DNA-Methylierung verursachte Gen-Silencing zu identifizieren, ein häufiger Grund für Produktivitätsrückgang [7]. Werkzeuge wie der Loop Out Detection Assay (LODA) verwenden RT-PCR, um DNA-Umlagerungen zu erkennen, wie zum Beispiel, wenn ein interessierendes Gen gelöscht wird, während der selektierbare Marker erhalten bleibt [7].
Tests sollten mit der Produktionsphase übereinstimmen: Frühphasentests konzentrieren sich auf Klonierung und Plasmidverifizierung, Mittelphasentests bewerten Risiken unter kommerziellen Bedingungen, und Spätphasentests evaluieren Zellen an der Grenze ihrer in vitro Lebensdauer [6]. Experimente mit frischen, niedrigpassagierten Zellen aus einer Masterzellbank zu beginnen, reduziert das Risiko genetischer Drift [9].
Sterilitäts- und Kontaminationstests
Kontaminationstests sind unerlässlich, um Faktoren zu vermeiden, die die Genetik destabilisieren könnten. Mycoplasma ist besonders besorgniserregend, da es den Zellstoffwechsel und das Verhalten verändert, ohne sichtbare Veränderungen in der Kultur zu verursachen [1]. Studien zeigen, dass 19% der Zellbankproben mit Mykoplasmen kontaminiert sind, wobei einige spezialisierte Sammlungen Raten von bis zu 31% aufweisen [1].
Regelmäßiges Mykoplasmen-Screening mit empfindlichen Nukleinsäure-Amplifikationstechniken (NAT) oder Echtzeit-PCR kann halbquantitative Ergebnisse innerhalb von 2–3 Stunden liefern [1]. Hoechst 33258 Fluoreszenzfärbung ist eine weitere Methode, die charakteristische extrazelluläre Fluoreszenzmuster aufzeigt [9].
STR-Profiling erstellt einen DNA-Fingerabdruck für Zelllinien und dient als Basislinie zur Erkennung von Kreuzkontaminationen [9]. Zusätzlich kann SNP-Genotypisierung unter Verwendung von B-Allel-Frequenz (BAF)-Verteilungen Kontaminationen durch andere Zelllinien identifizieren und fremde Zellmischungen mit Raten von 20–25% erkennen [8].
Mikroskopische Beobachtung ist ein einfaches, aber effektives Frühwarninstrument, da abnorme Zellmorphologie oft auf Kulturprobleme hinweist [9]. Die Implementierung eines Qualitätsmanagementsystems, wie ISO 9001:2015, zusammen mit Good In Vitro Method Practices (GIVIMP), hilft, standardisierte und reproduzierbare Kulturbedingungen aufrechtzuerhalten und das Risiko genomischer Instabilität zu verringern [10].
Für Produzenten von kultiviertem Fleisch, die Zugang zu spezialisierten Testgeräten und Materialien benötigen, bieten Plattformen wie
sbb-itb-ffee270
Präventionsstrategien für genetische Instabilität
Genetische Instabilität zu erkennen ist das eine; sie zu verhindern, ist eine ganz andere Herausforderung.Um die genetische Stabilität intakt zu halten, benötigen Produzenten von kultiviertem Fleisch gut durchdachte Systeme, die verhindern, dass Zelllinien abdriften, bevor Probleme auftreten. Zwei Schlüsselstrategien führen hier den Weg: strukturiertes Zellbanking und gezielte genetische Veränderung. Zusammen bekämpfen diese Ansätze direkt die Risiken von genetischem Drift und Onkogenaktivierung.
Zellbanking und Kryokonservierung
Die Anhäufung von Mutationen ist ein echtes Anliegen, daher ist ein zuverlässiges Zellbanking-System ein Muss. Der Industriestandard umfasst ein zweistufiges System: eine Master Cell Bank (MCB) und eine Working Cell Bank (WCB). Dieses Setup gewährleistet einen konsistenten Ausgangspunkt für die Produktion. Die Begrenzung der Anzahl der Passagen ist entscheidend, da jede Passage die Wahrscheinlichkeit von Mutationen erhöht. Durch die Lagerung von Zellen in flüssigem Stickstoff wird die biologische Aktivität effektiv pausiert, wodurch das Risiko genetischer Veränderungen während der Lagerung verringert wird.
Statt die Zeit zu verfolgen, wird das Zellalter durch Populationsverdopplungen . gemessen. Zum Beispiel umfasst ein typischer 5.000-Liter-Produktionsbioreaktor etwa 30 Populationsverdopplungen[6]. Um die genetische Konsistenz zu wahren, begrenzt die kommerzielle Herstellung diese Zahl auf zwischen 45 und 60 Verdopplungen[6].
Screening-Methoden wie RT-PCR und Einzelzell-qPCR können Probleme frühzeitig erkennen, wie ungewöhnliches mRNA-Spleißen oder Transgen-Variabilität. Zelllinien, die eine große Variabilität in Kopienzahlen aufweisen, sollten verworfen werden, um zukünftige Probleme zu vermeiden.
Qualitätskontrolle ist nicht verhandelbar. Erschreckenderweise haben Studien gezeigt, dass bis zu 31 % der Zelllinien in einigen Banken mit Mykoplasmen kontaminiert waren [3]. Um dies zu verhindern, wird STR-Profiling verwendet, um die Authentizität der Zelllinien während des gesamten Bankprozesses zu bestätigen.Wie von der FSA-Forschung und -Evidenz:
Da die gelagerten Zellen das Ausgangsmaterial für das Endprodukt sind, könnten in Zukunft hohe Standards von den Regulierungsbehörden gefordert werden, um ein sicheres Fleischprodukt von hoher Qualität zu gewährleisten [2].
Gentechnik für Stabilität
Die Gentechnik bietet eine weitere Verteidigungsebene, indem sie die Stabilität der Zelllinien direkt verbessert. Techniken wie gezielte Integration (TI), insbesondere Rekombinase-vermittelte Kassettenaustausch (RMCE), ermöglichen die präzise Einfügung von Transgenen in spezifische genomische Positionen. Dieser Ansatz vermeidet die Unvorhersehbarkeit der zufälligen Integration, bei der Positionseffekte und Kopienzahlinstabilität Chaos anrichten können. Obwohl RMCE in CHO-Zellen Effizienzraten unter 0,1% aufweist[12], sind die resultierenden Klone vorhersehbarer und stabiler.
Auch das gewählte Expressionssystem ist wichtig. Zum Beispiel führt das Glutamin-Synthetase (GS)-System typischerweise zu etwa fünf Transgenkopien pro Zelle, während das Dihydrofolat-Reduktase (DHFR)-System die Kopienzahl auf bis zu 1.000 erhöhen kann[6]. Obwohl höhere Kopienzahlen verlockend klingen mögen, erhöhen sie die Wahrscheinlichkeit von DNA-Veränderungen, was GS-basierte Systeme zu einer klügeren Wahl für langfristige Stabilität macht.
Um Risiken weiter zu minimieren, sind ortspezifische Mutagenese und NGS-Screening vor der Transfektion entscheidend. Da die Sanger-Sequenzierung eine höhere Nachweisgrenze hat, kann NGS Plasmidmutationen unter 0,5% erkennen, was den Erfolg des Klon-Screenings auf über 90% verbessert[5].
Shuai Wang und Kollegen von WuXi Biologics betonen die Bedeutung dieser Wachsamkeit:
Da Prozessoptimierung Genmutationen nicht beheben kann, überwachen Sie die Mutationsniveaus in stabilen Klonen sorgfältig[5].
Für Produzenten, die spezialisierte Werkzeuge benötigen - sei es für Kryokonservierung, Gentechnik oder Zellliniencharakterisierung -
Integration der Qualitätskontrolle in die Produktion
Die Einbindung der Qualitätskontrolle in jede Produktionsphase ist entscheidend. Ohne ein strukturiertes System können selbst gut gepflegte Zelllinien während der Expansion und des Scale-ups Veränderungen erfahren. Qualitätskontrolle sollte kein nachträglicher Gedanke sein - sie muss ein zentraler Bestandteil der Produktion sein. Dies beginnt in der Scale-up-Phase, in der strenge Managementsysteme und kontrollierte Umgebungen eine Schlüsselrolle spielen.
Qualitätskontrolle während der Expansion und des Scale-ups
Wie bereits erwähnt, sind genomische und Kontaminationstests von entscheidender Bedeutung, insbesondere während des Scale-ups. Der Übergang von kleinen Volumina zu Tausenden von Litern birgt neue Risiken, wobei jede Zellpassage die Wahrscheinlichkeit von Mutationen erhöht. Ein Qualitätsmanagementsystem (QMS) hilft, diese Risiken effektiv zu managen. Zum Beispiel implementierten Josep M. Canals und sein Team an der Universität Barcelona zwischen 2017 und 2022 das ISO 9001:2015 QMS, um menschliche pluripotente Stammzellkulturen zu standardisieren. Ihre retrospektive Analyse von G-Banding- und aCGH-Daten zeigte eine signifikante Reduktion chromosomaler Aberrationen im Vergleich zu den Bedingungen vor der Anpassung[10][13] . Kanäle hoben die Bedeutung der laufenden Überwachung hervor:
Die genetische Instabilität, die von hPSCs in der Kultur gezeigt wird, macht die häufige Neubewertung der genomischen Integrität zu einer wesentlichen Anforderung, wenn geplant ist, sie für Experimente zu verwenden[10].
Routinemäßiges genomisches Screening ist ein Muss. Techniken wie G-Banding-Karyotypisierung und aCGH erkennen strukturelle Veränderungen, während Next-Generation Sequencing (NGS) Mutationen auf Ebenen unter 0,5% identifiziert[5]. Wachstumskurvenanalyse kann auch frühzeitig Probleme aufzeigen, wie z.B. Kontamination oder genetische Drift[9]. Umweltüberwachung fügt eine weitere Sicherheitsebene hinzu, mit Praktiken wie Sedimentplatten-Tests und halbjährlichen HEPA-Filterüberprüfungen, die sicherstellen, dass die Produktionsumgebung stabil und stressfrei für Zelllinien bleibt [4].
Konsistenz in Medien und Reagenzien ist ebenso wichtig. Die Verwendung von serumfreien, definierten Medien wie mTeSR1, zusammen mit Reagenzien mit einem Analysezertifikat, hilft, Chargenvariationen zu reduzieren und das Risiko einer viralen Kontamination zu begrenzen[10][4]. Regelmäßige Morphologiekontrollen - einfache mikroskopische Beobachtungen bei unterschiedlichen Kulturdichten - können frühe Anzeichen von Differenzierung oder Stress erkennen[9]. Für die Beschaffung von spezialisiertem Equipment oder Reagenzien verbinden Plattformen wie
Funktionelle Assays für Produktkonsistenz
Während die genomische Überwachung den Prozess absichert, stellen funktionelle Assays sicher, dass die Zellen wie beabsichtigt funktionieren.Genetische Stabilität allein reicht nicht aus; Zellen müssen auch ihre Fähigkeit beibehalten, ordnungsgemäß über Produktionschargen hinweg zu funktionieren. Bei kultiviertem Fleisch bedeutet dies, zu bestätigen, dass Stammzellen, wie z.B. Muskel-Satellitenzellen, sich nach der Expansion noch in reifes Muskel- oder Fettgewebe differenzieren können[2] . Differenzierungsassays sind unerlässlich, um dies zu überprüfen.
Metabolische Assays wie MTT, LDH und Resazurin geben Einblick in die Zellgesundheit und Lebensfähigkeit[4][9]. Diese, kombiniert mit Short Tandem Repeat (STR) Profiling, helfen zu bestätigen, dass Zelllinien während des gesamten Produktionsprozesses authentisch und frei von Kreuzkontaminationen bleiben[1][9].
Transkriptionelle Analyse ist ein weiterer kritischer Schritt.Xiaoyue Chen und Sam Zhang empfehlen:
cDNA anstelle von genomischer DNA-Sequenzierung wird zur Mutationsdetektion empfohlen, um Risiken auf Transkriptionsebene zu bewerten[5].
Diese Methode bietet ein genaueres Bild des Endprodukts, da sie widerspiegelt, wie Gene exprimiert werden, anstatt nur ihre genomischen Standorte. Durch die Kombination von genomischem Screening mit funktionellen Tests können Produzenten sicherstellen, dass jede Charge strenge Standards für Sicherheit, Qualität und Leistung in jeder Produktionsphase erfüllt.
Fazit
Die Aufrechterhaltung der genetischen Stabilität ist entscheidend für die sichere und konsistente Produktion von kultiviertem Fleisch. Francisco J. Molina-Ruiz und seine Kollegen vom Labor für Stammzellen und Regenerative Medizin heben die Risiken hervor:
Genetische Veränderungen in hPSCs könnten nicht nur die Sicherheit von hPSC-basierten Zellprodukten gefährden...aber auch zu einer heterogenen Differenzierungsneigung des Ausgangsmaterials, veränderten Genexpressionsprofilen und Ineffizienz des endgültigen Zellprodukts führen [10].
Die Einsätze sind erheblich - über 531 falsch identifizierte Zelllinien wurden vom International Cell Line Authentication Committee [1].
Die Bewältigung dieser Probleme erfordert ein robustes Qualitätskontrollrahmenwerk. Dies beinhaltet die Kombination von Methoden wie STR-Profiling, G-Banding-Karyotypisierung, aCGH und fortschrittlichem NGS [5] , neben Systemen wie ISO 9001:2015, um Prozesse zu standardisieren und chromosomale Anomalien zu minimieren [13].
Wirtschaftliche Faktoren treiben auch die Notwendigkeit für diese Maßnahmen voran.Genetische Drift kann dazu führen, dass mutierte Zellen einen Wachstumsvorteil erlangen, was potenziell ganze Produktionschargen verderben kann [10][11]. Mit dem zunehmenden Fokus auf menschliche pluripotente Stammzellen war die Nachfrage nach stabilen Zelllinien noch nie so groß. Wie Professor David L. Kaplan von Tufts University erklärt:
Unsterbliche Zelllinien werden im Allgemeinen als Voraussetzung für die Erzeugung großer Mengen essbaren Gewebes aus einem stabilen, robusten Bioprozess angesehen [14].
Für Produzenten von kultiviertem Fleisch muss die Qualitätskontrolle in jeden Schritt eingebettet sein - von der Plasmid-Screening bis zur Überwachung der Großproduktion. Durch die Kombination gründlicher Tests mit präventiven Strategien können Produzenten konsistente und zuverlässige Ergebnisse sicherstellen.
FAQs
Wie oft sollte die genetische Stabilität während des Scale-ups getestet werden?
Die genetische Stabilität ist ein entscheidender Schritt während des Scale-ups und sollte regelmäßig überprüft werden. Wie oft diese Tests durchgeführt werden, hängt weitgehend von der spezifischen Zelllinie und dem jeweiligen Prozess ab. Um die Wahrscheinlichkeit von Mutationen zu verringern und die Stammzellenfähigkeit der Zellen zu erhalten, ist es ratsam, ein Passagelimit festzulegen, das auf genetischen Analysen basiert.
Welche Tests erkennen am besten kleine Mutationen und große Chromosomenveränderungen?
Tests wie SNP-Array-Analyse und genomweite SNP-Genotypisierung sind e
Was ist der einfachste Weg, um genetische Drift über Produktionschargen hinweg zu verhindern?
Um genetische Drift zu minimieren, ist es entscheidend, regelmäßige genetische und funktionelle Analysen von Zelllinien durchzuführen und die Anzahl der Passagen, die sie durchlaufen, zu begrenzen. Implementieren Sie Praktiken wie die Einrichtung von Masterzellbanken und die routinemäßige Überprüfung der genetischen Stabilität, wie in Qualitätskontrollprotokollen empfohlen. Diese Maßnahmen sind entscheidend, um Konsistenz zu gewährleisten und zuverlässige Ergebnisse über verschiedene Produktionschargen hinweg sicherzustellen.











