वैलिडेटिंग विकास माध्यम यूके बाजार में अनुमोदन प्राप्त करने के लिए खेती किए गए मांस कंपनियों के लिए एक अनिवार्य कदम है। यह प्रक्रिया उत्पादों की सुरक्षा, गुणवत्ता, और सख्त नियामक ढांचे जैसे यूके नॉवेल फूड रेगुलेशन्स (EU 2015/2283) के तहत अनुपालन सुनिश्चित करती है। यहां आपको जानने की आवश्यकता है:
- मुख्य आवश्यकताएँ: विकास माध्यम को विषविज्ञान, संदूषण नियंत्रण, पोषण गुणवत्ता, और एलर्जेनिसिटी के मानकों को पूरा करना चाहिए।
- यूके नियमावली: फूड स्टैंडर्ड्स एजेंसी (FSA) को HACCP सिद्धांतों के अनुपालन और पशु उत्पत्ति के उत्पादों (POAO) के तहत वर्गीकरण की आवश्यकता होती है।
- वैश्विक मानक: जबकि यूके और ईयू के पास समान ढांचे हैं, अमेरिका FD&C अधिनियम के तहत CGMP नियमों का पालन करता है।
- वैलिडेशन प्रक्रिया: इसमें संरचना, शुद्धता, कार्यक्षमता, और आपूर्तिकर्ता अनुपालन का गहन परीक्षण शामिल है, साथ ही मजबूत दस्तावेजीकरण भी।
- समर्थन पहलें: यूके का £1.6 मिलियन नियामक सैंडबॉक्स, 2025 में लॉन्च किया गया, कंपनियों को इन मानकों को पूरा करने में सहायता करता है।
उचित सत्यापन सुरक्षा सुनिश्चित करता है, विश्वास बनाता है, और कानूनी आवश्यकताओं के साथ मेल खाता है। लेख परीक्षण विधियों, आपूर्तिकर्ता योग्यताओं, और नियामक सबमिशन युक्तियों सहित चरण-दर-चरण प्रक्रिया में गहराई से जाता है।
विकास मीडिया के लिए नियामक मानक
मानक और दिशानिर्देश
विकास मीडिया, संवर्धित मांस उत्पादन में एक महत्वपूर्ण घटक, को कठोर अंतरराष्ट्रीय नियामक मानकों को पूरा करना चाहिए। ये मानक क्षेत्रों के अनुसार भिन्न होते हैं, प्रत्येक में संरचना, सुरक्षा, और शुद्धता के लिए विशिष्ट आवश्यकताएँ होती हैं।
यूनाइटेड किंगडम में, विकास मीडिया को नॉवेल फूड रेगुलेशन्स (अनुकूलित रेगुलेशन (EU) 2015/2283) के तहत विनियमित किया जाता है। बाजार के लिए अनुमोदित होने से पहले, एक गहन सुरक्षा मूल्यांकन की आवश्यकता होती है [1]।खाद्य मानक एजेंसी (FSA) सेल-उत्पादित उत्पादों को Regulation (EC) 853/2004 के तहत पशु उत्पत्ति के उत्पाद (POAO) के रूप में वर्गीकृत करती है। यह वर्गीकरण उत्पादकों को खतरा विश्लेषण और महत्वपूर्ण नियंत्रण बिंदु (HACCP) सिद्धांतों पर आधारित खाद्य सुरक्षा प्रबंधन प्रणाली लागू करने का आदेश देता है [3]। FSA विकास मीडिया संरचना पर विस्तृत तकनीकी मार्गदर्शन विकसित करने की प्रक्रिया में भी है, और आगे के अपडेट की उम्मीद है [1]। ये ढांचे अधिक विशिष्ट नियामक आवश्यकताओं के लिए आधार प्रदान करते हैं।
संयुक्त राज्य अमेरिका में, दृष्टिकोण भिन्न है। विकास मीडिया घटकों को फेडरल फूड, ड्रग, और कॉस्मेटिक एक्ट (FD&C एक्ट) के सेक्शन 501(a)(4)(B) में उल्लिखित वर्तमान अच्छी विनिर्माण प्रथा (CGMP) आवश्यकताओं को पूरा करना चाहिए [4]। FDA मीडिया घटकों को "आपूर्ति और अभिकर्मक" के रूप में वर्गीकृत करता है, जो 21 CFR भाग 210 और 211 द्वारा शासित होते हैं।इन घटकों को प्रदूषण को रोकने के लिए गुणवत्ता सत्यापन से गुजरना चाहिए [4]। दिलचस्प बात यह है कि संवर्धित मांस मीडिया के सिंथेटिक घटक - जैसे कि अमीनो एसिड, विटामिन, और लवण - अक्सर 21 CFR 864.2220 के तहत क्लास I चिकित्सा उपकरणों के रूप में वर्गीकृत किए जाते हैं, जो उन्हें पूर्व-बाजार अधिसूचना आवश्यकताओं से छूट देते हैं[6][7].
यूरोपीय संघ में, नियामक ढांचा यूके के साथ निकटता से मेल खाता है, क्योंकि यह भी विनियमन (EU) 2015/2283 का पालन करता है। &यूरोपीय खाद्य सुरक्षा प्राधिकरण (EFSA) प्राधिकरण प्रक्रिया की देखरेख करता है[1] । ICH Q6B दिशानिर्देशों के अनुसार, वृद्धि मीडिया घटक, जिनमें एंटीबायोटिक्स, प्रेरक, और अन्य घटक शामिल हैं, प्रक्रिया-संबंधित अशुद्धियों के रूप में माने जाते हैं। इन अशुद्धियों को नियंत्रित और स्वीकार्य स्तरों तक कम किया जाना चाहिए[5]।जहाँ संभव हो, सहायक पदार्थ और अभिकर्मक फार्माकोपियल मानकों का पालन करना चाहिए [5]।
| न्याय क्षेत्र | प्राथमिक विनियमन | वर्गीकरण | सुरक्षा प्रणाली | मीडिया निगरानी |
|---|---|---|---|---|
| यूनाइटेड किंगडम (GB) | समाहित विनियमन (EU) 2015/2283 [1] | पशु उत्पत्ति का उत्पाद (POAO) [3] | HACCP (Reg 852/2004) [3] | FSA/FSS सैंडबॉक्स मार्गदर्शन [1] |
| यूरोपीय संघ / NI | विनियमन (EU) 2015/2283 [1] | पशु उत्पत्ति का उत्पाद (POAO) [3] | HACCP (Reg 852/2004) [3] | EFSA प्राधिकरण प्रक्रिया [1] |
| संयुक्त राज्य | FD&C Act Section 501(a)(4)(B) [4] | New Animal Drug / Food [4] | CGMP (21 CFR 210/211) [4] | FDA CVM / USDA-FSIS [4] |
संवर्धित मांस के लिए नियामक आवश्यकताएँ
संवर्धित मांस के उत्पादकों को यह सुनिश्चित करना चाहिए कि विकास मीडिया का हर बैच सख्त सुरक्षा और गुणवत्ता मानकों का पालन करता है।विकास मीडिया सत्यापन इन उत्पादों के व्यापक नियामक ढांचे का मुख्य पहलू है। HACCP सिद्धांतों (विनियमन (EC) 852/2004) के तहत, विकास मीडिया को एक प्राथमिक इनपुट और संक्रमण - रासायनिक, सूक्ष्मजीविकीय, या अन्यथा [3] के संभावित स्रोत के रूप में पहचाना गया है। FSA इस चिंता को उजागर करता है:
"कोशिका-संवर्धित उत्पादों के उत्पादन में मुख्य खतरों में कोशिका रेखा की पहचान (और स्थिरता), उत्पादन प्रक्रिया के दौरान उत्पन्न खतरे (सूक्ष्मजीविकीय संक्रमण, विकास मीडिया और अंतिम उत्पाद में अवशिष्ट घटक), और एलर्जेंस शामिल हैं।" [3]
यदि विकास मीडिया के सूत्रीकरण में परिवर्तन होते हैं, तो एक तात्कालिक HACCP समीक्षा की आवश्यकता होती है [3]।In the UK, validation must take place before implementation to ensure the accuracy of flow diagrams and the effectiveness of control measures [3] .
संयुक्त राज्य अमेरिका में, FDA यह अनिवार्य करता है कि सभी अभिकर्मक और मीडिया घटक कठोर गुणवत्ता मानकों को पूरा करें ताकि हानिकारक एजेंटों के परिचय से बचा जा सके [4]। आपूर्तिकर्ताओं और अनुबंध प्रयोगशालाओं को CGMP विनियमों का पालन करना चाहिए, और किसी भी आपूर्तिकर्ता को जो अनुपालन करने में विफल रहता है, उसे हटाया जाना चाहिए ताकि उत्पादों को "मिलावटी" के रूप में वर्गीकृत होने से रोका जा सके [4]। FDA इस बात के महत्व को रेखांकित करता है:
"सभी नए पशु दवाओं, जिनमें ACTPs शामिल हैं, को CGMP के अनुसार निर्मित किया जाना चाहिए ताकि यह सुनिश्चित किया जा सके कि ऐसी दवाएं संघीय खाद्य, औषधि, और प्रसाधन सामग्री अधिनियम (FD&C Act) की सुरक्षा आवश्यकताओं को पूरा करती हैं।" [4]
वर्तमान में, यूके के नियामक सैंडबॉक्स में भाग लेने वाली कई कंपनियाँ - जैसे BlueNalu, Gourmey, Hoxton Farms, Mosa Meat, Roslin Technologies, Vital Meat, और Vow - इन तकनीकी मानकों को परिष्कृत करने के लिए FSA के साथ सहयोग कर रही हैं [1] । यूके के नियमों के तहत, व्यवसाय प्राधिकरण प्रक्रिया के दौरान प्रस्तुत गोपनीय जानकारी के लिए पांच साल तक डेटा सुरक्षा का अनुरोध कर सकते हैं [1].
विकास मीडिया को मान्य करने के लिए कदम
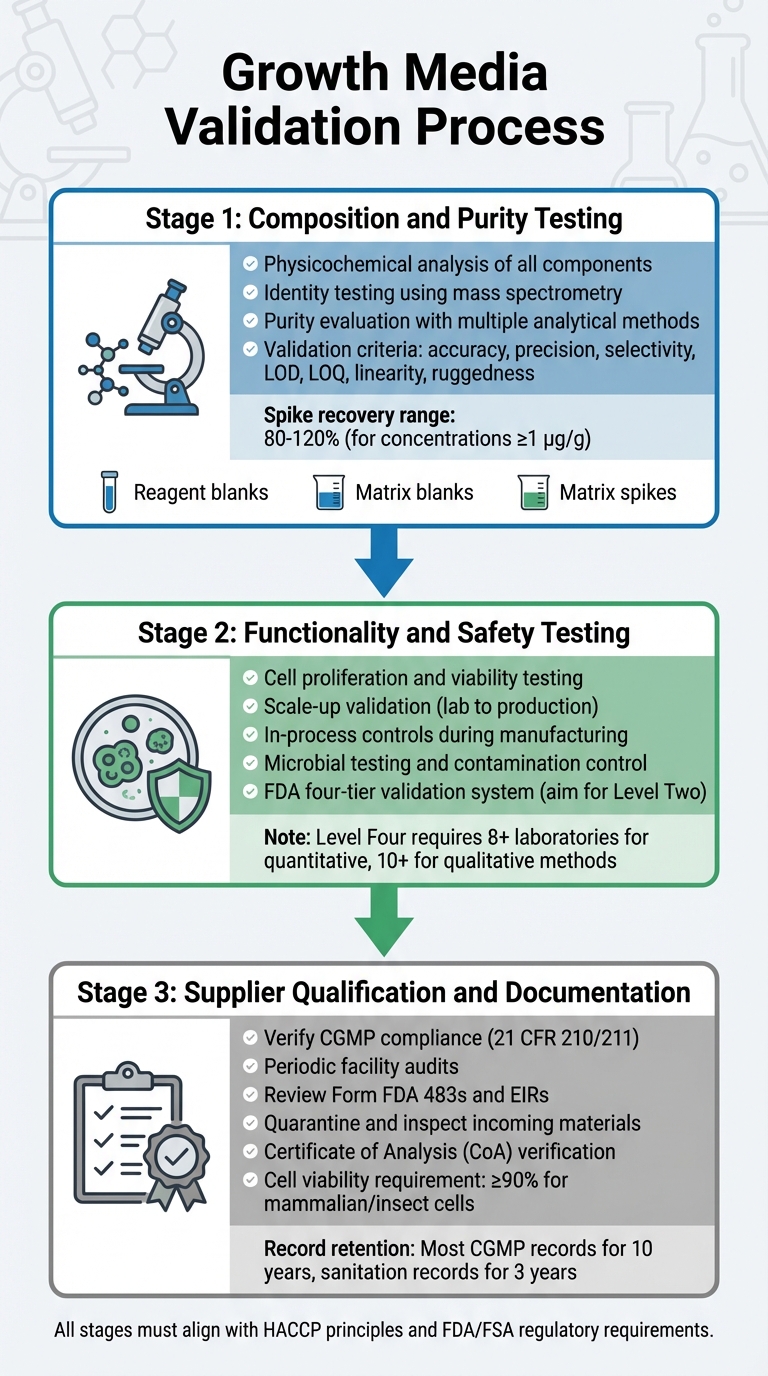
संवर्धित मांस नियामक अनुमोदन के लिए विकास मीडिया मान्यकरण प्रक्रिया
विकास मीडिया को मान्य करना एक विस्तृत प्रक्रिया है जो इसकी संरचना, कार्यक्षमता, सुरक्षा, और आपूर्तिकर्ता अनुपालन की जांच करती है।प्रत्येक चरण पिछले पर आधारित होता है, यह सुनिश्चित करते हुए कि एक मजबूत सत्यापन प्रक्रिया है जो नियामक आवश्यकताओं के साथ संरेखित होती है। इसमें संरचना, कार्यक्षमता, और बायोप्रोसेस मीडिया आपूर्तिकर्ता अनुपालन के लिए परीक्षण शामिल है।
संरचना और शुद्धता परीक्षण
पहला चरण प्रत्येक घटक के गहन भौतिक-रासायनिक विश्लेषण पर केंद्रित है। इसमें अमीनो एसिड, विटामिन, और अकार्बनिक लवण जैसे अवयवों की सटीक संरचना, भौतिक गुण, और आणविक संरचना की पहचान करना शामिल है [5]। आणविक संरचनाओं की पुष्टि करने के लिए, पहचान परीक्षण अत्यधिक विशिष्ट विधियों का उपयोग करता है, जिसमें भौतिक-रासायनिक, जैविक, और इम्यूनोकेमिकल तकनीकें शामिल हैं। उपकरण जैसे मास स्पेक्ट्रोमेट्री का उपयोग उनके विखंडन पैटर्न के माध्यम से आणविक पहचान की पुष्टि करने के लिए किया जाता है [8]।
शुद्धता मूल्यांकन के लिए अशुद्धियों से वांछित घटकों को अलग करने के लिए कई विश्लेषणात्मक विधियों की आवश्यकता होती है।इन परीक्षणों को प्रक्रिया-संबंधी और उत्पाद-संबंधी अशुद्धियों दोनों को संबोधित करना चाहिए [5]। विश्लेषणात्मक तकनीकों को सटीकता, परिशुद्धता, चयनात्मकता, पहचान की सीमाएं (LOD), मात्रात्मकता की सीमाएं (LOQ), रैखिकता, और मजबूती सहित सख्त सत्यापन मानदंडों को पूरा करना चाहिए [8]। सत्यापन प्रोटोकॉल में शामिल होना चाहिए:
- रिएजेंट ब्लैंक्स यह सुनिश्चित करने के लिए कि रिएजेंट्स एनालाइट्स से मुक्त हैं।
- मैट्रिक्स ब्लैंक्स यह पुष्टि करने के लिए कि नमूना वातावरण हस्तक्षेप नहीं करता है।
- मैट्रिक्स स्पाइक्स रिकवरी और सटीकता का अनुमान लगाने के लिए।
1 µg/g (ppm) सांद्रता पर मात्रात्मक विधियों के लिए, स्वीकार्य स्पाइक रिकवरी आमतौर पर 80% और 120% के बीच होती है [8]।
संगति बनाए रखने के लिए, निर्माताओं को उत्पादन-प्रतिनिधि लॉट से प्राप्त इन-हाउस प्राथमिक संदर्भ सामग्री स्थापित करनी चाहिए। ये कार्यशील संदर्भ सामग्री को अंशांकित करने के लिए अनुरेखनीय मानक के रूप में कार्य करते हैं [5]। एक बार शुद्धता परीक्षण पूरा हो जाने के बाद, मीडिया को प्रभावी सेल वृद्धि का समर्थन करने और सुरक्षा मानकों को पूरा करने की अपनी क्षमता का प्रदर्शन करना चाहिए।
कार्यक्षमता और सुरक्षा परीक्षण
संरचना की पुष्टि करने के बाद, मीडिया को संवर्धित मांस उत्पादन का समर्थन करने में अपनी प्रभावशीलता साबित करनी चाहिए। इसमें यह दिखाना शामिल है कि कोशिकाएं प्रजनन कर सकती हैं, जीवन शक्ति बनाए रख सकती हैं, और प्रयोगशाला की स्थितियों से उत्पादन मात्रा तक स्केल कर सकती हैं। इस संक्रमण के लिए अक्सर पायलट-स्केल सिस्टम की आवश्यकता होती है ताकि आवश्यक नियामक डेटा उत्पन्न किया जा सके।FDA निर्माण के दौरान प्रक्रिया नियंत्रण की आवश्यकता होती है, जो प्रारंभिक चरणों जैसे कि सेल पासेजिंग और हार्वेस्टिंग से शुरू होती है, ताकि उत्पाद की स्थिरता और सुरक्षा सुनिश्चित की जा सके [4].
सुरक्षा सत्यापन में कठोर माइक्रोबियल परीक्षण और संदूषण नियंत्रण शामिल होता है, जैसा कि FDA के पूर्व-बाजार मूल्यांकन में वर्णित है [9].
FDA रासायनिक विधि सत्यापन के लिए चार-स्तरीय प्रणाली का उपयोग करता है, जो स्तर एक (आपातकालीन या सीमित उपयोग) से लेकर स्तर चार (AOAC/ISO मानकों को पूरा करने वाले पूर्ण सहयोगात्मक अध्ययन) तक है [8]. नियमित नियामक परीक्षण के लिए, स्तर दो एकल-प्रयोगशाला सत्यापन का लक्ष्य रखें, जिसमें एक व्यापक प्रदर्शन मूल्यांकन शामिल है [8]. मात्रात्मक विधियों के लिए पूर्ण सहयोगात्मक अध्ययन में कम से कम आठ प्रयोगशालाओं की भागीदारी की आवश्यकता होती है, जबकि गुणात्मक विधियों के लिए दस की आवश्यकता होती है [8].एक बार जब मीडिया का प्रदर्शन सत्यापित हो जाता है, तो यह सुनिश्चित करना आवश्यक है कि सभी कच्चे माल अनुपालन करने वाले आपूर्तिकर्ताओं से आएं।
आपूर्तिकर्ता योग्यता और दस्तावेज़ीकरण
निर्माताओं को सत्यापित, CGMP-अनुपालन आपूर्तिकर्ताओं के साथ काम करना चाहिए। आपूर्तिकर्ताओं को 21 CFR 210/211 में उल्लिखित मानकों को पूरा करना चाहिए [4]। सत्यापन में गुणवत्ता कार्यक्रमों, प्रक्रियाओं और समग्र CGMP अनुपालन के पालन का आकलन करने के लिए आपूर्तिकर्ता सुविधाओं का समय-समय पर ऑडिट शामिल होता है [4]।
अनुबंधों में प्रवेश करने से पहले, एक आपूर्तिकर्ता के अनुपालन इतिहास की समीक्षा करें, जिसमें फॉर्म FDA 483s और स्थापना निरीक्षण रिपोर्ट (EIRs) शामिल हैं [4]।FDA इस दायित्व को रेखांकित करता है:
"किसी अन्य प्रतिष्ठान के साथ आपके लिए किसी भी निर्माण चरण को करने के लिए किसी अनुबंध, समझौते, या अन्य व्यवस्था में प्रवेश करने से पहले, आपको यह सत्यापित करना चाहिए कि प्रतिष्ठान लागू नियामक CGMP का पालन करता है।" [4]
सभी आने वाली सामग्रियों को रिलीज़ से पहले क्वारंटाइन और निरीक्षण किया जाना चाहिए, यह सुनिश्चित करते हुए कि वे मास्टर विनिर्देशों को पूरा करते हैं [10]। आपूर्तिकर्ताओं को एक विश्लेषण प्रमाणपत्र (CoA) या ट्रेस करने योग्य, CGMP/GLP-अनुपालन परीक्षण परिणाम प्रदान करने की आवश्यकता होती है [10]। स्थिर सेल लाइनों के लिए, दस्तावेज़ में एक ट्रेस करने योग्य क्लोनिंग इतिहास शामिल होना चाहिए [10]। स्तनधारी या कीट कोशिकाओं को आमतौर पर CGMP परियोजनाओं में स्वीकृति के लिए कम से कम 90% जीवन शक्ति की आवश्यकता होती है [10]। रिकॉर्ड को नियामक दिशानिर्देशों के अनुसार बनाए रखा जाना चाहिए [4]।
अनुबंधों में स्पष्ट रूप से CGMP जिम्मेदारियों का उल्लेख होना चाहिए और आपूर्तिकर्ताओं को परीक्षण किट या कार्यप्रणालियों में किसी भी प्रस्तावित परिवर्तन के बारे में निर्माताओं को सूचित करने की आवश्यकता होनी चाहिए [4]। यदि परीक्षण आउटसोर्स किया गया है, तो सुनिश्चित करें कि अनुबंध प्रयोगशालाएं मान्यताप्राप्त विश्लेषणात्मक विधियों का उपयोग करती हैं और FDA-पंजीकृत हैं [4]।
विनियामक प्रस्तुति दस्तावेज तैयार करना
एक बार जब आपका वृद्धि माध्यम मान्य हो जाता है, तो अगला कदम एक डोजियर तैयार करना है जो FDA और USDA-FSIS द्वारा आवश्यक सभी सुरक्षा और गुणवत्ता मानकों के अनुपालन को प्रदर्शित करता है। यह डोजियर मान्यता और विनियामक अनुपालन के बीच एक महत्वपूर्ण कड़ी के रूप में कार्य करता है, जिससे अधिकारियों को आपके माध्यम की सुरक्षा और उत्पादन प्रक्रियाओं का स्पष्ट दृष्टिकोण मिलता है।
प्रस्तुतिकरण डॉसियर के आवश्यक तत्व
आपके डॉसियर में मीडिया संरचना का विस्तृत विवरण शामिल होना चाहिए, जिसमें सभी अमीनो एसिड, विटामिन, अकार्बनिक लवण, और वृद्धि कारक सूचीबद्ध हों। FDA दिशानिर्देश इस बात पर जोर देते हैं कि समीक्षा प्रक्रिया केवल मीडिया ही नहीं बल्कि पूरे उत्पादन कार्यप्रवाह का मूल्यांकन करती है। इसमें प्राथमिक और अमर कोशिका रेखाओं और बैंकों की स्थापना, निर्माण नियंत्रणों का कार्यान्वयन, और सभी घटकों और इनपुट्स का सत्यापन शामिल है[11].
इसके अतिरिक्त, डॉसियर में एक व्यापक सुरक्षा और विषाक्तता मूल्यांकन शामिल होना चाहिए, जो यह साबित करता है कि संवर्धित सामग्री और उसके सभी इनपुट्स की खाद्य सुरक्षा है। आपके उत्पादन की निरंतरता और प्रदूषकों से मुक्त होने को प्रदर्शित करने के लिए निर्माण नियंत्रण रिकॉर्ड, प्रक्रिया सत्यापन डेटा, और गुणवत्ता कार्यक्रम दस्तावेज़ीकरण शामिल करें।
आपको आपूर्ति और अभिकर्मक सत्यापन रिकॉर्ड भी प्रदान करने चाहिए, जो मीडिया में उपयोग की गई सभी सामग्रियों के लिए सत्यापन दिखाते हैं, जिसमें वे भी शामिल हैं जो इन-हाउस तैयार किए गए हैं। USDA-FSIS द्वारा विनियमित उत्पादों के लिए, HACCP योजनाएं और स्वच्छता प्रोटोकॉल शामिल करें। FDA सलाह देता है कि अधिकांश CGMP रिकॉर्ड को कम से कम 10 वर्षों के लिए रखा जाए, जबकि सुविधा की सफाई और स्वच्छता रिकॉर्ड को कम से कम 3 वर्षों के लिए रखा जाना चाहिए[4]। यह आपूर्तिकर्ता योग्यता प्रयासों के साथ मेल खाता है, यह सुनिश्चित करते हुए कि सभी इनपुट CGMP और नियामक आवश्यकताओं को पूरा करते हैं।
सुविधा अनुपालन का दस्तावेजीकरण
मानव उपभोग के लिए संवर्धित मांस का उत्पादन, प्रसंस्करण, या भंडारण करने से पहले, सुविधाओं को FDA के साथ पंजीकरण करना होगा[12]।आपके दस्तावेज़ में एक व्यापक खाद्य सुरक्षा योजना शामिल होनी चाहिए जो खतरा विश्लेषण (जैविक, रासायनिक, और भौतिक), निवारक नियंत्रण (जैसे स्वच्छता, एलर्जेन प्रबंधन, और आपूर्ति श्रृंखला उपाय), और निगरानी प्रक्रियाओं[12] को संबोधित करती हो।
मीडिया फिल सिमुलेशन भी एक प्रमुख आवश्यकता है। इनमें 14-दिन की ऊष्मायन और वृद्धि संवर्धन परीक्षण शामिल हैं ताकि स्वच्छ प्रथाओं की पुष्टि की जा सके। जैसा कि FDA बताता है:
"मीडिया फिल को महत्वपूर्ण (निर्जल) उपकरणों की स्वच्छ असेंबली और संचालन का मूल्यांकन करना चाहिए, ऑपरेटरों की योग्यता और उनकी तकनीक का आकलन करना चाहिए, और यह प्रदर्शित करना चाहिए कि पर्यावरणीय नियंत्रण पर्याप्त हैं" [2]।
सुनिश्चित करें कि आपके रिकॉर्ड में आपूर्तिकर्ता योग्यता डेटा शामिल है, जैसे कि किसी विक्रेता से पहले तीन बैचों के माध्यम पर किए गए परीक्षण यह पुष्टि करने के लिए कि वे विश्लेषण प्रमाणपत्र से मेल खाते हैं।अन्य आवश्यक रिकॉर्ड में पर्यावरण नियंत्रण लॉग, उपकरण अंशांकन अनुसूचियाँ, और तापमान निगरानी डेटा शामिल हैं। USDA-नियंत्रित प्रक्रियाओं के लिए, HACCP योजनाएँ, लिखित स्वच्छता मानक संचालन प्रक्रियाएँ (SSOPs), और रिकॉल प्रक्रियाएँ तैयार करें [12][13].
sbb-itb-ffee270
Using Cellbase for Regulatory-Compliant Growth Media Procurement
संस्कृत मांस के लिए सत्यापित आपूर्तिकर्ता
एक बार जब आपने अपने ग्रोथ मीडिया फॉर्मूलेशन को मान्य कर लिया है, तो अगला कदम उन घटकों की सोर्सिंग करना है जो नियामक मानकों को पूरा करते हैं। यह सामान्य आपूर्तिकर्ताओं से ऑर्डर करने जितना सरल नहीं है। सेल-संस्कृत उत्पादों के लिए, सख्त स्वच्छता नियम लागू होते हैं, और हर ग्रोथ मीडिया घटक को नियामक अनुमोदन के लिए विशिष्ट दस्तावेजों के साथ आना चाहिए [3]। यहीं पर
खरीदारी विशेषताएँ
प्लेटफ़ॉर्म पारदर्शी मूल्य निर्धारण और एक सीधा संदेश सुविधा भी प्रदान करता है, जिससे टीमों को जल्दी से उद्धरण, विश्लेषण प्रमाणपत्र, और अन्य नियामक दस्तावेज़ों का अनुरोध करने में सक्षम बनाता है। इन महत्वपूर्ण खरीद कार्यों को एक प्रणाली में समेकित करके, जो कि संवर्धित मांस उत्पादन के लिए अनुकूलित है,
निष्कर्ष
विनियामक अनुमोदन के लिए वृद्धि मीडिया को मान्य करना सिर्फ एक बॉक्स को टिक करना नहीं है - यह कानूनी आवश्यकता है जो यूके बाजार में संवर्धित मांस उत्पादों को पेश करने के लिए आवश्यक है। इसमें संरचना और शुद्धता के लिए गहन परीक्षण, एक मजबूत HACCP योजना को लागू करना, और हर कदम पर विस्तृत दस्तावेज़ीकरण रखना शामिल है।
"खाद्य को बाजार में नहीं रखा जाना चाहिए यदि यह असुरक्षित है। इसका मतलब है कि यह न तो स्वास्थ्य के लिए हानिकारक है और न ही मानव उपभोग के लिए अनुपयुक्त।" - खाद्य मानक एजेंसी [3]
यूके खाद्य मानक एजेंसी का £1.6 मिलियन रेगुलेटरी सैंडबॉक्स उद्योग के खिलाड़ियों के साथ काम करने की अपनी प्रतिबद्धता को दर्शाता है ताकि वृद्धि मीडिया संरचना पर स्पष्ट तकनीकी मार्गदर्शन स्थापित किया जा सके [1]। जो कंपनियाँ अब उचित सत्यापन को प्राथमिकता देती हैं, वे इन दिशानिर्देशों के पूरी तरह से परिभाषित होने पर मजबूत स्थिति में होंगी।
अनुपालन मानकों को पूरा करना केवल नियामक बॉक्सों को टिक करने के बारे में नहीं है - यह उपभोक्ता विश्वास अर्जित करने और उत्पाद सुरक्षा सुनिश्चित करने के बारे में है। कठोर गुणवत्ता परीक्षण नियामक अनुमोदन और बाजार स्वीकृति प्राप्त करने के केंद्र में है। प्राधिकरण प्रक्रिया को सुव्यवस्थित करने के लिए, मजबूत सत्यापन प्रोटोकॉल बनाने, सटीक रिकॉर्ड बनाए रखने और विश्वसनीय आपूर्तिकर्ताओं के साथ साझेदारी करने पर ध्यान केंद्रित करें। ये कदम न केवल अनुमोदन को सरल बनाएंगे बल्कि उपभोक्ता विश्वास के लिए भी मार्ग प्रशस्त करेंगे।
सामान्य प्रश्न
विनियामक अनुमोदन के लिए वृद्धि मीडिया को मान्य करने के मुख्य चरण क्या हैं?
विनियामक अनुमोदन के लिए वृद्धि मीडिया को मान्य करना यह साबित करने के बारे में है कि सूत्रीकरण सुरक्षित, विश्वसनीय और संवर्धित मांस के उत्पादन के लिए उपयुक्त है। प्रक्रिया आमतौर पर इस प्रकार दिखती है:
- जोखिम मूल्यांकन: उस सेल लाइन को परिभाषित करके शुरू करें जिसका आप उपयोग करेंगे, उत्पाद के लक्ष्य और इसके महत्वपूर्ण गुणवत्ता विशेषताएँ (जैसे पीएच या पोषक तत्व संरचना)। किसी भी संभावित खतरों की पहचान करें, जैसे सूक्ष्मजीव संदूषण, और इन जोखिमों को नियंत्रित करने के उपाय निर्धारित करें।
- परीक्षण और विनिर्देश: नसबंदी, शुद्धता और शक्ति जैसे कारकों के लिए स्पष्ट स्वीकृति मानदंड निर्धारित करें। यह सुनिश्चित करने के लिए स्थापित परीक्षण विधियों का उपयोग करें कि ये मानक लगातार पूरे होते हैं।
- मान्यता अध्ययन: परिणामों की पुनरावृत्ति और स्थिरता की पुष्टि करने के लिए उपकरणों की योग्यता और कई बैचों का परीक्षण सहित व्यापक प्रक्रिया मान्यता का संचालन करें।
- स्थिरता परीक्षण: उचित भंडारण स्थितियों (आमतौर पर 2–8 °C) के तहत अपने निर्धारित शेल्फ जीवन के दौरान इसकी गुणवत्ता का मूल्यांकन करके मीडिया की स्थिरता की जांच करें।
- प्रलेखन: सभी को एक व्यापक मान्यता डोजियर में एकत्रित करें। इसमें सभी परीक्षण परिणाम और विश्लेषण शामिल होने चाहिए ताकि नियामक आवश्यकताओं को पूरा किया जा सके।
इनमें से प्रत्येक चरण को सावधानीपूर्वक संबोधित करके, आप यह दिखाने के लिए आवश्यक साक्ष्य एकत्र करेंगे कि मीडिया खेती किए गए मांस उत्पादन के लिए आवश्यक सुरक्षा और गुणवत्ता मानकों को पूरा करता है।
संवर्धित मांस के लिए प्रयुक्त वृद्धि माध्यम के लिए यूके और यूएस विनियमों के बीच मुख्य अंतर क्या हैं?
यूनाइटेड किंगडम में, संवर्धित मांस के लिए वृद्धि माध्यम का विनियमन नवीन खाद्य विनियमन (ईयू विनियमन 2015/2283) के अंतर्गत आता है, जिसे जीबी कानून में बनाए रखा गया है। किसी भी वृद्धि माध्यम का उपयोग उन उत्पादों में किया जाता है जो 15 मई 1997 से पहले आमतौर पर उपभोग नहीं किए जाते थे, उन्हें खाद्य मानक एजेंसी (FSA) द्वारा एक औपचारिक नवीन-खाद्य मूल्यांकन से गुजरना पड़ता है। इस प्रक्रिया के लिए विस्तृत दस्तावेज प्रस्तुत करना आवश्यक है, जिसमें माध्यम की संरचना, उत्पत्ति और शुद्धता की जानकारी शामिल है। इसके अतिरिक्त, HACCP-आधारित जोखिम मूल्यांकन आवश्यक है ताकि यह प्रदर्शित किया जा सके कि सेल-संस्कृति प्रक्रिया के दौरान संदूषकों को कैसे नियंत्रित किया जाता है।
दिसंबर 2025 से, FSA ने एक सेल-संवर्धित उत्पाद सैंडबॉक्स लागू किया है। यह पहल नवीन-खाद्य अनुप्रयोगों के लिए मार्गदर्शन और तेज डेटा संग्रह का समर्थन प्रदान करती है।अंतिम अनुमोदन प्राप्त करने के लिए, कंपनियों को एक व्यापक दस्तावेज़ प्रस्तुत करना होगा जो मीडिया सुरक्षा, स्थिरता, और निर्माण सत्यापन को संबोधित करता है। केवल इस अनुमोदन के बाद ही उत्पाद को ग्रेट ब्रिटेन में बेचा जा सकता है।
इसके विपरीत, संयुक्त राज्य अमेरिका में वृद्धि मीडिया के लिए एक विशिष्ट नवीन-खाद्य ढांचा नहीं है, जिससे सीधे नियामक तुलना करना चुनौतीपूर्ण हो जाता है। यूके-आधारित कंपनियों के लिए, उन मीडिया घटकों का स्रोत जो पहले से ही इन सख्त मानकों का पालन करते हैं, अनुमोदन प्रक्रिया को सरल बना सकता है।
यूके का नियामक सैंडबॉक्स वृद्धि मीडिया सत्यापन का समर्थन कैसे करता है?
संवर्धित उत्पादों के लिए यूके का नियामक सैंडबॉक्स एक सुव्यवस्थित सेटिंग प्रदान करता है जहां कंपनियां अपने वृद्धि मीडिया सूत्रों का परीक्षण और परिष्कृत कर सकती हैं।खाद्य मानक एजेंसी (FSA) और खाद्य मानक स्कॉटलैंड (FSS) द्वारा देखरेख में, यह कार्यक्रम छह महीने के चरणों में चलता है। इस समय के दौरान, व्यवसाय सुरक्षा परीक्षण कर सकते हैं, जोखिम आकलन कर सकते हैं, और दस्तावेजों की समीक्षा कर सकते हैं, जबकि नियामकों से मूल्यवान प्रतिक्रिया प्राप्त कर सकते हैं।
यह व्यावहारिक दृष्टिकोण व्यावहारिक परीक्षणों और चरण-दर-चरण सुधारों की अनुमति देता है, सुरक्षा डेटा के संग्रह को तेज करता है और कंपनियों को नियामक आवश्यकताओं के साथ संरेखित करने में मदद करता है। जो लोग संवर्धित मांस पर काम कर रहे हैं, उनके लिए











