培養肉の生産において、遺伝的安定性は非常に重要です。これがなければ、細胞株が変異し、品質の不一致、安全性のリスク、生産の失敗を引き起こす可能性があります。数千から数兆の細胞にスケールアップすることで、これらのリスクが増幅され、堅牢な品質管理システムが不可欠となります。FDAや EMAのような規制当局は、製品を承認する前に安定性の証明を要求します。なぜなら、わずかな遺伝的変化でもアレルギー反応や有害な結果を引き起こす可能性があるからです。
主な課題には、遺伝的ドリフト、変異の蓄積、癌遺伝子の活性化が含まれます。これらの問題は、細胞の継代培養、選択圧、そして生産中の環境ストレスから生じます。核型分析、SNPアレイ、次世代シーケンシング(NGS)などの高度な試験方法は、これらのリスクを検出し対処するのに役立ちます。構造化された細胞バンキングや標的遺伝子工学のような予防戦略は、不安定性に対するさらなる安全策となります。
生産者は、セルバンキングから大規模なバイオリアクターに至るまで、すべての生産段階で品質管理を統合する必要があります。STRプロファイリング、汚染テスト、機能アッセイなどのツールは、一貫性と安全性を確保します。
DNAからマスターセルバンクまでの細胞株開発の加速 - AGC Biologics
遺伝的安定性を維持する際の一般的な課題
培養肉の生産サイクル全体で遺伝的安定性を確保することは容易ではありません。生産の規模が大きいほど、遺伝的変化が発生し広がる機会が増えます。これらの課題を認識することは、効果的な品質管理システムを導入するための鍵です。
遺伝的浮動と突然変異の蓄積
拡張された細胞継代は、培養肉生産におけるゲノム不安定性の主要な原因です。不死化細胞株は、その性質上、ゲノムの変化を起こしやすく、長期培養中に自発的な突然変異を引き起こす可能性があります[6][5]. 細胞が複数回の集団倍加を経ると、DNA複製のエラーが蓄積し、多様な細胞集団が形成され、機能喪失の可能性があります。BioPharm Internationalのクリストファー・フライとルホン・ヒーはこの問題を強調しています:
クローン由来のCHO細胞株は、長期間のサブカルチャーを経て、しばしば異なる異質な集団になることが観察されています[6].
産業環境では、約20%の生産細胞株が世代を重ねるごとに顕著なトランスジーンの不均一性を示します[6]. これらの突然変異は、トランスフェクション後のDNA複製中や、外来遺伝子が宿主ゲノムに統合される際のエラーにより、早期に発生する可能性があります[5].
選択圧は複雑さをさらに増します。細胞株を安定化させるために使用される抗生物質や代謝マーカー(e.g. 、MTX)などのエージェントは、実際には突然変異率を増加させる可能性があります[6][5]. 場合によっては、これらのエージェントの濃度が高いほど、突然変異率も高くなります[6]. 栄養不足、スケールアップ中の最適でない培養条件、拡大による物理的ストレスなどの環境ストレッサーは、遺伝的完全性をさらに不安定にする可能性があります[6][5].
html細胞株開発ディレクターのShuai Wang氏、WuXi Biologics, は次のように述べています:
変異レベルは、チャイニーズハムスター卵巣(CHO)細胞のゲノムの可塑性のために、細胞の継代中に変化する可能性があります[5].
エピジェネティックな変化も役割を果たします。トランスジーンは、培養プロセス中に部分的または完全に失われたり、サイレンシングされたりすることがあり、長期的な安定性に影響を与えます。これらの蓄積された変異は、細胞機能を損なうだけでなく、癌遺伝子の活性化リスクを増加させます。
癌遺伝子活性化のリスク
癌遺伝子の活性化は、培養肉の生産者にとって重大な安全性の懸念を表しており、全生産バッチを危険にさらす可能性があります。遺伝的不安定性は、ハイパーメチル化のようなメカニズムを通じて癌遺伝子の活性化を引き起こし、腫瘍のようなプロファイルをもたらす可能性があります[3][1]. 生産における急速な拡大は、これらの有害な突然変異を蓄積する可能性をさらに高めます[5][6].
これはよく認識されている課題です。国際イノベーションコンソーシアム& 医薬品開発の品質(IQ)によれば、67%の回答者が、遺伝子変異が生産中のアミノ酸誤挿入よりも大きな脅威をもたらすと考えています[5] . 2024年5月の事例は、この問題の深刻さを示しています。WuXi Biologicsは、細胞株開発プログラムのクローンの43%が同じ遺伝子点突然変異を持っていることを発見しました。根本原因は?トランスフェクション中に使用されたプラスミドDNAの2.1%–2.2%の変異レベルが、従来のサンガーシーケンシングでは検出されなかったことです。これに対処するため、同社は次世代シーケンシング(NGS)を品質管理プロセスに組み込み、早期にそのような変異を検出するようにしました[5].
遺伝子異常の早期発見は重要であり、発がん性の変化は全体のバッチを危険にさらす可能性があります。標準的なGバンド核型分析は、20細胞の中期において14%のモザイク性で異常なサブポピュレーションを特定することができます[1]. NGSのようなより高度な技術は、0.5%の感度でクローン細胞の遺伝子変異を検出することができます[5].
DNAメチル化解析は、腫瘍形成の可能性を評価するためのもう一つの貴重なツールです:
DNAメチル化レベルと特定の遺伝子の過剰メチル化が癌の開始と進行において発生するため、DNAメチル化プロファイルの解析は、細胞の腫瘍形成の可能性に関する補完的な情報を提供するかもしれません[3].
本当の課題は、安全性を損なう前にこれらの変化を特定できる堅牢な監視システムを実装することにあります。培養肉の生産者にとって、急速な細胞増殖中の遺伝的安定性を維持することは、高度な品質管理措置を必要とします。
品質管理試験方法
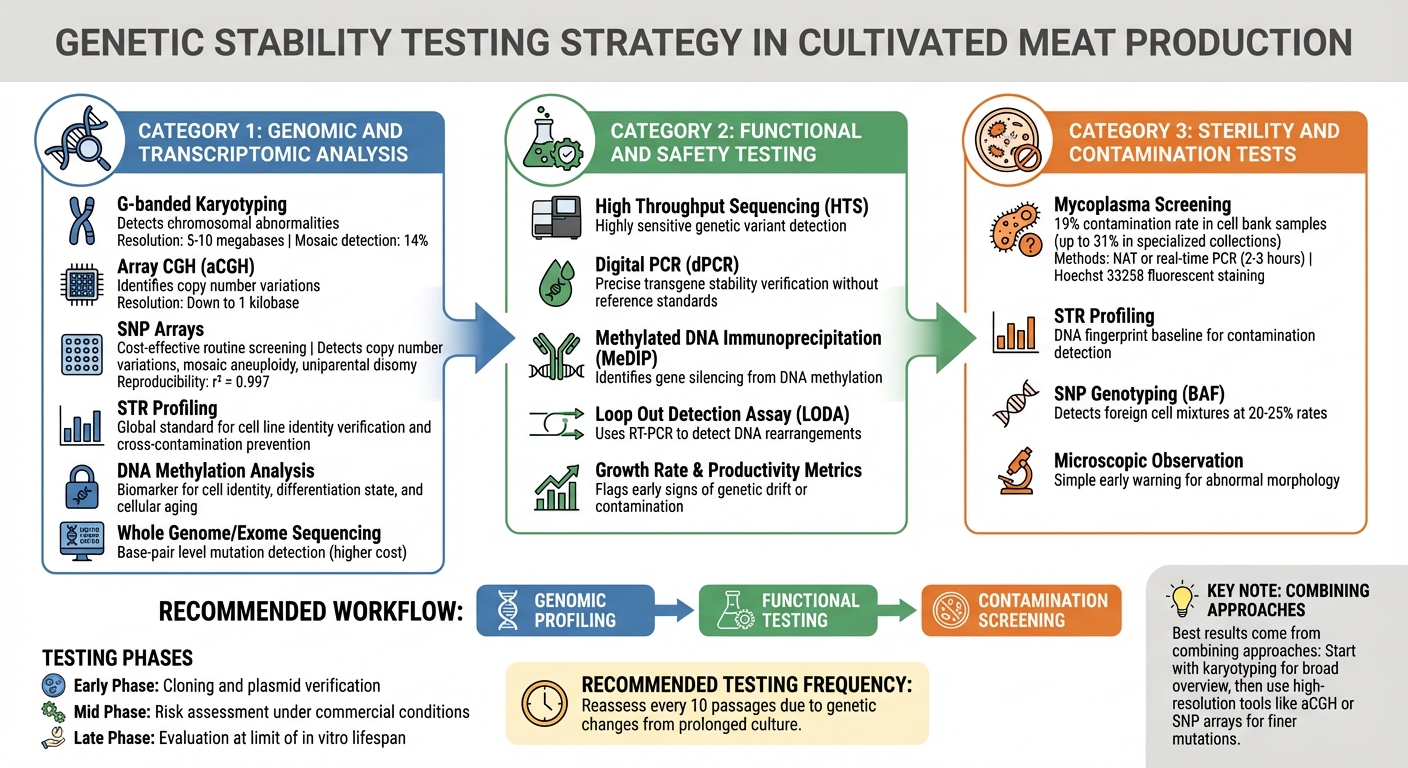
培養肉細胞株における遺伝的安定性のための品質管理試験方法
生産に影響を与える前に遺伝的不安定性を特定するには、多層的な試験戦略が必要です。培養肉の生産者は、大きな染色体変化から単一塩基変異までを検出する方法に依存しています。技術の選択は、各生産段階で存在するリスクに依存します。これらのゲノムツールは、詳細な機能評価や汚染評価に続く最初のチェックポイントとして機能します。
ゲノムおよびトランスクリプトーム解析
Gバンド染色体分析は、数的異常や転座のような大規模な構造再編成などの主要な染色体問題を特定するための重要なツールです。モザイクレベルを約14%検出できますが、その解像度は5〜10メガベースの変化に限定されており、小さな変化は見逃される可能性があります[1] .
アレイ比較ゲノムハイブリダイゼーション(aCGH)は、1キロベースまでのコピー数変異を特定する高い解像度を提供します。同様に、一塩基多型(SNP)アレイは、コピー数変異、モザイク性異数性、片親性ダイソミーを検出するための費用対効果の高いオプションを提供します。検証研究では、SNPアレイが非常に再現性が高いことが示されており、Bアレル頻度(BAF)の測定で印象的なr² = 0を達成しています。997 [8] [1].
アンダルシア公衆衛生システムバイオバンクのRocio Aguilar-Quesadaは、方法を組み合わせる価値を強調しています:
核型分析は、特に高解像度のテストと組み合わせることで、依然として多用途なアッセイです [1].
ショートタンデムリピート(STR)プロファイリングは、細胞株の同一性を確認し、交差汚染を防ぐための世界標準です[1] [9]. 一方、DNAメチル化解析は、細胞の同一性、分化状態、および細胞の老化のバイオマーカーとして機能します[1]. 塩基対レベルの突然変異検出には、 全ゲノムまたはエクソームシーケンシングがオプションですが、アレイベースの方法と比較してコストが高くなります[1].
これらのアプローチを組み合わせることで、最良の結果が得られます。広範な概要を得るために核型分析から始め、高解像度ツールであるaCGHやSNPアレイを使用してより細かい変異を捉えます。長期間の培養は遺伝的変化を引き起こす可能性があるため、定期的な再評価 - 理想的には10パッセージごと - が重要です[10]. これらのゲノムの洞察は、製造全体で一貫した細胞挙動を確保するために機能アッセイで補完されます。
機能および安全性試験
ゲノムプロファイリングだけでは不十分です。機能試験は、細胞が拡張中に意図した特性を維持していることを確認します。成長率や生産性などの指標は、遺伝的ドリフトや汚染の初期兆候を示すことができます[9].
ハイスループットシーケンシング (HTS) は遺伝子変異を検出するために非常に感度が高く、デジタルPCR (dPCR) は参照標準を必要とせずにトランスジーンの安定性を正確に検証します[11] . BioPharm InternationalのChristopher FryeとLuhong Heはこのステップの重要性を強調しています:
生産細胞株はあらゆるバイオプロセスの基盤であり、したがって、生産細胞株の適切な遺伝子特性評価はプロセス開発の成功にとって絶対に重要です[6].
エピジェネティックな安定性も重要です。メチル化DNA免疫沈降 (MeDIP) は、DNAメチル化によって引き起こされる遺伝子サイレンシングを特定するのに役立ち、生産性低下の一般的な理由です[7]. ツールとして、ループアウト検出アッセイ(LODA) はRT-PCRを使用してDNAの再編成を検出します。例えば、選択マーカーが残っている間に目的の遺伝子が削除された場合などです[7].
テストは生産段階に合わせて行うべきです。初期段階のテストはクローニングとプラスミドの検証に焦点を当て、中期段階のテストは商業条件下でのリスクを評価し、後期段階のテストはin vitroでの寿命の限界にある細胞を評価します[6]. マスターセルバンクからの新鮮で低継代の細胞で実験を開始することは、遺伝的ドリフトのリスクを減少させます[9].
無菌性および汚染テスト
汚染テストは、遺伝子を不安定にする可能性のある要因を避けるために不可欠です。マイコプラズマは特に懸念されるもので、培養に目に見える変化を引き起こさずに細胞の代謝と行動を変化させます[1]. 研究によると、細胞バンクサンプルの19%にマイコプラズマ汚染が見られ、特定のコレクションでは31%に達することもあります[1] .
感度の高い核酸増幅技術(NAT)やリアルタイムPCRを使用した定期的なマイコプラズマスクリーニングにより、2〜3時間以内に準定量的な結果を提供できます[1]. Hoechst 33258蛍光染色は別の方法で、特徴的な細胞外蛍光パターンを明らかにします[9].
STRプロファイリングは、細胞株のDNAフィンガープリントを確立し、交差汚染を検出するための基準として機能します[9]. さらに、Bアレル頻度(BAF)分布を使用したSNPジェノタイピングにより、他の細胞株からの汚染を特定し、20〜25%の割合で異種細胞混合物を検出できます[8].
顕微鏡観察は、異常な細胞形態がしばしば培養の問題を示すため、シンプルでありながら効果的な早期警告ツールです[9]. ISO 9001:2015, やGood In Vitro Method Practices (GIVIMP)のような品質管理システムを導入することで、標準化された再現性のある培養条件を維持し、ゲノム不安定性のリスクを低減します[10].
特殊な試験装置や材料へのアクセスを必要とする培養肉生産者にとって、
sbb-itb-ffee270
遺伝的不安定性の予防戦略
遺伝的不安定性を検出することと、それを防ぐことは全く別の課題です。遺伝的安定性を維持するために、培養肉の生産者は、問題が発生する前に細胞株のドリフトを防ぐためのよく考えられたシステムが必要です。ここでの2つの主要な戦略は、 構造化された細胞バンキングとターゲットを絞った遺伝子工学. です。これらのアプローチは、遺伝的ドリフトと癌遺伝子活性化のリスクに直接対処します。
細胞バンキングと凍結保存
突然変異の蓄積は現実的な懸念事項であるため、信頼性のある細胞バンキングシステムが必要です。業界標準は、 マスターセルバンク (MCB)とワーキングセルバンク (WCB). の2層システムを含みます。このセットアップは、生産の一貫した出発点を保証します。継代の回数を制限することが重要であり、各継代は突然変異の可能性を高めます。細胞を液体窒素で保存することにより、生物学的活動が効果的に停止し、保存中の遺伝的変化のリスクが軽減されます。
時間を追跡する代わりに、細胞の年齢は増殖回数で測定されます。. 例えば、典型的な5,000リットルの生産用バイオリアクターでは、約30回の増殖が行われます。 [6]. 遺伝的一貫性を維持するために、商業生産ではこの数を45回から60回の増殖に制限しています。[6].
RT-PCRやシングルセルqPCRのようなスクリーニング方法は、異常なmRNAスプライシングやトランスジーンの変動性などの問題を早期に発見することができます。コピー数に大きな変動を示す細胞株は、将来の問題を避けるために廃棄されるべきです。
品質管理は妥協できません。驚くべきことに、いくつかのバンクでは最大31%の細胞株がマイコプラズマに汚染されていることが研究で判明しています。[3] . これを防ぐために、STRプロファイリング がバンキングプロセス全体で細胞株の真正性を確認するために使用されます。FSAの研究と証拠:
バンクされた細胞は最終製品の出発材料であるため、将来的に規制当局によって高品質で安全な肉製品を確保するために高い基準が要求される可能性があります[2] .
安定性のための遺伝子工学
遺伝子工学は、細胞株の安定性を直接強化することによって、もう一つの防御層を提供します。ターゲット統合 (TI), 特にリコンビナーゼ媒介カセット交換 (RMCE), のような技術は、特定のゲノム位置にトランスジーンを正確に挿入することを可能にします。このアプローチは、ランダムな統合の予測不可能性を回避し、位置効果やコピー数の不安定性が混乱を引き起こす可能性があります。CHO細胞におけるRMCEの効率は0.1%未満ですが[12], 、結果として得られるクローンはより予測可能で安定しています。
発現システムの選択も重要です。例えば、グルタミン合成酵素(GS)システムは通常、1細胞あたり約5つのトランスジーンコピーを生成しますが、ジヒドロ葉酸還元酵素(DHFR)システムはコピー数を最大1,000まで増幅することができます[6]. コピー数が多い方が魅力的に思えるかもしれませんが、DNAの変化の可能性が高まるため、長期的な安定性を考えるとGSベースのシステムが賢明な選択です。
リスクをさらに最小限に抑えるために、 部位特異的変異導入と トランスフェクション前のNGSスクリーニングが重要です。サンガーシーケンシングは検出限界が高いため、NGSは0.5%未満のプラスミド変異を検出でき、クローンスクリーニングの成功率を90%以上に向上させます[5].
WuXi BiologicsのShuai Wang氏と同僚は、この警戒の重要性を強調しています:
プロセスの最適化では遺伝子レベルの変異を修正できないため、安定したクローンの変異レベルを厳密に監視する必要があります[5].
凍結保存、遺伝子工学、または細胞株の特性評価のための専門的なツールを必要とする生産者向けに、
生産への品質管理の統合
生産の各段階に品質管理を組み込むことは非常に重要です。体系的なシステムがなければ、よく維持された細胞株でさえ、拡大やスケールアップの過程で変化を経験する可能性があります。品質管理は後回しにすべきではなく、生産の中心的な部分でなければなりません。これはスケールアップ段階から始まり、厳格な管理システムと制御された環境が重要な役割を果たします。
拡大とスケールアップ中の品質管理
前述の通り、スケールアップ中にはゲノムおよび汚染テストが重要です。小規模から数千リットルに移行する際、新たなリスクが生じ、各細胞継代で突然変異の可能性が高まります。品質管理システム (QMS) はこれらのリスクを効果的に管理するのに役立ちます。例えば、2017年から2022年にかけて、バルセロナ大学のJosep M. Canalsと彼のチームは、ISO 9001:2015 QMSを導入してヒト多能性幹細胞培養を標準化しました。GバンディングとaCGHデータの回顧的分析により、適応前の条件と比較して染色体異常の大幅な減少が明らかになりました[10][13]. 運河は継続的な監視の重要性を強調しました:
hPSCsが培養中に示す遺伝的不安定性は、実験に使用する際にゲノムの完全性を頻繁に再評価することが不可欠な要件であることを示しています[10].
定期的なゲノムスクリーニングは必須です。Gバンド染色体分析やaCGHのような技術は構造変化を検出し、次世代シーケンシング(NGS)は0.5%未満のレベルで変異を特定します[5]. 成長曲線分析も、汚染や遺伝的ドリフトなどの問題を早期に示すことができます[9]. 環境モニタリングは、セトルプレートテストや半年ごとのHEPAフィルターチェックのような実践により、細胞株の生産環境が安定しストレスフリーであることを保証することで、もう一つのセキュリティ層を追加します[4] .
メディアと試薬の一貫性は同様に重要です。mTeSR1のような血清不使用の定義済みメディアを使用し、分析証明書付きの試薬を使用することで、バッチ間の変動を減らし、ウイルス汚染のリスクを制限します[10][4]. 定期的な形態チェック - 異なる培養密度での簡単な顕微鏡観察 - は、分化やストレスの初期兆候を捉えることができます[9]. 特殊な機器や試薬の調達には、
製品の一貫性のための機能アッセイ
ゲノムモニタリングがプロセスを保護する一方で、機能アッセイは細胞が意図した通りに機能することを保証します。遺伝的安定性だけでは不十分であり、細胞は生産バッチ全体で適切に機能する能力を維持する必要があります。培養肉では、筋肉衛星細胞のような幹細胞が、拡張後も成熟した筋肉や脂肪組織に分化できることを確認することを意味します[2]. 分化アッセイはこれを検証するために不可欠です。
MTT、LDH、Resazurinのような代謝アッセイは、細胞の健康と生存率に関する洞察を提供します[4][9]. これらは、ショートタンデムリピート(STR)プロファイリング, と組み合わせて、細胞株が生産プロセス全体で真正であり、交差汚染がないことを確認するのに役立ちます[1][9].
転写解析はもう一つの重要なステップです。Xiaoyue ChenとSam Zhangの推奨:
転写レベルでのリスク評価のためには、変異検出にはゲノムDNAシーケンシングよりもcDNAが推奨されます[5].
この方法は、遺伝子の発現を反映しているため、ゲノムの位置だけでなく、最終生成物のより正確なイメージを提供します。ゲノムスクリーニングと機能アッセイを組み合わせることで、生産者は生産の各段階で安全性、品質、性能の厳しい基準を満たすことを保証できます。
結論
遺伝的安定性を維持することは、培養肉を安全かつ一貫して生産するために重要です。幹細胞と再生医療の研究室のFrancisco J. Molina-Ruizと彼の同僚は、リスクを強調しています:
hPSCにおける遺伝的変化は、hPSCベースの細胞製品の安全性を危険にさらす可能性があります...しかし、出発材料の異質な分化傾向、遺伝子発現プロファイルの変化、最終細胞製品の非効率性も引き起こします。[10].
問題は重大です - 531以上の誤認識された細胞株が国際細胞株認証委員会によって記録されています。[1].
これらの問題に取り組むには、強力な品質管理フレームワークが必要です。これには、STRプロファイリング、Gバンド染色体分析、aCGH、先進的なNGS[5], といった方法を組み合わせ、ISO 9001:2015のようなシステムと共にプロセスを標準化し、染色体異常を最小限に抑えることが含まれます。 [13].
経済的要因もこれらの対策の必要性を促進します。遺伝的浮動は、変異した細胞が成長の優位性を得る結果をもたらし、全体の生産バッチを台無しにする可能性があります。[10][11]. ヒト多能性幹細胞への注目が高まる中、安定した細胞株の需要はかつてないほど高まっています。タフツ大学のデビッド・L・カプラン教授
は次のように説明しています:不死化細胞株は、安定した強固なバイオプロセスから大量の食用組織を生成するための要件と一般的に考えられています。[14].
培養肉の生産者にとって、品質管理はプラスミドスクリーニングから大規模生産の監視に至るまで、すべてのステップに組み込まれていなければなりません。徹底的なテストと予防戦略を組み合わせることで、生産者は一貫した信頼性のある結果を確保できます。
よくある質問
スケールアップ中に遺伝的安定性のテストはどのくらいの頻度で行うべきですか?
遺伝的安定性のテストはスケールアップ中の重要なステップであり、定期的に実施する必要があります。このテストの頻度は、主に特定の細胞株とプロセスに依存します。突然変異の可能性を減らし、細胞の幹細胞性を維持するために、遺伝子分析に基づいた継代限界を設定することが賢明です。
小さな変異と大きな染色体変化を最もよく検出するテストはどれですか?
SNPアレイ解析や全ゲノムSNPジェノタイピングなどのテストは、小さな変異、コピー数変化、異数性を検出するのに優れています。これらの方法は、細胞株における大きな染色体変化を特定するのに特に有用です。
生産バッチ間での遺伝的ドリフトを防ぐ最も簡単な方法は何ですか?
遺伝的ドリフトを最小限に抑えるためには、細胞株の定期的な遺伝的および機能的解析を行い、通過回数を制限することが重要です。マスターセルバンクの確立や遺伝的安定性の定期的なチェックなど、品質管理プロトコルで推奨される実践を実施します。これらの対策は、一貫性を維持し、異なる生産バッチ間で信頼できる結果を確保するための鍵です。











