Genetik stabilite, kültür et üretimi için kritik öneme sahiptir. Bu olmadan, hücre hatları mutasyona uğrayabilir, bu da tutarsız kalite, güvenlik riskleri ve üretim hatalarına yol açabilir. Binlerce hücreden trilyonlarca hücreye ölçeklendirme, bu riskleri artırır ve sağlam kalite kontrol sistemlerini gerekli kılar. FDA ve EMA gibi düzenleyiciler, ürünleri onaylamadan önce stabilite kanıtı talep eder, çünkü küçük genetik değişiklikler bile alerjik veya zararlı sonuçları tetikleyebilir.
Ana zorluklar arasında genetik sürüklenme, mutasyon birikimi ve onkogen aktivasyonu yer alır. Bu sorunlar, uzun süreli hücre pasajlaması, seçici baskılar ve üretim sırasında çevresel stres faktörlerinden kaynaklanır. Karyotipleme, SNP dizileri ve yeni nesil dizileme (NGS) gibi ileri test yöntemleri, bu riskleri tespit etmeye ve ele almaya yardımcı olur. Yapılandırılmış hücre bankacılığı ve hedefe yönelik genetik mühendislik gibi önleyici stratejiler, istikrarsızlığa karşı ek koruma sağlar.
Üreticiler, kalite kontrolünü üretimin her aşamasına entegre etmelidir - hücre bankacılığından büyük ölçekli biyoreaktörlere kadar. STR profilleme, kontaminasyon testleri ve fonksiyonel analizler gibi araçlar, tutarlılığı ve güvenliği sağlar.
DNA'dan Ana Hücre Bankasına Hücre Hattı Gelişimini Hızlandırma - AGC Biologics
Genetik Stabiliteyi Korumada Ortak Zorluklar
Kültive edilmiş etin üretim döngüsü boyunca genetik stabiliteyi sağlamak kolay bir iş değildir. Üretimin büyük ölçeği, genetik değişikliklerin gelişmesi ve yayılması için birçok fırsat sunar. Bu zorlukları tanımak, etkili kalite kontrol sistemlerini devreye sokmanın anahtarıdır.
Genetik Sürüklenme ve Mutasyon Birikimi
Genişletilmiş hücre pasajı, kültive edilmiş et üretiminde genomik kararsızlığın ana kaynaklarından biridir. Ölümsüzleştirilmiş hücre hatları, doğaları gereği, uzun süreli kültür sırasında kendiliğinden mutasyonlara yol açabilecek genomik değişikliklere eğilimlidir [6][5]. Hücreler birden fazla popülasyon çoğalmasından geçerken, DNA replikasyonundaki hatalar birikir, bu da çeşitli hücre popülasyonlarına ve potansiyel olarak işlev kaybına yol açar. Christopher Frye ve Luhong He, BioPharm International'dan bu konuyu vurguluyor:
Klonal olarak türetilmiş CHO hücre hatlarının, uzun süreli alt kültürleme dönemlerinde heterojen bir popülasyon haline gelerek sıklıkla farklılaştığı gözlemlenmiştir [6].
Endüstriyel ortamlarda, üretim hücre hatlarının yaklaşık %20'si ardışık nesiller boyunca önemli ölçüde transgen heterojenliği gösterir [6]. Bu mutasyonlar, transfeksiyondan sonra DNA replikasyonu sırasında veya yabancı genler konak genomuna entegre edildiğinde meydana gelen hatalar nedeniyle erken aşamada ortaya çıkabilir [5].
Seçici baskılar başka bir karmaşıklık katmanı ekler. Hücre hatlarını stabilize etmek için kullanılan antibiyotikler ve metabolik belirteçler (e.g. , MTX) gibi ajanlar aslında mutasyon oranlarını artırabilir [6][5]. Bazı durumlarda, bu ajanların konsantrasyonu arttıkça mutasyon oranı da artar [6]. Besin kıtlıkları, ölçek büyütme sırasında optimal olmayan kültür koşulları ve genişlemeden kaynaklanan fiziksel stres gibi çevresel stres faktörleri genetik bütünlüğü daha da istikrarsızlaştırabilir [6][5].
Shuai Wang, Hücre Hattı Geliştirme Direktörü, WuXi Biologics, belirtiyor:
Mutasyon seviyeleri, Çin hamsteri yumurtalık (CHO) hücrelerinin genomik esnekliği nedeniyle hücre pasajı sırasında değişebilir [5].
Epigenetik değişiklikler de bir rol oynar. Transgenler, kültür süreci sırasında kısmen veya tamamen kaybolabilir veya susturulabilir, bu da uzun vadeli kararlılığı etkiler. Bu birikmiş mutasyonlar sadece hücre fonksiyonuna zarar vermekle kalmaz, aynı zamanda onkogenlerin aktive olma riskini de artırır.
Onkogen Aktivasyon Riskleri
Onkogen aktivasyonu, tüm üretim partilerini tehlikeye atabileceği için kültive edilmiş et üreticileri için kritik bir güvenlik endişesini temsil eder. Genetik kararsızlık, hipermetilasyon gibi mekanizmalarla onkogen aktivasyonuna yol açabilir ve bu da tümör benzeri profillerle sonuçlanabilir [3][1]. Üretimde gerekli olan hızlı genişleme, bu zararlı mutasyonların birikme olasılığını daha da artırır [5][6].
Bu, iyi bilinen bir zorluktur. Uluslararası İnovasyon Konsorsiyumu'na (IQ) göre, katılımcıların %67'si genetik mutasyonların üretim sırasında amino asit yanlış yerleştirilmesinden daha büyük bir tehdit oluşturduğuna inanmaktadır [5]. Mayıs 2024'ten bir vaka, bu sorunun ciddiyetini göstermektedir: WuXi Biologics, bir hücre hattı geliştirme programından klonların %43'ünün aynı genetik nokta mutasyonunu taşıdığını keşfetti. Temel neden? Transfeksiyon sırasında kullanılan plazmid DNA'daki %2.1–%2.2 varyant seviyesi, geleneksel Sanger dizilemesi tarafından tespit edilemedi. Bunu ele almak için, şirket bu tür varyantları erken yakalamak amacıyla kalite kontrol süreçlerine Yeni Nesil Dizileme (NGS) ekledi [5].
Genetik anormalliklerin erken tespiti çok önemlidir, çünkü onkojenik değişiklikler tüm partileri tehlikeye atabilir. Standart G-bant karyotipleme, yirmi hücre metafazında %14 mozaizm kadar az olan anormal alt popülasyonları tanımlayabilir [1]. Daha gelişmiş teknikler olan NGS, klonal hücrelerdeki genetik mutasyonları %0.5 hassasiyetle tespit edebilir [5].
DNA metilasyon analizi, tümörijenik potansiyeli değerlendirmek için başka bir değerli araçtır:
DNA metilasyon seviyeleri ve belirli genlerin hipermetilasyonu kanserin başlangıcı ve ilerlemesinde meydana geldiğinden, DNA metilasyon profillerinin analizi hücrelerin tümörijenik potansiyeli hakkında tamamlayıcı bilgiler sağlayabilir [3].
Asıl zorluk, bu değişiklikleri güvenliği tehlikeye atmadan önce tespit edebilecek sağlam izleme sistemlerini uygulamaktır. Kültürlenmiş et üreticileri için, hızlı hücre genişlemesi sırasında genetik kararlılığı korumak, gelişmiş kalite kontrol önlemleri gerektirir.
Kalite Kontrol Test Yöntemleri
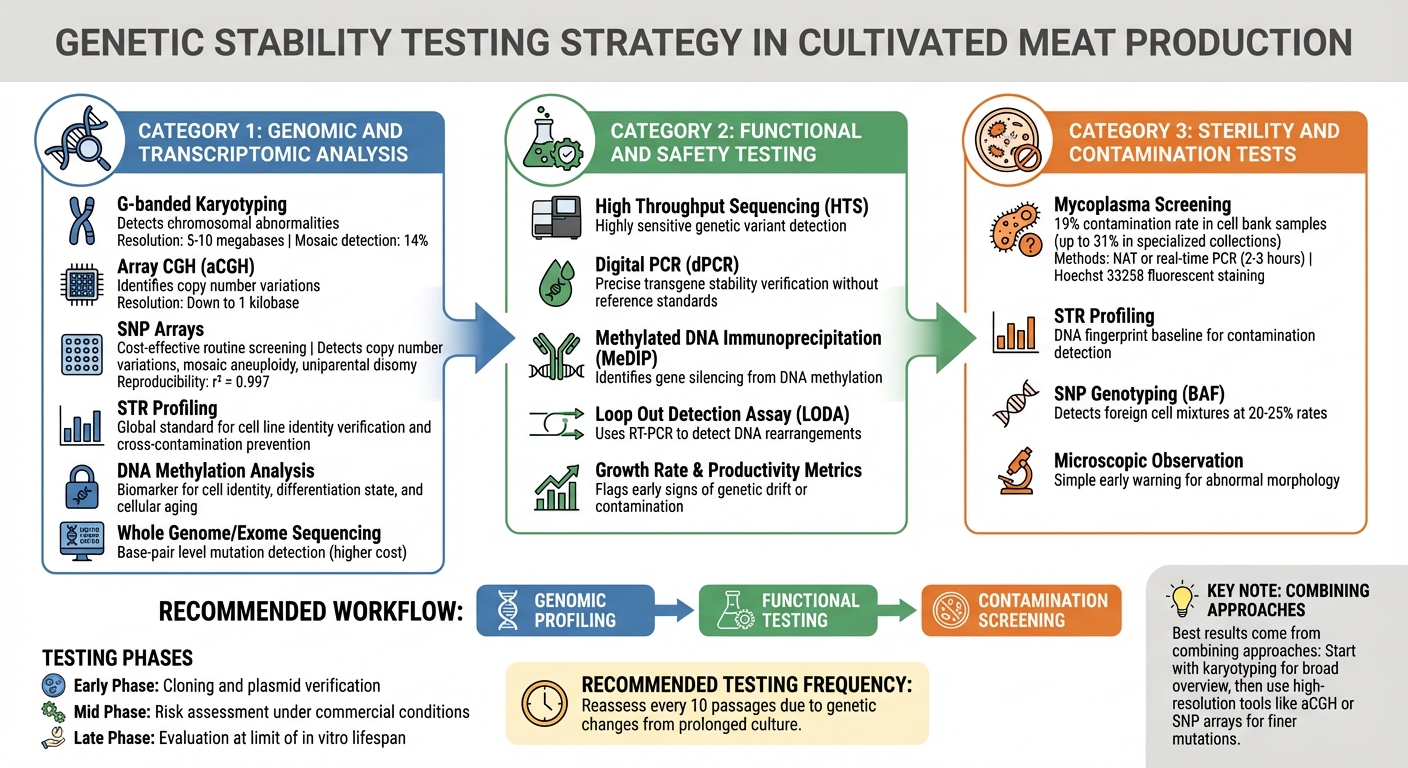
Kültürlenmiş Et Hücre Hatlarında Genetik Kararlılık için Kalite Kontrol Test Yöntemleri
Üretimi etkilemeden önce genetik kararsızlığı belirlemek, çok katmanlı bir test stratejisi gerektirir. Kültürlenmiş et üreticileri, büyük kromozomal değişikliklerden tek baz mutasyonlarına kadar her şeyi tespit eden yöntemlere güvenirler. Tekniklerin seçimi, her üretim aşamasında mevcut olan risklere bağlıdır. Bu genomik araçlar, detaylı işlevsel ve kontaminasyon değerlendirmelerinin ardından ilk kontrol noktası olarak görev yapar.
Genomik ve Transkriptomik Analiz
G-bantlı karyotipleme, sayısal anormallikler ve translokasyonlar gibi büyük yapısal yeniden düzenlemeler gibi büyük kromozomal sorunları tanımlamak için önemli bir araçtır. Mozaik seviyelerini yaklaşık %14 oranında tespit edebilse de, çözünürlüğü 5–10 megabazlık değişikliklerle sınırlıdır, bu da daha küçük değişikliklerin fark edilmeyebileceği anlamına gelir [1].
Dizi Karşılaştırmalı Genomik Hibridizasyon (aCGH) daha yüksek çözünürlük sunar ve 1 kilobaza kadar kopya sayısı varyasyonlarını tanımlar. Benzer şekilde, Tek Nükleotid Polimorfizmi (SNP) dizileri, kopya sayısı varyasyonlarını, mozaik anöploidi ve uniparental disomiyi tespit etmek için rutin tarama için maliyet etkin bir seçenek sunar. Doğrulama çalışmaları, SNP dizilerinin son derece tekrarlanabilir olduğunu göstermiştir ve B Allel Frekansı (BAF) ölçümleri etkileyici bir r² = 0 değerine ulaşmaktadır.997 [8] [1] .
Andalusian Kamu Sağlık Sistemi Biyobankası'ndan Rocio Aguilar-Quesada yöntemlerin birleştirilmesinin değerini vurguluyor:
Karyotipleme, yüksek çözünürlüklü testlerle tamamlandığında özellikle çok yönlü bir test olmaya devam ediyor [1].
Kısa Tandem Tekrar (STR) profilleme, hücre hattı kimliğini doğrulamak ve çapraz kontaminasyonu önlemek için küresel standarttır [1][9] . Bu arada, DNA metilasyon analizi, hücre kimliği, farklılaşma durumu ve hücresel yaşlanma için bir biyomarker olarak hizmet eder [1]. Çift baz seviyesinde mutasyon tespiti için, tüm genom veya ekzon dizileme bir seçenektir, ancak dizi tabanlı yöntemlere kıyasla daha yüksek maliyetlerle gelir [1].
En iyi sonuçlar, bu yaklaşımların birleştirilmesiyle elde edilir. Geniş bir genel bakış için karyotipleme ile başlayın, ardından daha ince mutasyonları yakalamak için aCGH veya SNP dizileri gibi yüksek çözünürlüklü araçlar kullanın. Uzun süreli kültür genetik değişikliklere yol açabileceğinden, düzenli yeniden değerlendirme - ideal olarak her 10 pasajda bir - kritiktir [10]. Bu genomik içgörüler daha sonra üretim boyunca tutarlı hücre davranışını sağlamak için fonksiyonel testlerle desteklenir.
Fonksiyonel ve Güvenlik Testleri
Yalnızca genomik profil oluşturma yeterli değildir. Fonksiyonel testler, hücrelerin genişleme sırasında amaçlanan özelliklerini koruduğunu doğrular. Büyüme oranları ve üretkenlik gibi metrikler, genetik kayma veya kontaminasyonun erken belirtilerini işaret edebilir [9].
Yüksek Verimli Dizileme (HTS), genetik varyantları tespit etmede son derece hassastır, dijital PCR (dPCR) ise referans standartlara ihtiyaç duymadan transgen stabilitesini kesin bir şekilde doğrular [11]. BioPharm International'dan Christopher Frye ve Luhong He bu adımın önemini vurguluyor:
Üretim hücre hattı, herhangi bir biyoprosesin temelidir ve bu nedenle, üretim hücre hattının uygun genetik karakterizasyonu, proses geliştirme başarısı için kesinlikle çok önemlidir [6].
Epigenetik stabilite de kritiktir. Metile DNA İmmünopresipitasyonu (MeDIP), DNA metilasyonunun neden olduğu gen susturmayı, verim düşüşünün yaygın bir nedeni olarak tanımlamaya yardımcı olur [7]. Araçlar, Loop Out Detection Assay (LODA) gibi, RT-PCR kullanarak DNA yeniden düzenlemelerini tespit eder, örneğin, seçilebilir belirteç kalırken ilgi çekici bir gen silindiğinde [7].
Testler üretim aşamasıyla uyumlu olmalıdır: erken aşama testleri klonlama ve plazmid doğrulamasına odaklanır, orta aşama testleri ticari koşullar altında riskleri değerlendirir ve geç aşama testleri hücreleri in vitro ömürlerinin sınırında değerlendirir [6]. Deneylere, bir ana hücre bankasından taze, düşük pasajlı hücrelerle başlamak genetik kayma riskini azaltır [9].
Sterilite ve Kontaminasyon Testleri
Kontaminasyon testi, genetiği istikrarsızlaştırabilecek faktörlerden kaçınmak için esastır. Mycoplasma özellikle endişe vericidir, çünkü hücre metabolizmasını ve davranışını kültürde görünür değişiklikler olmadan değiştirir [1]. Çalışmalar, hücre bankası örneklerinin %19'unda mikoplazma kontaminasyonu olduğunu ortaya koymaktadır, bazı özel koleksiyonlarda bu oran %31'e kadar çıkmaktadır [1] .
Hassas Nükleik Asit Amplifikasyon Teknikleri (NAT) veya gerçek zamanlı PCR kullanılarak düzenli mikoplazma taraması, 2-3 saat içinde yarı-kantitatif sonuçlar sağlayabilir [1]. Hoechst 33258 floresan boyama, karakteristik ekstraselüler floresan desenlerini ortaya çıkaran bir başka yöntemdir [9].
STR profilleme, hücre hatları için bir DNA parmak izi oluşturur ve çapraz kontaminasyonu tespit etmek için bir temel olarak işlev görür [9]. Ayrıca, B Allel Frekansı (BAF) dağılımlarını kullanan SNP genotiplemesi, diğer hücre hatlarından gelen kontaminasyonu tespit edebilir ve yabancı hücre karışımlarını %20-25 oranında tespit edebilir [8].
Mikroskopik gözlem, basit ama etkili bir erken uyarı aracıdır, çünkü anormal hücre morfolojisi genellikle kültür sorunlarını işaret eder [9]. Kalite Yönetim Sistemi'nin uygulanması, ISO 9001:2015, ve İyi İn Vitro Yöntem Uygulamaları (GIVIMP) ile birlikte, standartlaştırılmış ve tekrarlanabilir kültür koşullarını korumaya yardımcı olur, genomik kararsızlık riskini azaltır [10].
Özel test ekipmanlarına ve malzemelerine erişim ihtiyacı duyan kültür et üreticileri için,
sbb-itb-ffee270
Genetik Kararsızlık İçin Önleme Stratejileri
Genetik kararsızlığı tespit etmek bir şeydir; bunu önlemek tamamen başka bir zorluktur.Genetik kararlılığı korumak için, kültür et üreticilerinin hücre hatlarının sorunlar ortaya çıkmadan önce sapmasını önleyen iyi düşünülmüş sistemlere ihtiyacı vardır. Burada iki anahtar strateji öne çıkıyor: yapılandırılmış hücre bankacılığı ve hedeflenmiş genetik mühendisliği. Bu yaklaşımlar birlikte, genetik sapma ve onkogen aktivasyonu risklerini doğrudan ele alır.
Hücre Bankacılığı ve Kriyoprezervasyon
Mutasyon birikimi gerçek bir endişe kaynağıdır, bu yüzden güvenilir bir hücre bankacılığı sistemi şarttır. Endüstri standardı iki aşamalı bir sistem içerir: bir Master Hücre Bankası (MCB) ve bir Çalışma Hücre Bankası (WCB). Bu yapı, üretim için tutarlı bir başlangıç noktası sağlar. Geçiş sayısını sınırlamak çok önemlidir, çünkü her geçiş mutasyon olasılığını artırır. Hücreleri sıvı nitrojen içinde saklayarak, biyolojik aktivite etkili bir şekilde durdurulur ve depolama sırasında genetik değişiklik riski azaltılır.
Zamanı takip etmek yerine, hücre yaşı popülasyon katlanmaları ile ölçülür.. Örneğin, tipik bir 5.000 litrelik üretim biyoreaktörü yaklaşık 30 popülasyon katlanması içerir. [6]. Genetik tutarlılığı korumak için, ticari üretim bu sayıyı 45 ile 60 katlanma arasında sınırlar.[6].
RT-PCR ve tek hücre qPCR gibi tarama yöntemleri, olağandışı mRNA eklenmesi veya transgen değişkenliği gibi sorunları erken yakalayabilir. Kopya sayılarında geniş değişkenlik gösteren hücre hatları, gelecekteki sorunları önlemek için atılmalıdır.
Kalite kontrolü tartışılmazdır. Alarm verici bir şekilde, bazı bankalardaki hücre hatlarının %31'ine kadarının mikoplazma ile kontamine olduğu bulunmuştur.[3] . Bunu önlemek için, STR profilleme bankacılık süreci boyunca hücre hatlarının özgünlüğünü doğrulamak için kullanılır.FSA Araştırma ve Kanıt tarafından vurgulandığı gibi: Bankalanmış hücreler nihai ürünün başlangıç malzemesi olduğundan, gelecekte düzenleyiciler tarafından yüksek kaliteli güvenli bir et ürünü sağlamak için yüksek standartlar gerekebilir. Stabilite için Genetik Mühendislik Genetik mühendislik, hücre hattı stabilitesini doğrudan artırarak başka bir savunma katmanı sağlar. Hedefli entegrasyon (TI) gibi teknikler, özellikle Rekombinaz Aracılı Kaset Değişimi (RMCE), transgenlerin belirli genomik konumlara hassas bir şekilde yerleştirilmesine olanak tanır. Bu yaklaşım, konum etkileri ve kopya numarası kararsızlığının zarar verebileceği rastgele entegrasyonun öngörülemezliğinden kaçınır. CHO hücrelerinde RMCE'nin verimlilik oranları %0.1'in altında olmasına rağmen, ortaya çıkan klonlar daha öngörülebilir ve stabildir.
İfade sistemi seçimi de önemlidir. Örneğin, Glutamin Sentetaz (GS) sistemi tipik olarak hücre başına yaklaşık beş transgen kopyası ile sonuçlanırken, Dihidrofolat Redüktaz (DHFR) sistemi kopya sayılarını 1.000'e kadar artırabilir [6]. Daha yüksek kopya sayıları cazip gelebilir, ancak DNA değişikliklerinin olasılığını artırır, bu da GS tabanlı sistemleri uzun vadeli stabilite için daha akıllıca bir seçim yapar.
Riskleri daha da minimize etmek için, yer-spesifik mutagenez ve ön-transfeksiyon NGS taraması çok önemlidir. Sanger dizilemesinin daha yüksek bir tespit sınırı olduğundan, NGS %0.5'in altındaki plazmid mutasyonlarını yakalayabilir ve klon tarama başarısını %90'ın üzerine çıkarır[5].
WuXi Biologics'ten Shuai Wang ve meslektaşları bu dikkatin önemini vurguluyor:
Proses optimizasyonu gen seviyesindeki mutasyonları düzeltemediğinden, stabil klonlardaki mutasyon seviyelerini titizlikle izleyin[5].
Özel araçlara ihtiyaç duyan üreticiler için - ister kriyoprezervasyon, genetik mühendislik veya hücre hattı karakterizasyonu için olsun -
Üretime Kalite Kontrol Entegrasyonu
Kalite kontrolün her üretim aşamasına dahil edilmesi çok önemlidir. Yapılandırılmış bir sistem olmadan, iyi bakılan hücre hatları bile genişleme ve ölçek büyütme sırasında değişiklikler yaşayabilir. Kalite kontrol sonradan düşünülmemeli - üretimin merkezi bir parçası olmalıdır. Bu, sıkı yönetim sistemlerinin ve kontrollü ortamların önemli bir rol oynadığı ölçek büyütme aşamasında başlar.
Genişleme ve Ölçek Büyütme Sırasında Kalite Kontrol
Daha önce tartışıldığı gibi, genomik ve kontaminasyon testleri, özellikle ölçek büyütme sırasında hayati öneme sahiptir. Küçük hacimlerden binlerce litreye geçiş, her hücre geçişinin mutasyon olasılığını artırmasıyla yeni riskler getirir. Bir Kalite Yönetim Sistemi (KYS) bu riskleri etkili bir şekilde yönetmeye yardımcı olur. Örneğin, 2017 ve 2022 yılları arasında, Josep M. Canals ve Barselona Üniversitesi 'ndeki ekibi, insan pluripotent kök hücre kültürlerini standartlaştırmak için ISO 9001:2015 KYS'yi uyguladı. G-bantlama ve aCGH verilerinin retrospektif analizi, adaptasyon öncesi koşullara kıyasla kromozomal anormalliklerde önemli bir azalma olduğunu ortaya koydu[10][13]. Kanallar, sürekli izlemenin önemini vurguladı:
Kültürde hPSC'lerin gösterdiği genetik kararsızlık, deneylerde kullanılmaları planlandığında genomik bütünlüğün sık sık yeniden değerlendirilmesini zorunlu bir gereklilik haline getirir[10].
Rutin genomik tarama bir zorunluluktur. G-bantlama karyotipleme ve aCGH gibi teknikler yapısal değişiklikleri tespit ederken, Yeni Nesil Dizileme (NGS) %0.5'in altındaki seviyelerde mutasyonları tanımlar[5]. Büyüme eğrisi analizi, kontaminasyon veya genetik kayma gibi sorunları erken aşamada işaret edebilir[9]. Çevresel izleme, yerleşim plakası testi ve altı aylık HEPA filtre kontrolleri gibi uygulamalarla üretim ortamının hücre hatları için istikrarlı ve stressiz kalmasını sağlayarak başka bir güvenlik katmanı ekler[4].
Medya ve reaktiflerde tutarlılık eşit derecede önemlidir. mTeSR1 gibi serum içermeyen, tanımlanmış medya kullanmak, Analiz Sertifikası olan reaktiflerle birlikte, partiye bağlı değişkenliği azaltır ve viral kontaminasyon riskini sınırlar. [10][4]. Regüler morfoloji kontrolleri - farklı kültür yoğunluklarında basit mikroskobik gözlemler - farklılaşma veya stresin erken belirtilerini yakalayabilir.[9]. Özel ekipman veya reaktif temini için,
Ürün Tutarlılığı için Fonksiyonel Testler
Genomik izleme süreci korurken, fonksiyonel testler hücrelerin amaçlandığı gibi çalışmasını sağlar.Genetik stabilite tek başına yeterli değildir; hücreler ayrıca üretim partileri boyunca düzgün çalışabilme yeteneklerini de korumalıdır. Kültür eti üretiminde, bu, kas uydu hücreleri gibi kök hücrelerin genişleme sonrasında olgun kas veya yağ dokusuna farklılaşabildiğini doğrulamak anlamına gelir[2] . Farklılaşma testleri bunu doğrulamak için gereklidir.
MTT, LDH ve Resazurin gibi metabolik testler hücre sağlığı ve canlılığı hakkında bilgi sağlar[4][9]. Bunlar, Kısa Tandem Tekrar (STR) profillemesi, ile birleştirildiğinde, hücre hatlarının üretim süreci boyunca otantik ve çapraz kontaminasyondan uzak kaldığını doğrulamaya yardımcı olur[1][9].
Transkripsiyonel analiz bir diğer kritik adımdır.Xiaoyue Chen ve Sam Zhang öneriyor:
Mutasyon tespiti için transkripsiyon seviyesindeki riskleri değerlendirmek amacıyla cDNA yerine genomik-DNA dizilimi önerilmektedir [5].
Bu yöntem, genlerin sadece genomik konumlarını değil, nasıl ifade edildiğini yansıttığı için nihai ürünün daha doğru bir resmini sunar. Genomik taramayı fonksiyonel testlerle eşleştirerek, üreticiler her partinin üretimin her aşamasında güvenlik, kalite ve performans için katı standartları karşıladığından emin olabilirler.
Sonuç
Genetik kararlılığı korumak, kültürlenmiş etin güvenli ve tutarlı bir şekilde üretilmesi için kritik öneme sahiptir. Francisco J. Molina-Ruiz ve Kök Hücreler ve Rejeneratif Tıp Laboratuvarı'ndaki meslektaşları riskleri vurguluyor:
hPSC'lerdeki genetik değişiklikler, sadece hPSC bazlı hücre ürünlerinin güvenliğini tehlikeye atmakla kalmaz...ancak aynı zamanda başlangıç malzemesinin heterojen farklılaşma eğilimine, değişmiş gen ifade profillerine ve nihai hücre ürününün verimsizliğine yol açar [10].
Riskler önemli - 531'den fazla yanlış tanımlanmış hücre hattı Uluslararası Hücre Hattı Doğrulama Komitesi tarafından kaydedilmiştir [1].
Bu sorunların üstesinden gelmek sağlam bir kalite kontrol çerçevesi gerektirir. Bu, STR profilleme, G-bantlama karyotipleme, aCGH ve gelişmiş NGS gibi yöntemlerin [5], ISO 9001:2015 gibi sistemlerle birlikte kullanılarak süreçlerin standartlaştırılması ve kromozomal anormalliklerin en aza indirilmesini içerir [13].
Ekonomik faktörler de bu önlemlerin gerekliliğini artırmaktadır.Genetik sürüklenme, mutasyona uğramış hücrelerin büyüme avantajı kazanmasına neden olabilir ve potansiyel olarak tüm üretim partilerini bozabilir [10][11]. İnsan pluripotent kök hücrelerine artan odaklanma ile birlikte, kararlı hücre hatlarına olan talep hiç bu kadar büyük olmamıştı. Tufts Üniversitesi'nden Profesör David L. Kaplan'ın açıkladığı gibi:
Ölümsüzleştirilmiş hücre hatları, kararlı ve sağlam bir biyoprosesten büyük miktarlarda yenilebilir doku üretimi için genellikle bir gereklilik olarak kabul edilir [14].
Yetiştirilmiş et üreticileri için, kalite kontrolü her adımda - plazmid taramasından büyük ölçekli üretim izlemeye kadar - yerleştirilmelidir. Üreticiler, kapsamlı testleri önleyici stratejilerle birleştirerek tutarlı ve güvenilir sonuçlar elde edebilirler.
SSS
Genetik kararlılık testi ölçek büyütme sırasında ne sıklıkla yapılmalıdır?
Genetik kararlılık testi, ölçek büyütme sırasında kritik bir adımdır ve düzenli olarak yapılmalıdır. Bu testin ne sıklıkta yapılacağı büyük ölçüde belirli hücre hattına ve söz konusu sürece bağlıdır. Mutasyon olasılığını azaltmak ve hücrelerin kök hücre özelliklerini korumak için genetik analizle bilgilendirilmiş bir geçiş limiti belirlemek akıllıca olacaktır.
Küçük mutasyonları ve büyük kromozom değişikliklerini en iyi hangi testler tespit eder?
SNP dizi analizi ve genom çapında SNP genotipleme gibi testler, küçük mutasyonları, kopya sayısı değişikliklerini ve anöploidi tespit etmek için etkilidir. Bu yöntemler, hücre hatlarındaki büyük kromozomal değişiklikleri belirlemek için özellikle faydalıdır.
Üretim partileri arasında genetik sürüklenmeyi önlemenin en basit yolu nedir?
Genetik sürüklenmeyi en aza indirmek için, hücre hatlarının düzenli genetik ve fonksiyonel analizlerini yapmak ve geçirdikleri pasaj sayısını sınırlamak önemlidir. Ana hücre bankaları kurmak ve genetik stabiliteyi düzenli olarak kontrol etmek gibi uygulamaları hayata geçirmek, kalite kontrol protokollerinde önerildiği gibi, tutarlılığı korumak ve farklı üretim partileri arasında güvenilir sonuçlar sağlamak için anahtardır.











