الاستقرار الجيني أمر حاسم لإنتاج اللحوم المزروعة. بدونه، قد تتحور خطوط الخلايا، مما يؤدي إلى جودة غير متسقة، ومخاطر على السلامة، وفشل في الإنتاج. يؤدي التوسع من آلاف إلى تريليونات الخلايا إلى تضخيم هذه المخاطر، مما يجعل أنظمة مراقبة الجودة القوية ضرورية. تتطلب الجهات التنظيمية مثل FDA و EMA إثبات الاستقرار قبل الموافقة على المنتجات، حيث يمكن أن تؤدي حتى التغييرات الجينية الطفيفة إلى نتائج مسببة للحساسية أو ضارة.
تشمل التحديات الرئيسية الانجراف الجيني، وتراكم الطفرات، وتنشيط الجينات المسرطنة. تنشأ هذه القضايا من تمرير الخلايا الممتد، والضغوط الانتقائية، والعوامل البيئية الضاغطة أثناء الإنتاج. تساعد طرق الاختبار المتقدمة، مثل تحليل الكروموسومات، ومصفوفات SNP، وتسلسل الجيل التالي (NGS)، في اكتشاف ومعالجة هذه المخاطر. استراتيجيات الوقاية مثل بنوك الخلايا المنظمة والهندسة الجينية المستهدفة توفر حماية إضافية ضد عدم الاستقرار.
يجب على المنتجين دمج مراقبة الجودة في كل مرحلة من مراحل الإنتاج - من تخزين الخلايا إلى المفاعلات الحيوية الكبيرة. تضمن الأدوات مثل تحليل STR، واختبارات التلوث، والاختبارات الوظيفية الاتساق والسلامة. تربط المنصات مثل
تسريع تطوير خطوط الخلايا من الحمض النووي إلى بنك الخلايا الرئيسي - AGC Biologics
التحديات الشائعة في الحفاظ على الاستقرار الجيني
ضمان الاستقرار الجيني طوال دورة إنتاج اللحوم المزروعة ليس بالأمر السهل. إن حجم الإنتاج الكبير يوفر العديد من الفرص لتطور وانتشار التغيرات الجينية. التعرف على هذه التحديات هو المفتاح لوضع أنظمة فعالة لمراقبة الجودة.
الانحراف الجيني وتراكم الطفرات
يُعتبر تمرير الخلايا الممتد مصدرًا رئيسيًا لعدم الاستقرار الجينومي في إنتاج اللحوم المزروعة. خطوط الخلايا الخالدة، بطبيعتها، عرضة للتغيرات الجينومية، مما يمكن أن يؤدي إلى طفرات عفوية أثناء الثقافة طويلة الأمد [6][5]. مع مرور الخلايا عبر مضاعفات سكانية متعددة، تتراكم الأخطاء في تكرار الحمض النووي، مما يؤدي إلى تنوع في السكان الخلويين، وربما فقدان الوظيفة. يبرز كريستوفر فراي ولوهونغ هي من BioPharm International هذه القضية:
غالبًا ما لوحظ أن خطوط خلايا CHO المشتقة من استنساخ تتباعد، لتصبح مجموعة غير متجانسة على مدى فترات طويلة من الثقافة الفرعية [6].
في البيئات الصناعية، تظهر حوالي 20% من خطوط إنتاج الخلايا تباينًا كبيرًا في الجينات المحورة عبر الأجيال المتعاقبة [6]. يمكن أن تحدث هذه الطفرات في وقت مبكر، أثناء تكرار الحمض النووي بعد النقل الجيني، أو بسبب الأخطاء عند دمج الجينات الأجنبية في جينوم المضيف [5].
تضيف الضغوط الانتقائية طبقة أخرى من التعقيد. العوامل مثل المضادات الحيوية والعلامات الأيضية (e.g. , MTX) المستخدمة لتثبيت خطوط الخلايا يمكن أن تزيد فعليًا من معدلات الطفرات [6][5]. في بعض الحالات، كلما زادت تركيزات هذه العوامل، زادت معدلات الطفرات [6]. يمكن أن تؤدي الضغوط البيئية - مثل نقص المغذيات، وظروف الزراعة غير المثلى أثناء التوسع، والضغط الفيزيائي من التوسع - إلى زعزعة استقرار السلامة الجينية بشكل أكبر [6][5].
شواي وانغ، مدير تطوير خطوط الخلايا في ووكسى بيولوجيكس, يلاحظ:
من المحتمل أن تتغير مستويات الطفرات خلال تمرير الخلايا بسبب مرونة الجينوم في خلايا مبيض الهامستر الصيني (CHO) [5].
تلعب التغيرات فوق الجينية أيضًا دورًا. يمكن أن تفقد الجينات المنقولة جزئيًا أو كليًا أو يتم إسكاتها خلال عملية الزراعة، مما يؤثر على الاستقرار طويل الأمد. هذه الطفرات المتراكمة لا تضر فقط بوظيفة الخلايا ولكنها تزيد أيضًا من خطر تنشيط الجينات المسرطنة.
مخاطر تنشيط الجينات المسرطنة
يمثل تنشيط الجينات المسرطنة مصدر قلق أمني حرج لمنتجي اللحوم المزروعة، حيث يمكن أن يهدد دفعات الإنتاج بأكملها. يمكن أن يؤدي عدم الاستقرار الجيني إلى تنشيط الجينات المسرطنة من خلال آليات مثل فرط الميثلة، مما قد يؤدي إلى ظهور ملفات شبيهة بالأورام [3][1]. التوسع السريع المطلوب في الإنتاج يزيد من احتمالية تراكم هذه الطفرات الضارة [5][6].
هذا تحدٍ معروف جيدًا. وفقًا للاتحاد الدولي للابتكار & الجودة في تطوير الأدوية (IQ)، يعتقد 67% من المستجيبين أن الطفرات الجينية تشكل تهديدًا أكبر من دمج الأحماض الأمينية بشكل خاطئ أثناء الإنتاج [5] . حالة من مايو 2024 توضح خطورة هذه المشكلة: اكتشفت شركة WuXi Biologics أن 43% من النسخ المستنسخة من برنامج تطوير خطوط الخلايا تحمل نفس الطفرة الجينية النقطية. السبب الجذري؟ مستوى متغير بنسبة 2.1%–2.2% في الحمض النووي البلازميدي المستخدم أثناء النقل، والذي لم يتم اكتشافه بواسطة تسلسل سانجر التقليدي. لمعالجة هذا، قامت الشركة بدمج التسلسل الجيني من الجيل التالي (NGS) في عمليات مراقبة الجودة الخاصة بها لاكتشاف مثل هذه المتغيرات مبكرًا [5].
الكشف المبكر عن الشذوذات الجينية أمر بالغ الأهمية، حيث يمكن للتغيرات المسببة للسرطان أن تؤثر على دفعات كاملة. يمكن لتقنية التصوير الكروموسومي G-band القياسية تحديد التجمعات الفرعية غير الطبيعية بنسبة تصل إلى 14% من الفسيفساء في عشرين خلية في الطور الاستوائي [1]. تقنيات أكثر تقدماً مثل NGS يمكنها اكتشاف الطفرات الجينية في الخلايا المستنسخة بحساسية تصل إلى 0.5% [5].
تحليل مثيلة الحمض النووي هو أداة قيمة أخرى لتقييم الإمكانية الورمية:
لأن مستويات مثيلة الحمض النووي وفرط المثيلة لبعض الجينات تحدث في بدء وتطور السرطان، قد يوفر تحليل أنماط مثيلة الحمض النووي معلومات تكميلية حول الإمكانية الورمية للخلايا [3].
التحدي الحقيقي يكمن في تنفيذ أنظمة مراقبة قوية قادرة على تحديد هذه التغيرات قبل أن تؤثر على السلامة.بالنسبة لمنتجي اللحوم المزروعة، فإن الحفاظ على الاستقرار الجيني أثناء التوسع السريع للخلايا يتطلب تدابير متقدمة لمراقبة الجودة. منصات متخصصة مثل
طرق اختبار مراقبة الجودة
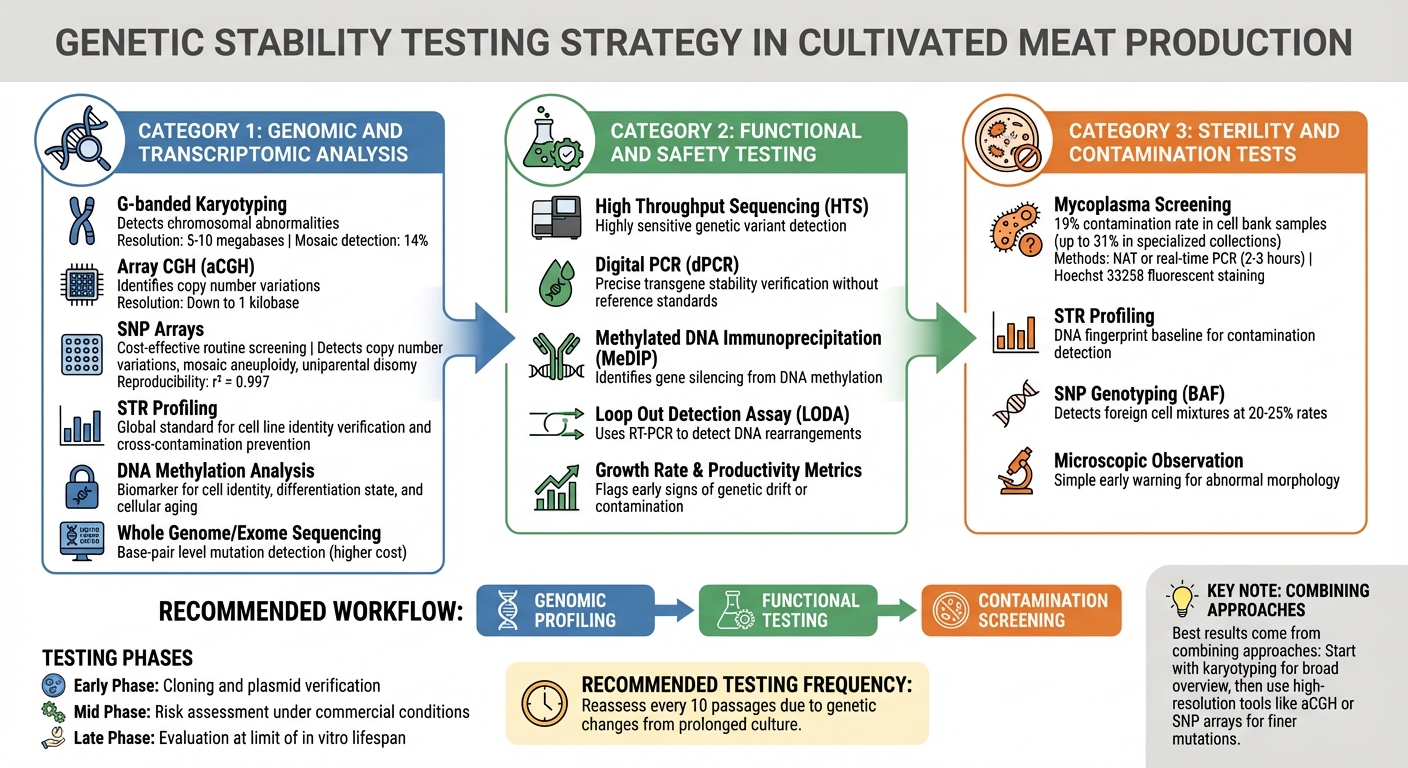
طرق اختبار مراقبة الجودة للاستقرار الجيني في خطوط خلايا اللحوم المزروعة
يتطلب تحديد عدم الاستقرار الجيني قبل أن يؤثر على الإنتاج استراتيجية اختبار متعددة الطبقات. يعتمد منتجو اللحوم المزروعة على طرق تكتشف كل شيء من التغيرات الكروموسومية الكبيرة إلى الطفرات في قاعدة واحدة. يعتمد اختيار التقنيات على المخاطر الموجودة في كل مرحلة من مراحل الإنتاج. تعمل هذه الأدوات الجينومية كنقطة تفتيش أولى، تليها تقييمات وظيفية وتلوثية مفصلة.
تحليل الجينوم والنسخ
التنميط النووي باستخدام تقنية G-banded هو أداة رئيسية لتحديد المشاكل الكروموسومية الكبرى مثل الشذوذات العددية وإعادة الترتيبات الهيكلية الكبيرة، مثل الانتقالات. بينما يمكنه اكتشاف مستويات الفسيفساء حوالي 14%، فإن دقته محدودة بالتغيرات التي تتراوح بين 5-10 ميغابايت، مما يعني أن التغيرات الأصغر قد تمر دون ملاحظة [1].
التهجين الجينومي المقارن باستخدام المصفوفات (aCGH) يوفر دقة أعلى، حيث يحدد تباينات عدد النسخ حتى 1 كيلوباز. وبالمثل، مصفوفات تعدد الأشكال النوكليوتيدي الفردي (SNP) توفر خيارًا فعالًا من حيث التكلفة للفحص الروتيني، حيث تكتشف تباينات عدد النسخ، والفسيفساء الصبغية، والخلل الوالدي الأحادي. أظهرت دراسات التحقق أن مصفوفات SNP تتمتع بإعادة إنتاجية عالية، حيث تحقق قياسات تردد الأليل B (BAF) قيمة r² = 0 مثيرة للإعجاب.997 [8] [1].
روكيو أغيلار-كيسادا من بنك الأنسجة العامة لنظام الصحة الأندلسي يبرز قيمة الجمع بين الأساليب:
لا يزال تحليل الكاريوتايب اختبارًا متعدد الاستخدامات، خاصة عند تكامله مع الاختبارات عالية الدقة [1].
تحليل التكرارات القصيرة المتتالية (STR) هو المعيار العالمي للتحقق من هوية خطوط الخلايا ومنع التلوث المتبادل [1] [9]. وفي الوقت نفسه، تحليل مثيلة الحمض النووي يعمل كعلامة حيوية لهوية الخلية، وحالة التمايز، وشيخوخة الخلايا [1]. لاكتشاف الطفرات على مستوى أزواج القواعد، تسلسل الجينوم الكامل أو الإكسوم هو خيار، على الرغم من أنه يأتي بتكاليف أعلى مقارنة بالطرق القائمة على المصفوفات [1].
تأتي أفضل النتائج من الجمع بين هذه الأساليب. ابدأ بتحليل الكروموسومات للحصول على نظرة عامة شاملة، ثم استخدم أدوات عالية الدقة مثل aCGH أو مصفوفات SNP لالتقاط الطفرات الدقيقة. إعادة التقييم المنتظمة - ويفضل كل 10 تمريرات - أمر حاسم، حيث يمكن أن يؤدي الاستنبات المطول إلى تغييرات جينية [10]. ثم تُستكمل هذه الرؤى الجينومية باختبارات وظيفية لضمان سلوك الخلايا المتسق طوال عملية الإنتاج.
الاختبارات الوظيفية واختبارات السلامة
التحليل الجينومي وحده ليس كافياً. تؤكد الاختبارات الوظيفية أن الخلايا تحافظ على خصائصها المقصودة أثناء التوسع. يمكن لمقاييس مثل معدلات النمو والإنتاجية أن تشير إلى علامات مبكرة على الانحراف الجيني أو التلوث [9].
التسلسل عالي الإنتاجية (HTS) حساس للغاية للكشف عن المتغيرات الجينية، بينما الـ PCR الرقمي (dPCR) يتحقق بدقة من استقرار الجين المنقول دون الحاجة إلى معايير مرجعية [11] . يشدد كريستوفر فراي ولوهونغ هي من BioPharm International على أهمية هذه الخطوة:
خط إنتاج الخلايا هو الأساس لأي عملية حيوية، وبالتالي، فإن التوصيف الجيني المناسب لخط إنتاج الخلايا ضروري للغاية لنجاح تطوير العملية [6].
الاستقرار الجيني مهم أيضًا. الترسيب المناعي للحمض النووي المثيلي (MeDIP) يساعد في تحديد إسكات الجينات الناجم عن مثيلة الحمض النووي، وهو سبب شائع لانخفاض الإنتاجية [7]. أدوات مثل اختبار الكشف عن الحلقة الخارجية (LODA) تستخدم RT-PCR للكشف عن إعادة ترتيب الحمض النووي، مثل عندما يتم حذف الجين المستهدف بينما يبقى العلامة القابلة للاختيار [7].
يجب أن تتماشى الاختبارات مع مرحلة الإنتاج: تركز اختبارات المرحلة المبكرة على الاستنساخ والتحقق من البلازميد، وتقييم اختبارات المرحلة المتوسطة المخاطر في ظل الظروف التجارية، وتقييم اختبارات المرحلة المتأخرة الخلايا عند الحد الأقصى لعمرها في المختبر [6]. بدء التجارب بخلايا جديدة ومنخفضة المرور من بنك الخلايا الرئيسي يقلل من خطر الانجراف الجيني [9].
اختبارات العقم والتلوث
اختبار التلوث ضروري لتجنب العوامل التي قد تزعزع استقرار الجينات. الميكوبلازما مقلقة بشكل خاص، لأنها تغير من أيض الخلايا وسلوكها دون التسبب في تغييرات مرئية في الثقافة [1]. تكشف الدراسات عن تلوث الميكوبلازما في 19% من عينات بنوك الخلايا، مع إظهار بعض المجموعات المتخصصة لمعدلات تصل إلى 31% [1].
يمكن للفحص المنتظم للميكوبلازما باستخدام تقنيات تضخيم الحمض النووي الحساسة (NAT) أو PCR في الوقت الحقيقي أن يوفر نتائج شبه كمية في غضون 2-3 ساعات [1]. التلوين الفلوري Hoechst 33258 هو طريقة أخرى، تكشف عن أنماط فلورية خارج الخلية مميزة [9].
يؤسس تحليل STR بصمة DNA لخطوط الخلايا، ويعمل كخط أساس للكشف عن التلوث المتبادل [9]. بالإضافة إلى ذلك، يمكن لتحديد النمط الجيني SNP باستخدام توزيعات تردد الأليل B (BAF) تحديد التلوث من خطوط خلايا أخرى، وكشف عن خليط الخلايا الأجنبية بمعدلات 20-25% [8].
يُعتبر الفحص المجهري أداة إنذار مبكر بسيطة وفعالة، حيث تشير التشوهات في شكل الخلايا غالبًا إلى مشاكل في الثقافة [9]. يساعد تنفيذ نظام إدارة الجودة، مثل ISO 9001:2015, جنبًا إلى جنب مع ممارسات الطرق الجيدة في المختبرات (GIVIMP)، في الحفاظ على ظروف الثقافة الموحدة والقابلة للتكرار، مما يقلل من خطر عدم استقرار الجينوم [10].
بالنسبة لمنتجي اللحوم المزروعة الذين يحتاجون إلى الوصول إلى معدات ومواد اختبار متخصصة، توفر منصات مثل
sbb-itb-ffee270
استراتيجيات الوقاية من عدم استقرار الجينات
اكتشاف عدم استقرار الجينات شيء؛ ومنعها تحدٍ آخر تمامًا. للحفاظ على الاستقرار الجيني، يحتاج منتجو اللحوم المزروعة إلى أنظمة مدروسة جيدًا تمنع خطوط الخلايا من الانحراف قبل ظهور المشكلات. هناك استراتيجيتان رئيسيتان تقودان الطريق هنا: البنوك الخلوية المنظمة و الهندسة الوراثية المستهدفة. معًا، تتعامل هذه الأساليب مباشرة مع مخاطر الانحراف الجيني وتفعيل الجينات المسرطنة.
البنوك الخلوية والحفظ بالتجميد
تراكم الطفرات هو مصدر قلق حقيقي، لذا فإن نظام البنوك الخلوية الموثوق به أمر لا بد منه. يتضمن المعيار الصناعي نظامًا من مستويين: بنك الخلايا الرئيسي (MCB) و بنك الخلايا العامل (WCB). يضمن هذا الإعداد نقطة انطلاق متسقة للإنتاج. الحد من عدد التمريرات أمر حاسم، حيث أن كل تمريرة تزيد من فرصة الطفرات. من خلال تخزين الخلايا في النيتروجين السائل، يتم إيقاف النشاط البيولوجي بشكل فعال، مما يقلل من خطر التغيرات الجينية أثناء التخزين.
بدلاً من تتبع الوقت، يتم قياس عمر الخلية بواسطة مضاعفات السكان . على سبيل المثال، يتضمن مفاعل حيوي إنتاجي نموذجي بسعة 5000 لتر حوالي 30 مضاعفة للسكان[6]. للحفاظ على التناسق الجيني، تحدد التصنيع التجاري هذا العدد بين 45 و60 مضاعفة[6].
طرق الفحص مثل RT-PCR و qPCR أحادي الخلية يمكنها اكتشاف المشاكل مبكرًا، مثل الربط غير المعتاد للـ mRNA أو تباين الجينات المنقولة. يجب التخلص من خطوط الخلايا التي تظهر تباينًا واسعًا في أعداد النسخ لتجنب المشاكل المستقبلية.
مراقبة الجودة أمر لا يمكن التفاوض عليه. بشكل مثير للقلق، وجدت الدراسات أن ما يصل إلى 31% من خطوط الخلايا في بعض البنوك كانت ملوثة بالميكوبلازما [3]. لمنع ذلك، يتم استخدام تحليل STR لتأكيد أصالة خطوط الخلايا طوال عملية التخزين.كما أبرزته أبحاث وأدلة FSA:
نظرًا لأن الخلايا المخزنة هي المادة الأولية للمنتج النهائي، قد تتطلب الجهات التنظيمية في المستقبل معايير عالية لضمان منتج لحوم آمن وعالي الجودة [2].
الهندسة الوراثية للاستقرار
توفر الهندسة الوراثية طبقة أخرى من الدفاع من خلال تعزيز استقرار خطوط الخلايا بشكل مباشر. تقنيات مثل الإدماج المستهدف (TI), خاصة تبادل الكاسيت بوساطة الإنزيم المدمج (RMCE), تسمح بإدخال دقيق للجينات المنقولة في مواقع جينومية محددة. هذا النهج يتجنب عدم القدرة على التنبؤ بالإدماج العشوائي، حيث يمكن أن تسبب تأثيرات الموقع وعدم استقرار عدد النسخ مشاكل كبيرة. على الرغم من أن RMCE في خلايا CHO لديها معدلات كفاءة أقل من 0.1%[12], إلا أن النسخ المستنسخة الناتجة تكون أكثر قابلية للتنبؤ وأكثر استقرارًا.
يهم اختيار نظام التعبير أيضًا. على سبيل المثال، نظام جلوتامين سينثيتاز (GS) ينتج عادةً حوالي خمسة نسخ من الجين المحول لكل خلية، بينما يمكن لنظام ديهيدروفولات ريدوكتاز (DHFR) أن يضخم أعداد النسخ حتى 1,000[6]. بينما قد تبدو أعداد النسخ الأعلى جذابة، فإنها تزيد من احتمالية حدوث تغييرات في الحمض النووي، مما يجعل الأنظمة القائمة على GS اختيارًا أذكى للاستقرار على المدى الطويل.
لتقليل المخاطر بشكل أكبر، فإن التطفير الموجه بالموقع وفحص NGS قبل النقل أمران حاسمان. نظرًا لأن تسلسل سانجر لديه حد كشف أعلى، يمكن لـ NGS اكتشاف الطفرات في البلازميد أقل من 0.5%، مما يحسن نجاح فحص النسخ إلى أكثر من 90%[5].
شواي وانغ وزملاؤه من WuXi Biologics يؤكدون على أهمية هذه اليقظة:
نظرًا لأن تحسين العمليات لا يمكنه تصحيح الطفرات على مستوى الجينات، يجب مراقبة مستويات الطفرات في النسخ المستقرة بدقة[5].
بالنسبة للمنتجين الذين يحتاجون إلى أدوات متخصصة - سواء للتجميد، أو الهندسة الوراثية، أو توصيف خطوط الخلايا -
دمج مراقبة الجودة في الإنتاج
يعد دمج مراقبة الجودة في كل مرحلة من مراحل الإنتاج أمرًا حيويًا. بدون نظام منظم، حتى خطوط الخلايا التي يتم صيانتها جيدًا يمكن أن تتعرض لتغييرات أثناء التوسع والتكبير. لا ينبغي أن تكون مراقبة الجودة فكرة لاحقة - يجب أن تكون جزءًا أساسيًا من الإنتاج.يبدأ هذا في مرحلة التوسع، حيث تلعب أنظمة الإدارة الصارمة والبيئات الخاضعة للرقابة دورًا رئيسيًا.
مراقبة الجودة أثناء التوسع والتكبير
كما نوقش سابقًا، تعتبر اختبارات الجينوم والتلوث حيوية، خاصة أثناء التوسع. الانتقال من أحجام صغيرة إلى آلاف اللترات يقدم مخاطر جديدة، مع كل مرور للخلية يزيد من فرصة الطفرات. يساعد نظام إدارة الجودة (QMS) في إدارة هذه المخاطر بفعالية. على سبيل المثال، بين عامي 2017 و2022، قام جوزيب م. كانالز وفريقه في جامعة برشلونة بتطبيق نظام إدارة الجودة ISO 9001:2015 لتوحيد ثقافات الخلايا الجذعية البشرية متعددة القدرات. كشف تحليلهم الاستعادي لبيانات G-banding وaCGH عن انخفاض كبير في الشذوذات الكروموسومية مقارنة بظروف ما قبل التكيف[10][13] . أبرزت القنوات أهمية المراقبة المستمرة:
عدم الاستقرار الجيني الذي تظهره الخلايا الجذعية البشرية المستحثة في الثقافة يجعل إعادة التقييم المتكرر لسلامة الجينوم متطلبًا أساسيًا عند التخطيط لاستخدامها في التجارب[10].
الفحص الجينومي الروتيني ضروري. تقنيات مثل تحليل النمط النووي G-banding وaCGH تكتشف التغيرات الهيكلية، بينما التسلسل الجيني من الجيل التالي (NGS) يحدد الطفرات عند مستويات أقل من 0.5%[5]. يمكن لتحليل منحنى النمو أيضًا الإشارة إلى المشكلات مبكرًا، مثل التلوث أو الانحراف الجيني[9]. تضيف المراقبة البيئية طبقة أخرى من الأمان، مع ممارسات مثل اختبار الأطباق المستقرة وفحوصات مرشحات HEPA نصف السنوية لضمان بقاء بيئة الإنتاج مستقرة وخالية من الإجهاد لخطوط الخلايا [4].
الاتساق في الوسائط والكواشف مهم بنفس القدر. استخدام وسائط محددة وخالية من المصل مثل mTeSR1، إلى جانب الكواشف مع شهادة تحليل، يساعد في تقليل التباين بين الدفعات ويحد من خطر التلوث الفيروسي[10][4]. الفحوصات المنتظمة للشكل - ملاحظات مجهرية بسيطة عند كثافات زراعة مختلفة - يمكن أن تكتشف علامات مبكرة للتمايز أو الإجهاد[9]. للحصول على المعدات أو الكواشف المتخصصة، توفر منصات مثل
الاختبارات الوظيفية لاتساق المنتج
بينما يضمن المراقبة الجينومية سلامة العملية، تضمن الاختبارات الوظيفية أن الخلايا تؤدي كما هو مقصود.الثبات الجيني وحده ليس كافياً؛ يجب على الخلايا أيضاً الحفاظ على قدرتها على العمل بشكل صحيح عبر دفعات الإنتاج. في اللحوم المزروعة، يعني هذا التأكد من أن الخلايا الجذعية، مثل خلايا الأقمار الصناعية العضلية، لا تزال قادرة على التمايز إلى نسيج عضلي أو دهني ناضج بعد التوسع[2] . تعتبر اختبارات التمايز ضرورية للتحقق من ذلك.
توفر اختبارات الأيض مثل MTT وLDH وResazurin نظرة ثاقبة على صحة الخلايا وقابليتها للحياة[4][9]. هذه، جنباً إلى جنب مع تحليل التكرارات القصيرة المتتالية (STR), تساعد في التأكد من أن خطوط الخلايا تظل أصيلة وخالية من التلوث المتبادل طوال عملية الإنتاج[1][9].
يعتبر التحليل النسخي خطوة حاسمة أخرى.Xiaoyue Chen و Sam Zhang يوصيان:
يوصى بتسلسل cDNA بدلاً من تسلسل الجينوم-DNA للكشف عن الطفرات لتقييم المخاطر على مستوى النسخ[5].
تقدم هذه الطريقة صورة أكثر دقة للمنتج النهائي، حيث تعكس كيفية التعبير عن الجينات بدلاً من مجرد مواقعها الجينومية. من خلال إقران الفحص الجينومي بالاختبارات الوظيفية، يمكن للمنتجين ضمان أن كل دفعة تلبي معايير صارمة للسلامة والجودة والأداء في كل مرحلة من مراحل الإنتاج.
الخاتمة
الحفاظ على الاستقرار الجيني أمر حاسم لإنتاج اللحوم المزروعة بأمان وباستمرار. يبرز فرانسيسكو ج. مولينا-رويز وزملاؤه من مختبر الخلايا الجذعية والطب التجديدي المخاطر:
يمكن أن تعرض التغيرات الجينية في hPSCs للخطر ليس فقط سلامة منتجات الخلايا القائمة على hPSC...ولكنها تؤدي أيضًا إلى تباين في ميل التمايز للمواد الأولية، وتغير في ملفات التعبير الجيني وكفاءة منخفضة للمنتج الخلوي النهائي [10].
المخاطر كبيرة - تم تسجيل أكثر من 531 خطًا خلويًا تم تحديده بشكل خاطئ من قبل اللجنة الدولية لمصادقة الخطوط الخلوية [1].
معالجة هذه القضايا تتطلب إطارًا قويًا لمراقبة الجودة. يتضمن ذلك دمج طرق مثل تحديد النمط الجيني STR، وتصوير الكروموسومات G-banding، وaCGH، وNGS المتقدمة [5] , إلى جانب أنظمة مثل ISO 9001:2015 لتوحيد العمليات وتقليل الشذوذات الكروموسومية [13].
العوامل الاقتصادية تدفع أيضًا الحاجة إلى هذه التدابير.يمكن للانحراف الجيني أن يؤدي إلى اكتساب الخلايا المتحورة ميزة نمو، مما قد يفسد دفعات الإنتاج بأكملها [10][11]. مع التركيز المتزايد على الخلايا الجذعية البشرية متعددة القدرات، لم يكن الطلب على خطوط الخلايا المستقرة أكبر من أي وقت مضى. كما يوضح البروفيسور ديفيد إل. كابلان من جامعة تافتس:
تعتبر خطوط الخلايا الخالدة بشكل عام متطلبًا لإنتاج كميات ضخمة من الأنسجة الصالحة للأكل من خلال عملية حيوية مستقرة وقوية [14].
بالنسبة لمنتجي اللحوم المزروعة، يجب أن يكون التحكم في الجودة جزءًا من كل خطوة - من فحص البلازميد إلى مراقبة الإنتاج على نطاق واسع. من خلال الجمع بين الاختبارات الشاملة والاستراتيجيات الوقائية، يمكن للمنتجين ضمان نتائج متسقة وموثوقة.
الأسئلة الشائعة
كم مرة يجب إجراء اختبار الاستقرار الجيني أثناء التوسع؟
يعد اختبار الاستقرار الجيني خطوة حاسمة أثناء التوسع ويجب إجراؤه بانتظام. يعتمد تكرار هذا الاختبار بشكل كبير على خط الخلايا المحدد والعملية المعنية. لتقليل فرص حدوث الطفرات والحفاظ على خصائص الخلايا الجذعية، من الحكمة تحديد حد للتمرير مستند إلى التحليل الجيني.
ما هي الاختبارات التي تكشف بشكل أفضل عن الطفرات الصغيرة والتغيرات الكبيرة في الكروموسومات؟
الاختبارات مثل تحليل مصفوفة SNP والتنميط الجيني SNP على مستوى الجينوم فعالة في الكشف عن الطفرات الصغيرة، وتغيرات عدد النسخ، والاختلال الصبغي. هذه الطرق مفيدة بشكل خاص في تحديد التغيرات الكروموسومية الكبيرة في خطوط الخلايا.
ما هي أبسط طريقة لمنع الانجراف الجيني عبر دفعات الإنتاج؟
لتقليل الانجراف الجيني، من الضروري إجراء تحليلات جينية ووظيفية منتظمة لخطوط الخلايا وتقييد عدد المرات التي تمر بها. تنفيذ ممارسات مثل إنشاء بنوك خلايا رئيسية وفحص الاستقرار الجيني بشكل دوري، كما هو موصى به في بروتوكولات مراقبة الجودة. هذه التدابير أساسية للحفاظ على الاتساق وضمان نتائج موثوقة عبر دفعات الإنتاج المختلفة.











