- Zweck: Stellt sicher, dass Bioreaktoren den regulatorischen und Produktionsstandards entsprechen, die Sterilität, präzise Umweltkontrolle und Lebensmittelsicherheit gewährleisten.
- Hauptmerkmale: Rührkessel-Bioreaktoren wurden aufgrund ihrer Eignung für Rindermuskelzellen ausgewählt, da sie kontrollierte Scherkräfte und Skalierbarkeit bieten.
- Herausforderungen: Die Skalierung von Bioreaktoren für hohe Zelldichten und die Senkung der Kosten erforderten ein Umdenken bei Materialien, Sterilisationsmethoden und Prozessdesign.
- Lösungen: Der Wechsel zu lebensmitteltauglichen Materialien, die Verwendung kostengünstiger Sterilisationsmethoden und die Integration von maschinellem Lernen zur Prozessoptimierung reduzierten die Kosten erheblich.
- Ergebnisse: Die Produktionskosten sanken von £437,000/kg auf £1.95/kg, mit einer 15-fachen Steigerung der Produktivität und bis zu 92% Reduzierung der Treibhausgasemissionen bei Nutzung erneuerbarer Energien. html
Diese Studie beschreibt, wie Validierungsprotokolle und intelligente Designentscheidungen kultiviertes Fleisch näher an die Preisparität mit konventionellem Fleisch bringen.
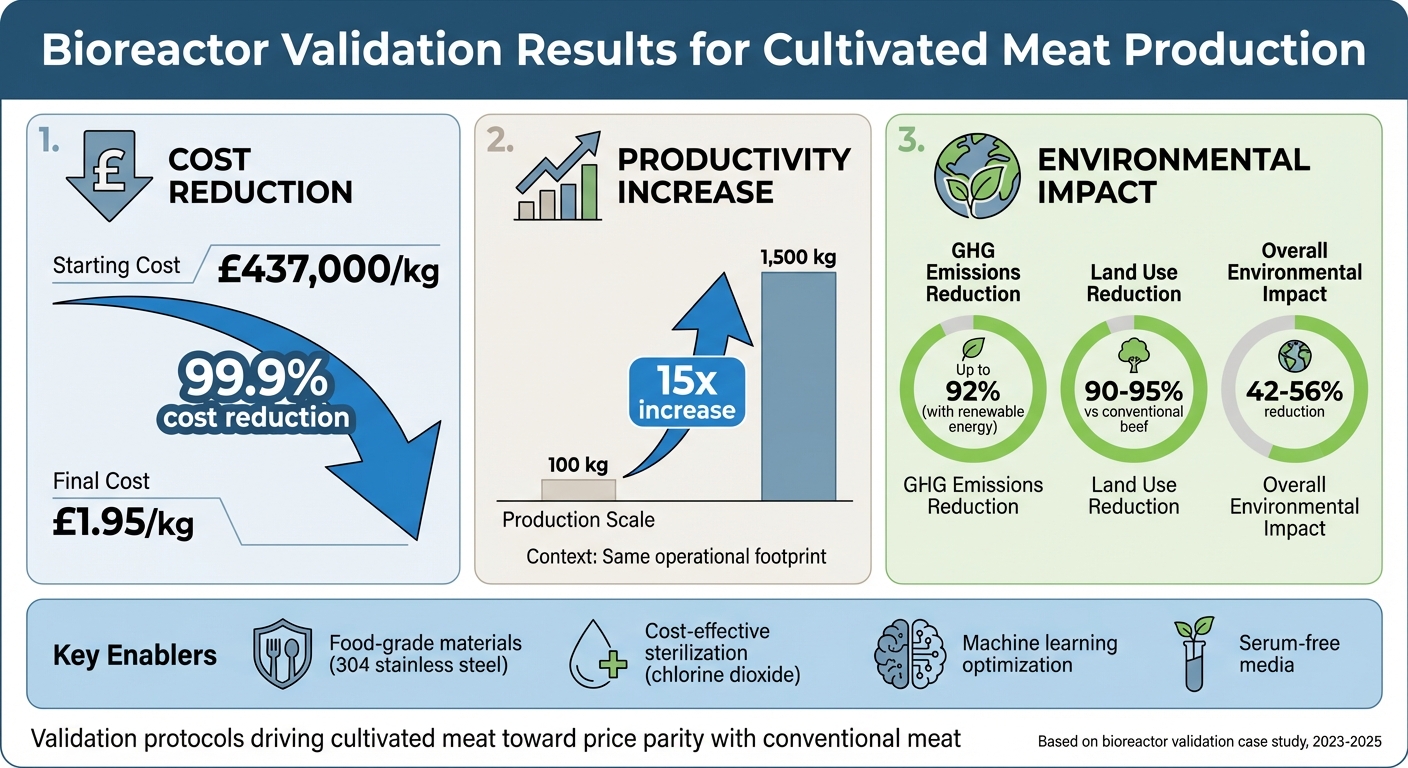
Auswirkungen der Bioreaktorvalidierung: Kostenreduktion und Umweltvorteile in der Produktion von kultiviertem Fleisch
Regulatorische Anforderungen für die Bioreaktorvalidierung
Anwendbare regulatorische Standards
In der kultivierten Fleischindustrie ist die Einhaltung strenger regulatorischer Standards ein kritischer Bestandteil des Bioreaktorvalidierungsprozesses. Im Vereinigten Königreich kategorisieren die Food Standards Agency (FSA) und Food Standards Scotland (FSS) kultiviertes Fleisch unter "Produkte tierischen Ursprungs" (POAO). Diese Klassifizierung stellt sicher, dass Lebensmittelsicherheits- und Hygieneverordnungen in allen Produktionsstufen, einschließlich der Bioreaktoroperationen, gelten. Allerdings fallen diese Produkte laut britischer Richtlinien (Dezember 2025) zwar unter die Kategorie POAO, qualifizieren sich jedoch rechtlich nicht als "Fleisch". Diese Unterscheidung bedeutet, dass bestimmte konventionelle Tierschutz- und mikrobiologische Anforderungen ausgeschlossen sind, was die spezifischen Validierungsprotokolle im Vereinigten Königreich beeinflusst.
Weltweit variieren die Sicherheitsbewertungen in ihrer Dauer. Singapur und die Vereinigten Staaten schließen Überprüfungen typischerweise innerhalb von 12 Monaten ab, während die Europäische Union im Durchschnitt etwa 18 Monate benötigt. Das Vereinigte Königreich hat mit dem CCP Sandbox Programme, das bis Februar 2027 finanziert wird, seinen eigenen Weg eingeschlagen. Diese Initiative ermöglicht es den Regulierungsbehörden, direkt mit Unternehmen wie Gourmey, Hoxton Farms, und Mosa Meat, zusammenzuarbeiten, um die Datenanforderungen zu optimieren und Sicherheitsbewertungen zu beschleunigen.
"Das Sandbox-Programm ermöglicht es uns, regulatorisches Wissen schnell zu erlangen, um Barrieren für aufstrebende Lebensmitteltechnologien zu reduzieren, ohne die Sicherheitsstandards zu beeinträchtigen."
– Dr. Thomas Vincent, stellvertretender Direktor für Innovation, FSA [3]
Unabhängig von der Gerichtsbarkeit müssen Unternehmen detaillierte Sicherheitsdossiers einreichen, bevor sie den Markt betreten. Diese Dossiers beschreiben Produktionsprozesse, Produktzusammensetzung und Sicherheitsdaten. Sie müssen auch bestätigen, dass kultiviertes Fleisch ernährungsphysiologisch mit herkömmlichem Fleisch vergleichbar ist, einschließlich Analysen von Makro- und Mikronährstoffen sowie Amino- und Fettsäureprofilen.
Validierungsprotokollanforderungen
Regulatorische Standards verlangen strenge Validierungsprotokolle für Bioreaktoren, um sichere und kontrollierte Abläufe zu gewährleisten. Ein wesentlicher Bestandteil ist die Implementierung eines Hazard Analysis and Critical Control Point (HACCP) Plans. Dieses Rahmenwerk identifiziert und mindert Risiken in jeder Phase der Produktion, von der anfänglichen Zellbiopsie bis zur endgültigen Ernte der Zellmasse. Angesichts der Neuheit der Produktion von kultiviertem Fleisch müssen Sicherheitsbewertungen potenzielle Gefahren während des gesamten Prozesses berücksichtigen.
Validierungsprotokolle müssen nachweisen, dass Bioreaktorsysteme während der Produktionszyklen sterile Bedingungen aufrechterhalten und so eine mikrobielle Kontamination wirksam verhindern. Darüber hinaus müssen diese Protokolle bewerten, ob Proteine in kultiviertem Fleisch allergische Reaktionen bei Verbrauchern auslösen könnten.
"Unsere neue Anleitung bietet Unternehmen Klarheit und hilft ihnen, den britischen Lebensmittelregulierungsbehörden zu verstehen und korrekt nachzuweisen, wie ihre Produkte sicher sind. Insbesondere stellt diese Anleitung sicher, dass Unternehmen potenzielle allergene Risiken bewertet haben und dass sie ernährungsphysiologisch geeignet sind, bevor sie zum Verkauf zugelassen werden können."
– Dr. Thomas Vincent, stellvertretender Direktor für Innovation, FSA [2]
In Großbritannien konzentriert sich die Validierung darauf, ausreichende Daten für eine wissenschaftliche Risikobewertung bereitzustellen, anstatt eine Marktzulassung zu erteilen. Nicolas Morin-Forest, Mitbegründer & CEO von GOURMEY, hob diesen Unterschied hervor:
"Die Validierung in Großbritannien markiert einen entscheidenden Schritt in unserer regulatorischen Reise für neuartige Lebensmittel und bestätigt, dass wir nun zur vollständigen Risikobewertung übergehen, was uns einen Schritt näher bringt, unsere Produkte den Verbrauchern zugänglich zu machen." [4]
Bioreaktor-Auswahl und System-Spezifikationen
Ausgewählte Bioreaktor-Technologie
Die Anlage entschied sich für einen Rührkessel-Bioreaktor, eine Wahl, die durch seine zuverlässige Leistung mit Rinder-Muskelvorläuferzellen. Wichtige Faktoren, die diese Entscheidung beeinflussten, waren die spezifischen Bedürfnisse der Zellen, der gewünschte Produktionsmaßstab und die Gesamtkostenüberlegungen.
Rindermuskelzellen, die anhaftungsabhängig sind, erfordern geringe Scherkräfte - unter 0,1 N/m² - um Schäden während der Kultivierung zu vermeiden. Das Rührkesseldesign erfüllte diese Anforderung und erwies sich als anpassungsfähig sowohl für Pilotversuche als auch für die kommerzielle Produktion. Kosten waren ein weiterer wichtiger Faktor, wobei Pilotanlagen zwischen £50.000 und £100.000 kosten, was sie für Budgets im Bereich der kultivierten Fleischindustrie zugänglich macht, im Gegensatz zur Pharmaindustrie[5][7].
Der Produktionsmaßstab zielte auf Volumina zwischen 100 und 1.000 Litern ab, um die kommerzielle Machbarkeit sicherzustellen. Modulare Rührkesselsysteme wurden gegenüber Alternativen mit Festbett gewählt, da sie in der Lage sind, um den Faktor 10 zu skalieren, ohne die Grenzen des Stofftransfers zu überschreiten, wobei kLa-Werte über 50 h⁻¹ beibehalten werden. Diese Systeme zielen darauf ab, 1–10 kg kultiviertes Fleisch pro Charge zu produzieren und das Kapitalinvestment bei etwa £200 pro Liter Kapazität auszugleichen [7][8].
Systemdesignmerkmale
Sobald der Rührkessel-Bioreaktor ausgewählt wurde, wurde sein Design mit fortschrittlichen Merkmalen ausgestattet, um optimales Zellwachstum zu fördern. Das Gasaustauschsystem verwendet Mikro-Sparger-Technologie, die Blasen zwischen 20–100 µm liefert. Diese Konfiguration erreicht kLa-Werte von 100–200 h⁻¹ bei 37°C und hält die gelösten Sauerstoffwerte bei 30–50% Sättigung. Um CO₂-Abstreifung zu steuern, wird die Kopfraumbelüftung mit Membrankontaktoren und Antischaumsensoren kombiniert[5][6].
Für effizientes Mischen verwendet der Bioreaktor zwei Rushton-Rührer, , die mit Geschwindigkeiten von 50–150 U/min arbeiten. Dies gewährleistet eine gleichmäßige Durchmischung mit Scherungsraten unter 5.000 s⁻¹, , wodurch die Zellen vor Schäden geschützt werden, während die Nährstoffgradienten unter 10% gehalten werden. Die Rührung wird PID-gesteuert, mit Echtzeit-Feedback zu pH-Wert und gelöstem Sauerstoffgehalt, was Perfusionsraten von 1–5 Gefäßvolumen pro Tag unterstützt[5][7].
Skalierbarkeit war ein zentraler Aspekt des Designs. Der Bioreaktor hält geometrische Ähnlichkeit über verschiedene Maßstäbe hinweg aufrecht und folgt einem Höhen-Durchmesser-Verhältnis von 2:1. CFD-optimierte Rührer gewährleisten eine lineare Skalierung, und Pilotversuche zeigten eine 95%ige Erhaltung der Zellviabilität beim Skalieren von 10 Litern auf 200 Liter.Das modulare Design ermöglicht die Integration in größere Produktionssysteme und erfüllt dabei die GxP-Compliance-Standards [7][8].
Prozessanalytische Technologie ist ebenfalls integriert und bietet Raman-Spektroskopie für die Echtzeitüberwachung kritischer Parameter wie pH (6,8–7,2) und Laktat (unter 2 g/L gehalten). Prädiktive Modelle, die aus der Produktion monoklonaler Antikörper adaptiert wurden, verfolgen Glukosespiegel mit R²-Werten über 0,95 und gewährleisten eine präzise Prozesskontrolle [5][6][7].
Diese Funktionen verbessern nicht nur die Zellkultivierung, sondern erfüllen auch die strengen Validierungsstandards, die von britischen Regulierungsbehörden gefordert werden.
Validierungsprotokollausführung
Kernvalidierungsverfahren
Um die betriebliche Integrität zu gewährleisten, wurde ein gründliches Validierungsprotokoll durchgeführt, das fortschrittliche Designmerkmale einbezog. Die Echtzeitüberwachung spielte eine Schlüsselrolle, wobei Prozessanalysentechnologie (PAT)-Sensoren kontinuierlich kritische Parameter wie gelösten Sauerstoff, pH-Wert und CO₂-Werte während jedes Kultivierungslaufs verfolgten[6] . Der Prozess begann mit Zellen, die mit einer Dichte von 1×10⁵ Zellen/mL ausgesät wurden und eine Woche lang in einem Medium mit 3 g/L Glukose kultiviert wurden. Raman-Spektroskopie wurde eingesetzt, um Laktat- und Glukosespiegel während des gesamten Prozesses zu überwachen[5].
Die Scherstressanalyse bestätigte, dass die Rührkräfte unter 0,1 Pa blieben, was das kritische Limit für Rindermuskelzellen ist. Nach dem Stresstest zeigte sich, dass die Zellviabilität über 90% blieb[6].
Sterilitätstests wurden auf alle Rohstoffe ausgeweitet, mit besonderem Augenmerk auf Nährmedien. Die Lieferanten mussten Analysezertifikate vorlegen, die durch Tests von Drittanbietern gemäß den Standards der britischen Einrichtung überprüft wurden. Das Protokoll umfasste ELISA-Immunoassays zur Erkennung von Endotoxinen aus gramnegativen Bakterien sowie Durchflusszytometrie zur Identifizierung von Verunreinigungen basierend auf Zellgröße, -form und Fluoreszenzeigenschaften [9] .
Prozessoptimierungsmethoden
Sobald die Systemstabilität bestätigt war, verlagerte sich der Fokus auf die Verfeinerung des Prozesses mithilfe fortschrittlicher Analytik. Maschinelle Lernalgorithmen passten die Medienflussraten und Rührgeschwindigkeiten dynamisch basierend auf kontinuierlichen PAT-Daten an. Diese Modelle, die auf Design of Experiments (DoE)-Datensätzen trainiert wurden, identifizierten kosteneffiziente Fütterungsstrategien, indem sie Permittivitätsmessungen mit der Biomassequalität korrelierten[6] . Dieser Ansatz war besonders effektiv während der Proliferationsphase, in der konstante Wachstumsraten für die kommerzielle Produktion entscheidend sind.
Die Raman-Spektroskopie, die ursprünglich für die Produktion monoklonaler Antikörper entwickelt wurde, wurde erfolgreich für Anwendungen in der kultivierten Fleischproduktion angepasst. Ihre Analytenspezifität ermöglichte es der Anlage, etablierte Validierungsprotokolle zu übernehmen und gleichzeitig die Präzision zu wahren, die für die Echtzeitüberwachung während des gesamten Kultivierungszyklus erforderlich ist[5].
Technische Herausforderungen und Lösungen
Skalierungs- und Produktivitätsprobleme
Die Skalierung von Bioreaktoren von Laboreinstellungen auf die kommerzielle Produktion war keine leichte Aufgabe.Die Anlage zielte darauf ab, 10–100 kg kultiviertes Fleisch zu produzieren, was enorme 10¹²–10¹³ Zellen erforderte, um dieses Ziel zu erreichen [11]. Allerdings erwies sich das Erreichen hoher Zelldichten als bedeutende Hürde. Während Hohlfaser-Bioreaktoren theoretisch Dichten von 10⁸ bis 10⁹ Zellen/mL erreichen können [13], blieben konventionelle Bioreaktordesigns für die Produktion von kultiviertem Fleisch hinter den Erwartungen zurück.
Matt McNulty, ein GFI Research Fellow, erklärte die Wurzel des Problems: "Die in kultiviertem Fleisch verwendeten Bioreaktoren sind noch weitgehend an konventionelle Lebensmittel- und Pharmadesigns angepasst. Diese Designs sind nicht speziell auf die Bedürfnisse der Produktion von kultiviertem Fleisch zugeschnitten und treiben daher durch Ineffizienzen in dieser Unangepasstheit höhere Kosten" [12]. Diese Diskrepanz zwischen Design und Zweck erforderte ein vollständiges Umdenken der Ausrüstung und Prozesse.
Implementierte Lösungen und Leistungsdaten
Um diese Herausforderungen zu bewältigen, hat die Einrichtung ihre Ausrüstung und Protokolle überarbeitet, um besser mit den spezifischen Anforderungen der Produktion von kultiviertem Fleisch übereinzustimmen. Eine der wichtigsten Änderungen bestand darin, von pharmazeutischen auf lebensmitteltaugliche Standards umzustellen. Zum Beispiel ersetzte das Team 316-Edelstahlbehälter durch Alternativen aus 304-Edelstahl, die die Lebensmittelsicherheitsanforderungen erfüllten und gleichzeitig die Investitionskosten erheblich senkten [12]. Zusätzlich wurde der traditionelle Dampf-Sterilisationsprozess durch eine Behandlung mit Chlordioxid-Gas ersetzt. Diese Anpassung ermöglichte die Verwendung von dünnwandigeren Behältern aus alternativen Materialien, was die Kosten weiter senkte [12].
Eine weitere kostensparende Maßnahme bestand darin, von pharmazeutischem Wasser auf als "Allgemein als sicher anerkannt" (GRAS) eingestuftes Lebensmittelwasser für die Medienvorbereitung umzusteigen [12]. Das Team führte auch essbare Mikrokapseln und Gerüste ein, die nicht nur Probleme mit der Zellablösung lösten, sondern auch den Lebensmittelsicherheitsvorschriften entsprachen [11].
Um die Abläufe weiter zu optimieren, implementierte die Anlage multiplexierte Sensorsysteme. Diese Sensoren lieferten Echtzeit-Leistungsdaten, die in maschinellen Lernanwendungen genutzt werden konnten, um Prozesse fein abzustimmen [12]. Insgesamt hatten diese Änderungen einen dramatischen Einfluss auf die Produktionskosten und reduzierten sie von £437,000/kg auf nur £1.95/kg [10]. Diese bemerkenswerte Kostenreduktion zeigt, wie die Ausrichtung der Produktionsprotokolle an regulatorische Standards eine kommerzielle Skalierbarkeit erreichen kann, ohne Sicherheit oder Qualität zu opfern.
sbb-itb-ffee270
Validierungsergebnisse und Branchenauswirkungen
Gemessene Leistungsresultate
Durch rigorose Tests zeigte das System einen beeindruckenden Produktivitätssprung. Mit der blasenfreien kontinuierlichen Bioreaktortechnologie stieg die Zellwachstumsproduktivität um das 15-fache, und erhöhte die Produktion von 100 kg auf 1.500 kg - alles innerhalb desselben betrieblichen Rahmens[16]. Während der Differenzierungsphase führten Anpassungen zur Optimierung der Zellbiomasse zu einem 128%igen Anstieg, was die gesamte Umweltbelastung erheblich um 42–56%. verringerte.Der Übergang vom C2C12- zum CHO-Zellstoffwechsel spielte ebenfalls eine große Rolle bei der Reduzierung der Umweltauswirkungen und erreichte Einsparungen von bis zu 67%, wenn erneuerbare Energiequellen genutzt wurden[14]. Noch bemerkenswerter ist, dass die Nutzung erneuerbarer Energien die Treibhausgasemissionen um bis zu 92% senkte und den Landverbrauch um 90–95% im Vergleich zu herkömmlichen Rindfleischproduktionsmethoden reduzierte [15] [16]. Diese Ergebnisse ebnen den Weg für eine breitere Akzeptanz in der gesamten Branche.
Beiträge zu Branchenpraktiken
Die Validierungsergebnisse haben die Standards für Bioreaktordesign und regulatorische Konformität in der Produktion von kultiviertem Fleisch neu definiert. Indem gezeigt wurde, dass Lebensmittelstandards pharmazeutische Standards effektiv ersetzen können, ohne die Sicherheit zu beeinträchtigen, hat der Prozess eine kostensparende Roadmap für die Branche eingeführt.Zum Beispiel führte der Wechsel von 316 zu 304 Edelstahl, kombiniert mit Chlordioxid-Sterilisation und der Verwendung von GRAS-klassifiziertem Wasser, zu einer erheblichen Senkung der Investitionskosten bei gleichzeitiger Einhaltung der Vorschriften.
Über den Nachweis der technischen Machbarkeit hinaus verschieben diese Fortschritte die Branchenmaßstäbe. Wirtschaftliche Modelle deuten darauf hin, dass integrierte kontinuierliche Verarbeitung 55% Einsparungen bei Kapital- und Betriebskosten über ein Jahrzehnt liefern könnte[1]. Für Beschaffungsteams bieten Plattformen wie
Fazit
Hauptbefunde
Diese Analyse zeigt auf, wie die Produktion von kultiviertem Fleisch durch kluge Geräteauswahl und Verfeinerung der Betriebsprotokolle kommerziellen Erfolg erzielen kann. Die Wahl von lebensmitteltauglichen Materialien wie 304 Edelstahl anstelle des teureren 316 Edelstahls gewährleistet Sicherheit und Compliance bei gleichzeitiger Kostensenkung. Der Wechsel zu serumfreien Medien, wie durch die Genehmigung der Singapore Food Agency für die Formulierungen von GOOD Meat Anfang 2023 validiert, beseitigt die ethischen und finanziellen Herausforderungen, die mit tierischen Inputs verbunden sind[15].
Die Skalierung der Produktion mit Airlift-Reaktoren, insbesondere bei 260.000 L, hat das Potenzial gezeigt, die Kosten auf etwa £10,50/kg zu senken. Dies ist eine signifikante Verbesserung im Vergleich zu den £24,50/kg Kosten, die mit kleineren 42.000 L Rührkesselreaktoren verbunden sind[17]. Allerdings erfordert das Erreichen hoher Zelldichten - bis zu 2 × 10⁸ Zellen/mL - fortschrittliche Perfusionssysteme, um mit Stoffwechselabfällen wie Ammoniak und Laktat umzugehen. Die Prozessoptimierung hat sich als wesentlich erwiesen, um diese Herausforderungen zu bewältigen[11]. Für Beschaffungsteams bieten Plattformen wie
Zukünftige Entwicklungen
Mit validierter Kosteneffizienz und Prozesskontrolle verlagert sich der Fokus nun auf Mega-Bioreaktoren, die das Produktionsökonomien neu definieren könnten.Die Ankündigung von GOOD Meat im Mai 2022 über eine Anlage mit zehn 250.000 L Bioreaktoren - fähig, jährlich 13.700 metrische Tonnen kultiviertes Huhn und Rind zu produzieren - markiert einen bedeutenden Schritt von Pilotprojekten zur industriellen Produktion[11][15]. Dies stimmt mit dem wirtschaftlichen Maßstab überein, der von Patrick G. Negulescu et al. von der University of California, Davis:
"Um direkt mit Rindfleisch konkurrieren zu können, müssen die Kosten für CM-Produkte oder zumindest die Produktionskosten auf ein Niveau unter $9/kg Fleisch sinken"[17]
Prognosen zeigen, dass dieses Ziel in Reichweite ist, insbesondere da die Medienkosten weiter sinken, mit Zielen von weniger als £0,20 pro Liter.
Innovationen wie essbare Mikrokapseln und Hybridsysteme, die Zellvermehrung und -differenzierung in einem einzigen Gefäß kombinieren, sollen die Validierungsprozesse vereinfachen und das Kontaminationsrisiko senken. Die in dieser Fallstudie beschriebenen Protokolle bieten ein reproduzierbares Modell für Unternehmen, die ihre Betriebe ausweiten, und beweisen, dass strenge Tests mit Kostensenkungen koexistieren können. Da mehr Einrichtungen diese validierten Methoden übernehmen, nähert sich die kultivierte Fleischindustrie der Preisparität mit traditionellem Fleisch. Gleichzeitig bietet der Sektor bemerkenswerte Umweltvorteile, darunter eine Reduzierung der Treibhausgasemissionen um bis zu 92 %, wenn er mit erneuerbaren Energiequellen betrieben wird[15].
Bioreaktoren Zusammenfassung: Sensoren, Modellierung, Hochskalierung und alternatives Reaktordesign
FAQs
Welche Nachweise erwarten die Regulierungsbehörden in einem Validierungsdossier für Bioreaktoren für kultiviertes Fleisch?
Regulierungsbehörden verlangen Validierungsdossiers für Bioreaktoren, um zu bestätigen, dass Systeme innerhalb definierter Parameter funktionieren. Dies beinhaltet die Sicherstellung von konstanter Prozessleistung und Echtzeitüberwachung von Schlüsselfaktoren wie pH-Werten, gelöstem Sauerstoff, und Temperatur. Zusätzlich spielt die Sterilitätsprüfung eine entscheidende Rolle bei der Vermeidung von Kontaminationen. Die Einhaltung von Standards wie ISO 14644-1 und EU GMP Anhang 1 ist obligatorisch, um die mikrobiologische Kontrolle aufrechtzuerhalten und sterile Herstellungspraktiken zu gewährleisten.
Wie kann ein Rührkessel-Bioreaktor skaliert werden, ohne Rindermuskelzellen zu schädigen?
Die Skalierung eines Rührkessel-Bioreaktors für die Produktion von kultiviertem Fleisch erfordert das Management von Scherspannung , , die Rindermuskelzellen schädigen kann. Um dies zu bewältigen, werden Werkzeuge wie Computational Fluid Dynamics (CFD) und Scale-Down-Modelle verwendet, um Strömungsmuster vorherzusagen. Diese Erkenntnisse leiten Anpassungen am Rührerdesign und den Rührgeschwindigkeiten, um Zellschäden zu reduzieren.
Ebenso wichtig ist die gleichmäßige Verteilung von Nährstoffen und Sauerstoff. Fortschrittliche Überwachungssysteme, kombiniert mit effektiven Mischtechniken, sind entscheidend, um konsistente Bedingungen zu schaffen. Dieser Ansatz hilft, lokale Spannungen zu minimieren und unterstützt die Zellgesundheit während der großtechnischen Produktion.
Welche Änderungen bei der Kostenreduzierung haben den größten Einfluss auf £/kg?
Die Einführung von Einweg-Bioreaktoren hat einen spürbaren Effekt auf die Senkung der Kosten, gemessen in £/kg. Während diese Systeme die anfänglichen Investitionen und Arbeitskosten reduzieren, sind die Verbrauchskosten höher. Darüber hinaus steigern Echtzeitüberwachung und Medien-Recycling-Technologien die Betriebseffizienz. Diese Fortschritte rationalisieren nicht nur die Prozesse, sondern führen auch zu langfristigen Kosteneinsparungen.











