การคัดกรอง CRISPR ที่มีประสิทธิภาพสูงกำลังเปลี่ยนแปลงภาคส่วนเนื้อสัตว์เพาะเลี้ยงโดยการเปิดโอกาสให้มีการปรับเปลี่ยนพันธุกรรมอย่างแม่นยำเพื่อปรับปรุงประสิทธิภาพของสายเซลล์ นี่คือสิ่งที่คุณจำเป็นต้องรู้:
- ความท้าทายหลัก: การผลิตเนื้อสัตว์เพาะเลี้ยงต้องการสายเซลล์ที่เติบโตอย่างมีประสิทธิภาพ ต้านทานการเสื่อมสภาพ และแยกตัวเป็นเนื้อเยื่อกล้ามเนื้อและไขมัน
- บทบาทของ CRISPR: โดยการกำหนดเป้าหมายยีนหลายพันตัวพร้อมกัน แพลตฟอร์มเหล่านี้สามารถระบุการแก้ไขพันธุกรรมที่ช่วยเพิ่มการเติบโต ชะลอการเสื่อมสภาพ และสนับสนุนการแยกตัว
- ผลการค้นพบที่น่าสังเกต: การศึกษาพบว่าการทำให้ยีนเช่น TP53 และ PTEN ใน เซลล์ต้นกำเนิดมีเซนไคม์ของวัว สามารถเพิ่มการขยายตัวได้ถึง 1,000 เท่าใน 30 วันและยืดอายุการใช้งานจาก 100 เป็น 200 วัน
- การประยุกต์ใช้: เครื่องมือ CRISPR เช่น knockout screens, CRISPRi และ CRISPRa กำลังถูกใช้เพื่อเพิ่มประสิทธิภาพการเจริญเติบโตของเซลล์ ควบคุมการแสดงออกของยีน และปรับสมดุลการเพิ่มจำนวนกับการแยกตัว
- เครื่องมืออุตสาหกรรม: เทคนิคขั้นสูงเช่น RMCE, RNA-seq และแพลตฟอร์มเซลล์เดี่ยวรวมผลลัพธ์ CRISPR กับข้อมูล multi-omics เพื่อให้มั่นใจถึงการปรับปรุงที่แม่นยำและขยายได้
สำหรับวิศวกรกระบวนการชีวภาพและผู้เชี่ยวชาญด้านการวิจัยและพัฒนา& นวัตกรรมเหล่านี้แก้ไขปัญหาคอขวดที่สำคัญใน การขยายกระบวนการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ในขณะที่รักษาคุณภาพและการทำงานของเซลล์ การรวม CRISPR กับระบบอัตโนมัติและทรัพยากรที่ปรับแต่งเช่น
พื้นฐานของ CRISPR-Cas9 สำหรับการคัดกรองการทำลายยีนทั่วทั้งจีโนม
วิธีการทำงานของ CRISPR-Cas9 ในการแก้ไขยีนขนาดใหญ่
ระบบ CRISPR-Cas9 อาศัยนิวคลีเอส Cas9 ที่จับคู่กับ RNA ไกด์เดี่ยว (sgRNA) เพื่อกำหนดเป้าหมายลำดับ DNA เฉพาะ เมื่อ sgRNA นำทาง Cas9 ไปยังตำแหน่งจีโนมที่ต้องการ เอนไซม์จะสร้างการแตกหักของสายคู่ใน DNA การแตกหักนี้ส่วนใหญ่ได้รับการซ่อมแซมผ่านการเชื่อมปลายที่ไม่เป็นเนื้อเดียวกัน (NHEJ) ซึ่งเป็นกระบวนการที่มีข้อผิดพลาดซึ่งมักจะแนะนำการแทรกหรือการลบขนาดเล็ก (indels) indels เหล่านี้สามารถทำให้เกิดการกลายพันธุ์แบบเฟรมชิฟต์ ซึ่งจะรบกวนการทำงานของยีนเป้าหมายอย่างมีประสิทธิภาพ [1]. กลไกที่แม่นยำนี้เป็นรากฐานสำหรับการดำเนินการคัดกรองการทำลายยีนทั่วทั้งจีโนม ซึ่งมีความสำคัญในการระบุผู้ควบคุมพฤติกรรมของเซลล์ที่สำคัญ
สำหรับการคัดกรองในขนาดใหญ่ นักวิจัยใช้ห้องสมุด sgRNAs ที่หลากหลาย โดยปกติจะส่งไปยังประชากรเซลล์ผสมผ่านการถ่ายโอน lentiviral เพื่อให้แน่ใจว่าแต่ละเซลล์ได้รับการเปลี่ยนแปลงทางพันธุกรรมเพียงหนึ่งครั้ง จะรักษาความเข้มข้นของการติดเชื้อ (MOI ประมาณ 0.3) [1]. เมื่อเวลาผ่านไป เซลล์ที่มีการกลายพันธุ์ที่เป็นประโยชน์มักจะเจริญเติบโตได้ดีกว่าเซลล์อื่น ๆ ซึ่งเป็นปรากฏการณ์ที่พบในเซลล์ประเภทต่าง ๆ และสภาวะการทดลองที่หลากหลาย
วิธีการส่งอื่น ๆ เช่น การแลกเปลี่ยนแคสเซ็ตต์ที่ควบคุมโดย recombinase (RMCE) เสนอความแม่นยำเพิ่มเติมโดยการกำหนดเป้าหมาย "แผ่นลงจอด" ทางพันธุกรรมเฉพาะเพื่อลดความแปรปรวนในไซต์การรวมตัว ตัวอย่างเช่น การศึกษาที่ใช้เซลล์ CHO-K1 ใช้วิธี RMCE ที่ปราศจากไวรัสเพื่อคัดกรอง gRNAs ที่ไม่ซ้ำกัน 111,651 ตัวใน 21,585 ยีน วิธีการนี้ระบุยีนที่จำเป็นสำหรับความฟิตของเซลล์ในช่วงเวลา 16 และ 37 วัน [7].
ประโยชน์ของการคัดกรองทั่วทั้งจีโนม
การคัดกรองการลบยีนทั่วทั้งจีโนมใช้ความแม่นยำของ CRISPR-Cas9 เพื่อศึกษายีนหลายพันตัวอย่างเป็นระบบ ซึ่งช่วยให้นักวิจัยค้นพบยีนที่มีอิทธิพลต่อการอยู่รอดของเซลล์ การเจริญเติบโต และการตอบสนองต่อความเครียด นอกเหนือจากปัจจัยทางพันธุกรรม การปรับปรุงการทำงานของพื้นผิวเป็นสิ่งสำคัญสำหรับการปรับปรุงการยึดเกาะและการเจริญเติบโตของเซลล์ในระบบเหล่านี้ การสำรวจที่ไม่มีอคติเช่นนี้มีความเกี่ยวข้องโดยเฉพาะกับการผลิตเนื้อสัตว์เพาะเลี้ยง, ซึ่งเซลล์ต้นกำเนิดมีเซนไคม์ (ซึ่งประกอบด้วยแหล่งเซลล์ประมาณ 25%) มักเผชิญกับความท้าทาย เช่น การเพิ่มจำนวนที่จำกัดและการแก่ก่อนวัย [1].
sbb-itb-ffee270
วิธีการคัดกรองห้องสมุด CRISPR แบบรวมกลุ่ม
การสร้างห้องสมุด CRISPR แบบรวมกลุ่ม
ห้องสมุด CRISPR แบบรวมกลุ่มเริ่มต้นด้วยการรวบรวม RNA ไกด์เดี่ยว (sgRNA) ที่คัดเลือกมาอย่างดีในบริบทของการวิจัยเนื้อสัตว์ที่เพาะเลี้ยง ห้องสมุดที่มีเป้าหมายมักถูกออกแบบมาเพื่อมุ่งเน้นไปที่กลุ่มยีนเฉพาะ เช่น ปัจจัยการถอดรหัสหรือการควบคุมการเพิ่มจำนวนเซลล์ วิธีการนี้ช่วยให้สามารถปรับสมดุลระหว่างต้นทุนกับความสามารถในการขยายขนาด ในขณะที่ยังคงมุ่งเน้นไปที่ลักษณะที่เกี่ยวข้องกับฟีโนไทป์ที่ต้องการ [1].
กระบวนการเริ่มต้นด้วยการสังเคราะห์โอลิโกนิวคลีโอไทด์เป็นกลุ่ม ขยายจำนวนผ่าน PCR และโคลนเข้าไปในเวกเตอร์ส่งตัวอย่างเช่น ห้องสมุดเฉพาะของโคที่สร้างขึ้นในต้นปี 2025 รวมถึง sgRNA 3,000 ตัวที่มุ่งเป้าไปที่ยีน 603 ยีนเพื่อระบุปัจจัยที่มีผลต่อการขยายตัวของเซลล์ต้นกำเนิด [1]. ในระดับที่ใหญ่ขึ้น การคัดกรองทั่วทั้งจีโนมสามารถเข้าถึงความซับซ้อนที่สูงขึ้นได้ ตัวอย่างหนึ่งคือการคัดกรองเซลล์รังไข่ของหนูแฮมสเตอร์จีน (CHO) ซึ่งใช้ gRNA ที่ไม่ซ้ำกัน 111,651 ตัวเพื่อมุ่งเป้าไปที่ยีน 21,585 ยีน [7].
การถ่ายโอน lentiviral มักใช้ในการส่งมอบห้องสมุดเหล่านี้ที่ความหลากหลายของการติดเชื้อต่ำ (ประมาณ 0.3) เพื่อให้แน่ใจว่าแต่ละเซลล์ได้รับการดัดแปลงพันธุกรรมเพียงครั้งเดียว [1]. ในทางเลือกหนึ่ง วิธีที่ปราศจากไวรัสเช่น recombinase-mediated cassette exchange (RMCE) จะรวม gRNA library เข้ากับ "landing pads" ในจีโนมที่กำหนดไว้ล่วงหน้าในสายเซลล์หลัก เทคนิคนี้บรรลุการครอบคลุม gRNA 99.9% โดยมีการเบี่ยงเบนเพียงเล็กน้อย [7].
เพื่อรักษาความน่าเชื่อถือทางสถิติ นักวิจัยมั่นใจว่ามีการครอบคลุมสูง - โดยทั่วไป 500 ถึง 600 เซลล์ต่อ sgRNA [1] [7] . บางแพลตฟอร์มใช้ระบบ inducible Cas9 (iCas9) ซึ่งช่วยให้สามารถควบคุมได้อย่างแม่นยำเมื่อการแก้ไขยีนเกิดขึ้น ตัวอย่างเช่น การแก้ไขสามารถถูกกระตุ้นหลังจากเซลล์ถึงสถานะเฉพาะ เช่น ความหนาแน่นสูงหรือการเริ่มต้นของความชรา การควบคุมชั่วคราวนี้มีประโยชน์อย่างยิ่งสำหรับการศึกษาขั้นตอนที่ไม่เพิ่มจำนวน ซึ่งมีความสำคัญในการเอาชนะอุปสรรคของการชราภาพโดยการเลือก เซลล์สายพันธุ์หลักเทียบกับเซลล์สายพันธุ์ที่เป็นอมตะ สำหรับการขยายการผลิตเนื้อสัตว์ที่เพาะเลี้ยง [4] .
เมื่อสร้างห้องสมุดเสร็จแล้ว นักวิจัยจะดำเนินการทดสอบการคัดกรองเป้าหมายเพื่อประเมินการทำงานของยีน
วิธีการคัดกรองสำหรับเซลล์สายพันธุ์เนื้อสัตว์ที่เพาะเลี้ยง
หลังจากสร้างห้องสมุดเสร็จแล้ว นักวิจัยจะประเมินประสิทธิภาพของเซลล์โดยใช้การทดสอบการแข่งขันและเทคนิคการคัดแยกตามหน้าที่ วิธีที่ใช้กันอย่างแพร่หลายคือการทดสอบการเพิ่มจำนวนตามการแข่งขัน ซึ่งระบุการเปลี่ยนแปลงทางพันธุกรรมที่ให้ความต้านทานต่อการเจริญเติบโตหรือการชราภาพ - ลักษณะสำคัญสำหรับการเพิ่มประสิทธิภาพเซลล์สายพันธุ์สำหรับเนื้อสัตว์ที่เพาะเลี้ยง
การคัดกรองระยะสั้น (ประมาณ 30 วัน) ระบุยีนที่มีผลต่อวัฏจักรของเซลล์ทันที ในขณะที่การคัดกรองระยะยาว (สูงสุด 200 วัน) มุ่งเน้นไปที่ยีนที่ช่วยให้เซลล์เอาชนะการชราภาพในการจำลองแบบ นี่เป็นความท้าทายที่สำคัญในการขยายการผลิตเนื้อสัตว์ที่เพาะเลี้ยง [1]. สำหรับลักษณะที่ซับซ้อนมากขึ้น เช่น การหลั่งโปรตีนที่เพิ่มขึ้นหรือการแสดงออกของเครื่องหมายเฉพาะ จะใช้การคัดแยกเซลล์ด้วยการกระตุ้นด้วยฟลูออเรสเซนส์ (FACS) ตัวอย่างหนึ่งคือ "การทดสอบการหลั่งจับเย็น" ซึ่งแยกประชากรเซลล์ที่ผลิตได้โดยการจับโปรตีนที่หลั่งออกมาบนพื้นผิวเซลล์ก่อนการคัดแยก [7] [5].
การตรวจสอบความถูกต้องเป็นขั้นตอนสำคัญในการยืนยันผลการคัดกรอง การทดสอบความฟิตของเซลล์ (CelFi) ตัวอย่างเช่น ติดตามอัตราส่วนของการกลายพันธุ์ที่อยู่นอกกรอบต่อการกลายพันธุ์ในกรอบเมื่อเวลาผ่านไปหากเซลล์ที่มีการกลายพันธุ์นอกกรอบหายไปจากประชากร แสดงว่ายีนที่ถูกกำหนดเป้าหมายมีความสำคัญต่อความฟิตของเซลล์ [2].
ในเดือนมิถุนายน 2025 นักวิจัยที่นำโดย Shijie Ding ที่ มหาวิทยาลัยเกษตรนานกิง ใช้ CRISPR/Cas9 เพื่อสร้าง CDKN2A–/– เซลล์ดาวเทียมสุกร . เซลล์ที่ถูกดัดแปลงเหล่านี้ยังคงมีการเพิ่มจำนวนอย่างเสถียรอย่างน้อย 15 รุ่นในสภาวะที่ไม่มีเซรั่มในขณะที่ยังคงรักษาเครื่องหมายสเต็มเนส เมื่อถูกหว่านลงบนโครงสร้าง 3 มิติที่กินได้จากพืช พวกมันก่อตัวเป็นโครงสร้างคล้ายเนื้อที่มีเนื้อสัมผัสที่ดีขึ้น รวมถึงความเหนียวและความหนืดที่เพิ่มขึ้น [8].
"ผลการวิจัยเหล่านี้แสดงให้เห็นถึงประโยชน์ของการคัดกรอง CRISPR สำหรับการเพิ่มประสิทธิภาพลักษณะของเซลล์ต้นกำเนิดโคและเสนอเส้นทางสู่การผลิตเนื้อสัตว์เพาะเลี้ยงที่สามารถขยายขนาดได้มากขึ้นในอนาคต" – Communications Biology [1]
Pooled CRISPR-Genetic Screens in Mammalian Cells | Protocol Preview
CRISPRi and CRISPRa for Reversible Gene Regulation Screens
CRISPR Gene Editing Methods for Cultivated Meat: Knockout vs CRISPRi/CRISPRa Comparison
Using CRISPRi and CRISPRa in Functional Genomics
เมื่อพูดถึงการปรับปรุงการผลิตเนื้อสัตว์ที่เพาะเลี้ยง การแทรกแซง CRISPR (CRISPRi) และการกระตุ้น CRISPR (CRISPRa) เป็นเครื่องมือที่ทรงพลัง เทคนิคเหล่านี้ใช้โปรตีน Cas9 ที่ไม่ทำงานร่วมกับตัวกดหรือกระตุ้น ทำให้นักวิจัยสามารถปรับการแสดงออกของยีนชั่วคราวโดยไม่ทำการเปลี่ยนแปลงถาวรต่อ DNA [10].
ความสามารถในการย้อนกลับนี้มีความสำคัญอย่างยิ่งสำหรับการจัดการกับความท้าทายหลัก: ยีนที่ส่งเสริมการเจริญเติบโตของเซลล์อย่างรวดเร็วมักจะรบกวนขั้นตอนต่อมาของการเปลี่ยนแปลงเป็นเนื้อเยื่อกล้ามเนื้อหรือไขมัน ตัวอย่างเช่น การทำให้ยีน TP53 ในเซลล์ต้นกำเนิดมีเซนไคม์ของวัวไม่ทำงานอย่างถาวรสามารถเพิ่มการแพร่กระจายได้มากกว่า 1,000 เท่าในเวลาเพียง 30 วัน แต่ทำให้ความสามารถในการเปลี่ยนแปลงของพวกมันลดลงอย่างมาก [1]. CRISPRi เสนอวิธีแก้ปัญหาที่มีความยืดหยุ่นมากขึ้นโดยการบล็อกชั่วคราวเส้นทางที่ยับยั้งการเปลี่ยนแปลงระหว่างการขยายตัวของชีวมวลใน เครื่องปฏิกรณ์ชีวภาพสำหรับเนื้อสัตว์ที่เพาะเลี้ยง. เมื่อเซลล์พร้อมสำหรับการเจริญเติบโตของเนื้อเยื่อแล้ว การทำงานของยีนปกติสามารถฟื้นฟูได้
ในเดือนตุลาคม 2025 นักวิจัยเช่น Gabriele Casagrande Raffi และ Roderick L. Beijersbergen จาก Netherlands Cancer Institute ได้พัฒนาระบบ CRISPR ที่สามารถเหนี่ยวนำได้วิธีการนี้ชะลอการแก้ไขยีนจนกว่าที่เซลล์จะถึงสถานะเฉพาะ เช่น ความหนาแน่นสูงหรือระยะที่ไม่เพิ่มจำนวน ช่วยในการรักษาความมีชีวิตของเซลล์ [4].
CRISPRi ยังโดดเด่นในเรื่องความแม่นยำเมื่อเทียบกับการแทรกแซง RNA แบบดั้งเดิม (RNAi) RNAi มักนำไปสู่ผลลัพธ์ที่ไม่สม่ำเสมอและผลกระทบที่ไม่ตรงเป้าหมาย ในขณะที่ CRISPRi ให้การยับยั้งยีนที่น่าเชื่อถือและเฉพาะเจาะจงมากขึ้น [2]. ข้อดีอีกประการหนึ่งคือ CRISPRi หลีกเลี่ยงการกระตุ้นความเป็นพิษที่เกี่ยวข้องกับ p53 ซึ่งมักเกิดจากการตอบสนองต่อความเสียหายของ DNA ในการศึกษาปี 2025 ที่นำโดย Liqin Wang ที่ Sun Yat-sen University Cancer Centre, นักวิจัยใช้ระบบ KRAB–dCas9 ที่สามารถเหนี่ยวนำด้วย doxycycline เพื่อคัดกรองยีน 262 ยีนในเซลล์ต้นกำเนิด pluripotent ที่เหนี่ยวนำในมนุษย์ (เซลล์ hiPS) พวกเขาพบว่า 76% ของยีนที่เกี่ยวข้องกับการแปลเป้าหมาย (200 จาก 262) มีความจำเป็นต่อการเจริญเติบโต แสดงให้เห็นถึงประสิทธิภาพของระบบ [10].
ความสามารถในการปรับแต่งการแสดงออกของยีนนี้ทำให้ CRISPRi และ CRISPRa เป็นเครื่องมือที่มีคุณค่าสำหรับการปรับสมดุลการเพิ่มจำนวนและการแยกแยะเซลล์ในการวิจัยจีโนมิกส์เชิงหน้าที่
การปรับหน้าจอแบบย้อนกลับสำหรับการประยุกต์ใช้เนื้อสัตว์ที่เพาะเลี้ยง
การควบคุมยีนแบบย้อนกลับเสนอวิธีแก้ปัญหาสำคัญในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง ตัวอย่างเช่น CRISPRa สามารถกระตุ้นยีนที่เกี่ยวข้องกับการขนส่งสารอาหารหรือเส้นทางเมตาบอลิซึมชั่วคราวในระหว่างการเพาะเลี้ยงความหนาแน่นสูง เมื่อเซลล์ถึงความหนาแน่นที่ต้องการ ระบบสามารถคืนการแสดงออกของยีนสู่ระดับปกติ สนับสนุนการแยกแยะที่เหมาะสมเป็นเนื้อเยื่อกล้ามเนื้อหรือไขมัน
ระบบที่สามารถเหนี่ยวนำได้ยังทำให้สามารถแยกขั้นตอนการขยายตัวของชีวมวลออกจากการเจริญเติบโตของเนื้อเยื่อ CRISPRi สามารถยับยั้งยีนที่เกี่ยวข้องกับความชราในระหว่างกระบวนการขยายขนาด เพิ่มระยะเวลาการเพิ่มจำนวนของเซลล์โคจากประมาณ 100 วันเป็นมากกว่า 200 วัน[1]. หลังจากที่ได้มวลชีวภาพเพียงพอแล้ว นักวิจัยสามารถฟื้นฟูการแสดงออกของยีนให้เป็นปกติเพื่อให้เกิดการแยกตัวได้ วิธีการนี้มีประโยชน์อย่างยิ่งสำหรับเซลล์ต้นกำเนิดมีเซนไคม์ ซึ่งมักจะเข้าสู่ภาวะชราภาพในระยะแรกของการเพาะเลี้ยง [1].
"การแก้ไขยีนที่มีเป้าหมายเฉพาะของกระบวนการคู่เหล่านี้สามารถเพิ่มประสิทธิภาพการขยายตัวของ MSC ในขณะที่ยังคงรักษาความสามารถในการแยกตัวและความสามารถในการแยกตัวที่จำเป็นไว้ได้ ซึ่งจะช่วยพัฒนาระบบเนื้อสัตว์เพาะเลี้ยงที่สามารถขยายขนาดได้ในที่สุด" – Communications Biology [1]
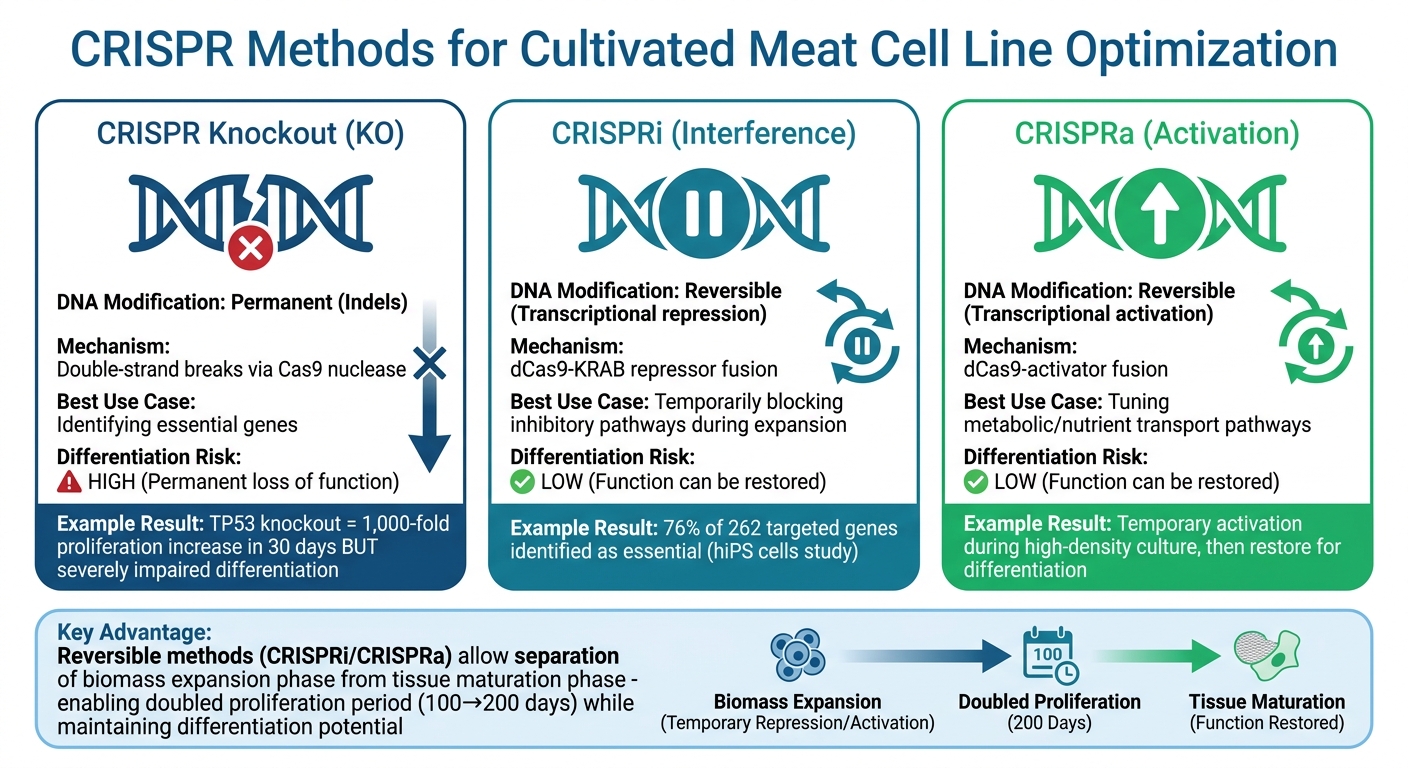
ตารางด้านล่างแสดงความแตกต่างระหว่างวิธีการควบคุมยีนแบบย้อนกลับได้และถาวร:
| คุณสมบัติ | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| การดัดแปลง DNA | ถาวร (Indels) | ย้อนกลับได้ (Transcriptional) |
| กลไก | การแตกของสายคู่ | การหลอมรวม dCas9-effector |
| กรณีการใช้งานที่ดีที่สุด | การระบุยีนที่จำเป็น | การปรับเส้นทางเมตาบอลิซึม/การเจริญเติบโต |
| ความเสี่ยงในการแยกแยะ | สูง (การสูญเสียฟังก์ชันถาวร) | ต่ำ (สามารถคืนฟังก์ชันได้) |
การเปรียบเทียบนี้แสดงให้เห็นว่าวิธีการควบคุมยีนแบบย้อนกลับสามารถปรับให้เหมาะสมกับความท้าทายเฉพาะในการพัฒนาเซลล์ไลน์สำหรับการผลิตเนื้อสัตว์เพาะเลี้ยงได้อย่างไร
การรวม CRISPR Screens กับเทคโนโลยี Cell Panel และ Genotyping
การเชื่อมโยง CRISPR Screens กับการวิเคราะห์ Multi-Omics
การบูรณาการ multi-omics และการทำ genotyping อัตโนมัติเข้ากับ CRISPR screens ช่วยปรับปรุงประโยชน์ของมัน โดยเฉพาะในการพัฒนาสายเซลล์เนื้อสัตว์เพาะเลี้ยง
การรวม CRISPR screens กับ multi-omics เช่น RNA sequencing ช่วยให้นักวิจัยสามารถทำแผนที่ผลกระทบของการทำ gene knockout เฉพาะต่อเส้นทางเซลล์ได้ ซึ่งมีความสำคัญอย่างยิ่งสำหรับเนื้อสัตว์เพาะเลี้ยง ที่การเข้าใจวิธีที่เซลล์สมดุลการเพิ่มจำนวนและการแยกแยะเป็นสิ่งสำคัญ
ตัวอย่างเช่น การทำ pooled CRISPR knockout screen ที่มุ่งเป้าไปที่ 600 ยีนใน เซลล์ต้นกำเนิด mesenchymal ที่ได้จากไขมันของวัว, ที่จับคู่กับ RNA-seq พบว่าการทำ knockout ของ TP53 และ PTEN ชะลอการแก่ตัวเซลล์เหล่านี้รักษาโปรไฟล์การแสดงออกของยีนที่อ่อนเยาว์ โดยมียีนวงจรเซลล์ที่เพิ่มขึ้น นำไปสู่การเพิ่มขึ้นของอัตราการเพิ่มจำนวนเป็นสองเท่า 50% ภายในวันที่ 50 หลังการถ่ายโอน [1].
แพลตฟอร์มเซลล์เดี่ยวเช่น CROP-seq นำไปสู่การตรวจจับทั้ง sgRNA และการเปลี่ยนแปลงของทรานสคริปโตมิกในเซลล์เดี่ยวพร้อมกัน [6]. ระดับความแม่นยำนี้มีคุณค่าอย่างยิ่งสำหรับการระบุการดัดแปลงทางพันธุกรรมที่เพิ่มการแยกแยะกล้ามเนื้อหรือการสังเคราะห์โปรตีน - ปัจจัยสำคัญสำหรับการบรรลุ เนื้อสัมผัสและคุณสมบัติทางโภชนาการที่ต้องการ ในเนื้อสัตว์ที่เพาะเลี้ยง
อีกวิธีหนึ่งที่มีแนวโน้มคือการคัดกรองแผงเซลล์ ซึ่งการรบกวน CRISPR ถูกทดสอบในสายเซลล์ที่หลากหลายจากผู้บริจาค สถานที่ทางกายวิภาค และสายพันธุ์ต่างๆ ตัวอย่างเช่น นักวิจัยได้ตรวจสอบห้องสมุด MyoCRISPR-KOLib ในสายเซลล์ myoblast ของมนุษย์จากผู้บริจาคเจ็ดรายใช้ระบบการคัดเลือกสารพิษแบบแยก พวกเขาระบุยีน 250 ยีนที่จำเป็นสำหรับการรวมตัวของไมโอบลาสต์ ในจำนวนนี้ ยีน 41 ยีนได้รับการยืนยันผ่านฐานข้อมูลทางการแพทย์ว่ามีบทบาทในโครงสร้างของกล้ามเนื้อลาย [6]. การตรวจสอบหลายบรรทัดนี้ทำให้มั่นใจได้ว่าเป้าหมายทางพันธุกรรมยังคงแข็งแกร่งท่ามกลางความแปรปรวนทางชีวภาพ ซึ่งเป็นข้อพิจารณาที่สำคัญสำหรับการขยายการผลิตเนื้อสัตว์ที่เพาะเลี้ยง
ข้อมูลเชิงลึกเหล่านี้กำลังปูทางไปสู่แพลตฟอร์มอัตโนมัติที่สามารถขยายได้ ซึ่งรวมการคัดกรองทางพันธุกรรมเข้ากับการทำจีโนไทป์อย่างละเอียดสำหรับการใช้งานในอุตสาหกรรม
ระบบอัตโนมัติและการขยายขนาดในแพลตฟอร์มแบบบูรณาการ
ระบบอัตโนมัติมีความจำเป็นสำหรับการจัดการชุดข้อมูลและตัวอย่างจำนวนมากที่สร้างขึ้นโดยแพลตฟอร์ม CRISPR และการทำจีโนไทป์แบบบูรณาการ ระบบ RMCE ซึ่งช่วยให้ส่งมอบห้องสมุด sgRNA แบบเฉพาะจุดโดยไม่ใช้ไวรัส เป็นก้าวสำคัญไปข้างหน้า แพลตฟอร์มเหล่านี้ทำให้มั่นใจได้ว่าแต่ละเซลล์ได้รับสำเนา sgRNA ที่สอดคล้องกันเพียงชุดเดียว ลดความแปรปรวน RMCE ได้แสดงให้เห็นถึงความครอบคลุมของห้องสมุดที่สูงด้วยอคติที่น้อยที่สุดในเซลล์รังไข่แฮมสเตอร์จีน (CHO) [5].
"แพลตฟอร์มการคัดกรองทางพันธุกรรมที่มีความเที่ยงตรงสูงและไม่ลำเอียงเป็นสิ่งจำเป็นสำหรับการพัฒนาโรงงาน CHO รุ่นต่อไป" - ทีมวิจัยรังไข่แฮมสเตอร์จีน [5]
ความสามารถในการขยายขนาดได้รับการปรับปรุงเพิ่มเติมโดยเครื่องมือการตรวจสอบเช่นการทดสอบ Cellular Fitness (CelFi) การทดสอบนี้ใช้การจัดลำดับลึกที่มีเป้าหมายเพื่อตรวจสอบโปรไฟล์ indel ตามเวลา โดยติดตามอัตราส่วนของการกลายพันธุ์ในกรอบเทียบกับนอกกรอบ โดยการเชื่อมโยงการกลายพันธุ์เหล่านี้กับข้อได้เปรียบหรือข้อเสียในการเจริญเติบโต นักวิจัยสามารถตรวจสอบเป้าหมายทางพันธุกรรมในสายเซลล์เนื้อสัตว์ที่เพาะเลี้ยงได้อย่างมีประสิทธิภาพ [2].
| เทคโนโลยี | วิธีการบูรณาการ | ประโยชน์หลักสำหรับเนื้อสัตว์ที่เพาะเลี้ยง |
|---|---|---|
| RNA-seq / Multi-omics | การเชื่อมโยง CRISPR กับโปรไฟล์ทรานสคริปโตมิก | การทำความเข้าใจว่าจีนควบคุมการเจริญเติบโตและการแยกแยะอย่างไร[1][6] |
| ระบบสารพิษแยกส่วน | การเชื่อมโยงการหลอมรวมเซลล์กับการคัดเลือกความมีชีวิต | การคัดเลือกเชิงปริมาณของเซลล์ที่สามารถหลอมรวมได้หรือมีข้อบกพร่อง[6] |
| แพลตฟอร์ม RMCE | การบูรณาการเฉพาะจุดของห้องสมุด gRNA | การคัดกรองที่มีประสิทธิภาพสูง ปราศจากไวรัส ด้วยจำนวนสำเนาจีนที่สม่ำเสมอ[5] |
| CROP-seq | Single-cell CRISPR + RNA-seq | การตรวจจับ sgRNA และการเปลี่ยนแปลงของทรานสคริปโตมพร้อมกัน [6] |
| CelFi Assay | การหาลำดับดีเอ็นเอที่มีการแทรกหรือขาดหายอย่างลึกซึ้งแบบเจาะจง | การตรวจสอบเป้าหมายทางพันธุกรรมอย่างรวดเร็วโดยการติดตามการเปลี่ยนแปลงความถี่ของอัลลีล [2] |
แพลตฟอร์มขั้นสูงเหล่านี้ช่วยให้กระบวนการตั้งแต่การระบุเป้าหมายทางพันธุกรรมไปจนถึงการตรวจสอบผลกระทบต่อความฟิตของเซลล์เป็นไปอย่างราบรื่น ประสิทธิภาพนี้สนับสนุนการพัฒนาสายเซลล์ที่แข็งแรงพอสำหรับการผลิตเนื้อสัตว์เพาะเลี้ยงในขนาดใหญ่
การใช้ CRISPR Screens เพื่อปรับปรุงการเจริญเติบโตและการแพร่กระจายของสายเซลล์
วิธีการคัดกรอง CRISPR ได้กลายเป็นเครื่องมือที่ทรงพลังในการเพิ่มประสิทธิภาพของสายเซลล์ ซึ่งให้ประโยชน์โดยตรงต่อการผลิตเนื้อสัตว์เพาะเลี้ยง
ตัวอย่างของการปรับปรุงสายเซลล์ด้วย CRISPR
CRISPR screens ได้ปรับปรุงประสิทธิภาพของสายเซลล์ในการวิจัยเนื้อสัตว์เพาะเลี้ยงได้สำเร็จ ตัวอย่างเช่น การคัดกรอง knockout แบบรวมที่มุ่งเป้าไปที่ยีน 600 ยีนในเซลล์ต้นกำเนิด mesenchymal ที่ได้จากไขมันของวัวได้ระบุ TP53 และ PTEN เป็นตัวยับยั้งการเจริญเติบโตที่สำคัญ การทำ knockout TP53 ทำให้จำนวนเซลล์เพิ่มขึ้นอย่างมีนัยสำคัญภายใน 30 วัน[1] . นอกจากนี้ เซลล์ต้นกำเนิด mesenchymal ของวัวที่ถูกแก้ไขแสดงอัตราการเพิ่มจำนวนเป็นสองเท่าเฉลี่ยสูงขึ้น 12%[1] .
โดยการกำหนดเป้าหมายไปที่ยีนยับยั้งเนื้องอก นักวิจัยได้ขยายอายุการเพิ่มจำนวนของเซลล์จากประมาณ 100 วันเป็นมากกว่า 200 วัน ซึ่งสามารถหลีกเลี่ยงขีดจำกัดของ Hayflick ได้อย่างมีประสิทธิภาพ การชะลอความชรานี้ช่วยให้การขยายตัวของชีวมวลในช่วงเวลาที่เกี่ยวข้องกับอุตสาหกรรม[1].
ในอีกตัวอย่างหนึ่ง นักวิจัยจากมหาวิทยาลัยเกษตรนานกิง นำโดย Shijie Ding, Chunbao Li, และ Guanghong Zhou ใช้ CRISPR/Cas9 ในการพัฒนา CDKN2A−/− สายเซลล์ดาวเทียมของสุกร เซลล์ที่ถูกออกแบบเหล่านี้สามารถคงการเพิ่มจำนวนได้อย่างเสถียรอย่างน้อย 18 รุ่นในสื่อที่ปราศจากเซรั่มที่มีส่วนประกอบ 19 ชนิด (A19) นอกจากนี้ยังสามารถปลูกลงบน โครงสร้างที่กินได้, สร้างโครงสร้างคล้ายเนื้อที่มีความเหนียวและความหนืดที่ดีขึ้น[8]. เซลล์คงความมีชีวิตมากกว่า 90% ในหลายรุ่นในสภาวะที่ปราศจากเซรั่ม[8].
"เซลล์ที่ถูกทำให้ไม่ทำงานของ CDKN2A โดยใช้ CRISPR เป็นแหล่งที่มาของเซลล์ต้นกำเนิดกล้ามเนื้อที่สามารถต่ออายุได้ ลดการพึ่งพาการเก็บตัวอย่างเนื้อเยื่อสัตว์ซ้ำๆ"
ตัวอย่างเหล่านี้แสดงให้เห็นว่า CRISPR screens สามารถระบุการดัดแปลงทางพันธุกรรมที่ช่วยปรับปรุงอัตราการเจริญเติบโต ชะลอการแก่ของเซลล์ และทำให้สามารถเพาะเลี้ยงโดยไม่ใช้เซรั่มได้ - สามปัจจัยสำคัญสำหรับการขยายการผลิตเนื้อสัตว์ที่เพาะเลี้ยง
ความท้าทายในการขยายขนาดสำหรับสายเซลล์ที่ปรับปรุงด้วย CRISPR
แม้ว่าสายเซลล์ที่ปรับปรุงด้วย CRISPR จะแสดงข้อได้เปรียบที่ชัดเจน แต่การขยายขนาดเพื่อการใช้งานในอุตสาหกรรมยังคงมีความท้าทาย การเพิ่มการแบ่งตัวมักจะมาพร้อมกับการลดความสามารถในการเปลี่ยนแปลงเซลล์ For instance, TP53 knockouts in bovine mesenchymal stem cells have been associated with reduced expression of muscle-differentiation genes, which can hinder their ability to mature into edible tissue[1]. To address this, additional strategies, such as adding media supplements or activating specific transcription factors, may be needed to restore differentiation after expansion[1].
Another critical issue is maintaining genetic stability. Variations in gene copy numbers (aneuploidy) and off-target effects during CRISPR editing can lead to inconsistent results or false positives in screening studies[2]. Tools like the Cellular Fitness (CelFi) assay help mitigate these risks by monitoring the ratio of out-of-frame indels over time, ensuring that observed growth benefits are directly linked to the intended edits[2].
อุปสรรคทางเศรษฐกิจและเทคนิคยังคงมีอยู่ เซลล์ต้นกำเนิดเมเซนไคม์ซึ่งประกอบด้วยประมาณ 25% ของแหล่งเซลล์ในอุตสาหกรรมเนื้อสัตว์เพาะเลี้ยง เผชิญกับความท้าทายเช่นต้นทุนสูงของปัจจัยการเจริญเติบโต ความจำเป็นในการปรับปรุง สื่อที่ปราศจากเซรั่ม, และการพัฒนาชีวปฏิกรณ์ขนาดใหญ่ (ความจุ 10,000–50,000 ลิตร)[1][9][11]. นอกจากนี้ การรับรองเนื้อสัมผัสที่ต้องการเมื่อเซลล์ถูกหว่านลงบนโครงสร้าง 3 มิติยังคงเป็นงานที่ซับซ้อน[11].
"สถานะปัจจุบันของเนื้อสัตว์เพาะเลี้ยงเผชิญกับความท้าทายที่สำคัญ รวมถึงต้นทุนสูง ปัญหาการขยายขนาด และความจำเป็นในการพัฒนาเทคโนโลยีเพิ่มเติม"
- Communications Biology [1]
การเอาชนะความท้าทายเหล่านี้ต้องการแนวทางที่ครอบคลุมซึ่งรวมการเพิ่มประสิทธิภาพทางพันธุกรรมเข้ากับความก้าวหน้าในการสร้างสูตรสื่อ เทคโนโลยีเครื่องปฏิกรณ์ชีวภาพ และโปรโตคอลการแยกแยะ ในขณะที่การตรวจคัดกรอง CRISPR ให้ข้อมูลเชิงลึกทางพันธุกรรมที่สำคัญ การแปลผลการค้นพบเหล่านี้ไปสู่โซลูชันที่ปรับขนาดได้จะต้องใช้ระบบบูรณาการและกระบวนการตรวจสอบที่เข้มงวด ความพยายามเหล่านี้มีความสำคัญต่อการย้ายการผลิตเนื้อสัตว์ที่เพาะเลี้ยงจากห้องปฏิบัติการไปสู่ความเป็นไปได้ในเชิงพาณิชย์
How Cellbase Supports CRISPR Research in Cultivated Meat
การตรวจคัดกรอง CRISPR ได้แสดงศักยภาพแล้ว แต่การปรับขนาดเพื่อการใช้งานในอุตสาหกรรมต้องการการเข้าถึงเครื่องมือและทรัพยากรเฉพาะทาง นี่คือที่ที่
การเข้าถึงทรัพยากร CRISPR ผ่าน Cellbase
ไม่เหมือนกับผู้จัดจำหน่ายยาที่มีขอบเขตกว้าง
In November 2025,
"ทุกบริษัทที่ผลิตเนื้อสัตว์เพาะเลี้ยงที่เราพูดคุยด้วยกำลังเสียเวลาไปกับปัญหาการจัดซื้อเดียวกัน การหาซัพพลายเออร์สำหรับส่วนประกอบที่สำคัญหมายถึงการค้นหาผ่านหน้าของซัพพลายเออร์ด้านเภสัชกรรมที่ไม่เข้าใจการประยุกต์ใช้ในอาหาร"
- David Bell, ผู้ก่อตั้ง Cultigen Group [15]
โดยการรวมทรัพยากรเหล่านี้ไว้ที่ศูนย์กลาง
การส่งเสริมความร่วมมือในการพัฒนาการผลิตเนื้อสัตว์จากการเพาะเลี้ยง
แพลตฟอร์มนี้ถูกออกแบบมาเพื่อรองรับความต้องการของโครงการเชิงพาณิชย์ขนาดใหญ่ เช่น โครงการที่ดำเนินการโดย Believer Meats และ Aleph Farms . โครงการเหล่านี้ต้องการโครงสร้างพื้นฐานสำหรับเครื่องปฏิกรณ์ชีวภาพขนาด 50,000 ลิตร และ ห่วงโซ่อุปทานการผลิตที่ได้รับการปรับปรุง, ซึ่ง
บทสรุป
การคัดกรอง CRISPR ที่มีประสิทธิภาพสูงได้เปลี่ยนจากแนวคิดที่มีศักยภาพไปสู่เครื่องมือสำคัญในการพัฒนาการผลิตเนื้อสัตว์เพาะเลี้ยง ผลกระทบของเทคโนโลยีนี้ในการเพิ่มประสิทธิภาพของสายเซลล์นั้นไม่อาจปฏิเสธได้ ตัวอย่างเช่น ความก้าวหน้าล่าสุดได้แสดงให้เห็นว่าการดัดแปลงพันธุกรรมสามารถเพิ่มอายุการขยายตัวของเซลล์ต้นกำเนิดของวัวจาก 100 เป็น 200 วัน ลดประชากรเซลล์ชราภาพจาก 60% เหลือเพียง 10% และเพิ่มจำนวนเซลล์ได้ถึง 1,000 เท่าในเวลาเพียงหนึ่งเดือน [1]. ความก้าวหน้าเหล่านี้แสดงถึงการเปลี่ยนแปลงที่ชัดเจนจากการวิจัยเชิงทดลองไปสู่การประยุกต์ใช้ในอุตสาหกรรมจริง
แพลตฟอร์มที่กะทัดรัดและห้องสมุดที่มีเป้าหมายกำลังแก้ไขปัญหาที่เร่งด่วนที่สุดในสาขานี้ ระบบไมโครฟลูอิดิกส์ดิจิทัลในปัจจุบันช่วยให้สามารถคัดกรองด้วยเซลล์เพียง 3,000 เซลล์ต่อสภาวะ ทำให้สามารถทำงานกับเซลล์สัตว์ปฐมภูมิที่มีจำกัดซึ่งไม่มีจำหน่ายในเชิงพาณิชย์ได้ในขณะเดียวกัน ห้องสมุดที่เน้นเฉพาะอย่าง MyoCRISPR-KOLib สามารถกำหนดเป้าหมายไปที่ 90% ของทรานสคริปต์ที่เกี่ยวข้องในขณะที่ครอบคลุมเพียงหนึ่งในสามของจีโนม [3][6]. ระดับความแม่นยำและประสิทธิภาพนี้มีความสำคัญอย่างยิ่งในการเอาชนะข้อจำกัดด้านทรัพยากรและ การขยายการผลิต.
"ผลการวิจัยเหล่านี้แสดงให้เห็นถึงประโยชน์ของการคัดกรอง CRISPR ในการเพิ่มประสิทธิภาพลักษณะของเซลล์ต้นกำเนิดของวัวและเสนอเส้นทางสู่การผลิตเนื้อสัตว์ที่เพาะเลี้ยงได้มากขึ้นในอนาคต" [1]
แม้จะมีความก้าวหน้าเหล่านี้ ความสำเร็จขึ้นอยู่กับการเข้าถึงโครงสร้างพื้นฐานที่เหมาะสม นักวิจัยต้องการห้องสมุด gRNA ที่เฉพาะเจาะจงสำหรับสายพันธุ์ สื่อการเจริญเติบโตที่ออกแบบมาสำหรับการใช้งานด้านอาหาร, เครื่องปฏิกรณ์ชีวภาพที่เข้ากันได้ และเครื่องมือวิเคราะห์ที่ปรับให้เหมาะกับการผลิตเนื้อสัตว์ที่เพาะเลี้ยงแทนการใช้ในทางเภสัชกรรมการตอบสนองต่อความต้องการเหล่านี้,
สำหรับทีมที่ทำงานเพื่อพัฒนาสายเซลล์เนื้อสัตว์เพาะเลี้ยงรุ่นต่อไป เครื่องมือและเทคโนโลยีพร้อมแล้ว ความท้าทายตอนนี้อยู่ที่การนำการคัดกรอง CRISPR ไปใช้ได้อย่างรวดเร็วและมีประสิทธิภาพเพื่อให้บรรลุศักยภาพสูงสุด.
คำถามที่พบบ่อย
คุณจะเลือกใช้ระหว่าง CRISPR knockout, CRISPRi และ CRISPRa สำหรับการคัดกรองได้อย่างไร?
การเลือกใช้ระบบเหล่านี้ขึ้นอยู่กับคำถามทางชีววิทยาเฉพาะของคุณและผลลัพธ์ที่คุณต้องการ:
- CRISPR knockout: วิธีนี้ทำให้การทำงานของยีนหยุดชะงักโดยสิ้นเชิง ทำให้เหมาะสำหรับการศึกษาผลกระทบจากการสูญเสียหรือการยับยั้งยีน.
- CRISPRi: การยับยั้งการแสดงออกของยีนโดยไม่ตัด DNA วิธีนี้เหมาะสำหรับการศึกษายีนที่จำเป็นหรือเมื่อจำเป็นต้องมีการยับยั้งที่สามารถกลับคืนได้
- CRISPRa: หากคุณต้องการเพิ่มการแสดงออกของยีน ระบบนี้เป็นตัวเลือกที่เหมาะสม โดยเฉพาะอย่างยิ่งสำหรับการตรวจสอบผลของการแสดงออกเกิน เช่น การส่งเสริมการเพิ่มจำนวนหรือการแยกแยะเซลล์
เมื่อทำการตัดสินใจ ควรพิจารณารูปแบบเซลล์ของคุณ ยีนที่คุณกำลังมุ่งเป้า และเป้าหมายโดยรวมของการทดลองของคุณ
คุณจะสามารถเพิ่มการเพิ่มจำนวนโดยไม่ทำลายการแยกแยะของกล้ามเนื้อหรือไขมันได้อย่างไร?
การเพิ่มจำนวนของเซลล์กล้ามเนื้อหรือไขมันในขณะที่ยังคงความสามารถในการแยกแยะเป็นความท้าทายสำคัญในการผลิตเนื้อสัตว์ที่เพาะเลี้ยงOne promising approach involves การแก้ไขยีนด้วย CRISPR, ซึ่งช่วยให้สามารถจัดการยีนได้อย่างแม่นยำเพื่อเพิ่มการเจริญเติบโตหรือยืดอายุเซลล์ ตัวอย่างเช่น การกำหนดเป้าหมาย myostatin (MSTN) สามารถส่งเสริมการเจริญเติบโตของเซลล์ ในขณะที่การแก้ไข CDKN2A ช่วยให้เซลล์หลีกเลี่ยงการแก่ชราได้
อย่างไรก็ตาม การบรรลุสมดุลระหว่างการเพิ่มจำนวนและการแยกแยะเป็นสิ่งสำคัญ การจัดการเป้าหมายบางอย่างผิดพลาด เช่น P53 (TP53), อาจทำให้การแยกแยะบกพร่อง ซึ่งอาจส่งผลต่อคุณภาพของเนื้อเยื่อ เพื่อจัดการกับความซับซ้อนเหล่านี้ การคัดกรอง CRISPR แบบความเร็วสูง มีความสำคัญ เทคนิคนี้ช่วยระบุผู้ควบคุมยีนที่มีประสิทธิภาพมากที่สุด เปิดทางสำหรับการพัฒนาเนื้อเยื่อที่สามารถขยายได้และมีสุขภาพดีในการผลิตเนื้อสัตว์ที่เพาะเลี้ยง
สิ่งที่จำเป็นในการตรวจสอบความถูกต้องของ CRISPR screen hits ก่อนที่จะขยายสายเซลล์คืออะไร?
การตรวจสอบความถูกต้องของ CRISPR screen hits สำหรับการผลิตเนื้อสัตว์เพาะเลี้ยงต้องการวิธีการที่เป็นระบบ ก่อนอื่นต้องยืนยันการทำงานของยีนผ่านการทดลองอิสระ เช่น การทำให้ยีนไม่ทำงาน เพื่อให้แน่ใจว่าผลที่สังเกตได้สามารถทำซ้ำได้ จากนั้นจำเป็นต้องประเมินความเกี่ยวข้องทางชีวภาพของยีนเหล่านี้โดยการตรวจสอบผลกระทบต่อปัจจัยต่างๆ เช่น การเพิ่มจำนวนเซลล์ ความมีชีวิต และอายุยืน
การประเมินความปลอดภัยมีความสำคัญเท่าเทียมกันเพื่อขจัดผลกระทบที่ไม่ตรงเป้าหมายหรือความไม่เสถียรทางพันธุกรรมที่อาจทำให้กระบวนการเสียหาย การตรวจสอบความถูกต้องของการทำงานภายใต้สภาวะที่เลียนแบบการตั้งค่าอุตสาหกรรม เช่น เครื่องปฏิกรณ์ชีวภาพ เป็นอีกขั้นตอนสำคัญ ซึ่งจะช่วยให้มั่นใจได้ว่าการแก้ไขทางพันธุกรรมทำงานตามที่คาดไว้ในสภาพแวดล้อมการผลิตขนาดใหญ่ การทดสอบอย่างละเอียดในทุกขั้นตอนเป็นสิ่งที่ไม่สามารถต่อรองได้ก่อนที่จะพิจารณาการขยายขนาด











