İskele tabanlı biyoreaktörlerde sıvıların hareket etme şekli, kültür et üretimi için oyunun kurallarını değiştiriyor. Uygun akış, hücrelerin yeterli besin ve oksijen almasını sağlarken, özellikle kalın doku yapıları için atıkların uzaklaştırılmasını sağlar. İşte neden önemli:
- Difüzyon sınırları: Besinler sadece 100–200 μm'ye kadar difüzyonla nüfuz eder, iç hücreler aç kalır.
- Perfüzyon biyoreaktörleri: Bu sistemler, kültür ortamını iskeleler aracılığıyla aktif olarak iter, besin dağıtımını ve atık uzaklaştırılmasını iyileştirir.
- Kesme gerilimi dengeleri: Kontrollü akış büyümeyi teşvik eder, ancak aşırı kesme hücrelere zarar verebilir.
Anahtar faktörler arasında perfüzyon hızları, iskele tasarımı (gözenek boyutu, gözeneklilik) ve akış davranışını tahmin etmek için hesaplamalı modeller bulunur.
Akış kontrolü, iskele tasarımı ve hesaplamalı araçların bu alanı nasıl şekillendirdiği hakkında içgörüler için okumaya devam edin.
Perfüzyon Biyoreaktör Modelleme ANSYS Fluent Kullanarak - Bölüm 1
Perfüzyon Oranları ve Kesme Gerilmesi Açıklaması
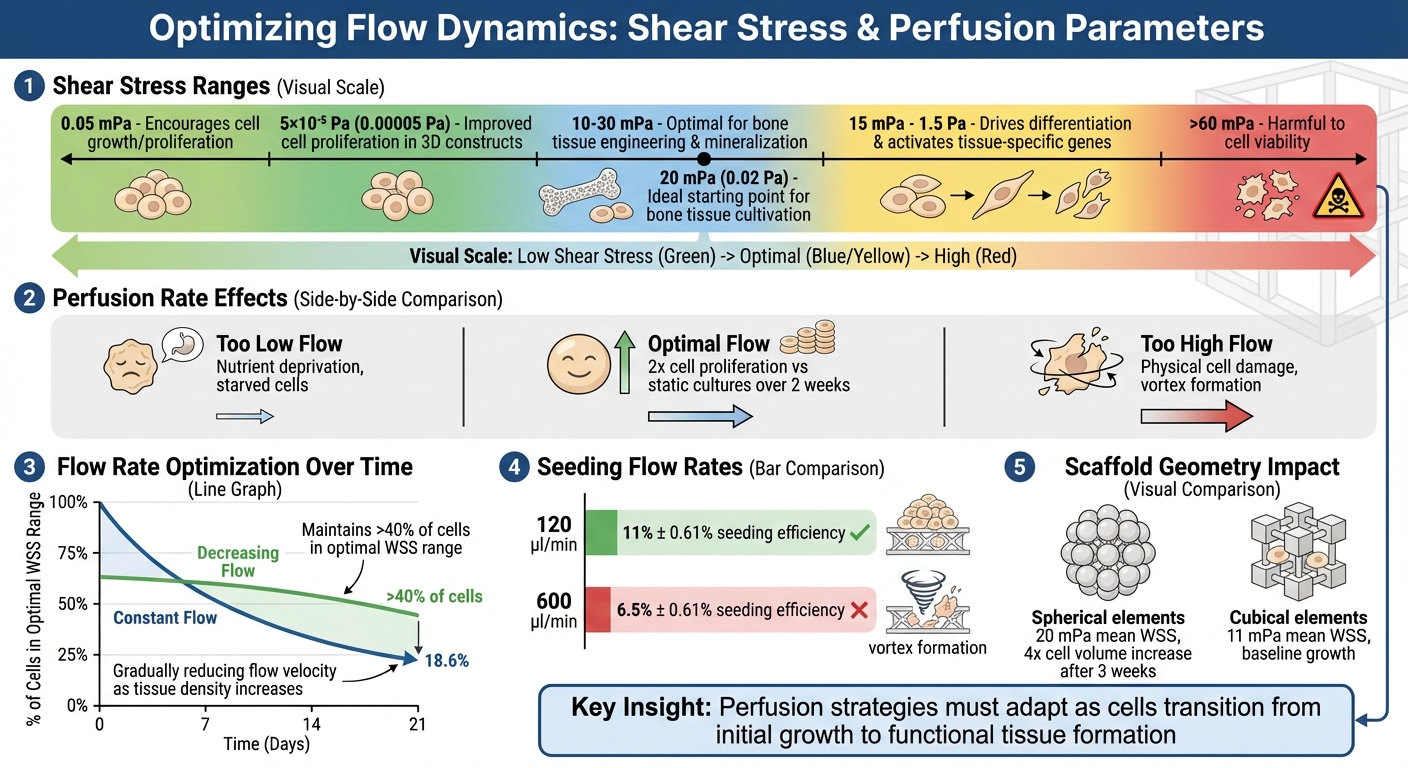
İskele Tabanlı Biyoreaktörler için Optimal Kesme Gerilmesi Aralıkları ve Akış Parametreleri
Perfüzyon Oranlarının Hücre Büyümesini Nasıl Etkilediği
Perfüzyon oranları, besinlerin nasıl iletildiğini ve atıkların ortam akışı yoluyla nasıl uzaklaştırıldığını kontrol etmek için çok önemlidir. Akış çok düşükse, hücreler temel besinlerden mahrum kalır. Öte yandan, aşırı akış hücrelere fiziksel zarar verebilir. Anahtar, besin değişimini maksimize ederken zarar vermeden doğru dengeyi bulmaktır.
Çalışmalar, perfüzyon kültürlerinin, iki hafta boyunca statik kültürlere kıyasla hücre proliferasyonunu iki katından fazla artırabileceğini göstermektedir [4]. Bazı durumlarda, fark daha da çarpıcıdır. Örneğin, küresel iskelelerde, hücre hacmi üç hafta perfüzyon sonrasında kübik iskelelere kıyasla dört kat artmıştır [7]. Bu sadece akış hızını artırmakla ilgili değil - büyüme için doğru mekanik koşulları yaratmakla ilgilidir.
"Perfüzyonun neden olduğu karışım ve sıvı kayma gerilimi, hücreleri mekanik olarak uyararak gelişimi iyileştirecek ve istenen hücre tipine farklılaşmalarını sağlayacaktır." – SN Applied Sciences [4]
Kayma gerilimi de kritik bir rol oynar. Düşük seviyeler (~0.05 mPa) hücre büyümesini teşvik ederken, daha yüksek seviyeler (15 mPa–1.5 Pa) farklılaşmayı yönlendirir ve dokuya özgü genleri aktive eder [2][8]. Bu, perfüzyon stratejilerinin, hücreler başlangıç büyümesinden fonksiyonel doku oluşturmaya geçerken uyum sağlaması gerektiği anlamına gelir. Bir sonraki bölüm, hücre canlılığını korumak için kayma gerilimini nasıl etkili bir şekilde yönetileceğine dalıyor.
Hücre Canlılığını Korumak İçin Kayma Gerilimini Kontrol Etme
Duvar kayma gerilimi (WSS) iki ucu keskin bir kılıçtır. Kemik doku mühendisliği için ideal aralık 10–30 mPa arasındadır, bu da mineralizasyonu destekler. Ancak, 60 mPa'yı aşmak hücre canlılığına zarar verebilir [5]. Hücre yoğunluğu arttıkça, iskele gözenekliliği azalır, bu da akış yollarını kısıtlayabilir ve akış hızları sabit kalırsa kayma geriliminde lokalize artışlara yol açabilir.
Bunu ele almanın bir yolu, doku yoğunluğu arttıkça akış hızını kademeli olarak azaltmaktır.Örneğin, sürekli akış koşulları, optimal WSS'ye maruz kalan hücrelerin yüzdesini 21 gün boyunca %50'den %18,6'ya düşürür. Buna karşılık, akış hızının zamanla düşürülmesi, hücrelerin %40'ından fazlası için optimal koşulları korur [5]. Ekim aşamasında, hassas kalibrasyon esastır; 120 µl/dak akış hızı idealdir, 600 µl/dak gibi daha yüksek hızlar ise girdaplar oluşturarak uygun iskele bağlantısını engelleyebilir [3].
İskele geometrisi de büyük bir etkiye sahiptir. Akışın iskele yapısıyla etkileşimi, hücre sağlığını korumak ve doku büyümesini desteklemek için mimarisiyle uyumlu olmalıdır. Örneğin, aynı akış koşulları altında, küresel iskele elemanları ortalama 20 mPa WSS üretirken, kübik elemanlarda bu değer 11 mPa'dır [7]. Bu, doğru iskele tasarımının, dikkatli akış kontrolü ile birleştirildiğinde sonuçları optimize etmek için ne kadar önemli olduğunu vurgular.
Akış Kontrolü için Biyoreaktör Tasarımı
İskelet Gözenekliliği ve Akış Kanalı Tasarımı
Bir iskeletin yapısı, sıvı akışını ve hücre dağılımını yönetmede kritik bir rol oynar. Gözenek boyutu, gözeneklilik yüzdesi ve gözenek düzenlemesi gibi anahtar faktörler, sıvının nasıl hareket ettiğini ve hücreler üzerindeki kayma kuvvetlerini doğrudan etkiler [1] . Özünde, gözeneklerin boyutu ve yerleşimi, akış hızını ve kayma geriliminin iskelet boyunca nasıl dağıldığını belirler.
"Uygulanan perfüzyon koşulları altında, hücre birikimi esas olarak yerel duvar kayma gerilimi tarafından belirlenir ve bu da sırasıyla iskeletin gözenek ağı yapısından güçlü bir şekilde etkilenir." – Biomaterials Journal [1]
İskelet tasarımları tipik olarak ya izotropik ya da gradyanlıdır.İzotropik iskeleler, yaklaşık 412 μm'lik ve %62 poroziteye sahip uniform gözenek boyutlarına sahiptir - bu da 15 ila 24 s⁻¹ arasında sabit kayma hızları ile sonuçlanır. Buna karşılık, gradyan iskeleler değişen gözenek boyutları (250–500 μm) ve porozite seviyeleri (%35–%85) sunar, bu da 12–38 s⁻¹ arasında daha geniş bir kayma aralığı oluşturur [1]. Bu gradyan tasarımı, hücrelerin belirli bölgelerde birikmesini teşvik ederken, izotropik iskeleler yapının tamamında eşit bir dağılım sağlar.
Hücreler büyüyüp iskelelerin boşluklarını doldurdukça, porozitesini azaltarak akışkan dinamiklerini değiştirirler. Daha yoğun iskeleler, akışı sürdürmek için daha yüksek basınç gerektirir, bu da aşırı kayma gerilimi oluşturma riski taşır. Etkili doku büyümesi için, yaklaşık 100 μm'lik bir gözenek yarıçapı önemlidir [2][6]. Ancak, ideal gözenek boyutu, yetiştirilen doku türüne bağlı olarak değişir.Bu faktörler, akışı etkili bir şekilde yöneten biyoreaktörlerin tasarımı için gereklidir.
Biyoreaktör Türleri ve Akış Kontrol Yöntemleri
Perfüzyon biyoreaktörleri, besinleri eşit bir şekilde dağıtırken kontrollü kayma gerilimi uygulamada etkilidir. Ortamı iskele boyunca yönlendirerek, daha kalın dokuların gelişimini desteklerler [2] .
Paket yataklı reaktörler, öte yandan, yüksek hacimli operasyonlar için tasarlanmıştır ancak düzensiz radyal gözeneklilikle ilgili zorluklarla karşılaşır. Bu, sıvının belirli alanları atlayarak "kanallama"ya yol açabilir ve bu da eşit dağılımı bozar. Örneğin, Kasım 2017'de araştırmacılar, 3D Biotek'in ticari PCL iskelelerini (5 mm çap, 1.5 mm yükseklik) test ettiler. 120 μl/dak'lık bir akış hızının %11 ± 0.61%'lik bir tohumlama verimliliği sağladığını buldular. Ancak, 600 μl/dak'da verimlilik %6.5 ± 0.61% hücrelerin iskele liflerine yapışmasına izin vermek yerine, hücreleri dolaşım bölgelerinde hapseden girdap oluşumu nedeniyle [3]. Bu, tutarlı hücre ekimi elde etmek için akış kontrolünün ne kadar kritik olduğunu vurgulamaktadır.
Farklı sistemler, akışı yönetmek için farklı yöntemler kullanır. Perfüzyon biyoreaktörleri, akışı iskele boyunca yönlendirmeye odaklanırken, boş lif sistemleri, kılcal damarlara benzer şekilde besin teslimatını simüle etmek için hem lümen giriş akışını hem de çıkış geri basıncını düzenler [9]. Gelişmiş sistemler, kararlı koşulları korumak için sensörler ve monitörler içerir [8]. Ayrıca, hücrelere zarar verebilecek veya akışı bozabilecek hava kabarcıklarından kaçınmak için, ortam rezervuarını kültür odasının üzerine yerleştirmek hidrostatik basıncı etkili bir şekilde kullanır [8].
sbb-itb-ffee270
Akış Davranışını Tahmin Etmek İçin Hesaplamalı Modellerin Kullanımı
Biyoreaktör Tasarımında CFD'nin Faydaları
Hesaplamalı akışkanlar dinamiği (CFD) modelleri, akışkanların iskele yapıları boyunca nasıl hareket ettiğini tahmin etmek için güçlü araçlardır. Navier-Stokes denklemlerini çözerek, bu modeller kayma gerilimi ve besin dağılımı hakkında içgörüler sağlar - fiziksel prototiplere ihtiyaç duymadan. Bu, sadece geliştirme maliyetlerini azaltmakla kalmaz, aynı zamanda tekrarlanan deneysel denemeler sırasında meydana gelebilecek kontaminasyon riskini de ortadan kaldırır [11][3][10].
İskele geometrileri, standart şekiller için CAD kullanılarak veya daha karmaşık yapılar için μCT görüntüleme ile tasarlanabilir [2][10]. Mart 2005'te, araştırmacılar, silindirik iskeleler aracılığıyla medyanın nasıl aktığını simüle etmek için 34 μm voksel çözünürlüğünde μCT görüntüleme ile Lattice-Boltzmann yöntemini kullandılar. Modelleri, ortalama yüzey kayma geriliminin 5×10⁻⁵ Pa olmasının, hücre çoğalmasının iyileşmesiyle bağlantılı olduğunu gösterdi [2].
CFD ayrıca, hücreler büyüdükçe ve iskeleler içindeki boşlukları doldurdukça akış desenlerinin nasıl geliştiğini tahmin etmeye yardımcı olur. Örneğin, Kasım 2021'de bir çalışma, COMSOL Multiphysics kullanarak hiyerarşik 3DP/TIPS iskeleler aracılığıyla sıvı akışını simüle etti. Araştırmacılar, 10 mm çapında bir iskelede 38 giriş kanalını modelleyerek, murin preosteoblastik hücreler için ideal olan 20 mPa duvar kayma gerilimini elde etmek amacıyla peristaltik pompa hızını ince ayarladılar [4]. Bu modeller, Michaelis-Menten denklemlerini kullanarak hücre büyüme kinetiği ve oksijen tüketim oranları gibi karmaşık faktörleri bile içerebilir.Bu, tasarımcıların doku gelişiminin zamanla akışkan dinamiklerini nasıl etkileyeceğini öngörmelerini sağlar [11][12].
"CFD, gerekli deneylerin doğasında bulunan maliyet, zaman ve kontaminasyon riskini azaltmaya yardımcı olabilir." – Future Foods Mini-Review [11]
Bu öngörü yetenekleri, akış koşullarını dinamik olarak ayarlamak için sensör geri bildirimini entegre etmenin yolunu açar.
Sensörlerle Gerçek Zamanlı İzleme
Sensörleri hesaplamalı modellerle eşleştirmek, biyoreaktör tasarımını bir adım öteye taşıyarak optimal koşulları korumak için gerçek zamanlı ayarlamalar yapılmasını sağlar. Örneğin, Aralık 2025'te araştırmacılar, oksijen dağılımını ve akışkan hızını simüle etmek için COMSOL Multiphysics 6.3 kullanarak BioAxFlow biyoreaktörünü test ettiler.PLA iskeleler üzerinde SAOS-2 hücreleri için hücre-normalize edilmiş oksijen tüketim oranı olarak 2 nmol dk⁻¹ 10⁻⁶ hücre uyguladılar. Sonuçlar, odanın geometrisinin mekanik karıştırıcılara ihtiyaç duymadan eşit hücre dağılımını desteklediğini gösterdi [13].
Gelişmiş sistemler artık izlenen oksijen seviyelerine göre akış hızlarını ayarlayabilir, bu da iskeletin merkezinin bile düzgün bir şekilde oksijenlenmesini sağlar [13]. Ancak, bir zorluk devam ediyor: iskeleler içinde yerel kayma gerilimini ölçmek. Saskatchewan Üniversitesi'nden X. Yan'ın vurguladığı gibi: "Yeterli sensörlerin eksikliği nedeniyle, bir iskele içinde yerel kayma gerilimi dağılımını ölçmek zor, hatta imkansızdır" [10]. Bu sınırlama, fiziksel sensörlerin şu anda başaramadığı ayrıntılı tahminler sağlayabilen CFD modellemenin değerini vurgulamaktadır.
Akış Dinamiklerinin Kültive Edilmiş Et Üretimine Uygulanması
Doku Kalitesini Akış Kontrolü ile İyileştirmeKontrollü akış dinamiklerinin kullanılması, hücrelerin iskele boyunca eşit dağılımını sağlayarak kültive edilmiş etin kalitesini önemli ölçüde artırabilir. Statik kültürlerdeki en büyük sorunlardan biri, hücre büyümesinin genellikle iskele kenarlarında yoğunlaşması ve merkezin gelişmemiş kalmasıdır. Akış dinamikleri, kütle taşınımını iyileştirerek oksijen ve besin maddelerinin iskele çekirdeğine ulaşmasını sağlarken atıkların verimli bir şekilde uzaklaştırılmasını sağlar. Bu denge, yüksek kaliteli, yapısal olarak sağlam kültive edilmiş et ürünleri üretmek için esastır.Kesme gerilimi burada kritik bir rol oynar. Örneğin, çalışmalar, ortalama yüzey kesme geriliminin 5×10⁻⁵ Pa olmasının 3D yapılarında hücre çoğalmasını teşvik ettiğini göstermektedir. Karşılaştırıldığında, kemik dokusu için tasarlanan iskeleler genellikle yaklaşık 20 mPa (0.02 Pa) yetiştirmenin başlangıcında mekanik uyarım sağlamak için [2][4]. Ancak, hücreler iskeletin gözeneklerini doldurdukça, akış kanalları daralır ve pompa hızı sabit kalsa bile kayma gerilimi doğal olarak artar [4].
"Matriks sentezindeki gözlemlenen heterojenliğin, yapılar içinde besinlerin yetersiz dağılımı ve atık ürünlerin uzaklaştırılmasının bir sonucu olduğuna inanılmaktadır." – Robert Guldberg [2]
Başlangıç hücre ekiminin etkinliği, akış dinamiklerinin doku sonuçlarını nasıl etkilediğini de vurgular. PCL iskeletleri kullanılarak yapılan araştırmalar, 120 μl/dak'lık bir akış hızının ekim için ideal olduğunu, 600 μl/dak gibi daha yüksek hızların ise hücreleri dolaşım bölgelerinde hapseden girdap oluşumu nedeniyle verimliliği azalttığını bulmuştur [3]. Başlangıç hücre dağılımının eşit olması, nihai ürünün kalitesini sağlamak için çok önemlidir. Bu bulgular, hassas akış gereksinimlerini karşılayabilecek ekipmanların kullanılmasının önemini vurgulamaktadır.
Ekipman Tedariki Cellbase
Hassas akış kontrolü sağlamak ve doku kalitesini optimize etmek, özel ekipmanlara erişim gerektirir. İşte burada
Üretimi artıranlar için,
Sonuç
İskele tabanlı biyoreaktörlerde akış dinamiklerini yönetmek, yüksek kaliteli kültive edilmiş et üretimi için esastır. Başarı, perfüzyon oranlarını ve kesme gerilimini kültivasyon süreci boyunca etkili bir şekilde kontrol etmeye bağlıdır. Statik kültürler, ticari ölçekli üretim için gerekli olan kalın, uniform doku yapılarının desteklenmesinde yetersiz kalır. Yüzeyden 100–200 μm'den daha uzakta bulunan hücreler genellikle yeterli besin ve oksijen alamaz, bu da biyoreaktör tasarımında gelişmiş akış yönetiminin önemini vurgular [4].
Akış parametreleri optimize edildiğinde, perfüzyon biyoreaktörleri, statik kültürlere kıyasla hücre çoğalmasını iki katından fazla artırabilir [4]. Perfüzyon ve kesme gerilimini ayarlamak, tutarlı doku büyümesi elde etmek için özellikle önemlidir.Örneğin, Nisan 2020'de Sheffield Üniversitesi'nde yapılan bir araştırma, sabit bir hız yerine zamanla akışkan akışını kademeli olarak azaltmanın sonuçları önemli ölçüde iyileştirdiğini buldu. 21 gün sonra, hücre yüzeyinin %40.9'u optimal kayma gerilimi aralığında kaldı, bu oran sabit akış koşullarında sadece %18.6 idi [5]. Bu tek değişiklik, hem doku kalitesini hem de üretim verimliliğini büyük ölçüde artırabilir.
"Daha mineralize doku elde etmek için, perfüzyon biyoreaktörlerinin yüklenmesinin geleneksel yöntemi (i.e. sabit akış hızı/velositesi) zamanla azalan bir akışa dönüştürülmelidir." – F. Zhao ve ark. [5]
Kütle taşınımı ile mekanik uyarım arasında doğru dengeyi kurmak çok önemlidir.Yetersiz akış, iç hücrelerin mahrum kalmasına neden olurken, aşırı akış onları yerinden oynatma riski taşır [10][3]. Hesaplamalı Akışkanlar Dinamiği (CFD) modellemesi, yerel akış koşullarını tahmin etmede ve biyoreaktör performansını optimize etmede önemli bir rol oynar [2][10].
Üretimi ölçeklendirmek de ekipman zorluklarını beraberinde getirir. Hiyerarşik yapıya sahip iskelelerden hassas akış kontrolüne sahip biyoreaktörlere kadar, doğru araçları temin etmek hayati önem taşır.
SSS
İskeletim için güvenli bir perfüzyon hızını nasıl seçebilirim?
Perfüzyon hızını dengelemek, hücrelerin başarılı bir şekilde tutunmasını ve iskelet performansını sağlarken olası hasarları önlemek için anahtardır. Orta derecede akış hızlarıyla başlamak genellikle mantıklı bir yaklaşımdır. Buradan, hücre canlılığını ve iskelet bütünlüğünü yakından izleyerek kademeli ayarlamalar yapabilirsiniz. Özel iskelet tasarımınıza uygun hesaplamalı modeller veya deneysel veriler kullanmak değerli bilgiler sağlayabilir. Bu, perfüzyon hızını, hücre büyümesini ve besin taşınmasını destekleyecek şekilde ince ayar yapmanıza yardımcı olurken, kesme gerilimi hasarı riskini en aza indirir.
Doku kalınlaştıkça kesme gerilimi hasarını nasıl önleyebilirim?
Doku kalınlaştıkça kesme gerilimi hasarı riskini azaltmak için, yetiştirme sırasında perfüzyon akış hızını kademeli olarak düşürmek önemlidir.Bu ayarlama, hücreleri aşırı zorlanmadan korurken mineralizasyonu teşvik etmeye devam eden 10–30 mPa, ideal aralığında duvar kayma gerilimini (WSS) tutmaya yardımcı olur. Hesaplamalı çalışmalar bu yöntemi destekler, yüksek kayma gerilimine maruz kalan doku miktarını önemli ölçüde azaltabileceğini gösterir, gelişmekte olan dokuyu zarardan korumaya yardımcı olur.
Gerçekçi akış tahminleri için CFD modellemesi ne içermelidir?
CFD modellemesi, iskeletin mikro yapısını içermeli, hassas akışkan akışı simülasyonunu sağlamalı ve kayma geriliminin detaylı bir analizini sunmalıdır. Ayrıca, tahminlerin gerçek dünya koşullarıyla uyumlu olmasını sağlamak için deneysel veri doğrulaması çok önemlidir. Bu faktörler birlikte, iskelet tabanlı biyoreaktörlerdeki akış dinamiklerinin daha derin bir şekilde anlaşılmasına katkıda bulunur.











