Yüksek verimli CRISPR taraması, hücre hattı performansını artırmak için hassas genetik modifikasyonlara olanak tanıyarak kültürlenmiş et sektörünü dönüştürüyor. İşte bilmeniz gerekenler:
- Ana Zorluk: Kültürlenmiş et üretimi, verimli bir şekilde büyüyen, yaşlanmaya dirençli ve kas ile yağ dokusuna farklılaşabilen hücre hatları gerektirir.
- CRISPR'ın Rolü: Bu platformlar, binlerce geni aynı anda hedefleyerek büyümeyi artıran, yaşlanmayı geciktiren ve farklılaşmayı destekleyen genetik düzenlemeleri belirler.
- Dikkate Değer Bulgular: Çalışmalar, TP53 ve PTEN gibi genlerin sığır mezenkimal kök hücrelerinde devre dışı bırakılmasının, 30 gün içinde çoğalmayı 1.000 katına kadar artırabileceğini ve ömürlerini 100 günden 200 güne kadar uzatabileceğini göstermiştir.
- Uygulamalar: Knockout taramaları, CRISPRi ve CRISPRa gibi CRISPR araçları, hücre büyümesini optimize etmek, gen ekspresyonunu düzenlemek ve çoğalmayı farklılaşma ile dengelemek için kullanılmaktadır.
- Endüstri Araçları: RMCE, RNA-seq ve tek hücre platformları gibi ileri teknikler, CRISPR sonuçlarını çoklu omik verilerle entegre ederek kesin ve ölçeklenebilir iyileştirmeler sağlar.
Biyoproses mühendisleri ve Ar&Ge profesyonelleri için, bu yenilikler kültive edilmiş et süreçlerini ölçeklendirmede kritik darboğazları ele alırken hücre kalitesini ve işlevselliğini korur. CRISPR'ın otomatik sistemler ve
Genom Çapında Knockout Taramalar için CRISPR-Cas9 Temelleri
CRISPR-Cas9'un Büyük Ölçekli Gen Düzenlemede Çalışma Prensibi
CRISPR-Cas9 sistemi, belirli DNA dizilerini hedeflemek için tek kılavuz RNA (sgRNA) ile eşleştirilmiş bir Cas9 nükleazına dayanır. sgRNA, Cas9'u istenen genomik konuma yönlendirdikten sonra, enzim DNA'da çift sarmallı bir kırık oluşturur. Bu kırık, çoğunlukla, genellikle küçük ekleme veya silme (indel) hataları tanıtan hataya açık bir süreç olan homolog olmayan uç birleştirme (NHEJ) yoluyla onarılır. Bu indeller, hedeflenen genin işlevini etkili bir şekilde bozarak çerçeve kayması mutasyonlarına neden olabilir [1]. Bu hassas mekanizma, hücresel davranışın kritik düzenleyicilerini belirlemede önemli olan genom çapında knockout taramaları yürütmenin temelidir.
Büyük ölçekli taramalar için araştırmacılar, genellikle lentiviral transdüksiyon yoluyla karışık bir hücre popülasyonuna iletilen çeşitli bir sgRNA kütüphanesi kullanır. Her hücrenin yalnızca bir genetik değişiklik almasını sağlamak için düşük bir enfeksiyon çokluğu (yaklaşık 0.3 MOI) korunur [1]. Zamanla, avantajlı mutasyonlara sahip hücreler, diğerlerine göre daha başarılı bir şekilde çoğalma eğilimindedir, bu fenomen çeşitli hücre tipleri ve deneysel koşullar arasında gözlemlenmiştir.
Rekombinaz aracılı kaset değişimi (RMCE) gibi alternatif iletim yöntemleri, entegrasyon bölgelerindeki değişkenliği azaltmak için belirli genomik "iniş pedlerini" hedefleyerek ek hassasiyet sunar. Örneğin, CHO-K1 hücrelerini kullanan bir çalışma, 21,585 gen üzerinde 111,651 benzersiz gRNA'yı taramak için virüssüz bir RMCE yöntemi kullandı. Bu yaklaşım, 16 ve 37 günlük süreler boyunca hücre uygunluğu için gerekli genleri belirledi [7].
Genom Çapında Tarama Faydaları
Genom çapında knockout taramaları, CRISPR-Cas9'un doğruluğunu kullanarak binlerce geni sistematik olarak araştırır. Bu, araştırmacıların hücre hayatta kalmasını, büyümesini ve strese tepkilerini etkileyen genleri ortaya çıkarmasını sağlar. Genetik faktörlerin ötesinde, yüzey fonksiyonelleştirmesinin optimize edilmesi, bu sistemlerde hücre tutunması ve büyümesini iyileştirmek için kritiktir. Bu tür tarafsız keşifler, mezenkimal kök hücrelerin (hücre kaynaklarının yaklaşık %25'ini oluşturan) sınırlı çoğalma ve erken yaşlanma gibi zorluklarla sıkça karşılaştığı kültür et üretimi, için özellikle önemlidir [1].
sbb-itb-ffee270
Havuzlanmış CRISPR Kütüphane Tarama Yöntemleri
Havuzlanmış CRISPR Kütüphanelerinin Oluşturulması
Havuzlanmış CRISPR kütüphaneleri, dikkatlice seçilmiş bir tek kılavuz RNA (sgRNA) koleksiyonu ile başlar.Kültürlenmiş et araştırmaları bağlamında, hedeflenen kütüphaneler genellikle transkripsiyon faktörleri veya hücre çoğalmasının düzenleyicileri gibi belirli gen ailelerine odaklanacak şekilde tasarlanır. Bu yaklaşım, maliyeti ölçeklenebilirlikle dengelemeye yardımcı olurken, istenen fenotipe ilişkin özelliklere odaklanmayı sürdürür [1].
Süreç, oligonükleotidlerin bir havuz olarak sentezlenmesi, PCR ile çoğaltılması ve bir taşıyıcı vektöre klonlanması ile başlar. Örneğin, 2025'in başlarında inşa edilen sığıra özgü bir kütüphane, kök hücre genişlemesini etkileyen faktörleri belirlemek için 603 geni hedefleyen 3,000 sgRNA içeriyordu [1]. Daha büyük ölçekte, genom çapında taramalar çok daha yüksek karmaşıklığa ulaşabilir. Bir örnek, 21,585 geni hedeflemek için 111,651 benzersiz gRNA kullanan bir Çin Hamsteri Yumurtalık (CHO) hücre taramasıdır [7].
Lentiviral transdüksiyon, bu kütüphaneleri düşük enfeksiyon çokluğu (yaklaşık 0.3) ile iletmek için yaygın olarak kullanılır, bu da her hücrenin yalnızca tek bir genetik modifikasyona uğramasını sağlar [1]. Alternatif olarak, rekombinaz aracılı kaset değişimi (RMCE) gibi virüssüz yöntemler, gRNA kütüphanesini ana hücre hattı içindeki önceden belirlenmiş genomik "iniş pedlerine" entegre eder. Bu teknik, minimal sapma ile %99.9 gRNA kapsama alanı sağlar [7].
İstatistiksel güvenilirliği korumak için, araştırmacılar yüksek kapsama alanı sağlarlar - tipik olarak her sgRNA başına 500 ila 600 hücre [1] [7] . Bazı platformlar, gen düzenlemenin ne zaman gerçekleşeceği üzerinde hassas kontrol sağlayan indüklenebilir Cas9 (iCas9) sistemlerini kullanır. Örneğin, düzenleme, hücreler belirli bir duruma ulaştığında, örneğin yüksek yoğunluk veya yaşlanma başlangıcı gibi, tetiklenebilir. Bu zamansal kontrol, birincil ve ölümsüzleştirilmiş hücre hatları arasında seçim yaparak yaşlanma engellerini aşmak için kritik olan proliferatif olmayan fazları incelemek için özellikle yararlıdır ve kültürlenmiş et üretimini ölçeklendirmek için [4] .
Kütüphane oluşturulduktan sonra, araştırmacılar gen fonksiyonunu değerlendirmek için hedefe yönelik tarama testlerine geçerler.
Kültürlenmiş Et Hücre Hatları için Tarama Yaklaşımları
Kütüphane oluşturulduktan sonra, araştırmacılar hücre performansını rekabet testleri ve fonksiyonel ayırma teknikleri kullanarak değerlendirirler. Yaygın olarak kullanılan bir yöntem, büyüme veya yaşlanma direnci sağlayan genetik değişiklikleri tanımlayan rekabete dayalı proliferasyon testidir - kültürlenmiş et için hücre hatlarını optimize etmek için anahtar özellikler.
Kısa vadeli taramalar (yaklaşık 30 gün süren), hücre döngüsünü hemen etkileyen genleri tanımlar, uzun vadeli taramalar (200 güne kadar) ise hücrelerin replikatif yaşlanmayı aşmasına yardımcı olan genlere odaklanır. Bu, kültürlenmiş et üretimini ölçeklendirmede kritik bir zorluktur [1]. Daha karmaşık özellikler için, örneğin artırılmış protein salgısı veya belirli belirteçlerin ifadesi gibi, floresanla aktive edilmiş hücre ayırma (FACS) kullanılır. Bir örnek, salgılanan proteinleri hücre yüzeyinde ayırmadan önce yakalayarak üretken hücre popülasyonlarını izole eden "soğuk yakalama salgı testi"dir [7] [5].
Doğrulama, tarama sonuçlarını teyit etmede kritik bir adımdır. Örneğin, Hücresel Uygunluk (CelFi) testi, zaman içinde çerçeve dışı mutasyonların çerçeve içi mutasyonlara oranını izler.Eğer çerçeve dışı mutasyonlara sahip hücreler popülasyondan kayboluyorsa, bu durum hedeflenen genin hücresel uygunluk için gerekli olduğunu gösterir [2].
Haziran 2025'te, Shijie Ding liderliğindeki araştırmacılar Nanjing Tarım Üniversitesi CRISPR/Cas9 kullanarak CDKN2A–/– domuz uydu hücre hatları . oluşturdular. Bu modifiye edilmiş hücreler, kök hücre belirteçlerini korurken serum içermeyen koşullarda en az 15 pasaj boyunca stabil proliferasyon sağladı. Bitki bazlı 3D yenilebilir bir iskeleye ekildiklerinde, geliştirilmiş dokuya sahip, çiğneme ve yapışkanlık gibi özellikleri artırılmış et benzeri yapılar oluşturdular [8].
"Bu bulgular, CRISPR taramasının sığır kök hücre özelliklerini optimize etmek için faydasını göstermekte ve gelecekte daha ölçeklenebilir kültür et üretimi için bir yol sunmaktadır." – Communications Biology [1]
Mamali Hücrelerde Havuzlanmış CRISPR-Genetik Taramalar | Protokol Önizlemesi
Geri Dönüşümlü Gen Regülasyonu Taramaları için CRISPRi ve CRISPRa
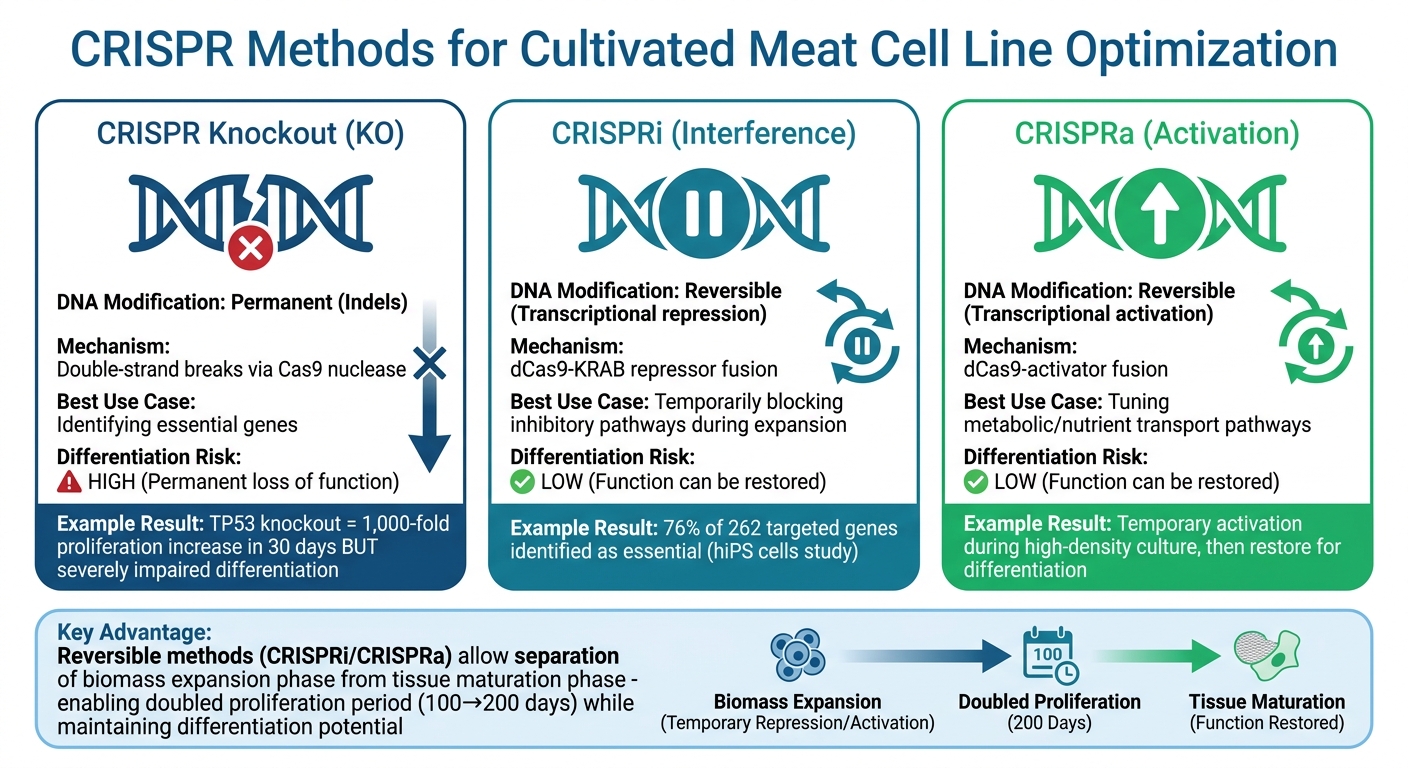
Yetiştirilmiş Et için CRISPR Gen Düzenleme Yöntemleri: Knockout ve CRISPRi/CRISPRa Karşılaştırması
Fonksiyonel Genomikte CRISPRi ve CRISPRa Kullanımı
Yetiştirilmiş et üretimini geliştirmek söz konusu olduğunda, CRISPR interferansı (CRISPRi) ve CRISPR aktivasyonu (CRISPRa) güçlü araçlar sunar. Bu teknikler, DNA'da kalıcı değişiklikler yapmadan gen ekspresyonunu geçici olarak ayarlamaya olanak tanıyan baskılayıcılar veya aktivatörlerle eşleştirilmiş etkisiz bir Cas9 proteini kullanır [10].
Bu tersine çevrilebilirlik, özellikle büyük bir zorlukla başa çıkmak için önemlidir: hızlı hücre büyümesini teşvik eden genler genellikle kas veya yağ dokusuna farklılaşmanın sonraki aşamalarına müdahale eder. Örneğin, sığır mezenkimal kök hücrelerinde TP53 genini kalıcı olarak devre dışı bırakmak, sadece 30 gün içinde çoğalmayı 1.000 kat artırabilir ancak farklılaşma yeteneklerini ciddi şekilde bozabilir [1]. CRISPRi, biyoreaktörlerde kültive edilmiş et için biyokütle genişlemesi sırasında farklılaşmayı engelleyen yolları geçici olarak bloke ederek daha esnek bir çözüm sunar . Hücreler doku olgunlaşmasına hazır olduğunda, normal gen fonksiyonu geri yüklenebilir.
Ekim 2025'te, Hollanda Kanser Enstitüsü'nden Gabriele Casagrande Raffi ve Roderick L. Beijersbergen gibi araştırmacılar, indüklenebilir bir CRISPR sistemi geliştirdiler.Bu yaklaşım, hücrelerin belirli durumlara - yüksek yoğunluk veya proliferatif olmayan bir faz gibi - ulaşmasını bekleyerek gen düzenlemesini geciktirir ve hücre canlılığını korumaya yardımcı olur [4].
CRISPRi, geleneksel RNA interferansına (RNAi) kıyasla hassasiyetiyle de öne çıkar. RNAi genellikle tutarsız sonuçlara ve hedef dışı etkilere yol açarken, CRISPRi daha güvenilir ve spesifik gen baskılaması sağlar [2]. Bir diğer avantajı ise CRISPRi'nin DNA hasar yanıtları nedeniyle sıklıkla tetiklenen p53 ile ilgili toksisiteyi önlemesidir. 2025 yılında Liqin Wang liderliğinde Sun Yat-sen Üniversitesi Kanser Merkezi, tarafından yürütülen bir çalışmada, araştırmacılar insan indüklenmiş pluripotent kök hücrelerinde (hiPS hücreleri) 262 geni taramak için doksisiklin-indüklenebilir KRAB–dCas9 sistemini kullandılar. Hedeflenen çeviri ile ilgili genlerin %76'sının (262'den 200'ü) büyüme için gerekli olduğunu buldular ve bu da sistemin etkinliğini gösterdi [10].
Gen ekspresyonunu ince ayarlama yeteneği, CRISPRi ve CRISPRa'yı fonksiyonel genomik araştırmalarında hücre çoğalması ve farklılaşmasını dengelemek için değerli araçlar haline getirir.
Kültür Et Uygulamaları için Geri Dönüşümlü Ekranların Uyarlanması
Geri dönüşümlü gen düzenlemesi, kültür et üretimindeki temel zorluklara çözümler sunar. Örneğin, CRISPRa, yüksek yoğunluklu kültür sırasında besin taşınımı veya metabolik yollarla ilgili genleri geçici olarak aktive edebilir. Hücreler istenen yoğunluğa ulaştığında, sistem gen ekspresyonunu normal seviyelere döndürebilir ve kas veya yağ dokusuna uygun farklılaşmayı destekler.
İndüklenebilir sistemler ayrıca biyokütle genişleme aşamasını doku olgunlaşmasından ayırmayı mümkün kılar. CRISPRi, ölçek büyütme sürecinde yaşlanma ile ilişkili genleri baskılayarak, sığır hücrelerinin çoğalma süresini yaklaşık 100 günden 200 günden fazla bir süreye etkili bir şekilde iki katına çıkarabilir [1]. Yeterli biyokütle elde edildikten sonra, araştırmacılar farklılaşmayı sağlamak için normal gen ekspresyonunu geri yükleyebilirler. Bu yaklaşım, kültürde erken yaşlanma eğiliminde olan mezenkimal kök hücreler için özellikle faydalıdır [1].
"Bu iki sürecin hedeflenmiş genetik düzenlemesi, MSC genişleme verimliliğini optimize ederken, onların temel çok potansiyelliğini ve farklılaşma potansiyelini koruyabilir, nihayetinde ölçeklenebilir kültür et sistemlerini ilerletebilir." – İletişim Biyolojisi [1]
Aşağıdaki tablo, geri dönüşümlü ve kalıcı gen düzenleme yöntemleri arasındaki farkları vurgulamaktadır:
| Özellik | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| DNA Modifikasyonu | Kalıcı (Indels) | Geri dönüşümlü (Transkripsiyonel) |
| Mekanizma | Çift sarmal kırıkları | dCas9-efektör füzyonu |
| En İyi Kullanım Durumu | Temel genleri tanımlama | Metabolik/büyüme yollarını ayarlama |
| Diferansiyasyon Riski | Yüksek (Kalıcı fonksiyon kaybı) | Düşük (Fonksiyon geri kazanılabilir) |
Bu karşılaştırma, tersine çevrilebilir gen düzenleme yöntemlerinin, kültürlenmiş et üretimi için hücre hatları geliştirme konusundaki belirli zorluklara nasıl uyarlanabileceğini göstermektedir.
CRISPR Taramalarını Hücre Paneli ve Genotipleme Teknolojileri ile Birleştirme
CRISPR Taramalarını Multi-Omik Analiz ile Bağlama
Multi-omikleri ve otomatik genotiplemeyi CRISPR taramalarına entegre etmek, özellikle kültürlenmiş et hücre hattı geliştirmede faydalarını artırır.
CRISPR taramalarını RNA dizilimi gibi multi-omiklerle birleştirmek, araştırmacıların belirli gen silmelerinin hücresel yollar üzerindeki etkilerini haritalamalarına olanak tanır. Bu, özellikle hücrelerin çoğalma ve farklılaşmayı nasıl dengelediğini anlamanın kritik olduğu kültürlenmiş et için önemlidir.
Örneğin, sığır yağ dokusu kaynaklı mezenkimal kök hücrelerinde, 600 geni hedef alan bir havuzlanmış CRISPR knockout taraması, RNA-seq ile eşleştirildiğinde, TP53 ve PTEN genlerinin silinmesinin yaşlanmayı geciktirdiğini ortaya çıkardı.Bu hücreler, genç bir gen ekspresyon profili koruyarak, hücre döngüsü genlerinin yukarı regüle edilmesiyle, transdüksiyondan sonraki 50. günde ikiye katlanma oranlarında %50 artış sağladı [1].
CROP-seq gibi tek hücreli platformlar, bireysel hücrelerde hem sgRNA hem de transkriptomik değişiklikleri aynı anda tespit ederek bunu daha da ileriye taşır [6]. Bu düzeydeki hassasiyet, kas farklılaşmasını veya protein sentezini artıran genetik modifikasyonları tanımlamak için paha biçilmezdir - kültürlenmiş etin istenen doku ve besin özelliklerine ulaşmak için kritik faktörler.
Başka bir umut verici yaklaşım, CRISPR bozulmalarının çeşitli bağışçılardan, anatomik bölgelerden ve türlerden gelen farklı hücre hatlarında test edildiği hücre paneli taramasını içerir. Örneğin, araştırmacılar MyoCRISPR-KOLib kütüphanesini yedi bağışçıdan alınan insan miyoblast hatlarında doğruladı.Split-toksin seçim sistemi kullanarak, miyoblast füzyonu için gerekli olan 250 geni tanımladılar. Bunlardan 41 genin iskelet kası morfolojisinde rol oynadığı tıbbi veritabanları aracılığıyla doğrulandı [6]. Bu çok hatlı doğrulama, genetik hedeflerin biyolojik varyasyonlar arasında sağlam kalmasını sağlar, bu da kültürlenmiş et üretiminin ölçeklendirilmesi için önemli bir husustur.
Bu bulgular, genetik taramaları ayrıntılı genotipleme ile birleştiren otomatik, ölçeklenebilir platformların endüstriyel uygulamalar için yolunu açıyor.
Entegre Platformlarda Otomasyon ve Ölçeklenebilirlik
Otomasyon, entegre CRISPR ve genotipleme platformları tarafından üretilen geniş veri setleri ve örneklerin işlenmesi için gereklidir. Virüssüz, yer spesifik sgRNA kütüphanelerinin teslimatını sağlayan RMCE sistemleri, büyük bir ilerlemedir. Bu platformlar, her hücrenin tek, tutarlı bir sgRNA kopyası almasını sağlayarak değişkenliği azaltır.RMCE, Çin hamsteri over (CHO) hücrelerinde minimal yanlılıkla yüksek kütüphane kapsama alanı göstermiştir [5].
"Tarafsız bir yüksek verimli genetik tarama platformu, yeni nesil CHO fabrikalarının geliştirilmesi için esastır." - Çin Hamsteri Over Araştırma Ekibi [5]
Ölçeklenebilirlik, Cellular Fitness (CelFi) testi gibi doğrulama araçlarıyla daha da artırılır. Bu test, zaman içinde indel profillerini izlemek için hedeflenmiş derin dizileme kullanır ve çerçeve içi ve çerçeve dışı mutasyonların oranını takip eder. Bu mutasyonları büyüme avantajları veya dezavantajları ile ilişkilendirerek, araştırmacılar kültive edilmiş et hücre hatlarındaki genetik hedefleri verimli bir şekilde doğrulayabilir [2].
| Teknoloji | Entegrasyon Yöntemi | Kültive Edilmiş Et için Birincil Fayda |
|---|---|---|
| RNA-seq / Multi-omik | CRISPR bulgularını transkriptomik profillerle ilişkilendirme | Genlerin büyüme ve farklılaşmayı nasıl düzenlediğini anlama[1][6] |
| Split-Toksin Sistemleri | Hücre füzyonunu yaşanabilirlik seçimiyle ilişkilendirme | Füzyon yeteneğine sahip veya kusurlu hücrelerin nicel seçimi[6] |
| RMCE Platformları | gRNA kütüphanelerinin yer spesifik entegrasyonu | Tutarlı gen kopya sayıları ile yüksek verimli, virüssüz tarama[5] |
| CROP-seq | Tek hücreli CRISPR + RNA-seq | sgRNA ve transkriptomik değişikliklerin eşzamanlı tespiti [6] |
| CelFi Assay | İndellerin hedeflenmiş derin dizilimi | Genetik hedeflerin hızlı doğrulaması, alel frekansı değişimlerini izleyerek yapılır [2] |
Bu gelişmiş platformlar, genetik hedeflerin belirlenmesinden hücre uygunluğu üzerindeki etkilerinin doğrulanmasına kadar süreci kolaylaştırır. Bu verimlilik, büyük ölçekli kültive edilmiş et üretimi için yeterince sağlam hücre hatlarının geliştirilmesini destekler.
Hücre Hattı Büyümesi ve Çoğalmasını İyileştirmek İçin CRISPR Taramaları Kullanma
CRISPR tarama yöntemleri, hücre hattı performansını artırmak için güçlü bir araç haline gelmiştir ve kültive edilmiş et üretimi için doğrudan faydalar sunar.
CRISPR Tabanlı Hücre Hattı İyileştirmeleri Örnekleri
CRISPR taramaları, kültive edilmiş et araştırmalarında hücre hattı performansını başarıyla iyileştirmiştir. Örneğin, sığır yağ dokusu kaynaklı mezenkimal kök hücrelerde 600 geni hedefleyen bir havuzlanmış knockout taraması, büyümenin anahtar inhibitörleri olarak TP53 ve PTEN'i tanımladı. TP53'ün knockout edilmesi, 30 gün içinde hücre bolluğunu önemli ölçüde artırdı[1]. Ayrıca, düzenlenmiş sığır mezenkimal kök hücreleri ortalama olarak %12 daha yüksek bir ikiye katlanma oranı gösterdi [1] .
Tümör baskılayıcı genleri hedef alarak, araştırmacılar hücrelerin çoğalma ömrünü yaklaşık 100 günden 200 günün üzerine çıkardı ve bu şekilde Hayflick sınırını etkili bir şekilde aştılar. Bu yaşlanma gecikmesi, endüstriyel olarak ilgili zaman dilimlerinde biyokütle genişlemesini mümkün kılar[1].
Başka bir örnekte, Nanjing Tarım Üniversitesi'nden Shijie Ding, Chunbao Li ve Guanghong Zhou liderliğindeki araştırmacılar, CRISPR/Cas9 kullanarak CDKN2A−/− domuz uydu hücre hatları geliştirdi. Bu mühendislik ürünü hücreler, özel 19 bileşenli serumsuz bir ortamda (A19) en az 18 pasaj boyunca stabil çoğalmayı sürdürdü. Ayrıca yenilebilir iskelelere, başarıyla ekilerek çiğneme ve yapışkanlık özellikleri geliştirilmiş et benzeri yapılar oluşturuldu[8]. Hücreler, serumsuz koşullarda birden fazla pasaj boyunca %90'ın üzerinde canlılıklarını korudu[8].
"CRISPR tabanlı CDKN2A knockout hücreleri, kas progenitörlerinin yenilenebilir bir kaynağını sağlar ve tekrarlanan hayvan biyopsilerine olan bağımlılığı azaltır."
Bu örnekler, CRISPR taramalarının büyüme oranlarını iyileştiren, hücresel yaşlanmayı geciktiren ve serumsuz kültürü mümkün kılan genetik modifikasyonları nasıl tanımlayabileceğini vurgulamaktadır - kültive edilmiş et üretimini ölçeklendirmek için üç temel unsur.
CRISPR-Optimizasyonlu Hücre Hatları için Ölçeklendirme Zorlukları
CRISPR-optimizasyonlu hücre hatları belirgin avantajlar gösterse de, bunları endüstriyel kullanım için ölçeklendirmek zorluklar sunar. Artan proliferasyon genellikle farklılaşma pahasına gelir.Örneğin, TP53 geninin devre dışı bırakılması, sığır mezenkimal kök hücrelerinde kas farklılaşma genlerinin ifadesinin azalmasıyla ilişkilendirilmiştir, bu da yenilebilir dokuya olgunlaşma yeteneklerini engelleyebilir[1]. Bunu ele almak için, genişlemeden sonra farklılaşmayı geri kazandırmak amacıyla medya takviyeleri eklemek veya belirli transkripsiyon faktörlerini aktive etmek gibi ek stratejilere ihtiyaç duyulabilir[1].
Bir diğer kritik sorun ise genetik kararlılığı korumaktır. Gen kopya sayılarındaki varyasyonlar (anöploidi) ve CRISPR düzenlemesi sırasında hedef dışı etkiler, tarama çalışmalarında tutarsız sonuçlara veya yanlış pozitiflere yol açabilir [2]. Cellular Fitness (CelFi) testi gibi araçlar, zaman içinde çerçeve dışı indel oranını izleyerek bu riskleri azaltmaya yardımcı olur ve gözlemlenen büyüme faydalarının doğrudan hedeflenen düzenlemelerle bağlantılı olmasını sağlar[2].
Ekonomik ve teknik engeller de devam etmektedir. Kültürlenmiş et endüstrisinde hücre kaynaklarının yaklaşık %25'ini oluşturan mezenkimal kök hücreler, büyüme faktörlerinin yüksek maliyeti, optimize edilmiş serumsuz ortamlar, ve büyük ölçekli biyoreaktörlerin (10.000–50.000 L kapasiteler) geliştirilmesi gibi zorluklarla karşı karşıyadır[1][9][11]. Ayrıca, hücrelerin 3D iskelelere ekildiğinde istenen dokunun sağlanması karmaşık bir görev olmaya devam etmektedir[11].
"Kültürlenmiş etin mevcut durumu, yüksek maliyetler, ölçeklenebilirlik sorunları ve daha fazla teknolojik ilerlemeye duyulan ihtiyaç gibi önemli zorluklarla karşı karşıyadır."
- İletişim Biyolojisi [1]
Bu zorlukların üstesinden gelmek, genetik optimizasyonu medya formülasyonu, biyoreaktör teknolojisi ve farklılaşma protokollerindeki ilerlemelerle birleştiren kapsamlı bir yaklaşım gerektirir. CRISPR taramaları kritik genetik içgörüler sağlarken, bu bulguları ölçeklenebilir çözümlere dönüştürmek, entegre sistemler ve titiz doğrulama süreçleri gerektirecektir. Bu çabalar, laboratuvardan ticari uygulanabilirliğe kültive edilmiş et üretimini taşımak için hayati öneme sahiptir.
Nasıl Cellbase CRISPR Araştırmalarını Destekliyor Kültive Edilmiş Et Üretiminde
CRISPR taraması potansiyelini zaten göstermiştir, ancak endüstriyel kullanım için ölçeklendirilmesi, özel araçlara ve kaynaklara erişim gerektirir. İşte burada
CRISPR Kaynaklarına Cellbase Üzerinden Erişim
Geniş spektrumlu ilaç tedarikçilerinin aksine,
Kasım 2025'te,
"Görüştüğümüz her kültive et şirketi, aynı tedarik sıkıntısı üzerinde zaman kaybediyordu. Kritik bileşenler için tedarikçi bulmak, gıda uygulamalarını anlamayan ilaç tedarikçileri arasında sayfalarca arama yapmak anlamına geliyordu."
- David Bell, Cultigen Group Kurucusu [15]
Bu kaynakları merkezileştirerek,
Yetiştirilmiş Et Geliştirmede İşbirliğini Etkinleştirme
Platform, Believer Meats ve Aleph Farms gibi büyük ölçekli ticari projelerin taleplerini karşılamak üzere tasarlanmıştır.. Bu girişimler, 50.000 litrelik biyoreaktörler ve optimize edilmiş üretim tedarik zincirleri, için altyapı gerektirir ve
Sonuç
Yüksek verimli CRISPR taraması, umut verici bir kavramdan kültürlenmiş et geliştirmede kritik bir araca dönüşmüştür. Bu teknolojinin hücre hatlarını optimize etme üzerindeki etkisi tartışılmaz. Örneğin, son dönemdeki atılımlar, genetik modifikasyonların sığır kök hücrelerinin çoğalma ömrünü 100 günden 200 güne çıkarabileceğini, yaşlanmış hücre popülasyonlarını %60'tan sadece %10'a düşürebileceğini ve tek bir ay içinde hücre bolluğunda 1.000 kat artış sağlayabileceğini göstermiştir [1]. Bu gelişmeler, deneysel araştırmalardan pratik endüstriyel uygulamalara net bir geçişi işaret etmektedir.
Kompakt platformlar ve hedeflenmiş kütüphaneler, alandaki en acil zorluklardan bazılarını ele almaktadır. Dijital mikroakışkan sistemler artık koşul başına sadece 3.000 hücre ile tarama yapılmasına olanak tanımakta, ticari olarak bulunmayan sınırlı birincil hayvan hücreleri ile çalışmayı mümkün kılmaktadır.Bu arada, MyoCRISPR-KOLib gibi odaklanmış kütüphaneler, genomun yalnızca üçte birini kapsarken ilgili transkriptlerin %90'ını etkili bir şekilde hedef alır [3][6]. Bu düzeyde hassasiyet ve verimlilik, kaynak kısıtlamalarının üstesinden gelmek ve üretimi ölçeklendirmek.
"Bu bulgular, sığır kök hücre özelliklerini optimize etmek için CRISPR taramasının faydasını göstermekte ve gelecekte daha ölçeklenebilir kültive edilmiş et üretimine giden bir yol sunmaktadır." [1]
Bu ilerlemelere rağmen, başarı doğru altyapıya erişime bağlıdır. Araştırmacıların türlere özgü gRNA kütüphanelerine, gıda uygulamaları için tasarlanmış büyüme ortamlarına, uyumlu biyoreaktörlere ve farmasötik kullanım yerine kültive edilmiş et üretimine yönelik analitik araçlara ihtiyacı vardır.Bu ihtiyaçları karşılamak için,
Bir sonraki dalga kültive edilmiş et hücre hatlarını mühendislik yapmak için çalışan ekipler için araçlar ve teknolojiler hazır. Şimdi zorluk, CRISPR taramasının tam potansiyelini gerçekleştirmek için hızlı ve etkili bir şekilde uygulanmasında yatmaktadır.
SSS
Bir tarama için CRISPR knockout, CRISPRi ve CRISPRa arasında nasıl seçim yaparsınız?
Bu sistemler arasındaki seçim, belirli biyolojik sorunuza ve ulaşmayı hedeflediğiniz sonuca bağlıdır:
- CRISPR knockout: Bu yöntem, gen fonksiyonunu tamamen bozar ve gen kaybı veya inaktivasyonunun etkilerini incelemek için idealdir.
- CRISPRi: DNA'yı kesmeden gen ekspresyonunu baskılayarak, bu yaklaşım, temel genleri araştırmak veya geri dönüşümlü baskılama gerektiğinde iyi bir seçenektir.
- CRISPRa: Eğer gen ekspresyonunu artırmanız gerekiyorsa, bu sistem tercih edilen seçenektir. Özellikle aşırı ekspresyonun etkilerini incelemek için faydalıdır, örneğin hücre çoğalmasını veya farklılaşmasını teşvik etmek.
Karar verirken, hücresel modelinizi, hedeflediğiniz genleri ve deneyinizin genel hedeflerini göz önünde bulundurun.
Kası veya yağ farklılaşmasını zarar vermeden nasıl artırabilirsiniz?
Kültür et üretiminde, kas veya yağ hücrelerinin çoğalmasını artırırken farklılaşma yeteneklerini korumak önemli bir zorluktur.Bir umut verici yaklaşım, genlerin büyümeyi artırmak veya hücre ömrünü uzatmak için hassas bir şekilde manipüle edilmesine olanak tanıyan CRISPR tabanlı gen düzenleme, içerir. Örneğin, myostatin (MSTN) hedeflenmesi hücre büyümesini teşvik edebilirken, CDKN2A düzenlenmesi hücrelerin yaşlanmayı atlatmasına yardımcı olur.
Bununla birlikte, çoğalma ve farklılaşma arasında bir denge sağlamak kritik öneme sahiptir. P53 (TP53), gibi belirli hedeflerin yanlış yönetimi farklılaşmayı bozabilir ve potansiyel olarak doku kalitesini tehlikeye atabilir. Bu karmaşıklıkları aşmak için yüksek verimli CRISPR taraması çok önemlidir. Bu teknik, en etkili gen düzenleyicilerini belirleyerek, kültür et üretiminde ölçeklenebilir ve sağlıklı doku gelişiminin yolunu açar.
CRISPR ekran vuruşlarını bir hücre hattında ölçeklendirmeden önce doğrulamak için ne gereklidir?
Kültürlü et üretimi için CRISPR ekran vuruşlarını doğrulamak metodik bir yaklaşım gerektirir. İlk olarak, gözlemlenen etkilerin tekrarlanabilir olduğundan emin olmak için gen fonksiyonu, gen nakavtları gibi bağımsız deneylerle doğrulanmalıdır. Daha sonra, bu genlerin biyolojik önemini değerlendirmek için hücre çoğalması, canlılık ve uzun ömür gibi faktörler üzerindeki etkilerini incelemek önemlidir.
Güvenlik değerlendirmeleri, süreci tehlikeye atabilecek hedef dışı etkileri veya genetik kararsızlığı dışlamak için eşit derecede önemlidir. Endüstriyel ortamları taklit eden koşullar altında fonksiyonel doğrulama, örneğin biyoreaktörler, başka bir kritik adımdır. Bu, genetik düzenlemelerin büyük ölçekli üretim ortamlarında beklendiği gibi performans gösterdiğinden emin olmayı sağlar. Her aşamada kapsamlı testler, ölçeklendirme düşünülmeden önce vazgeçilmezdir.











