Hydrogel-Gerüste sind entscheidend für die Produktion von kultiviertem Fleisch, da sie einen 3D-Rahmen für das Zellwachstum und die Gewebebildung bieten. Ihre Sicherheit und Wirksamkeit erfordern jedoch gründliche Biokompatibilitätstests. Zu den wichtigsten Herausforderungen gehören:
- Chemische Rückstände: Toxische Nebenprodukte aus Polymerisation und Vernetzungsmitteln können Zellen schädigen.
- Oberflächenchemie-Probleme: Synthetische Hydrogele weisen oft nicht die Bioaktivität auf, die für die Zelladhäsion erforderlich ist.
- Immunreaktionen und Abbau: Einige Gerüste provozieren Entzündungen oder bauen sich auf eine Weise ab, die das umliegende Gewebe schädigt.
Lösungen für diese Herausforderungen umfassen Reinigungsmethoden, Oberflächenmodifikationen (e.g. , RGD-Peptide) und hybride Gerüstdesigns, die synthetische und natürliche Materialien kombinieren. Testmethoden wie Zytotoxizitätsassays, Bewertungen der mechanischen Eigenschaften und Abbaustudien stellen sicher, dass Gerüste sowohl Sicherheits- als auch Funktionsanforderungen erfüllen. Plattformen wie
3D-Hydrogel-Gerüste für die Kultur von artikulären Chondrozyten & Knorpelgeneration l Protokollvorschau
Häufige Herausforderungen bei der Biokompatibilitätsprüfung
Die Biokompatibilitätsprüfung von Hydrogel-Gerüsten bringt einige Herausforderungen mit sich, insbesondere wenn es darum geht, die Zellviabilität und die effektive Gewebebildung sicherzustellen. Die Hauptverursacher? Chemische Rückstände, Oberflächeneigenschaften und Abbauverhalten. Diese Faktoren können die Zelladhäsion, das Wachstum und das Überleben erheblich beeinflussen. Werfen wir einen genaueren Blick auf diese Herausforderungen.
Resttoxizität von chemischen Komponenten
Sicherheit hat bei der Produktion von kultiviertem Fleisch oberste Priorität, und die Kontrolle von restlichen toxischen Chemikalien ist ein kritischer Teil des Prozesses. Nicht umgesetzte Monomere aus der radikalischen Polymerisation, wie HEMA und Acrylate, können das Überleben der Zellen ernsthaft gefährden. Acrylate sind besonders problematisch, da sie toxischer sind als Methacrylate, die ihrerseits schädlicher sind als Acrylamide [2].
Vernetzer wie Ethylendimethacrylat können toxische Rückstände hinterlassen, die sich nicht leicht abbauen [2]. Zusätzlich stellen Polymerisationstrigger - wie Initiatoren und radikalinduzierende Mittel - Risiken dar, wenn sie nicht vollständig umgesetzt oder ordnungsgemäß entfernt werden [2].
Um dies anzugehen, wird oft die Reinigung durch Dialyse eingesetzt, um diese verbleibenden Monomere und Vernetzungsmittel zu entfernen, bevor Gerüste mit Zellen besiedelt werden [2]. Das Erreichen hoher Umwandlungsraten während der Polymerisation ist ebenfalls entscheidend, insbesondere für In-situ-Gelationsmethoden, bei denen das Risiko des Auslaugens erhöht ist [2]. Ein systematischer Bewertungsansatz, im Einklang mit ISO 10993 Standards, kann helfen, die Quelle der Zytotoxizität zu identifizieren - sei es Sterilisationsrückstände, pH-Änderungen oder Mediumabsorption - anstatt sich auf Annahmen aus der bestehenden Literatur zu verlassen [4].
Oberflächenchemieprobleme, die die Zelladhäsion beeinflussen
Synthetische Hydrogele wie PEG, PHEMA und PVA sind von Natur aus hydrophil und bioinert.Während dies das Risiko einer Fremdkörperreaktion verringert, erschwert es auch das Anhaften von Serumproteinen [2]. Christopher D. Spicer von der University of York hebt das Problem hervor:
"Die hohe Hydrophilie von PHEMA macht es bioinert und widersteht der Zell- und Proteinadhäsion" [2].
Im Gegensatz zur nativen extrazellulären Matrix, die die notwendigen chemischen Signale für die Zellbindung liefert, fehlen diesen synthetischen Materialien solche Hinweise. Infolgedessen neigen Zellen dazu, eine abgerundete Form anzunehmen, was auf eine schlechte Interaktion mit dem Gerüstmaterial hinweist [2]. Darüber hinaus bedeutet das Fehlen einer ausreichenden Oberflächenladung, dass diese Gerüste nicht in der Lage sind, elektrostatische Wechselwirkungen zu nutzen, die für die anfängliche Zelladhäsion wesentlich sind [2].
Interessanterweise haben Forscher herausgefunden, dass das Hinzufügen von mikrometergroßen topografischen Mustern zu PHEMA-Oberflächen menschlichen mesenchymalen Stammzellen helfen kann, sich auszubreiten und zu verlängern, wodurch einige der Einschränkungen des Materials überwunden werden [2]. Spicer bemerkt:
"Im Gegensatz zur abgerundeten Morphologie, die auf flachen Oberflächen angenommen wird und auf schlechte Interaktionen mit dem darunterliegenden Material hinweist, konnten sich die Zellen als Reaktion auf die bereitgestellten topografischen Hinweise ausbreiten und verlängern" [2].
Immunantwort und Abbauprodukte
Gerüste können Immunantworten hervorrufen, die zu einer faserigen Verkapselung führen, die das Material isoliert [2]. Dieses Problem ist besonders ausgeprägt bei chemischen Vernetzungsmitteln wie Glutaraldehyd, die dafür bekannt sind, starke Entzündungsreaktionen auszulösen.Zum Beispiel entwickelten in subkutanen Implantationsstudien bei Ratten glutaraldehyd-vernetzte Schwämme dicke Gewebeschichten (0,85 ± 0,34 mm), während mit mikrobieller Transglutaminase vernetzte Schwämme viel dünnere Schichten zeigten (0,19 ± 0,16 mm) [5].
Das Timing und die Nebenprodukte des Abbaus von Gerüsten fügen eine weitere Komplexitätsebene hinzu. Polyesterbasierte Gerüste, wie PLA oder PGA, setzen saure Monomere frei, wenn sie sich zersetzen, was zu einem lokalen pH-Anstieg und Gewebeschäden führen kann. Wie Spicer erklärt:
"Der Aufbau von Glykol- und Milchsäuremonomeren nach dem Abbau von poly(ester)-basierten Gerüsten hat gezeigt, dass er zu einem lokalen pH-Anstieg und daraus resultierenden Gewebeschäden führt" [2].
Gerüste, die zu schnell abgebaut werden, verlieren ihre strukturelle Integrität, die für die Zelladhäsion und Gewebeentwicklung entscheidend ist [5]. Zum Beispiel behielten EDC-vernetzte Gelatineschwämme nach einem Monat Implantation nur 2,7% ± 1,7% ihres Volumens, während glutaraldehyd-vernetzte Schwämme 69,1% ± 4,3% beibehielten [5]. Sogar Materialien, die als bioinert gelten, wie PEG, können manchmal Immunreaktionen hervorrufen, wie die Entwicklung von Anti-PEG-Antikörpern bei bestimmten Patienten, was ihre Verwendung in vivo erschwert [2].
Standardprüfmethoden für Biokompatibilität
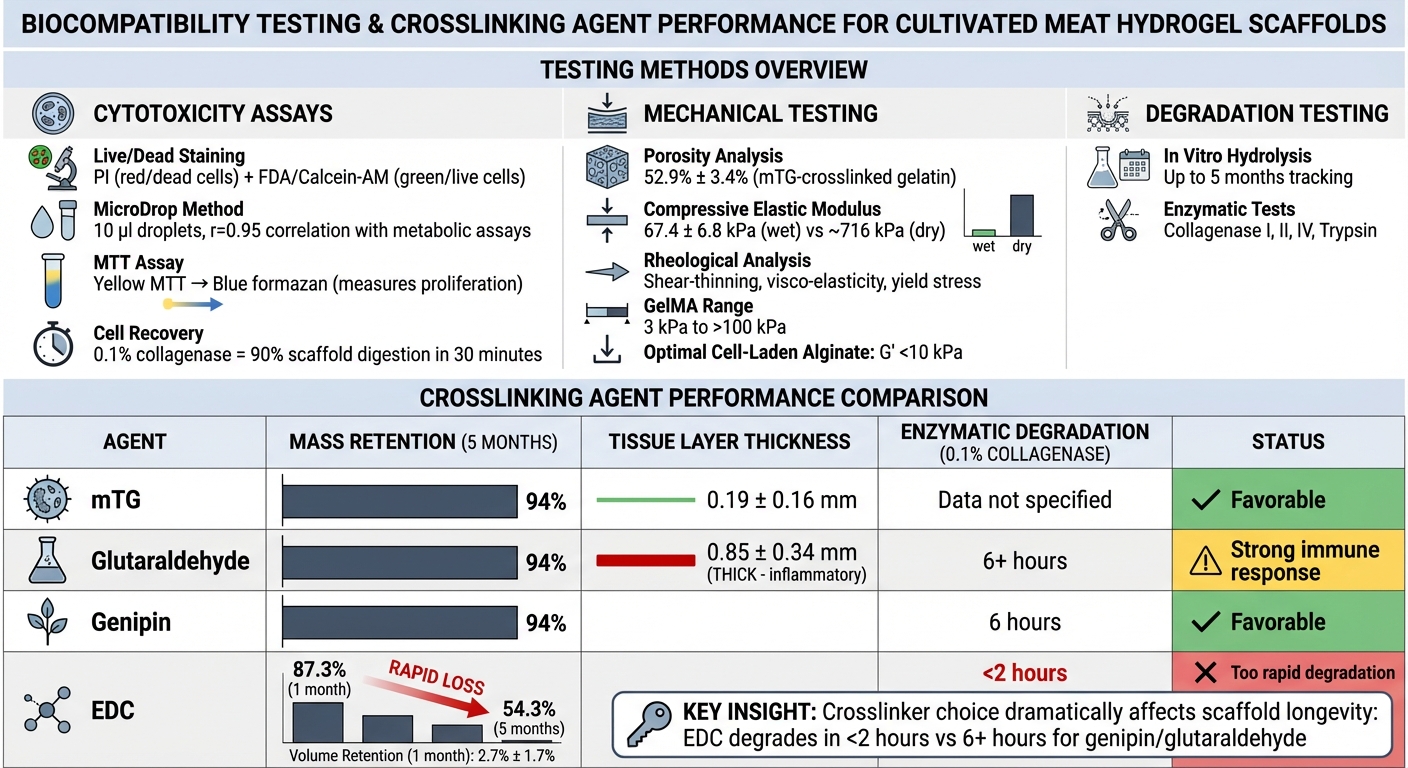
Biokompatibilitätstestmethoden und Vergleich der Vernetzungsleistung für Hydrogelgerüste
Die Bewertung der Biokompatibilität umfasst eine Kombination aus Zytotoxizitätstests, mechanischen Eigenschaftsbewertungen und Abbaustudien. Diese rigorosen Methoden stellen sicher, dass Hydrogelgerüste nicht nur das Zellwachstum unterstützen, sondern auch die Sicherheits- und Texturstandards erfüllen, die für kultiviertes Fleisch erforderlich sind.
Zytotoxizität und Zellviabilitäts-Assays
Live/Dead-Färbung ist eine bewährte Methode zur Bewertung der Zellviabilität innerhalb dreidimensionaler Hydrogelgerüste. Dieser Prozess verwendet Propidiumiodid (PI), um tote Zellkerne rot zu färben, während Fluoresceindiacetat (FDA) oder Calcein-AM lebende Zellen grün hervorhebt. Dieser Dual-Färbungsansatz bietet eine klare Visualisierung der Zelldistribution innerhalb der Gerüstmatrix [6] [7]. Die MicroDrop-Methode, , die 10 µl Tropfen verwendet, hat eine starke Korrelation (r=0,95) mit metabolischen Assays gezeigt und ist somit eine zuverlässige Alternative [6].
Der MTT-Assay ist ein weiteres wertvolles Werkzeug zur Messung von Zellproliferation und metabolischer Aktivität.Es funktioniert, indem es hellgelbes MTT in dunkelblaues Formazan umwandelt, was eine effektive Möglichkeit bietet, das langfristige Zellwachstum über verschiedene Gerüsttypen hinweg zu vergleichen [7] . Jedoch kann der CCK8-Assay in viskosen Hydrogelen aufgrund unspezifischer Wechselwirkungen falsch-positive Ergebnisse liefern [6] . Um Zellen aus 3D-Gerüsten zu gewinnen, ist eine 0,1%ige Kollagenase-Lösung hochwirksam, da sie bis zu 90% des Gerüsts innerhalb von 30 Minuten verdaut und gleichzeitig Zellschäden minimiert [7].
Sobald die Zellviabilität bestätigt ist, besteht der nächste Schritt darin, die strukturellen und mechanischen Eigenschaften des Gerüsts zu bewerten.
Testen der mechanischen und strukturellen Eigenschaften
Mechanische Tests stellen sicher, dass Gerüste das Zellwachstum physisch unterstützen können, während sie eine ordnungsgemäße Nährstoffdiffusion ermöglichen. Porositätsanalyse ist entscheidend für die Aufrechterhaltung der Zellviabilität, da sie einen ausreichenden Austausch von Nährstoffen, Sauerstoff und Abfall in 3D-Kulturen gewährleistet [1] . Der kompressive Elastizitätsmodul im hydratisierten Zustand wird verwendet, um zu messen, wie genau das Gerüst die Textur von herkömmlichem Fleisch nachahmt. Zum Beispiel zeigten mit mikrobieller Transglutaminase (mTG) vernetzte Gelatineschwämme eine Porosität von 52,9% ± 3,4% und einen kompressiven Elastizitätsmodul von 67,4 ± 6,8 kPa im nassen Zustand [7] .
Für biogedruckte Gerüste spielt die rheologische Analyse eine Schlüsselrolle bei der Bewertung von Eigenschaften wie Scherverdünnungsverhalten, viskoelastischen Eigenschaften und Fließgrenze. Diese Parameter gewährleisten einen reibungslosen Extrusionsprozess während des Druckens und die strukturelle Integrität nach der Ablagerung [3] . GelMA-Hydrogele können beispielsweise so angepasst werden, dass sie eine Steifigkeit von etwa 3 kPa bis über 100 kPa erreichen, je nach den Anforderungen des Gewebes. Für zellbeladenes Alginat sind jedoch optimale Druckbarkeit und Zellviabilität typischerweise mit Speicherelastizitätsmodul (G')-Werten unter 10 kPa verbunden [3]. Wie Rency Geevarghese und Kollegen festgestellt haben:
"Druckbarkeit, Stabilität und Biokompatibilität sind nicht unabhängig und müssen sorgfältig angepasst werden, um sich gegenseitig auszugleichen" [3].
Über die unmittelbaren mechanischen Eigenschaften hinaus ist die langfristige Stabilität des Gerüsts ebenso wichtig.
Langzeit-Biodegradation und Stabilitätstests
Um sicherzustellen, dass Gerüste während der Zellentwicklung funktional bleiben, bewertet der Abbau-Test ihre Langlebigkeit. In-vitro-Hydrolysetests verfolgen den Massenverlust über längere Zeiträume - bis zu fünf Monaten in wässrigen Umgebungen - um die Stabilität zu bewerten [7] . Enzymatische Abbauversuche, mit Proteasen wie Kollagenase I, II, IV und Trypsin bieten zusätzliche Einblicke in das Verhalten von Gerüsten unter biologischen Bedingungen [7].
Der Typ des Vernetzungsmittels beeinflusst die Abbauraten erheblich. Beispielsweise behielten in Hydrolysetests mit mTG, Glutaraldehyd oder Genipin vernetzte Gelatineschwämme nach fünf Monaten 94% ihrer ursprünglichen Masse. Im Gegensatz dazu zeigten EDC-vernetzte Schwämme einen starken Rückgang der Stabilität, wobei die Masse nach einem Monat auf 87,3% sank und nach fünf Monaten nur noch 54,3% verblieb [7]. Während des enzymatischen Abbaus mit 0.1% Kollagenase, EDC-Schwämme lösten sich fast vollständig innerhalb von zwei Stunden auf, während genipin-vernetzte Schwämme sechs Stunden benötigten, um vollständig abzubauen [7].
Die mechanische Stabilität nimmt auch nach Wasseraufnahme erheblich ab. Zum Beispiel sinkt der Druckelastizitätsmodul von trockenen mTG-Schwämmen, der etwa 716 kPa beträgt, auf etwa 67 kPa, wenn sie nass sind [7]. Das Testen der mechanischen Eigenschaften im hydratisierten Zustand ist daher für eine genaue Bewertung unerlässlich.
sbb-itb-ffee270
Lösungen zur Verbesserung der Biokompatibilität von Hydrogelen
Wenn die Biokompatibilität von Hydrogelen nicht ausreicht, gibt es bewährte Methoden zur Verbesserung der Gerüstleistung. Diese Ansätze adressieren Herausforderungen wie chemische Toxizität, schwache Zelladhäsion und schnelle Degradation, um sicherzustellen, dass Gerüste in der Produktion von kultiviertem Fleisch besser funktionieren.Der Schwerpunkt liegt auf der Verbesserung der Zellanhaftung, der Anpassung der mechanischen Eigenschaften und der Steuerung der Abbauraten.
Oberflächenmodifikationen für bessere Zellanhaftung
Synthetische Hydrogele, wie PEG, PVA und PHEMA, sind von Natur aus bioinert, was die Zellanhaftung ohne zusätzliche Signale erschwert. Eine gängige Lösung ist die Einbindung von RGD-Peptiden, die die benötigten Bindungsstellen für Zellen bereitstellen. Gelatine und ihr Derivat, GelMA, enthalten diese Peptide von Natur aus, was sie in kultivierten Fleischgerüsten weit verbreitet macht. Forscher an der Schlesischen Technischen Universität hoben dies hervor:
"Gelatine wurde als vielversprechende Bioink-Komponente identifiziert, die das Zellwachstum unterstützt, aufgrund der Anwesenheit von Zellanhaftungspeptid-Motiven wie RGD (Arginin–Glycin–Asparaginsäure)" [3].
Andere Techniken umfassen die mikrometergroße topografische Musterung, die physische Hinweise einführt, um die Zellverbreitung auf ansonsten flachen Oberflächen zu fördern [2]. Die Anpassung der Oberflächenladung kann auch elektrostatische Wechselwirkungen mit Zellen verbessern [2]. Zusätzlich können synthetische Polymere mit bioaktiven Motiven, wie RGDS oder IKVAV, modifiziert werden, um die Zellbindung effektiver zu unterstützen [2].
Materialzusammensetzung und Hybridgerüst-Designs
Hybridgerüste kombinieren die Stärke synthetischer Polymere mit der Bioaktivität natürlicher Materialien und adressieren die Einschränkungen von Einzelkomponenten-Designs.Synthetische Polymere wie PEG und PCL bieten vorhersehbare Chemie und starke mechanische Eigenschaften, während natürliche Polymere wie Kollagen, Chitosan und Alginat Umgebungen bieten, die die extrazelluläre Matrix (ECM) nachahmen und die Zelladhäsion und -wachstum fördern [9][2].
Zum Beispiel zeigte eine 2023 in Scientific Reports veröffentlichte Studie ein hybrides Gerüst, das durch die Kombination eines PEG-Gelatine-Hydrogels mit einem PCL-Netz hergestellt wurde. Dieses Design unterstützte die Bildung einer dichten epithelialen Zellschicht unter Verwendung von MDCK-Zellen über neun Tage, wobei das PCL-Netz mechanische Unterstützung für die 100 µm dicke Hydrogelmembran bot [8] . Ähnlich zeigte eine Studie aus dem Jahr 2012, dass die Immobilisierung von Gelatine auf hydrophoben PCL-Filmoberflächen die Anhaftung und das Wachstum von Humanen Nabelschnurvenen-Endothelzellen (HUVEC) verbesserte, wobei bessere Ergebnisse mit höheren Mengen an immobilisierter Gelatine verbunden waren [10].
Die Zugabe von Carboxymethylcellulose (CMC) zu alginatbasierten Tinten kann sowohl die mechanischen Eigenschaften als auch die Quellkapazität durch elektrostatische Wechselwirkungen verbessern [3]. Mechanisch robuste Hydrogele enthalten typischerweise 0,1–10% Polymer nach Gewicht, aber Gele mit Poren kleiner als 10 µm können die Zellbewegung und -infiltration behindern [2].
Diese Strategien verbessern nicht nur die Zellkompatibilität, sondern ermöglichen auch eine präzise Kontrolle über die Langlebigkeit des Gerüsts, die eng mit den Abbauraten verbunden ist.
Kontrollierte Degradation durch Anpassung der Vernetzungsdichte
Die Vernetzungsdichte spielt eine Schlüsselrolle sowohl bei den Abbauraten als auch bei der mechanischen Steifigkeit. Duale Vernetzungsmethoden, wie die Kombination von ionischer Vernetzung (e.g. , unter Verwendung von CaCl₂ für Alginat) mit Photovernetzung (e.g. , UV-Härtung für GelMA), bieten eine bessere Kontrolle über die Stabilität des Gerüsts. Die ionischen Bindungen bieten vorübergehende Unterstützung, während kovalente Bindungen die langfristige Struktur gewährleisten [3].
GelMA-Hydrogele können eine breite Palette von Speichermodulen (G') erreichen - von etwa 3 kPa bis über 100 kPa - abhängig von der Polymerkonzentration und der UV-Belichtung [3]. Für zellbeladenes Alginat sind G'-Werte unter 10 kPa oft optimal, um die Druckbarkeit und Zellviabilität zu erhalten [3]. Einschließlich abbaubarer Verbindungen, wie Disulfidbrücken oder Polyestersequenzen, ermöglicht es Gerüsten, sich in resorbierbare Makromere zu zersetzen, die Zellen durch native ECM ersetzen können [2]. Allerdings erfordern polyesterbasierte Vernetzungen wie PLA oder PGA eine sorgfältige pH-Überwachung, da die Freisetzung von Glykol- oder Milchsäure zu Gewebeschäden durch Säure führen kann [2].
Die Verwendung von Lithiumphenyl-2,4,6-trimethylbenzoylphosphinat (LAP) als Photoinitiator für die UV-Härtung ist eine weitere Möglichkeit, die Zytokompatibilität im Vergleich zu älteren Methoden zu verbessern [3][8]. Die strikte Temperaturkontrolle bei 37°C und die Einhaltung präziser Mischprotokolle gewährleisten eine gleichmäßige Vernetzung und vorhersehbare Degradation [3].
Verwendung von Cellbase für Gerüstbeschaffung
Die Suche nach den richtigen biokompatiblen Hydrogel-Gerüsten für die Produktion von kultiviertem Fleisch kann schwierig sein, insbesondere wenn man sich auf allgemeine Laborausrüster verlässt, die möglicherweise nicht über die Expertise in lebensmitteltauglichen Materialien und regulatorischer Konformität verfügen.
Verifizierte Lieferanten für kultiviertes Fleisch
"Alginat ist ideal, weil es die Textur von Fleisch sehr gut nachahmt und bereits als Lebensmittelzutat zugelassen ist" [11].
Die auf
Optimierte Beschaffungsprozesse
Über verifizierte Standards hinaus vereinfacht
Fazit
Die Biokompatibilitätstests für Hydrogelgerüste in der kultivierten Fleischproduktion sind ein Balanceakt, der mehrere miteinander verbundene Faktoren umfasst.Das "Biokompatibilität-Druckbarkeit-Stabilität"-Trilemma verdeutlicht, wie die Verbesserung einer Eigenschaft manchmal eine andere beeinträchtigen kann. Zum Beispiel kann die Verwendung hoher Polymerkonzentrationen die strukturelle Stabilität verbessern, aber auch die Scherspannung während der Extrusion erhöhen, was den Zellen schaden könnte [3]. Ähnlich können Abbauprodukte von Materialien wie PLA die umliegenden Zellen negativ beeinflussen [2][1].
Testmethoden müssen diese komplexen Wechselwirkungen berücksichtigen, um sicherzustellen, dass Gerüste die strengen Standards der kultivierten Fleischproduktion erfüllen. Techniken wie Zytotoxizitätstests, Bewertungen der mechanischen Eigenschaften und Langzeitabbau-Studien tragen gemeinsam dazu bei, sicherzustellen, dass Gerüste die Zellviabilität während ihres gesamten Lebenszyklus aufrechterhalten.Wie Małgorzata Katarzyna Włodarczyk-Biegun erklärt:
"Druckbarkeit, Stabilität und Biokompatibilität sind nicht unabhängig und müssen sorgfältig angepasst werden, um sich gegenseitig auszugleichen" [3].
Innovative Ansätze wie die doppelte Vernetzung - die ionische und kovalente Methoden kombiniert - können ein Speichermodul von ~3 kPa bis über 100 kPa erreichen und gleichzeitig die Zellviabilität unterstützen [3]. Andere Fortschritte, wie Oberflächenmodifikationen mit bioaktiven Peptiden wie RGD und hybride Gerüste, die natürliche und synthetische Polymere mischen, verbessern die Biokompatibilität. Kontrollierter Abbau durch präzise Vernetzung verfeinert die Leistung des Gerüsts weiter. Dennoch bleiben Herausforderungen bestehen, wie die Chargenvariabilität natürlicher Polymere, die die Konsistenz in der Großproduktion beeinflussen kann [1]. Diese technischen Anpassungen sind entscheidend für die Beschaffung von Materialien, die den spezifischen Anforderungen der Produktion von kultiviertem Fleisch entsprechen. Letztendlich ist das Erreichen des richtigen Gleichgewichts von chemischen, mechanischen und biologischen Eigenschaften der Schlüssel zum Erfolg von Hydrogel-Gerüsten.
FAQs
Wie kann ich toxische Rückstände in einem Hydrogel-Gerüst identifizieren?
Um toxische Rückstände in einem Hydrogel-Gerüst zu erkennen, ist Biokompatibilitätstests entscheidend. Dieser Prozess konzentriert sich auf die Erkennung von zytotoxischen Reaktionen, die schädliche Auswirkungen auf Zellen anzeigen. Ein weit verbreiteter Ansatz sind Zytotoxizitätstests, wie direkte Zellprobenahme, die die Zellviabilität und das Verhalten bewertet.
Anzeichen, auf die man achten sollte, sind Zellmembranschäden, Apoptose (programmierter Zelltod) oder direkter Zelltod. Durch die Kombination dieser Methoden können Sie schädliche Rückstände gründlich erkennen und bewerten, die das Zellwachstum behindern könnten.
Welche Tests sagen die Zelladhäsion in 3D-Hydrogelen am besten voraus?
Zelladhäsionstests sind eine zuverlässige Methode, um zu bewerten, wie gut Zellen an 3D-Hydrogele haften. Diese Tests messen wichtige Aspekte wie Zellanhaftung und -wachstum auf Hydrogelgerüsten und bieten wichtige Informationen über die Kompatibilität des Materials mit biologischen Systemen.
Wie kann ich den Abbau des Gerüsts abstimmen, ohne die Zellen zu schädigen?
Um den Abbau des Gerüsts fein abzustimmen, ohne die Zellgesundheit zu beeinträchtigen, können Sie die chemische Zusammensetzung des Hydrogels anpassen. Zum Beispiel kann das Anpassen der Vernetzungsdichte oder das Einfügen von biologisch abbaubaren Verbindungen helfen, ein Gleichgewicht zwischen Stabilität und Abbau zu erreichen. Die Verwendung bestimmter Polymere, wie kollagenbasierte Hydrogele, bietet einen weiteren Ansatz, der eine kontrollierte Degradation ermöglicht, um das Zellwachstum und die Differenzierung zu fördern. Durchdachte Anpassungen stellen sicher, dass das Gerüst in einem Tempo abgebaut wird, das die zellulären Prozesse unterstützt und die Zellen lebensfähig hält.











