Die Überwachung der Zelldichte in Echtzeit ist entscheidend für die Verbesserung der Produktion von kultiviertem Fleisch. Traditionelle Methoden, wie Trypanblau-Assays, sind langsam, anfällig für Kontaminationen und übersehen oft schnelle Veränderungen im Zellwachstum. Die Echtzeitmessung liefert kontinuierliche Daten, ermöglicht präzise Nährstoffanpassungen, frühzeitige Erkennung von Problemen und eine gleichbleibende Produktqualität.
Verschiedene analytische Methoden zur Überwachung lebender Zellen umfassen:
- Biokapazitätssensoren: Messen lebensfähige Zellen durch Erkennung intakter Membranen. Abtastfrequenzsysteme reduzieren Fehler auf 5,5–11%.
- Optische Trübungssensoren: Verfolgen die gesamte Zelldichte durch Lichtstreuung, können jedoch nicht zwischen lebenden und toten Zellen unterscheiden.
- RF-Impedanzüberwachung: Ideal für Hochdichtesysteme, mit Fokus auf lebende Zellen in Mikrokugel- oder immobilisierten Aufbauten.
- Raman-Spektroskopie: Bietet detaillierte chemische Profilierung, identifiziert lebensfähige Zellen und Metaboliten.
- NIR-Spektroskopie: Verfolgt schnell mehrere Parameter, hat jedoch Schwierigkeiten mit überlappenden Signalen.
Jede Methode hat Stärken und Einschränkungen, was Kalibrierung und Validierung für die Genauigkeit unerlässlich macht. Plattformen wie
Incyte Arc: Echtzeit-Überwachung der lebensfähigen Zelldichte für eine intelligentere Bioprozesssteuerung
sbb-itb-ffee270
Technologien zur Echtzeitmessung der Zelldichte
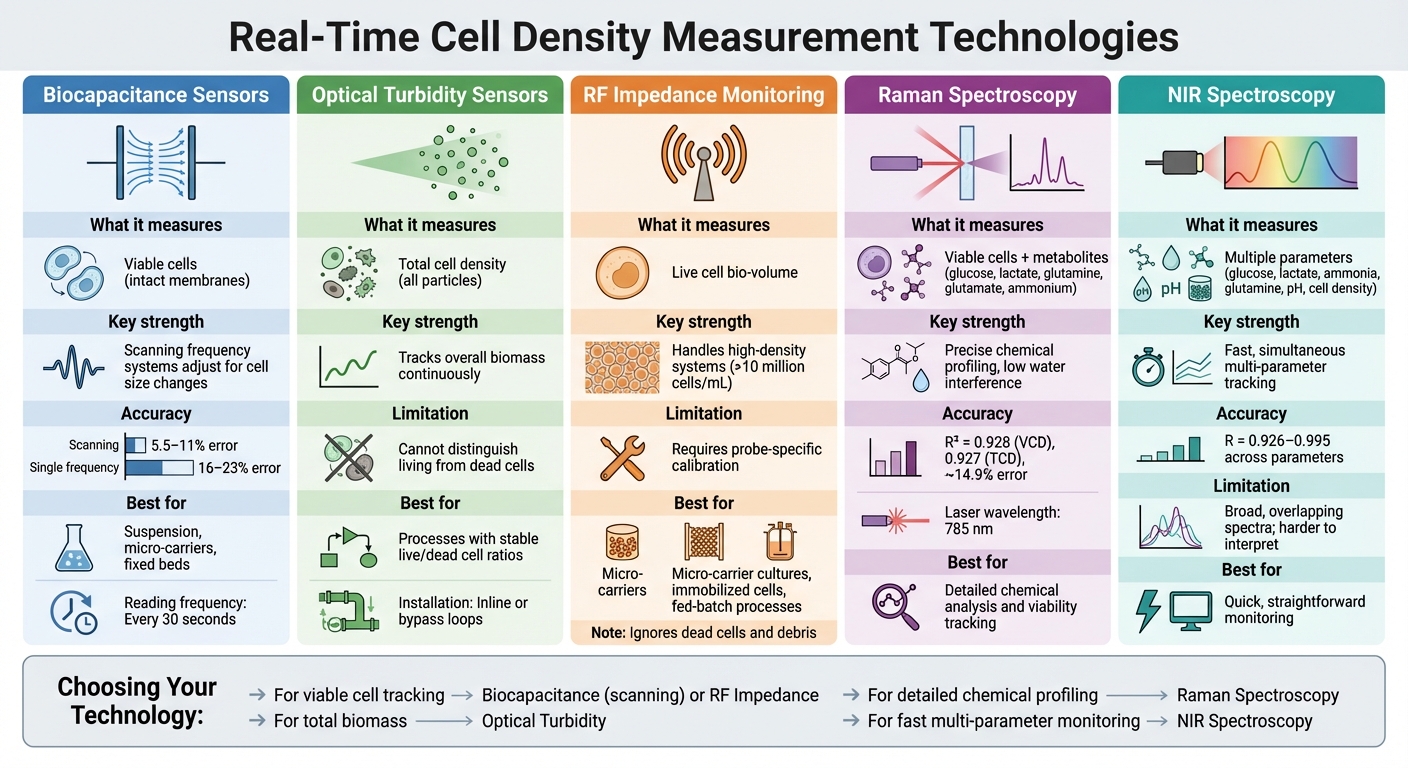
Vergleich von Technologien zur Echtzeitmessung der Zelldichte für kultiviertes Fleisch
Um die Nachfrage nach kontinuierlichem Prozessfeedback zu erfüllen, ermöglichen verschiedene Sensortechnologien für Bioreaktoren für kultiviertes Fleisch jetzt eine präzise Echtzeitmessung der Zelldichte. Jede Methode bietet einen einzigartigen Ansatz, der entweder auf lebensfähige Zellen oder die Gesamtbiomasse abzielt, je nach den spezifischen Anforderungen des Prozesses.
Biokapazitive Sensoren
Biokapazitive Sensoren arbeiten, indem sie ein elektrisches Feld auf eine Zellaufschlämmung anwenden. Lebende Zellen mit intakten Membranen wirken wie winzige Kondensatoren. Ihre Membranen verhindern, dass Ionen im Zytoplasma hindurchtreten, was zu einer Polarisierung führt und eine messbare Ladung erzeugt.Abgestorbene Zellen hingegen haben keine intakten Membranen und tragen nicht zum Signal bei[1].
Diese Technik basiert auf β-Dispersion, bei der sich Zellen bei Frequenzen unter 100 kHz vollständig polarisieren, was zu einer hohen Permittivität führt. Durch das Scannen eines Frequenzbereichs (50–20.000 kHz) und die Anwendung multivariater Analysen können diese Sensoren Änderungen in der Zellgröße korrigieren. Diese Anpassung reduziert Messfehler von 16–23% auf einen viel niedrigeren Bereich von 5,5–11%[1].
Um die Genauigkeit zu gewährleisten, muss die Sonde zuerst in sterilem Medium vor der Inokulation genullt werden, gefolgt von einer Kalibrierung mit der bekannten Zellkonzentration zu Beginn. Geräte wie das Aber FUTURA pico integrieren sich nahtlos in Bioreaktoren und liefern alle 30 Sekunden frische Messwerte.Diese Sensoren sind hochwirksam für Zellen in Suspension, an Mikrokörpern befestigt oder in festen Betten immobilisiert - Szenarien, in denen traditionelle Zählmethoden oft versagen[1][2].
Für die Messung der Gesamtbiomasse bieten optische Methoden eine weitere praktikable Option.
Optische Trübungssensoren
Optische Trübungssensoren bestimmen die Gesamtdichte der Zellen, indem sie das von allen Partikeln in der Kultur gestreute Licht messen, einschließlich lebender Zellen, toter Zellen und Ablagerungen. Während diese Sensoren nicht zwischen lebensfähiger und nicht lebensfähiger Biomasse unterscheiden können, sind sie besonders nützlich, wenn das Verhältnis von lebenden zu toten Zellen während des gesamten Prozesses stabil bleibt. Die Kalibrierung erfolgt durch Korrelation der Trübungswerte mit Offline-Zellzählungen in verschiedenen Stadien der Kultur. Diese Sensoren können inline oder in Bypass-Schleifen installiert werden und bieten eine kontinuierliche Überwachung, um den optimalen Erntezeitpunkt zu bestimmen.
Radiofrequenz-Impedanzüberwachung
Die Radiofrequenz (RF)-Impedanzüberwachung teilt einige Prinzipien mit Biokapazitätssensoren, indem sie sich auf die Erkennung von Zellen mit intakten Membranen konzentriert und tote Zellen sowie Ablagerungen ignoriert[1][2]. Diese Methode eignet sich besonders für Systeme mit immobilisierten Zellen oder Mikroträgerkulturen, , bei denen Offline-Probenahmen schwierig sein können. RF-Impedanz kann lebensfähige Zellkonzentrationen von über 10 Millionen Zellen/mL in Fed-Batch-Prozessen bewältigen, was sie zu einer e
| Technologie | Maßnahmen | Hauptstärke | Einschränkung |
|---|---|---|---|
| Biokapazität (Einzelfrequenz) | Lebensfähiges Zellvolumen | Einfache Implementierung | Empfindlich gegenüber Durchmesseränderungen (16–23% Fehler)[1] |
| Biokapazität (Scanning) | Lebensfähige Zellkonzentration | Passt sich Größenänderungen an (5.5–11% Fehler)[1] | Erfordert multivariate Analyse |
| Optische Trübung | Gesamte Zelldichte | Erkennt die gesamte Biomasse | Kann lebende nicht von toten Zellen unterscheiden[2] |
| RF-Impedanz | Lebende Zell-Bio-Volumen | Funktioniert gut mit Mikrokörpern und Festbetten | Erfordert eine sonden-spezifische Kalibrierung |
Spektroskopische Methoden für die Multi-Parameter-Analyse
Spektroskopische Methoden heben die Prozessüberwachung auf die nächste Stufe, indem sie über Einzelparameter-Messungen hinausgehen, wie sie von Kapazitäts- und Trübungssensoren bereitgestellt werden.Diese Techniken analysieren, wie Licht mit Molekülen in der Kultur interagiert und bieten Echtzeiteinblicke nicht nur in Zellzahlen, sondern auch in Nährstoffgehalte, Metabolitenkonzentrationen und andere wichtige Prozessvariablen. Durch die Erstellung detaillierter chemischer Profile ergänzen sie Kapazitäts- und Trübungssensoren und liefern reichhaltigere Daten für bessere Entscheidungsfindung.
Raman-Spektroskopie
Die Raman-Spektroskopie funktioniert, indem sie die unelastische Streuung von Licht misst. Wenn ein Laser (häufig bei 785 nm) auf eine Probe trifft, verschiebt sich das gestreute Licht in der Wellenlänge basierend auf den chemischen Bindungen der Moleküle, auf die es trifft. Das präzise chemische Profiling dieser Methode ermöglicht es, lebensfähige Zellen von toten zu unterscheiden und einzelne Metaboliten wie Glukose, Laktat, Glutamin, Glutamat und Ammonium zu identifizieren - alles ohne das System zu stören[3] [5].
Ein wesentlicher Vorteil von Raman ist seine geringe Empfindlichkeit gegenüber Wasser, einer häufigen Störung bei Infrarotmethoden. Dies macht es besonders geeignet für die nährstoffreichen Umgebungen, die in der Produktion von kultiviertem Fleisch zu finden sind[3][5]. Die Technologie kann mit faseroptischen Immersionssonden oder durch Messung durch Bioreaktor-Sichtfenster implementiert werden, um die Sterilität während des gesamten Prozesses zu gewährleisten[4][5].
Zwischen 2010 und 2011 demonstrierten Forscher bei Bristol-Myers Squibb das Potenzial der In-line-Raman-Spektroskopie in 500-L-Bioreaktoren. Mit einem Kaiser Optical Systems RamanRXN3-Instrument entwickelten sie Kalibriermodelle mit Bestimmtheitsmaßen (R²) von 0,928 für die lebensfähige Zelldichte (VCD) und 0,927 für die Gesamtdichte der Zellen (TCD). Der durchschnittliche Fehler lag bei etwa 14.9%, vergleichbar mit der 10% Fehlerquote der Referenzmethode selbst[3].
"Raman-Spektroskopie... scheint die vielversprechendste spektroskopische Methode für die Inline-Analyse komplexer Zellkultursysteme zu sein." - Nicholas R. Abu-Absi, Process Sciences, Bristol-Myers Squibb[3]
Um genaue Ergebnisse zu gewährleisten, sollte das System mit Offline-Daten zusammen mit PLS-Regression kalibriert werden. Die Anwendung von Erstableitung und SNV-Korrekturen kann helfen, Baseline-Verschiebungen und Fluoreszenzinterferenzen zu reduzieren[3][4]. Wenn neue Daten verfügbar werden, sollten Kalibriermodelle aktualisiert werden, um Variationen zwischen den Läufen zu berücksichtigen[3][4]. Für Anwendungen im Bereich kultiviertes Fleisch bieten Plattformen wie
Nahe-Infrarot (NIR) Spektroskopie
Während die Raman-Spektroskopie für detaillierte chemische Profilierung und die Unterscheidung zwischen lebensfähigen und toten Zellen geeignet ist, bietet die NIR-Spektroskopie eine schnelle und effiziente Mehrparameterverfolgung. Durch die Analyse von Obertönen und Kombinationsbändern erkennt NIR Analytenkonzentrationen mithilfe einer Durchflusszelle oder eines Eintauchsonde mit einer festen Pfadlänge (typischerweise 1,0 mm), was hilft, Wasserinterferenzen im Signal zu minimieren[6]. Diese Technik kann gleichzeitig Glukose, Laktat, Ammoniak, Glutamin, pH-Wert und Zelldichte messen[6].
NIR-Systeme erfassen hauptsächlich Zelldichtesignale durch Basiseffekte, die durch Lichtstreuung verursacht werden[6]. In Studien mit HEK293-Zellkulturen verfolgte NIR erfolgreich lebensfähige Zellpopulationen bei Dichten von 8,5–9,0 × 10⁶ Zellen/mL, mit Korrelationskoeffizienten im Bereich von 0,926 bis 0.995 über verschiedene Parameter[6].
Allerdings sind NIR-Spektren breit und überlappend, , was sie schwerer interpretierbar macht im Vergleich zu Raman. Während NIR in Geschwindigkeit und Einfachheit glänzt, kann es nicht mit Ramans Fähigkeit mithalten, zwischen lebensfähiger und gesamter Zelldichte basierend auf biochemischen Unterschieden zu unterscheiden[3]. Letztendlich hängt die Wahl zwischen diesen Methoden von Ihren spezifischen Bedürfnissen ab: NIR ist ideal für schnelle, unkomplizierte Überwachung, während Raman besser für detaillierte chemische Analysen und Lebensfähigkeitsverfolgung geeignet ist.
Validierung und Korrelation von Echtzeitdaten
Korrelation mit Offline-Analysedaten
Echtzeitsensoren erfordern eine präzise Kalibrierung mit Offline-Referenzmethoden, um zuverlässige Daten zu gewährleisten. Beispielsweise sind Einfrequenzmessungen effektiv zur Verfolgung des lebensfähigen Zellvolumens, dank ihrer Empfindlichkeit gegenüber Änderungen im Zelldurchmesser.
Frequenzscanning, das die Permittivität über einen breiten Frequenzbereich (typischerweise 50 bis 20.000 kHz) misst, bietet einen nuancierteren Ansatz. Diese Daten fließen in die Multivariate Datenanalyse (MVDA) ein, wodurch eine Unterscheidung zwischen Änderungen in Zellgröße und Zellzahl ermöglicht wird. Eine genaue Kalibrierung ist entscheidend für die Aufrechterhaltung der Produktionsqualität, insbesondere bei Echtzeitanpassungen des Prozesses. Ein bemerkenswertes Beispiel stammt aus dem Oktober 2019, als Forscher bei Sartorius Stedim Biotech eine Inline-Kapazitätssonde in 250 mL Bioreaktoren mit CHO-Zellen validierten. Sie entwickelten ein Orthogonales Partielles Kleinste-Quadrate (OPLS) Modell basierend auf Daten aus fünf Standard-Fed-Batch-Kultivierungen, wobei die Permittivität bei 25 verschiedenen Frequenzen gescannt wurde. Dieser Ansatz ermöglichte es dem Modell, lebensfähige Zellkonzentrationen (VCCs) von über 10 Millionen Zellen/mL vorherzusagen, wobei das Frequenzscanning die Fehler im Vergleich zu Einzelfrequenzdaten erheblich reduzierte [7].
"Das Modell lieferte eine Vorhersage der VCCs mit relativen Fehlern von 5,5 bis 11%, was eine gute Übereinstimmung mit dem Akzeptanzkriterium basierend auf der Genauigkeit der Offline-Referenzmethode (ungefähr 10% relativer Fehler) darstellt und im Vergleich zu Einzelfrequenzergebnissen (16 bis 23% relativer Fehler) stark verbessert ist." – Springer Nature [7]
Um die Genauigkeit weiter zu verfeinern, hilft die Anwendung eines Savitzky-Golay-Filters (zweiter Ordnung), das Signalrauschen vor dem Vergleich zu minimieren. Zusätzlich verbessert eine Einpunktkalibrierung in der Inokulationsphase die Sensorpräzision [7]. Diese Schritte legen gemeinsam den Grundstein für eine zuverlässige Validierung in verschiedenen Betriebsszenarien.
Validierungsprotokolle
Sobald die Kalibrierung abgeschlossen ist, stellt eine rigorose Validierung sicher, dass der Prozess zuverlässig bleibt. Eine effektive Methode ist die Leave-One-Batch-Out (LOB) Validierung. Dies beinhaltet die Erstellung mehrerer Modelle, indem systematisch eine Charge aus dem Trainingsdatensatz ausgeschlossen und als Testset verwendet wird, um die Vorhersageleistung zu bewerten.
Robustheitsprüfungen sind ein weiterer kritischer Schritt. In der Studie von 2019 führten Forscher absichtliche Prozessabweichungen ein, wie z.B. einen 30%igen Verdünnungsschritt und geänderte Fütterungsstrategien, um die Zuverlässigkeit des MVDA-Modells unter nicht standardmäßigen Bedingungen zu testen. Selbst mit diesen Variationen lieferte das Modell genaue Vorhersagen, mit relativen Fehlern zwischen 6,7% und 13,2%. Dieses Maß an Zuverlässigkeit ist besonders wichtig für die Produktion von kultiviertem Fleisch, wo Prozessvariabilität während der Hochskalierung häufig ist.
Schließlich sollten realistische Akzeptanzkriterien festgelegt werden, die mit der inhärenten 10%igen Fehlermarge von Offline-Methoden wie Trypanblau-Assays übereinstimmen. Die Verwendung standardisierter Eingaben für kultiviertes Fleisch kann weiter dazu beitragen, diese Baselines zu stabilisieren.Indem Sie einen relativen Fehlergrenzwert von 10 % für Echtzeitsensoren festlegen, stellen Sie sicher, dass die Validierung an einem praktischen Standard erfolgt, anstatt unerreichbare Präzisionsniveaus anzustreben [7].
Integration der Echtzeitüberwachung in die Prozesssteuerung
Entwicklung von Soft-Sensor-Modellen
Sobald die Kalibrierung festgelegt ist, besteht der nächste entscheidende Schritt darin, die Sensorausgaben in die Prozesssteuerung zu integrieren. Nach der Validierung von Echtzeitsensoren liegt der Fokus auf der Entwicklung von Soft-Sensor-Modellen. Diese Modelle verwandeln Rohsensordaten in umsetzbare Erkenntnisse, häufig unter Verwendung von Algorithmen wie Partial Least Squares (PLS) oder Orthogonal Partial Least Squares (OPLS). Diese Methoden helfen, komplexe Online-Signale, wie z.B. Multi-Frequenz-Kapazitätsscans, mit kritischen Prozesskennzahlen wie der lebensfähigen Zellkonzentration (VCC) zu verknüpfen.
Um diese Modelle zu erstellen, benötigen Sie gepaarte Online- und Offline-Daten.Vorverarbeitungsschritte - wie Mittelwertzentrierung und Skalierung - sind unerlässlich, bevor das Modell mit Standardkultivierungsdaten trainiert wird. Ein bemerkenswertes Beispiel stammt von Sartorius Stedim Cellca GmbH, wo Forscher eine Aber Instruments FUTURA pico Sonde mit CHO-Zellkulturen verwendeten. Ihre prädiktiven Modelle erreichten relative Fehler zwischen 5,5% und 11%, eine deutliche Verbesserung gegenüber Einfrequenzmessungen, die typischerweise Fehler im Bereich von 16% bis 23% zeigen [7].
Der Einsatz dieser Modelle ermöglicht automatisierte Prozessanpassungen. Zum Beispiel bieten in der Produktion von kultiviertem Fleisch unter Verwendung von Mikroträgern oder Festbetten, Hochfrequenzimpedanzsensoren einen einzigartigen Vorteil. Sie unterstützen die dynamische Nährstoffzufuhr und Abfallentfernung, basierend auf dem lebensfähigen Zellvolumen. Wie John P. Carvell und Jason E.Dowd hervorgehoben:
"RF-Impedanz wird verwendet, um die Konzentration lebender Zellen zu überwachen, die auf Mikrokörpern oder gepackten Betten in cGMP-Prozessen immobilisiert sind, bei denen traditionelle Offline-Methoden zur Zählung lebender Zellen ungenau oder unmöglich durchzuführen sind" [2].
Dieses Maß an Integration verbessert nicht nur die Prozesskontrolle, sondern bereitet auch den Weg für die Erfüllung regulatorischer Rahmenbedingungen, die als nächstes untersucht werden.
Ausrichtung an PAT-Rahmenwerken
In der Produktion von kultiviertem Fleisch stellt die Kombination von Echtzeitüberwachung mit Process Analytical Technology (PAT) und Quality-by-Design (QbD)-Prinzipien sowohl die Einhaltung von Vorschriften als auch die betriebliche Effizienz sicher. Der Prozess beginnt mit der Identifizierung kritischer Qualitätsmerkmale (CQAs) und kritischer Prozessparameter (CPPs). Dies erfordert eine funktionsübergreifende Zusammenarbeit zwischen F&E, Qualitätssicherung und Regulierungsbehörden [8]. Ein phasenweiser Ansatz funktioniert am besten: klare Ziele definieren, geeignete Werkzeuge auswählen, Fehlerartenanalysen durchführen, mit SCADA/MES-Systemen integrieren, Personal schulen und mit Validierung skalieren [8].
Zum Beispiel hat im Januar 2026 ein globales biopharmazeutisches Unternehmen diese PAT-integrierte Strategie erfolgreich bei einem Technologietransfer über Kontinente hinweg angewendet. Die Ergebnisse? Abweichungsraten bei kommerziellen Chargen unter 2 % und eine 30%ige Reduzierung der Chargenfreigabezeiten im Vergleich zu früheren Kampagnen [8].
Der Übergang zur kontinuierlichen Prozessverifizierung (CPV) verlagert den Fokus von retrospektiven Tests zu proaktiver, Echtzeitkontrolle. Biokapazitätssensoren überwachen beispielsweise die Dichte lebensfähiger Zellen und das Wachstumskinetik, während sie Nährstoffzufuhren steuern. Dieser Ansatz erfüllt nicht nur die CPV-Standards, sondern vertieft auch das Prozessverständnis [8]. Chemie- und Bioprozessingenieurin Akanksha Prasad fasste es gut zusammen:
"PAT ist nicht mehr nur ein nettes Extra. Es ist zur Grundlage geworden, um die nächste Generation von Medikamenten sicher, effizient und in großem Maßstab herzustellen." [8].
Dieses Prinzip gilt auch für die Produktion von kultiviertem Fleisch. Konsistentes Zellwachstum und Produktqualität erfordern einen rigorosen Ansatz zur Prozesskontrolle und Einhaltung von Vorschriften.
Für diejenigen im Bereich des kultivierten Fleisches können Plattformen wie
Praktische Überlegungen zur Implementierung
Die richtige Technologie auswählen
Die Auswahl des richtigen Überwachungssystems hängt von Ihren spezifischen Messzielen ab.Zum Beispiel werden Einfrequenz-Kapazitätssensoren oft mit dem Viable Cell Volume (VCV) anstelle der Viable Cell Concentration (VCC) in Verbindung gebracht. Dies liegt daran, dass ihr Signal sowohl die Zellanzahl als auch Veränderungen in der Zellgröße widerspiegelt, was manchmal zu überhöhten Messwerten führen kann - insbesondere wenn Zellen unter Stress stehen oder altern.
Andererseits messen Frequenz-Scanning-Systeme die Kapazität über einen Frequenzbereich (typischerweise 50 bis 20.000 kHz). Diese Systeme verlassen sich auf multivariate Modelle, um Veränderungen in der Zellgröße von der tatsächlichen Zelldichte zu trennen, was die Vorhersagefehler im Vergleich zu Einfrequenzsystemen erheblich reduziert.
Radiofrequenz-Impedanz bleibt aufgrund ihrer Erschwinglichkeit und ihrer Empfindlichkeit gegenüber lebensfähigen Zellen eine beliebte Wahl. Tote Zellen und Verunreinigungen polarisieren nicht, was bedeutet, dass sie das Signal nicht stören.Wenn Sie sich für ein System entscheiden, denken Sie daran, wie einfach es sich in sterile Bioreaktor-Umgebungen integrieren lässt und ob es mit Einweg- vs. wiederverwendbaren Bioreaktoren. arbeitet. Fortschrittliche Technologien wie Raman-Spektroskopie oder Frequenz-Scanning-Kapazität erfordern multivariate Modellierungsansätze (e.g. , OPLS oder PLS), um ihre komplexen Datensätze zu interpretieren [7].
Für Produzenten von kultiviertem Fleisch können Plattformen wie
Sobald Sie ein System ausgewählt haben, sind genaue Kalibrierung und effektive Fehlersuche entscheidend, um zuverlässige Messungen aufrechtzuerhalten.
Kalibrierung und Fehlersuche
Um genaue Messwerte sicherzustellen, beginnen Sie damit, die Kapazitätssonde im sterilen Medium vor der Inokulation auf null zu setzen.Dieser Schritt stellt sicher, dass nur wachstumsbezogene Änderungen erkannt werden. Führen Sie dann eine Einpunktkalibrierung durch, indem Sie den Online-Trajektorienversatz mit Ihrer bekannten Inokulationszellkonzentration abgleichen. Für zuverlässige Vorhersagen trainieren Sie multivariate Modelle mit Daten aus mindestens fünf Standardkultivierungen, um Variationen wie unterschiedliche Medienchargen zu berücksichtigen. Die Anwendung eines Savitzky-Golay-Filters (zweiter Polynomgrad) kann helfen, Signalrauschen zu reduzieren und Schwankungen zu glätten. Während Online-Systeme leistungsstark sind, bleiben tägliche Offline-Messungen unerlässlich. Wenn Offline-Ergebnisse über einen festgelegten Schwellenwert hinaus abweichen (e.g. , 0,05 Einheiten für den pH-Wert), kalibrieren Sie Ihr Online-System neu [7].
Signaldrift ist eine weitere Herausforderung, die oft durch Änderungen im Zelldurchmesser aufgrund von Nährstoffmangel, Stress oder Alterung verursacht wird. Multifrequenz-Scansysteme können dies durch den Einsatz multivariater Analysen zur Berücksichtigung dieser Variationen angehen.
Offline-Referenzmethoden, wie z.B. Trypanblau-Assays, haben typischerweise einen Messfehler von etwa 10%. Anstatt eine Abweichung von null zu erwarten, validieren Sie die Genauigkeit Ihres Online-Systems innerhalb dieser Marge. Darüber hinaus kann die Implementierung von Batch Evolution Models (BEM) helfen, "goldene Batch"-Trajektorien zu etablieren. Diese Modelle fungieren als automatisierte Alarme, die Prozessabweichungen in Echtzeit kennzeichnen [7].
Fazit
Echtzeit-Überwachung der Zelldichte hat sich zu einem kritischen Bestandteil der Produktion von kultiviertem Fleisch entwickelt. Die kontinuierliche Verfolgung der lebensfähigen Zellkonzentrationen bietet klare Vorteile: Reduzierung der Mediumkosten durch automatisierte Fütterung, schnelle Identifizierung von Prozessabweichungen und Minimierung von Kontaminationsrisiken. Wie ein Forschungsteam hervorhob, "VCC ist stark mit Produkttitern verbunden und wird auch als Prozessattribut betrachtet.Die Überwachung des VCC ermöglicht Prozessoptimierung und -kontrolle, die zu höheren Titern und effizienten Prozessen führen" [1].
Die heutige Technologielandschaft bietet mehrere zuverlässige Lösungen. Unter ihnen zeichnen sich Frequenz-Scanning-Systeme in Kombination mit multivariaten Modellen durch eine Genauigkeit aus, die mit Offline-Methoden vergleichbar ist.
Um diese Systeme effektiv zu implementieren, ist eine sorgfältige Planung unerlässlich. Der Erfolg hängt von einer robusten Kalibrierung durch mehrere Trainingsläufe und einer konsistenten Offline-Verifizierung ab.
Für Produzenten von kultiviertem Fleisch, die zelllinienspezifische Überwachungswerkzeuge,
Mit dem Wachstum der Betriebe steigt der Wert von Echtzeitdaten. Batch-Evolutionsmodelle ermöglichen es Ihnen, "goldene Batch"-Trajektorien zu definieren und Abweichungen automatisch zu identifizieren, bevor sie die Produktqualität beeinträchtigen können [1] . Dieser Wandel macht die Überwachung der Zelldichte zu einem strategischen Vorteil zur Verbesserung von Prozessen und zur Risikominderung.
FAQs
Welchen Sensor sollte ich für die messbare Zelldichte im Vergleich zur Gesamtbiomasse verwenden?
Kapazitätssensoren sind eine ausgezeichnete Option zur Messung der messbaren Zelldichte, da sie die durch polarisierte Zellmembranen erzeugte Kapazität erkennen. Dies macht sie direkt mit der Anwesenheit lebender Zellen verbunden, was eine effektive Echtzeitüberwachung ermöglicht.
Das gesagt, sind diese Sensoren nicht die beste Wahl zur Messung der Gesamtbiomasse. Da sie sich hauptsächlich auf lebende Zellen konzentrieren, berücksichtigen sie keine toten Zellen oder die Gesamtbiomasse. Für die Dichte lebensfähiger Zellen bleiben Kapazitätssensoren jedoch die bevorzugte Lösung.
Wie kalibriere und validiere ich eine Inline-Kapazitätssonde?
Um eine Inline-Kapazitätssonde zu kalibrieren, beginnen Sie mit bekannten Zellkonzentrationen, die aus Offline-Methoden wie Zellzählung gewonnen wurden. Dies ermöglicht es Ihnen, Kapazitätsmessungen mit tatsächlichen Zellzahlen abzugleichen. Die Validierung umfasst das Testen der Sonde unter verschiedenen Zelldichten und Medienbedingungen, um ihre Genauigkeit und Konsistenz zu bestätigen. Es ist auch wichtig, regelmäßige Kalibrierungsprüfungen gegen Offline-Messungen durchzuführen, insbesondere bei der Hochskalierung der Produktion oder der Änderung von Medienbedingungen. Dies stellt sicher, dass die Sonde weiterhin zuverlässige Messungen der lebensfähigen Zelldichte liefert.
Wie verwandle ich Online-Signale in Softsensoren für die Fütterungskontrolle?
Um Online-Signale in Softsensoren für die Fütterungskontrolle in der Produktion von kultiviertem Fleisch zu verwandeln, können Sie sich auf Echtzeit-Sensordaten, wie Kapazitätsfrequenz-Scanning verlassen. Durch die Verarbeitung dieser Signale mittels multivariater Modelle können Sie kritische Parameter wie lebensfähige Zelldichte.
Kapazitätsbasierte Sensoren spielen hier eine Schlüsselrolle. Sie messen die Zellmembrankapazität, die direkt die Zellgesundheit widerspiegelt. Wenn diese Sensorausgaben in Steuerungsalgorithmen integriert werden, wird es möglich, Nährstoffanpassungen zu automatisieren und ideale Wachstumsbedingungen während des gesamten Prozesses aufrechtzuerhalten.











