Die Produktion von kultiviertem Fleisch wird durch langsames Zellwachstum und frühe Seneszenz in primären vs. immortalisierten Zelllinien begrenzt. CRISPR-Gen-Editing bietet gezielte Lösungen, um diese Herausforderungen zu überwinden.
Hier sind die fünf wichtigsten CRISPR-Ziele und ihre Rollen bei der Verbesserung der Zellproliferation, Differenzierung und Skalierbarkeit für kultiviertes Fleisch:
- Myostatin (MSTN): Fördert das Wachstum von Muskelzellen, indem natürliche Wachstumsgrenzen entfernt werden.
- P53 (TP53): Verlängert die Lebensdauer der Zellen und erhöht die Proliferationsraten, obwohl es die Differenzierung verringern kann.
- HIF1A: Hilft Zellen, in sauerstoffarmen Umgebungen zu überleben, was für dichte Bioreaktorkulturen unerlässlich ist.
- Myogene Regulatorfaktoren (MYOD1, MYOG): Treibt die Bildung und Ausrichtung von Muskelzellen voran.
- CDKN2A: Umgeht die Seneszenz und ermöglicht eine langfristige Zellproliferation.
Diese Ziele befassen sich mit wichtigen Themen wie replikativer Seneszenz, niedrigen Erträgen und Serumabhängigkeit. Allerdings sind das Gleichgewicht zwischen Proliferation und Differenzierung sowie die Gewährleistung der Sicherheit entscheidend für den Erfolg.
Schneller Vergleich:
| CRISPR-Ziel | Hauptvorteil | Herausforderungen |
|---|---|---|
| Myostatin (MSTN) | Fördert Muskelwachstum | Risiko von Off-Target-Effekten; Lebensfähigkeitsthemen |
| P53 (TP53) | Verlängert die Lebensdauer, steigert die Proliferation | Reduzierte Differenzierung; Sicherheitsbedenken |
| HIF1A | Unterstützt Überleben bei niedrigem Sauerstoff | Erfordert präzise Bearbeitung, um Störungen zu vermeiden |
| MYOD1, MYOG | Verbessert Muskelbildung | Balance zwischen Proliferation und Differenzierung |
| CDKN2A | Ermöglicht langfristige Proliferation | Off-Target-Risiken; erfordert serumfreie Medien |
Die CRISPR-Technologie verändert die Produktion von kultiviertem Fleisch, indem sie auf höhere Erträge und niedrigere Produktionskosten abzielt und gleichzeitig ethische Bedenken anspricht.
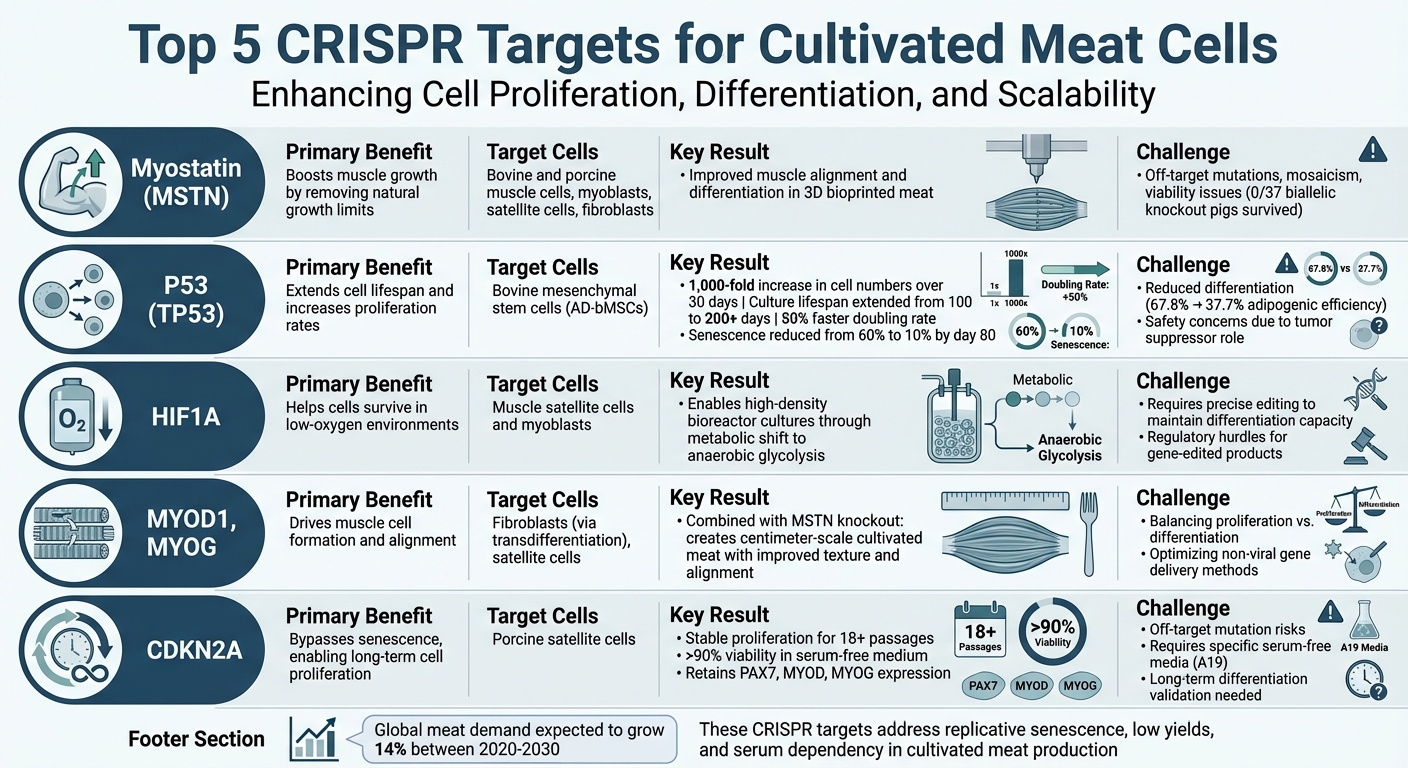
Top 5 CRISPR-Ziele für kultiviertes Fleisch: Vergleich von Vorteilen und Herausforderungen
1. Myostatin-Gen (MSTN)
Das Entfernen der natürlichen Bremse für das Muskelwachstum ist möglich, indem das MSTN-Gen ausgeschaltet wird. Dieser Prozess fördert die erhöhte Proliferation und Differenzierung von Muskelzellen sowohl durch Hyperplasie als auch durch Hypertrophie [5] [6].
Hauptvorteil
Im März 2025 machten Forscher der Seoul National University bedeutende Fortschritte, indem sie MSTN-Knockout-Rinderzellen mit digitalem Lichtverarbeitungs-3D-Bioprinting kombinierten. Dieser Ansatz verbesserte die Muskelausrichtung und Differenzierung, was zu kultiviertem Fleisch mit Eigenschaften führte, die traditionellem Steak ähneln [5] .
Im Mai 2022 nutzten Wissenschaftler der Northwest A&F University in China ein optimiertes CRISPR/Cas9-Liefersystem (100 ng/μL Cas9-mRNA und 200 ng/μL sgRNAs), um homozygote MSTN-Knockout-Schafe zu erzeugen. Von 16 geborenen Lämmern wurden vier als homozygote Knockouts bestätigt. Diese Lämmer zeigten signifikant höhere Körpergewichte an 30, 60 und 90 Tagen im Vergleich zu ihren nicht bearbeiteten Gegenstücken, während sie gleichzeitig Fleischqualitätsparameter wie pH-Wert, intramuskuläres Fett und Rohproteingehalt beibehielten [6] .
Zelltyp-Anwendbarkeit
Die Bearbeitung des MSTN-Gens verbessert das myogene Potenzial verschiedener Zelltypen, einschließlich primärer Myoblasten, Satellitenzellen, Fibroblasten (durch MYOD1-gesteuerte Transdifferenzierung) und mesenchymaler Stammzellen. Dies wird erreicht, indem die natürlichen Grenzen der Zellproliferation überwunden werden [5][1].
Potenzielle Herausforderungen
Trotz seiner Vorteile ist der MSTN-Knockout nicht ohne Komplikationen. Er wurde mit Lebensfähigkeitsproblemen bei lebenden Tieren und technischen Hürden wie Off-Target-Mutationen und Mosaizismus in Verbindung gebracht. Zum Beispiel berichtete eine Studie im Juni 2022, dass während MSTN-editierte Schweine ein erhöhtes Muskelwachstum zeigten, keines der 37 biallelischen Knockout-Schweine überlebte [7][8][6].
"MSTN-Knockout verbessert die Produktion von MYOD1-vermitteltem Steak-ähnlichem kultiviertem Fleisch." [5]
Als nächstes werden wir das P53-Tumorsuppressorgen und seine Bedeutung für die Sicherstellung einer nachhaltigen Zellproliferation untersuchen.
sbb-itb-ffee270
2. P53-Tumorsuppressorgen
Die Deaktivierung des TP53-Gens entfernt kritische Zellzyklus-Checkpoints, was die Zellproliferation erheblich beschleunigt.P53 spielt eine zentrale Rolle als Tumorsuppressor und initiiert den Zellzyklusarrest und die Seneszenz als Reaktion auf zellulären Stress. Ohne diesen Kontrollpunkt können Zellen Biomasse viel schneller akkumulieren und längere Kulturperioden aufrechterhalten [1].
Primärer Vorteil
Anfang 2025, Communications Biology veröffentlichte eine Studie, die die transformativen Effekte der TP53-Bearbeitung auf bovine mesenchymale Stammzellen hervorhob. Die Ergebnisse waren beeindruckend: eine 1.000-fache Zunahme der Zellzahlen über 30 Tage und eine verlängerte Kulturdauer von 100 auf über 200 Tage. Bearbeitete Zellen zeigten eine 50% schnellere Zellverdopplungsrate und bis zum 80. Tag sanken die Seneszenzwerte signifikant - von etwa 60% in unbearbeiteten Zellen auf nur 10% in den modifizierten.Darüber hinaus behielten diese Zellen ein "jüngeres" Genexpressionsprofil bei, gekennzeichnet durch verbesserte DNA-Replikation und anhaltende Proteinsynthese, was frühe Passagen von Zellen widerspiegelt [1].
Zelltyp-Anwendbarkeit
Aus Rinderfett gewonnene mesenchymale Stammzellen (AD‑bMSCs) sind besonders gut für TP53-Modifikationen geeignet. Diese Zellen stoßen natürlicherweise auf replikative Seneszenz, die ihr Expansionspotenzial begrenzt. Da mesenchymale Stammzellen etwa 25 % der Zellquellen ausmachen, die in der Produktion von kultiviertem Fleisch verwendet werden, bietet die TP53-Bearbeitung eine praktische Lösung, die ihre Fähigkeit, multipotent zu bleiben, mit industrieller Skalierbarkeit in Einklang bringt [1].
Potenzielle Herausforderungen
Diese Vorgehensweise ist jedoch nicht ohne Herausforderungen. Ein wesentlicher Nachteil ist die verringerte Differenzierungskapazität.Der Communications Biology Studie berichtete von einem Rückgang der Effizienz der adipogenen Differenzierung, von 67,8 % in nicht-editierten Zellen auf 37,7 % in TP53-Knockout-Klonen. Die Transkriptomanalyse zeigte eine Zunahme der Aktivität von Zellzyklusgenen, jedoch eine Abnahme der Gene, die mit Muskel-Differenzierung und -Adhäsion in Verbindung stehen. Da TP53 ein entscheidender Tumorsuppressor ist und seine Inaktivierung ein Kennzeichen von Krebs darstellt, wirft diese Strategie Sicherheits- und Regulierungsbedenken auf. Obwohl diese Zellen für den Verzehr und nicht für medizinische Zwecke bestimmt sind, erfordern solche Probleme eine sorgfältige Betrachtung [1].
"Unter allen Kandidaten zeigte der TP53-Knockout den ausgeprägtesten Effekt, mit einer über 1.000-fachen Zunahme der Häufigkeit bis Tag 30."
- Communications Biology [1]
Als nächstes wollen wir ein weiteres wichtiges CRISPR-Ziel untersuchen.
3.Hypoxie-induzierbarer Faktor 1-Alpha (HIF1A)
HIF1A spielt eine entscheidende Rolle dabei, kultivierten Fleischzellen zu helfen, sich an sauerstoffarme Umgebungen anzupassen, die häufig in Bioreaktoren mit integrierten Sensoren. anzutreffen sind. Dieser Regulator wird besonders wichtig, wenn die Sauerstoffdurchdringung begrenzt ist. Durch die Verwendung von CRISPR zur Stabilisierung von HIF1A können Zellen die Energieproduktion aufrechterhalten und lebensfähig bleiben, selbst bei reduziertem Sauerstoffgehalt.
Hauptvorteil
Die Bearbeitung von HIF1A reprogrammiert den Zellstoffwechsel und verlagert ihn von der sauerstoffabhängigen Atmung zur anaeroben Glykolyse. Diese Verschiebung stellt sicher, dass Zellen auch unter hypoxischen Bedingungen weiterhin Energie produzieren. Das Ergebnis? Die Fähigkeit, Zellen in höheren Dichten zu kultivieren, ohne das Risiko einer Sauerstoffverarmung. Dies ist ein Wendepunkt für die Skalierung der Produktion von kultiviertem Fleisch, insbesondere bei der Erstellung dickerer Gewebekonstrukte.
Zelltyp-Anwendbarkeit
Muskel-Satellitenzellen und Myoblasten profitieren am meisten von HIF1A-Änderungen. Diese sind die Hauptakteure bei der Entwicklung von Muskelfasern, und ihr Überleben in dicht gepackten Bioreaktoren ist entscheidend für hohe Erträge. Stabilisiertes HIF1A ermöglicht es diesen Zellen, Stoffwechselwege effektiv zu wechseln, wodurch sie auch während langer Kulturperioden lebensfähig bleiben.
Potenzielle Herausforderungen
Eine große Herausforderung besteht darin, sicherzustellen, dass bearbeitete Zellen ihre Fähigkeit zur Differenzierung in funktionelle Muskelfasern nach mehreren Passagen beibehalten. Dies erfordert technisches Feintuning, um einen Verlust der Differenzierungskapazität zu vermeiden. Über das Labor hinaus erschweren regulatorische Hürden und die öffentliche Wahrnehmung die Situation. Genbearbeitete Fleischprodukte müssen umfangreiche Sicherheitsbewertungen für den menschlichen Verzehr und die Umweltverträglichkeit bestehen, bevor sie auf den Markt kommen können.In der Zwischenzeit variiert die Akzeptanz solcher Produkte durch die Verbraucher stark in verschiedenen Regionen [3]. Diese Herausforderungen unterstreichen die Notwendigkeit, die Genbearbeitungstechniken zu perfektionieren, bevor man sich auf neue Ziele ausweitet. Als nächstes werden wir Gene untersuchen, die die myogene Differenzierung weiter verbessern.
4. Myogene Regulatorfaktoren (MRFs: MYOD1, MYOG)
MYOD1 spielt eine entscheidende Rolle bei der Verpflichtung von Zellen zur myogenen Linie, während MYOG die Fusion von Myoblasten zu reifen Myotuben erleichtert. Interessanterweise kann die Überexpression von MYOD1 Fibroblasten in myogene Zellen umprogrammieren und so die natürlichen Seneszenzgrenzen umgehen, die bei primären Satellitenzellen zu beobachten sind [5].
Hauptvorteil
Wenn die Überexpression von MYOD1 mit dem MSTN-Knockout in bovinen Fibroblasten kombiniert und mit DLP 3D-Bioprinting auf 100‑µm rillenmusterartigen Hydrogelen, integriert wird, sind die Ergebnisse beeindruckend.Dieser Ansatz verbessert die Muskelanordnung und -differenzierung und ermöglicht die Schaffung von kultivierten Fleischstrukturen im Zentimetermaßstab. Eine im März 2025 im Journal of Animal Science and Biotechnology veröffentlichte Studie stellte diese Methode vor, bei der nicht-virale Lieferung von MYOD1 zusammen mit CRISPR-vermitteltem MSTN-Knockout zur Manipulation von bovinen Fibroblasten eingesetzt wurde [5]. Durch die Eliminierung hemmender Signale auf die Muskeldifferenzierung lenkt diese Strategie die Zellen zu einer stärkeren myogenen Identität, was zu kultiviertem Fleisch mit besserer Textur führt. Dieser duale Ansatz unterstreicht die Bedeutung einer präzisen Balance zwischen Proliferations- und Differenzierungswegen.
Zelltyp-Anwendbarkeit
Fibroblasten sind ein e
Potenzielle Herausforderungen
Eines der Hauptprobleme besteht darin, das richtige Gleichgewicht zwischen Zellproliferation und Differenzierung zu finden. Zum Beispiel können genetische Modifikationen, die darauf abzielen, die Zellvermehrung zu steigern - wie TP53-Knockout - unbeabsichtigt wichtige Muskeldifferenzierungsfaktoren unterdrücken und möglicherweise die Fähigkeit der Zellen behindern, sich zu funktionalem Muskelgewebe zu entwickeln [1]. Zusätzlich erfordern nicht-virale Methoden wie das Piggybac-Transposon-System, die aus Gründen der Lebensmittelsicherheit bevorzugt werden, eine sorgfältige Optimierung, um eine effiziente Genübertragung sicherzustellen. Externe Faktoren, wie 3D-gedruckte Mikrorillen, bleiben entscheidend für das Erreichen einer korrekten Ausrichtung der Muskelfasern [5] .
5. Zellzyklusregulatoren (e.g. , CDKN2A)
CDKN2A spielt eine Schlüsselrolle bei der Auslösung von Seneszenz und stoppt effektiv die Zellteilung. Durch den Einsatz von CRISPR/Cas9 zur Ausschaltung von CDKN2A können Forscher die Hayflick-Grenze umgehen. Dies ermöglicht es Muskelstammzellen, weit über ihre übliche Lebensdauer hinaus weiter zu teilen, während sie dennoch ihre Fähigkeit zur Differenzierung in funktionelles Muskelgewebe beibehalten. Dieser Durchbruch bewältigt eine der größten Herausforderungen in der Produktion von kultiviertem Fleisch: die Herstellung der massiven Mengen an lebensfähigen, funktionalen Zellen, die für die industrielle Fertigung erforderlich sind.
Primärer Vorteil
Die direkte Ansprache von CDKN2A löst das Problem der begrenzten Zellproliferation in der Produktion von kultiviertem Fleisch.
Die Bearbeitung von CDKN2A verbessert die Skalierbarkeit und senkt die Kosten. Zum Beispiel veröffentlichte im Juni 2025 ein Forschungsteam der Nanjing Agricultural University, unter der Leitung von Shijie Ding, Chunbao Li und Guanghong Zhou ihre Ergebnisse in Food Materials Research. Sie entwickelten erfolgreich CRISPR-editierte porcine Satellitenzelllinien mit einem CDKN2A-Knockout. Diese Zellen zeigten eine stabile Proliferation über mehr als 18 Passagen in A19 serumfreiem Medium, mit Lebensfähigkeitsraten von über 90%. Wichtig ist, dass die Zellen die Expression von wichtigen myogenen Regulatoren (PAX7, MYOD und MYOG) beibehielten und sich zu reifen, MyHC-positiven Myotuben differenzierten.Wenn auf pflanzlichen 3D-Gerüsten ausgesät, bildeten diese bearbeiteten Zellen fleischähnliche Konstrukte mit verbesserter Kaubarkeit und Gummigkeit [2].
"Die auf CRISPR basierenden CDKN2A Knockout-Zellen bieten eine erneuerbare Quelle von Muskelvorläuferzellen, wodurch die Abhängigkeit von wiederholten Tierbiopsien verringert wird." – Food Materials Research [2]
Zelltyp-Anwendbarkeit
Schweine-Satellitenzellen, die für die Muskelregeneration entscheidend sind, reagieren besonders gut auf die CDKN2A-Bearbeitung. Dieser Ansatz bietet auch Potenzial für andere Nutztierarten. Ein wesentlicher Vorteil von CDKN2A-bearbeiteten Zellen ist ihre Kompatibilität mit serumfreien Medienformulierungen. Dies eliminiert die Notwendigkeit für teures und ethisch umstrittenes fötales Kälberserum, reduziert die Variabilität zwischen Chargen und minimiert Kontaminationsrisiken [2].
Potenzielle Herausforderungen
Während die Nanjing-Studie bedeutende Vorteile hervorhob, gibt es Herausforderungen bei der breiteren Anwendung von CRISPR in kultiviertem Fleisch. Off-Target-Mutationen bleiben ein Anliegen und müssen sorgfältig überwacht werden. Darüber hinaus müssen die regulatorischen Sicherheitsstandards für genetisch veränderte Lebensmittelprodukte streng eingehalten werden. Forscher müssen auch eine langfristige Differenzierung sicherstellen, um zu garantieren, dass das Endprodukt natürlichem Muskelgewebe nahekommt. Dies macht die Verfeinerung der Protokolle und die gründliche Validierung von 3D-Gerüsten unerlässlich [2].
Diese Ergebnisse, zusammen mit anderen CRISPR-Zielen, sind in der folgenden Vergleichstabelle zusammengefasst.
Vergleichstabelle
Tabelle: Die folgende Tabelle fasst die fünf CRISPR-Ziele zusammen, die die Zellproliferation, Differenzierung und metabolische Anpassung für eine skalierbare Produktion von kultiviertem Fleisch verbessern.
| CRISPR-Ziel | Hauptvorteil | Zielzelltypen | Herausforderungen |
|---|---|---|---|
| Myostatin (MSTN) | Fördert Muskelwachstum | Rinder- und Schweinemuskelzellen | Erfordert detailliertes genomisches Verständnis; Risiko unbeabsichtigter phänotypischer Veränderungen, wenn nicht sorgfältig verwaltet [4] |
| P53 (TP53) | Erhöht die Proliferation dramatisch; verzögert die replikative Alterung (über 1.000-fache Zunahme der Zellmenge bis Tag 30) [1] | Rinder-Mesenchymale Stammzellen (bMSCs) | Reduzierte Differenzierungskapazität; adipogene Differenzierung sinkt von 67,8% auf 37.7%; Herunterregulierung von muskelbezogenen Genen [1] |
| HIF1A | Verbessert die metabolische Anpassung | Rinder- und Schweinezellen | Erfordert sorgfältige Bearbeitung, um Stoffwechselstörungen zu vermeiden [4] |
| MRFs (MYOD1, MYOG) | Wichtig für die Bildung und Regeneration von Muskelfasern | Schweine-Satellitenzellen (Muskelstammzellen) [2] | Schwierig, hohe Expressionsniveaus während der schnellen Expansion für industrielle Skalierung aufrechtzuerhalten [2] |
| CDKN2A | Unterstützt stabile Proliferation über 18+ Passagen mit >90% Lebensfähigkeit; umgeht Alterung [2] | Schweine-Satellitenzellen (Muskelstammzellen) [2] | Benötigt spezifische serumfreie Medien (e.g. , A19) um Stammzellenfähigkeit und Differenzierung über eine langfristige Kultur zu bewahren [2] |
Die Auswahl der richtigen Ziele erfordert ein Gleichgewicht zwischen Zellproliferation und der Fähigkeit zur effektiven Differenzierung. Dies unterstreicht die Bedeutung der Feinabstimmung dieser Prozesse in der Zelltechnik für kultiviertes Fleisch.
Fazit
Die CRISPR-Technologie birgt enormes Potenzial zur Bewältigung kritischer Herausforderungen in der Produktion von kultiviertem Fleisch, einschließlich begrenzter Zellproliferation, Seneszenz und hoher Produktionskosten. Zum Beispiel wurde gezeigt, dass TP53-Knockout die Zellmenge innerhalb von nur 30 Tagen um über 1.000-fach erhöht [1]. Ähnlich ermöglichen CDKN2A-Edits den Zellen, stabil über 15–18 Passagen mit mehr als 90% Lebensfähigkeit in serumfreien Bedingungen zu proliferieren [2]. Dies reduziert die Abhängigkeit von teurem tierischem Serum und minimiert die Notwendigkeit wiederholter Tierbiopsien.
Jedoch bleibt es eine wesentliche Herausforderung, das richtige Gleichgewicht zwischen schneller Zellproliferation und der Fähigkeit zur Differenzierung in Muskelgewebe zu erreichen. Während der TP53-Knockout die Zellzahlen erheblich steigert, kann er die Differenzierung behindern. Daher ist es entscheidend, die Rolle von Regulatoren wie MYOD1 und MYOG aufrechtzuerhalten, um reifes Muskelgewebe zu erzeugen, das für kultiviertes Fleisch geeignet ist.
Für Forschungsteams, die diese genetischen Strategien anwenden möchten, bietet
Mit einer erwarteten globalen Fleischnachfrage, die zwischen 2020 und 2030 um 14 % steigen wird [1] , ebnen diese CRISPR-Ziele den Weg für skalierbare und kosteneffiziente Lösungen in der Produktion von kultiviertem Fleisch.
FAQs
Welches CRISPR-Ziel fördert das Wachstum am meisten, ohne die Differenzierung zu beeinträchtigen?
Das beste CRISPR-Ziel zur Förderung des Wachstums bei gleichzeitiger Aufrechterhaltung der Differenzierung ist das serumfreie, gentechnisch veränderte Satellitenzellensystem. Diese Methode unterstützt ein konsistentes Zellwachstum und eine effektive Differenzierung und ist daher eine starke Wahl für die großflächige Produktion von kultiviertem Fleisch.
Wie können TP53- oder CDKN2A-Bearbeitungen für kultiviertes Fleisch sicher gemacht werden?
Um sicherzustellen, dass TP53- oder CDKN2A-Bearbeitungen für kultiviertes Fleisch sicher sind, werden mehrere wichtige Schritte unternommen. Dazu gehören gründliche Tests der genetischen Stabilität, die Einrichtung von strukturierten Zellbankensystemen, und der Einsatz fortschrittlicher Werkzeuge wie Next-Generation-Sequencing, um Mutationen zu erkennen. Darüber hinaus sorgt die Einhaltung strenger regulatorischer Richtlinien sowohl für Sicherheit als auch für Konsistenz im gesamten Produktionsprozess.
Welche Bearbeitungen helfen Zellen, in sauerstoffarmen, hochdichten Bioreaktoren zu gedeihen?
Die Entwicklung von serumfreien Medien, die mit der richtigen Mischung aus Nährstoffen, Wachstumsfaktoren, Lipiden, nicht-essentiellen Aminosäuren und Antioxidantien abgestimmt sind, spielt eine Schlüsselrolle bei der Förderung der Zellproliferation und -differenzierung. Diese Anpassungen unterstützen nicht nur eine bessere Zellviabilität, sondern verbessern auch die Funktionalität, insbesondere unter herausfordernden Bedingungen wie sauerstoffarmen und hochdichten Umgebungen.











