क्लीनरूम सत्यापन यह सुनिश्चित करता है कि उत्पादन वातावरण सख्त संदूषण मानकों को पूरा करता है, जो कि संवर्धित मांस उत्पादन के लिए महत्वपूर्ण है। यह एक महत्वपूर्ण कदम है जब संवर्धित मांस प्रक्रियाओं का विस्तार. उचित सत्यापन संदूषण जोखिमों, को रोकता है, उत्पाद की गुणवत्ता की रक्षा करता है, और ISO 14644 और GMP जैसे नियमों का पालन करता है। इस प्रक्रिया में चार प्रमुख चरण शामिल हैं:
- डिज़ाइन योग्यता (DQ): पुष्टि करता है कि क्लीनरूम का डिज़ाइन संचालन और नियामक आवश्यकताओं को पूरा करता है।
- स्थापना योग्यता (IQ): यह सत्यापित करता है कि घटक सही ढंग से स्थापित हैं और विनिर्देशों से मेल खाते हैं।
- संचालन योग्यता (OQ): यह सुनिश्चित करने के लिए निष्क्रिय स्थिति में प्रणालियों का परीक्षण करता है कि वे इच्छित रूप से कार्य करते हैं।
- प्रदर्शन योग्यता (PQ): वास्तविक उत्पादन के दौरान क्लीनरूम के प्रदर्शन का आकलन करता है।
पार्टिकल काउंट्स, HEPA फिल्टर इंटेग्रिटी चेक्स, और एयरफ्लो माप सहित परीक्षण प्रोटोकॉल अनुपालन बनाए रखने के लिए महत्वपूर्ण हैं। निरंतर निगरानी और आवधिक पुन: मान्यता समय के साथ क्लीनरूम प्रदर्शन को बनाए रखने में मदद करती है। इन चरणों का पालन करने से संदूषण के जोखिम को कम किया जाता है, जो उत्पाद की स्थिरता और नियामक अनुमोदन दोनों की सुरक्षा करता है।
URS से PQ तक क्लीनरूम वैलिडेशन
sbb-itb-ffee270
क्लीनरूम वैलिडेशन के 4 चरण
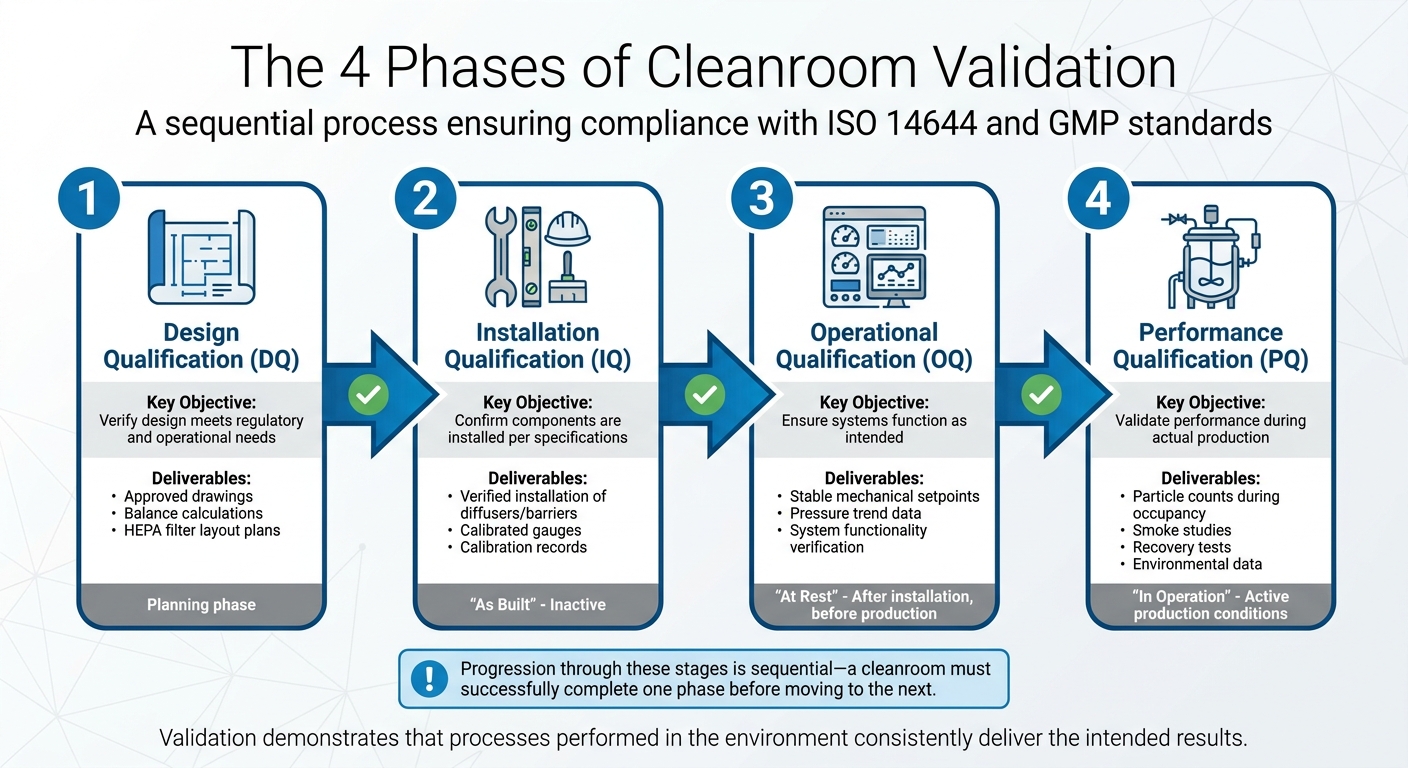
संवर्धित मांस उत्पादन के लिए क्लीनरूम वैलिडेशन के 4 चरण
क्लीनरूम वैलिडेशन एक चरण-दर-चरण प्रक्रिया है जिसमें चार विशिष्ट चरण होते हैं, प्रत्येक पिछले पर आधारित होता है। इन चरणों के माध्यम से प्रगति क्रमिक होती है - एक क्लीनरूम को अगले चरण में जाने से पहले एक चरण को सफलतापूर्वक पूरा करना होता है।जैसा कि Allied Cleanrooms उपयुक्त रूप से कहता है:
"मान्यता वह है जो एक क्लीनरूम को तैयार दिखने से अलग करती है और वास्तव में तैयार करती है" [8].
जबकि योग्यता यह सुनिश्चित करती है कि क्लीनरूम और इसकी प्रणालियाँ स्थापित हैं और डिज़ाइन के अनुसार कार्य करती हैं, मान्यता एक कदम आगे बढ़ती है। यह प्रदर्शित करती है कि पर्यावरण में किए गए प्रक्रियाएँ लगातार इच्छित परिणाम देती हैं [7]. चार चरण - डिज़ाइन योग्यता (DQ), स्थापना योग्यता (IQ), परिचालन योग्यता (OQ), और प्रदर्शन योग्यता (PQ) - सुविधाओं को मान्य उत्पादन प्रक्रियाओं के लिए तैयार करने के लिए डिज़ाइन किए गए हैं। ये चरण कठोर परीक्षण प्रोटोकॉल के लिए आधार भी तैयार करते हैं।
| मान्यता चरण | मुख्य उद्देश्य | विशिष्ट डिलीवेरेबल्स/परीक्षण |
|---|---|---|
| डिज़ाइन योग्यता (DQ) | डिज़ाइन को नियामक और परिचालन आवश्यकताओं को पूरा करने की पुष्टि करें। | स्वीकृत चित्र, संतुलन गणना, HEPA फ़िल्टर लेआउट योजनाएँ। |
| स्थापना योग्यता (IQ) | घटक निर्दिष्टीकरण के अनुसार स्थापित हैं, इसकी पुष्टि करें। | डिफ्यूज़र/बाधाओं की सत्यापित स्थापना, कैलिब्रेटेड गेज। |
| संचालन योग्यता (OQ) | सुनिश्चित करें कि सिस्टम इच्छानुसार कार्य करते हैं। | स्थिर यांत्रिक सेटपॉइंट्स, दबाव प्रवृत्ति डेटा। |
| प्रदर्शन योग्यता (PQ) | उत्पादन/अधिभोग के दौरान प्रदर्शन को मान्य करें। | कण गणना, धुआं अध्ययन, पुनर्प्राप्ति परीक्षण, पर्यावरण निगरानी डेटा। |
डिज़ाइन योग्यता (DQ)
डिज़ाइन योग्यता (DQ) चरण यह सुनिश्चित करता है कि क्लीनरूम का डिज़ाइन संवर्धित मांस उत्पादन की विशिष्ट आवश्यकताओं के अनुरूप है। इसमें यह सत्यापित करना शामिल है कि डिज़ाइन दस्तावेज़, जैसे संतुलन गणना और HEPA फ़िल्टर लेआउट, वास्तविक परिचालन आवश्यकताओं को दर्शाते हैं। प्रत्येक डिज़ाइन तत्व को सख्त स्वीकृति मानदंडों को पूरा करना चाहिए, जो अक्सर ISO 14644 मानकों या उपयोगकर्ता-परिभाषित आवश्यकताओं पर आधारित होते हैं [7].
स्थापना योग्यता (IQ)
स्थापना योग्यता (IQ) क्लीनरूम की "जैसा निर्मित" स्थिति को उसके निष्क्रिय अवस्था में सत्यापित करने पर केंद्रित है। यह चरण यह पुष्टि करता है कि विसारक, रिटर्न और बाधाएं डिज़ाइन विनिर्देशों से मेल खाते हैं। यह यह भी जांचता है कि दबाव मॉनिटर और गेज सही ढंग से कैलिब्रेटेड और पूरी तरह से परिचालित हैं।विस्तृत प्रलेखन, जिसमें अंशांकन रिकॉर्ड और परीक्षण स्थानों का मानचित्रण शामिल है, इस चरण के लिए महत्वपूर्ण है [7][8].
ऑपरेशनल क्वालिफिकेशन (OQ)
ऑपरेशनल क्वालिफिकेशन (OQ) क्लीनरूम का परीक्षण "आराम की स्थिति" में करता है - स्थापना के बाद लेकिन उत्पादन शुरू होने से पहले। यह चरण यह सुनिश्चित करता है कि सिस्टम इच्छित रूप से कार्य कर रहे हैं, स्थिर यांत्रिक सेटपॉइंट्स और सुसंगत दबाव प्रवृत्तियों का दस्तावेजीकरण करके। यदि कोई महत्वपूर्ण परिवर्तन होते हैं, जैसे उपकरणों का स्थानांतरण या वायु प्रवाह में संशोधन, तो संतुलन बनाए रखने के लिए लक्षित पुनः परीक्षण की आवश्यकता होती है [7][8]. एक बार जब सिस्टम सही ढंग से संचालित होने की पुष्टि हो जाती है, तो सुविधा सक्रिय परिस्थितियों के तहत प्रदर्शन सत्यापन के लिए तैयार होती है।
प्रदर्शन योग्यता (PQ)
अंतिम चरण, प्रदर्शन योग्यता (PQ), वास्तविक उत्पादन परिस्थितियों के दौरान क्लीनरूम के प्रदर्शन को मान्य करता है।इस चरण में यह आकलन किया जाता है कि क्या सुविधा खेती किए गए मांस उत्पादन के लिए उपयोग में रहते हुए प्रदर्शन लक्ष्यों को पूरा करती है। प्रमुख मूल्यांकनों में शामिल हैं: उपस्थिति के दौरान कणों की गिनती, महत्वपूर्ण क्षेत्रों के आसपास वायु प्रवाह का दृश्यांकन (जैसे धुआं अध्ययन), और यह मापने के लिए पुनर्प्राप्ति परीक्षण कि एक गड़बड़ी के बाद कमरा कितनी जल्दी आवश्यक स्वच्छता पर लौटता है। PQ शुरू करने से पहले, सुनिश्चित करें कि यांत्रिक सेटपॉइंट स्थिर हैं, बायोप्रोसेस नियंत्रण सॉफ़्टवेयर, के माध्यम से प्रबंधित किए जाते हैं, महत्वपूर्ण नमूना स्थानों की पहचान की जाती है, और सफाई रिकॉर्ड मान्य स्थितियों की पुष्टि करते हैं[7].
खेती किए गए मांस की सुविधाओं के लिए, स्वतंत्र तृतीय-पक्ष सत्यापन एजेंसियों का उपयोग अत्यधिक अनुशंसित है। यह निष्पक्ष सत्यापन नियामकों और लेखा परीक्षकों के साथ अधिक वजन रखता है। एलाइड क्लीनरूम्स जोर देता है:
"नियामक और लेखा परीक्षक उन परिणामों को अधिक महत्व देते हैं जो एक बाहरी पार्टी से आते हैं जिनका परिणाम में कोई हिस्सा नहीं है" [8].
यह स्वतंत्र दृष्टिकोण विशेष रूप से उन सुविधाओं के लिए महत्वपूर्ण है जो USDA निरीक्षण की अनुमति प्राप्त करना चाहती हैं, जिसके लिए FDA प्रीमार्केट परामर्श की सफलतापूर्वक पूर्णता की आवश्यकता होती है [5] [6].
क्लीनरूम वैलिडेशन के लिए आवश्यक परीक्षण प्रोटोकॉल
एक बार डिज़ाइन क्वालिफिकेशन (DQ), इंस्टॉलेशन क्वालिफिकेशन (IQ), ऑपरेशनल क्वालिफिकेशन (OQ), और परफॉर्मेंस क्वालिफिकेशन (PQ) पूर्ण हो जाने के बाद, अगला कदम क्लीनरूम के प्रदर्शन को सत्यापित करने के लिए परीक्षणों की एक श्रृंखला है। ये परीक्षण सुनिश्चित करते हैं कि क्लीनरूम अपने ISO वर्गीकरण का पालन करता है और खेती किए गए मांस के उत्पादन के लिए उपयुक्त है। नीचे प्रमुख परीक्षण प्रोटोकॉल का अवलोकन दिया गया है।
वायुवाहित कण गणना परीक्षण
यह परीक्षण हवा में कणों की संख्या को मापता है ताकि यह पुष्टि की जा सके कि क्लीनरूम अपने ISO वर्गीकरण का पालन करता है।उदाहरण के लिए, एक ISO 5 क्लीनरूम में 0.5 µm या उससे बड़े 3,520 कण प्रति घन मीटर से अधिक नहीं होने चाहिए। परीक्षण में "आराम की स्थिति" और "संचालन की स्थिति" दोनों के तहत निर्दिष्ट नमूना बिंदुओं पर कैलिब्रेटेड कण काउंटर का उपयोग शामिल है। ISO 14644-2 के अनुसार, ISO 5 और सख्त वर्गीकरणों के लिए कण सांद्रता परीक्षण हर छह महीने में और ISO 6 और उससे ऊपर के लिए वार्षिक रूप से किया जाना चाहिए [8].
HEPA फ़िल्टर अखंडता परीक्षण
ये परीक्षण सुनिश्चित करते हैं कि उच्च दक्षता वाले पार्टिकुलेट एयर (HEPA) फ़िल्टर सही ढंग से काम कर रहे हैं, बिना किसी रिसाव या दोष के। जबकि कण गणना परीक्षण कमरे की समग्र स्वच्छता का आकलन करते हैं, अखंडता परीक्षण स्वयं फ़िल्टर पर ध्यान केंद्रित करते हैं। किसी भी महत्वपूर्ण परिवर्तन, जैसे फ़िल्टर प्रतिस्थापन या कमरे में संशोधन, के लिए तुरंत पुनः परीक्षण की आवश्यकता होती है।कई सुविधाएं इन परीक्षणों को करने के लिए तृतीय-पक्ष एजेंसियों का चयन करती हैं, क्योंकि स्वतंत्र सत्यापन को अक्सर नियामकों द्वारा अत्यधिक सम्मानित किया जाता है [8].
वायु प्रवाह वेग और मात्रा माप
सफाई बनाए रखने के लिए उचित वायु प्रवाह महत्वपूर्ण है। एकदिशात्मक क्लीनरूम में वायु प्रवाह आमतौर पर 0.45 m/s ±20% (0.36 और 0.54 m/s के बीच) के भीतर होना चाहिए। माप आमतौर पर कार्य ऊंचाई पर लिया जाता है - जहां संवेदनशील संचालन, जैसे कि बायोरिएक्टर इनोकुलेशन, स्केलेबल बायोरिएक्टर सिस्टम के भीतर होते हैं - या फिल्टर के चेहरे से 150 से 300 मिमी की दूरी पर। ISO 14644-3:2005 यह बताता है कि नमूना बिंदुओं की संख्या कमरे के क्षेत्रफल (वर्ग मीटर में) के 10 के वर्गमूल के बराबर होनी चाहिए, जिसमें कम से कम चार रीडिंग और प्रत्येक फिल्टर के लिए कम से कम एक बिंदु होना चाहिए।धुआं अध्ययन या वायु प्रवाह दृश्यांकन मानचित्रण एक दिशा में वायु प्रवाह को और सत्यापित कर सकते हैं और स्थिर वायु के क्षेत्रों का पता लगा सकते हैं, जिन्हें "वेक क्षेत्र" के रूप में जाना जाता है [9] .
दबाव अंतर जांच
स्वच्छ कक्ष क्षेत्रों के बीच उचित दबाव अंतर बनाए रखना संदूषण को रोकने के लिए आवश्यक है। स्वच्छ क्षेत्रों को आसन्न, कम स्वच्छ क्षेत्रों की तुलना में सकारात्मक दबाव बनाए रखना चाहिए। कैलिब्रेटेड दबाव गेज और सेंसर का उपयोग स्थिर दबाव अंतर को दस्तावेज़ और सुनिश्चित करने के लिए किया जाता है।
तापमान और आर्द्रता सत्यापन
स्वच्छ कक्ष का तापमान और आर्द्रता स्तर सावधानीपूर्वक नियंत्रित किया जाना चाहिए ताकि संवर्धित मांस उत्पादन का समर्थन किया जा सके। ये स्थितियाँ उत्पाद की गुणवत्ता के साथ-साथ HEPA फिल्टर और अन्य प्रणालियों के प्रदर्शन को प्रभावित करती हैं। निरंतर निगरानी यह सुनिश्चित करने में मदद करती है कि ये पैरामीटर उत्पादन चक्रों के दौरान आवश्यक सेटपॉइंट्स के भीतर बने रहें।
निरंतर निगरानी और पुनः मान्यता
प्रणालियों के स्थापित होने के बाद मान्यता समाप्त नहीं होती। फ़िल्टर के घिसने, HVAC प्रणाली के क्षय, और प्रक्रिया में बदलाव के प्रभावों का मुकाबला करने के लिए निरंतर निगरानी और समय-समय पर पुनः मान्यता आवश्यक है। DQ, IQ, OQ, और PQ के माध्यम से प्रारंभिक अनुपालन प्राप्त करने के बाद, सक्रिय उत्पादन के दौरान प्रदर्शन बनाए रखने के लिए निरंतर निगरानी की आवश्यकता होती है।
पर्यावरण निगरानी कार्यक्रम
एक मजबूत पर्यावरण निगरानी कार्यक्रम एक निर्धारित समय सारणी के अनुसार वायुमंडलीय कण गणना, सूक्ष्मजीव संदूषण, तापमान, आर्द्रता, और दबाव भिन्नताओं का ट्रैक रखता है। ग्रेड A क्षेत्रों के लिए, निगरानी निरंतर होनी चाहिए, जबकि ग्रेड B क्षेत्रों के लिए हर 15-30 मिनट में जांच की आवश्यकता होती है। ग्रेड C और D क्षेत्रों को जोखिम आकलन के आधार पर प्रति घंटे या प्रति शिफ्ट की निगरानी की जा सकती है।[3][4].
सूक्ष्मजीव निगरानी सक्रिय वायु नमूना लेने को स्थिर प्लेटों के साथ जोड़ती है। यूके जीएमपी दिशानिर्देशों के अनुसार, स्थिर प्लेटों का परीक्षण कम से कम साप्ताहिक रूप से किया जाना चाहिए, जबकि गैर-जीवित कण गणना दैनिक रूप से की जानी चाहिए। रखरखाव गतिविधियों के बाद निगरानी की आवृत्ति बढ़नी चाहिए [3][4]. सभी डेटा को वास्तविक समय में लॉग किया जाना चाहिए, जिसमें परिभाषित चेतावनी सीमाएं हों। उदाहरण के लिए, एक ग्रेड ए क्षेत्र जीवित कणों के लिए 1 CFU/m³ की क्रिया सीमा निर्धारित कर सकता है [1][2]. इस डेटा में रुझानों का विश्लेषण करने से संभावित मुद्दों की पहचान जल्दी करने में मदद मिल सकती है।
रिमोट लेजर कण काउंटर, सक्रिय वायु नमूना लेने वाले और वास्तविक समय चेतावनी के साथ डेटा लॉगर जैसे उन्नत उपकरण निरंतर निगरानी सुनिश्चित करते हैं।वायरलेस सेंसर नेटवर्क डैशबोर्ड के माध्यम से 24/7 निगरानी प्रदान करते हैं, जिससे मैनुअल जांच पर निर्भरता कम होती है [2][10]. सटीकता बनाए रखने के लिए, सेंसर को हर छह महीने में निवारक रखरखाव से गुजरना चाहिए।
पुनर्मूल्यांकन अनुसूची
पुनर्मूल्यांकन सुनिश्चित करता है कि क्लीनरूम का प्रदर्शन आवश्यक विनिर्देशों के भीतर रहता है, भले ही उपकरण पुराना हो जाए, प्रक्रियाएं विकसित हों, या नियामक आवश्यकताएं बदलें। पुनर्मूल्यांकन के लिए ट्रिगर में प्रमुख परिवर्तन शामिल हैं, जैसे नए बायोरिएक्टर स्थापित करना, एचवीएसी सिस्टम को अपग्रेड करना, या सुविधा लेआउट को बदलना। संवर्धित मांस सुविधाओं के लिए, प्रक्रिया में परिवर्तन - जैसे मीडिया फॉर्मूलेशन में संशोधन - को भी संदूषण जोखिमों को प्रबंधित करने के लिए ध्यान में रखा जाना चाहिए [1] [3].
महत्वपूर्ण मापदंडों का वार्षिक पुनर्मूल्यांकन किया जाना चाहिए, जिसमें अर्ध-वार्षिक जांच और महत्वपूर्ण परिवर्तनों के बाद तत्काल पुनर्मूल्यांकन शामिल है। MHRA GMP दिशानिर्देशों के अनुसार, संवर्धित मांस के लिए उच्च-जोखिम वाले क्लीनरूम को अपने प्रदर्शन योग्यता (PQ) का हर 12 महीने में पुनर्मूल्यांकन करना चाहिए, जिसमें सभी IQ, OQ, और PQ तत्व शामिल हैं। HVAC उन्नयन के बाद, 30 दिनों के भीतर पुनः परीक्षण होना चाहिए [4] [10]. रोकथाम रखरखाव अनुसूचियों को भी GMP ऑडिट के साथ संरेखित करना चाहिए [2][3].
चल रहे सत्यापन आवश्यकताओं के लिए,
संवर्धित मांस क्लीनरूम के लिए अनुपालन मानक
मान्यता और परीक्षण प्रोटोकॉल को संबोधित करने के बाद, संवर्धित मांस उत्पादन के लिए अंतिम बाधा अनुपालन मानकों को पूरा करना है ताकि नियामक अनुमोदन सुरक्षित किया जा सके। इस प्रक्रिया में उपयोग किए जाने वाले क्लीनरूम को ISO 14644 के कण सीमाओं और परीक्षण विधियों के लिए पालन करना चाहिए, साथ ही गुड मैन्युफैक्चरिंग प्रैक्टिस (GMP) दिशानिर्देशों के लिए संदूषण नियंत्रण और मान्यता के लिए। इन ढाँचों का पालन करके, निर्माता यह सुनिश्चित कर सकते हैं कि उनकी सुविधाएं कठोर नियामक मांगों को पूरा करती हैं। आइए क्लीनरूम अनुपालन में प्रत्येक मानक की भूमिका को तोड़ें।
ISO 14644 क्लीनरूम वर्गीकरण के लिए मानक
ISO 14644 वायुमंडलीय कणों की सांद्रता के आधार पर क्लीनरूम वर्गीकरण को निर्दिष्ट करता है। यह प्रति घन मीटर ≥ 0.5 μm आकार के कणों को मापता है, जिसमें कक्षाएं ISO 1 (सबसे स्वच्छ) से लेकर ISO 9 तक होती हैं। संवर्धित मांस उत्पादन के लिए, सबसे प्रासंगिक वर्गीकरण ISO 5 से ISO 8 हैं, जो GMP ग्रेड A से D के साथ मेल खाते हैं। ये मानक "आराम की स्थिति" पर ध्यान केंद्रित करते हैं - जब क्लीनरूम पूरी तरह से सेट होता है लेकिन खाली होता है।
जबकि ISO 14644 क्लीनरूम को वर्गीकृत करने के लिए नींव स्थापित करता है, यह सक्रिय संचालन के दौरान सत्यापन को कवर नहीं करता है या सूक्ष्मजीव निगरानी की आवश्यकता नहीं होती है। यहीं पर GMP दिशानिर्देश काम में आते हैं, जो संवर्धित मांस सुविधाओं के लिए अनुपालन की एक अतिरिक्त परत जोड़ते हैं।
संवर्धित मांस के लिए GMP आवश्यकताएँ
ISO मानकों के विपरीत, GMP "आराम की स्थिति" (अप्रयुक्त) और "संचालन में" (प्रयुक्त) दोनों अवस्थाओं के लिए सत्यापन अनिवार्य करता है। उदाहरण के लिए, एक ग्रेड बी क्लीनरूम में आराम की स्थिति में 0.5 μm/m³ से अधिक के 3,520 कणों की अनुमति होती है, लेकिन संचालन के दौरान यह 352,000 कणों तक बढ़ जाता है [12] .
GMP एक संक्रमण नियंत्रण रणनीति (CCS), का उपयोग करता है जो गुणवत्ता जोखिम प्रबंधन (QRM) द्वारा निर्देशित होता है, ताकि संक्रमण जोखिमों की पहचान और न्यूनतम किया जा सके। दिशानिर्देश संरचनात्मक और सतह आवश्यकताओं को भी निर्दिष्ट करते हैं ताकि कणों के जमाव को रोका जा सके और प्रभावी सफाई को सक्षम किया जा सके। सतहें चिकनी, जलरोधक, और टिकाऊ होनी चाहिए, जबकि सफाई की कठिनाइयों के कारण स्लाइडिंग दरवाजों की अनुशंसा नहीं की जाती है। इसके अतिरिक्त, ग्रेड ए और बी क्षेत्रों में माइक्रोबियल जलाशयों से बचने के लिए सिंक और नालियों की अनुमति नहीं है।
चूंकि क्लीनरूम निरीक्षणों के दौरान 75-80% कणों के लिए मनुष्य जिम्मेदार होते हैं [11], जीएमपी सख्त गाउनिंग प्रोटोकॉल लागू करता है और महत्वपूर्ण प्रदर्शन योग्यता (पीक्यू) चरणों के दौरान कर्मियों की पहुंच को सीमित करता है।
उन उत्पादों के लिए जो बाँझ हैंडलिंग की आवश्यकता होती है, जीएमपी सत्यापन में एसेप्टिक प्रक्रिया सिमुलेशन (मीडिया फिल्स) शामिल होते हैं ताकि यह पुष्टि की जा सके कि उत्पादन प्रक्रिया सूक्ष्मजीव संदूषण को रोक सकती है। पर्यावरण निगरानी एक और महत्वपूर्ण पहलू है, जो गैर-जीवित कणों और जीवित सूक्ष्मजीवों दोनों को कवर करता है। ग्रेड ए क्षेत्रों में निरंतर निगरानी की आवश्यकता होती है, जबकि निम्न-ग्रेड क्षेत्रों में अनुपालन बनाए रखने के लिए बार-बार जांच की जाती है।
क्लीनरूम वैलिडेशन संसाधनों के लिए Cellbase का उपयोग करना
संवर्धित मांस सुविधाओं के लिए क्लीनरूम वैलिडेशन उपकरणों की सोर्सिंग एक जटिल प्रक्रिया हो सकती है, मुख्य रूप से ISO 14644 और GMP मानकों को पूरा करने के लिए आवश्यक विशेष निगरानी उपकरणों के कारण। सामान्य लैब सप्लाई प्लेटफॉर्म अक्सर इन विशेष वस्तुओं को स्टॉक करने में विफल रहते हैं, जिससे खरीदारी टीमों को खंडित आपूर्तिकर्ता नेटवर्क से समाधान जोड़ने के लिए मजबूर होना पड़ता है।
सत्यापित उपकरण और सामग्री तक पहुंच
उदाहरण के लिए, एक स्टार्टअप जिसने
प्रमाणीकरण आवश्यकताओं के लिए सरलित खरीदारी
सत्यापित उपकरणों की पेशकश से परे,
खरीद प्रबंधकों ने आवश्यक निगरानी उपकरणों, जिनमें वास्तविक समय कण काउंटर और डेटा लॉगर्स शामिल हैं, की तेजी से पुनःपूर्ति की सूचना दी है, जो प्रभावी पर्यावरण निगरानी कार्यक्रमों को बनाए रखने और GMP दिशानिर्देशों के तहत पुनः मान्यता की योजना बनाने के लिए महत्वपूर्ण हैं [18] . इसके अतिरिक्त,
निष्कर्ष
संवर्धित मांस उत्पादन में क्लीनरूम मान्यता एक सावधानीपूर्वक प्रक्रिया है जिसे यह सुनिश्चित करने के लिए डिज़ाइन किया गया है कि सुविधाएं ISO 14644 कण सीमाओं और GMP मानकों को पूरा करती हैं, इससे पहले कि बायोरिएक्टर संचालन शुरू हो सके। डेटा स्वयं के लिए बोलता है: मान्य क्लीनरूम लगातार 99.99% नसबंदी आश्वासन दर प्राप्त करते हैं, ISO 14644-अनुपालन सुविधाएं 1% से कम संदूषण दर की रिपोर्ट करती हैं।इसके विपरीत, गैर-मान्यीकृत वातावरण में संदूषण दरें 15% तक होती हैं - एक स्पष्ट अंतर जो उचित मान्यता की महत्वता को दर्शाता है[13] [14].
लेकिन प्रारंभिक मान्यता के बाद काम समाप्त नहीं होता। क्लीनरूम प्रदर्शन को बनाए रखना उतना ही महत्वपूर्ण है। क्लीनरूम टेक्नोलॉजी इंस्टीट्यूट के विशेषज्ञों के अनुसार, अपर्याप्त मान्यता बायोफार्मा में जीएमपी गैर-अनुरूपताओं के 40% के लिए जिम्मेदार है। संवर्धित मांस के लिए, यह एक गंभीर जोखिम प्रस्तुत करता है, क्योंकि एक भी संदूषण घटना उत्पादन रन को खतरे में डाल सकती है जो हजारों पाउंड के मूल्य की होती है, उच्च गुणवत्ता वाले इनपुट को सुरक्षित करने के लिए एक विश्वसनीय खरीद परत की आवश्यकता को उजागर करती है[13][14].
सामान्य प्रश्न
क्लीनरूम में योग्यता और प्रमाणीकरण के बीच क्या अंतर है?
क्लीनरूम अनुपालन बनाए रखने में योग्यता और प्रमाणीकरण अलग लेकिन समान रूप से महत्वपूर्ण भूमिकाएँ निभाते हैं।
योग्यता यह सुनिश्चित करने के बारे में है कि क्लीनरूम और इसकी प्रणालियाँ सही ढंग से स्थापित हैं और इच्छित रूप से कार्य करती हैं। इस प्रक्रिया में कई चरण शामिल होते हैं, जिनमें डिज़ाइन योग्यता (डीक्यू), स्थापना योग्यता (आईक्यू), और संचालन योग्यता (ओक्यू). प्रत्येक चरण यह पुष्टि करता है कि क्लीनरूम अपनी डिज़ाइन विशिष्टताओं को पूरा करता है और प्रभावी ढंग से संचालित होता है।
प्रमाणीकरण, दूसरी ओर, वास्तविक उत्पादन के दौरान आवश्यक वातावरण को लगातार प्रदान करने की क्लीनरूम की क्षमता पर केंद्रित है। यह दीर्घकालिक विश्वसनीयता, सुरक्षा और नियामक मानकों का पालन सुनिश्चित करने के बारे में है।
संवर्धित मांस क्षेत्रों के लिए सही ISO वर्ग/GMP ग्रेड कैसे चुनें?
संवर्धित मांस उत्पादन के लिए सही ISO वर्ग या GMP ग्रेड चुनते समय, यह सब उत्पादन के विशिष्ट चरण और संबंधित संदूषण जोखिमों पर निर्भर करता है।
- ISO वर्ग 5: प्रारंभिक संवर्धन चरणों के लिए सबसे उपयुक्त है जहाँ स्वच्छता बनाए रखना महत्वपूर्ण है।
- ISO वर्ग 6: बायोरिएक्टर संचालन के लिए आदर्श है, जो स्वच्छता और व्यावहारिकता के बीच संतुलन बनाता है।
- ISO वर्ग 8: कटाई और स्थानांतरण प्रक्रियाओं के लिए उपयुक्त है, जहाँ संदूषण जोखिम कम होते हैं।
उन क्षेत्रों में उच्च स्वच्छता मानकों को बनाए रखना आवश्यक है जहाँ स्वच्छता से समझौता नहीं किया जा सकता। इसके अतिरिक्त, नियामक आवश्यकताओं को पूरा करने के लिए उचित पर्यावरणीय नियंत्रण आवश्यक हैं।
कौन से परिवर्तन तत्काल क्लीनरूम पुन: मान्यता की आवश्यकता रखते हैं?
जब प्रमुख परिवर्तन होते हैं - जैसे क्लीनरूम लेआउट में बदलाव, नए उपकरणों का जोड़, या पर्यावरणीय नियंत्रणों में अपडेट जो नसबंदी या अनुपालन को प्रभावित कर सकते हैं - तत्काल पुन: मान्यता आवश्यक हो जाती है। ऐसे परिवर्तन महत्वपूर्ण स्थितियों को प्रभावित कर सकते हैं, इसलिए पुन: मान्यता सुनिश्चित करती है कि सब कुछ नियामक आवश्यकताओं को पूरा करता रहे।











