Stabilitas genetik sangat penting untuk produksi daging budidaya. Tanpa itu, garis sel dapat bermutasi, menyebabkan kualitas yang tidak konsisten, risiko keamanan, dan kegagalan produksi. Penskalaan dari ribuan menjadi triliunan sel memperbesar risiko ini, membuat sistem kontrol kualitas yang kuat menjadi penting. Regulator seperti FDA dan EMA memerlukan bukti stabilitas sebelum menyetujui produk, karena bahkan perubahan genetik kecil dapat memicu hasil yang alergi atau berbahaya.
Tantangan utama termasuk drift genetik, akumulasi mutasi, dan aktivasi onkogen. Masalah ini muncul dari perpanjangan passaging sel, tekanan selektif, dan stres lingkungan selama produksi. Metode pengujian lanjutan, seperti kariotiping, array SNP, dan sekuensing generasi berikutnya (NGS), membantu mendeteksi dan mengatasi risiko ini. Strategi pencegahan seperti perbankan sel terstruktur dan rekayasa genetika yang ditargetkan lebih lanjut melindungi terhadap ketidakstabilan.
Produsen harus mengintegrasikan pengendalian kualitas ke dalam setiap tahap produksi - dari penyimpanan sel hingga bioreaktor skala besar. Alat seperti profil STR, tes kontaminasi, dan uji fungsional memastikan konsistensi dan keamanan. Platform seperti
Mempercepat Pengembangan Garis Sel dari DNA ke Bank Sel Induk - AGC Biologics
Tantangan Umum dalam Mempertahankan Stabilitas Genetik
Memastikan stabilitas genetik sepanjang siklus produksi daging budidaya bukanlah hal yang mudah. Skala produksi yang besar memperkenalkan banyak peluang bagi perubahan genetik untuk berkembang dan menyebar. Mengenali tantangan ini adalah kunci untuk menempatkan sistem pengendalian kualitas yang efektif.
Genetic Drift dan Akumulasi Mutasi
Perpanjangan pemindahan sel adalah sumber utama ketidakstabilan genom dalam produksi daging yang dibudidayakan. Garis sel yang diabadikan, secara alami, rentan terhadap perubahan genom, yang dapat menyebabkan mutasi spontan selama kultur jangka panjang [6][5]. Seiring sel mengalami penggandaan populasi yang berulang, kesalahan dalam replikasi DNA menumpuk, menghasilkan populasi sel yang beragam dan, berpotensi, kehilangan fungsi. Christopher Frye dan Luhong He dari BioPharm International menyoroti masalah ini:
Garis sel CHO yang berasal dari klon sering diamati menyimpang, menjadi populasi heterogen selama periode sub-kultur yang panjang [6].
Dalam pengaturan industri, sekitar 20% dari lini sel produksi menunjukkan heterogenitas transgen yang signifikan selama beberapa generasi berturut-turut [6]. Mutasi ini dapat terjadi sejak awal, selama replikasi DNA setelah transfeksi, atau karena kesalahan saat gen asing diintegrasikan ke dalam genom inang [5].
Tekanan selektif menambah lapisan kompleksitas lainnya. Agen seperti antibiotik dan penanda metabolik (e.g. , MTX) yang digunakan untuk menstabilkan lini sel sebenarnya dapat meningkatkan tingkat mutasi [6][5]. Dalam beberapa kasus, semakin tinggi konsentrasi agen-agen ini, semakin tinggi tingkat mutasi [6]. Stres lingkungan - seperti kekurangan nutrisi, kondisi kultur yang tidak optimal selama peningkatan skala, dan stres fisik dari ekspansi - dapat lebih lanjut mengacaukan integritas genetik [6][5].
htmlShuai Wang, Direktur Pengembangan Garis Sel di WuXi Biologics, mencatat:
Tingkat mutasi kemungkinan akan berubah selama pemindahan sel karena plastisitas genomik sel ovarium hamster Cina (CHO) [5].
Perubahan epigenetik juga berperan. Transgen dapat sebagian atau sepenuhnya hilang atau terdiam selama proses kultur, mempengaruhi stabilitas jangka panjang. Mutasi yang terakumulasi ini tidak hanya merusak fungsi sel tetapi juga meningkatkan risiko aktivasi onkogen.
Risiko Aktivasi Onkogen
Aktivasi onkogen merupakan perhatian keamanan kritis bagi produsen daging budidaya, karena dapat mengkompromikan seluruh batch produksi. Ketidakstabilan genetik dapat menyebabkan aktivasi onkogen melalui mekanisme seperti hipermetilasi, yang dapat menghasilkan profil mirip tumor [3][1]. Ekspansi cepat yang diperlukan dalam produksi semakin meningkatkan kemungkinan akumulasi mutasi berbahaya ini [5][6].
Ini adalah tantangan yang diakui dengan baik. Menurut Konsorsium Internasional untuk Inovasi & Kualitas dalam Pengembangan Farmasi (IQ), 67% responden percaya bahwa mutasi genetik menimbulkan ancaman yang lebih besar daripada misinkorporasi asam amino selama produksi [5] . Sebuah kasus dari Mei 2024 menggambarkan keparahan masalah ini: WuXi Biologics menemukan bahwa 43% klon dari program pengembangan jalur sel membawa mutasi titik genetik yang sama. Penyebab utamanya? Tingkat varian 2,1%–2,2% dalam DNA plasmid yang digunakan selama transfeksi, yang tidak terdeteksi oleh pengurutan Sanger tradisional. Untuk mengatasi hal ini, perusahaan menggabungkan Pengurutan Generasi Berikutnya (NGS) ke dalam proses kontrol kualitasnya untuk mendeteksi varian tersebut lebih awal [5].
Deteksi dini kelainan genetik sangat penting, karena perubahan onkogenik dapat mengkompromikan seluruh batch. Kariotipe G-band standar dapat mengidentifikasi subpopulasi abnormal dengan hanya 14% mosaikisme dalam dua puluh metafase sel [1]. Teknik yang lebih maju seperti NGS dapat mendeteksi mutasi genetik dalam sel klonal dengan sensitivitas 0,5% [5].
Analisis metilasi DNA adalah alat berharga lainnya untuk menilai potensi tumorigenik:
Karena tingkat metilasi DNA dan hipermetilasi gen tertentu terjadi dalam inisiasi dan perkembangan kanker, analisis profil metilasi DNA mungkin memberikan informasi pelengkap tentang potensi tumorigenik sel [3].
Tantangan sebenarnya terletak pada penerapan sistem pemantauan yang kuat yang mampu mengidentifikasi perubahan ini sebelum mereka mengkompromikan keamanan.Untuk produsen daging budidaya, menjaga stabilitas genetik selama ekspansi sel yang cepat memerlukan langkah-langkah pengendalian kualitas yang canggih. Platform khusus seperti
Metode Pengujian Pengendalian Kualitas
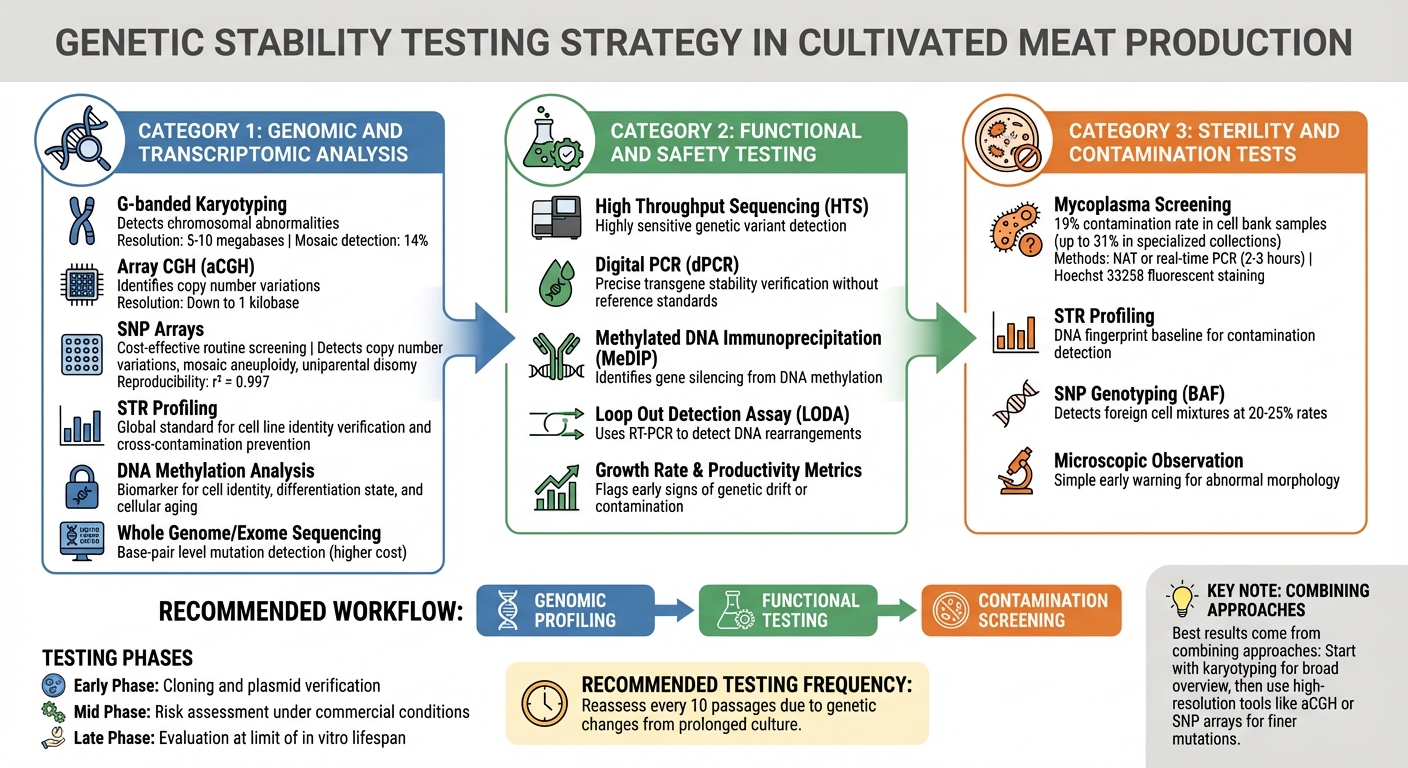
Metode Pengujian Pengendalian Kualitas untuk Stabilitas Genetik pada Garis Sel Daging Budidaya
Mengidentifikasi ketidakstabilan genetik sebelum berdampak pada produksi memerlukan strategi pengujian berlapis-lapis. Produsen daging budidaya mengandalkan metode yang mendeteksi segala sesuatu mulai dari perubahan kromosom besar hingga mutasi satu basa. Pilihan teknik tergantung pada risiko yang ada di setiap tahap produksi. Alat genomik ini bertindak sebagai pos pemeriksaan pertama, diikuti oleh penilaian fungsional dan kontaminasi yang mendetail.
Analisis Genomik dan Transkriptomik
Kariotipe G-banded adalah alat utama untuk mengidentifikasi masalah kromosom utama seperti kelainan numerik dan pengaturan ulang struktural besar, seperti translokasi. Meskipun dapat mendeteksi tingkat mosaik sekitar 14%, resolusinya terbatas pada perubahan 5–10 megabasa, yang berarti perubahan yang lebih kecil mungkin tidak terdeteksi [1] .
Array Hibridisasi Genomik Komparatif (aCGH) menawarkan resolusi lebih tinggi, mengidentifikasi variasi jumlah salinan hingga 1 kilobasa. Demikian pula, Array Polimorfisme Nukleotida Tunggal (SNP) menyediakan opsi yang hemat biaya untuk skrining rutin, mendeteksi variasi jumlah salinan, aneuploidi mosaik, dan disomi uniparental. Studi validasi telah menunjukkan bahwa array SNP sangat dapat direproduksi, dengan pengukuran Frekuensi Alel B (BAF) mencapai r² = 0.997 [8] [1].
Rocio Aguilar-Quesada dari Biobank Sistem Kesehatan Publik Andalusia menyoroti nilai dari menggabungkan metode:
Kariotipe tetap menjadi uji yang serbaguna, terutama ketika dilengkapi dengan pengujian resolusi tinggi [1].
Profiling Short Tandem Repeat (STR) adalah standar global untuk memverifikasi identitas garis sel dan mencegah kontaminasi silang [1] [9]. Sementara itu, analisis metilasi DNA berfungsi sebagai biomarker untuk identitas sel, keadaan diferensiasi, dan penuaan seluler [1] . Untuk deteksi mutasi tingkat pasangan basa, pengurutan genom atau eksom seluruhnya adalah pilihan, meskipun datang dengan biaya lebih tinggi dibandingkan dengan metode berbasis array [1] .
Hasil terbaik diperoleh dari menggabungkan pendekatan-pendekatan ini. Mulailah dengan kariotipe untuk gambaran umum yang luas, kemudian gunakan alat resolusi tinggi seperti aCGH atau array SNP untuk menangkap mutasi yang lebih halus. Penilaian ulang secara teratur - idealnya setiap 10 kali pasase - sangat penting, karena kultur yang berkepanjangan dapat menyebabkan perubahan genetik [10]. Wawasan genomik ini kemudian dilengkapi dengan uji fungsional untuk memastikan perilaku sel yang konsisten selama produksi.
Pengujian Fungsional dan Keamanan
Profiling genomik saja tidak cukup. Tes fungsional mengonfirmasi bahwa sel-sel mempertahankan karakteristik yang dimaksudkan selama ekspansi. Metrik seperti laju pertumbuhan dan produktivitas dapat menandai tanda-tanda awal dari pergeseran genetik atau kontaminasi [9].
High Throughput Sequencing (HTS) sangat sensitif untuk mendeteksi varian genetik, sementara digital PCR (dPCR) secara tepat memverifikasi stabilitas transgen tanpa memerlukan standar referensi [11]. Christopher Frye dan Luhong He dari BioPharm International menekankan pentingnya langkah ini:
Garis sel produksi adalah dasar dari setiap bioproses, dan dengan demikian, karakterisasi genetik yang tepat dari garis sel produksi sangat penting untuk keberhasilan pengembangan proses [6].
Stabilitas epigenetik juga sangat penting. Methylated DNA Immunoprecipitation (MeDIP) membantu mengidentifikasi penghambatan gen yang disebabkan oleh metilasi DNA, alasan umum untuk penurunan produktivitas [7]. Alat seperti Loop Out Detection Assay (LODA) menggunakan RT-PCR untuk mendeteksi pengaturan ulang DNA, seperti ketika gen yang diminati dihapus sementara penanda selektif tetap ada [7].
Pengujian harus selaras dengan fase produksi: pengujian fase awal berfokus pada kloning dan verifikasi plasmid, pengujian fase menengah menilai risiko di bawah kondisi komersial, dan pengujian fase akhir mengevaluasi sel pada batas umur in vitro mereka [6]. Memulai eksperimen dengan sel segar, berpasase rendah dari bank sel induk mengurangi risiko pergeseran genetik [9].
Uji Kemandulan dan Kontaminasi
Pengujian kontaminasi sangat penting untuk menghindari faktor yang dapat mengacaukan genetika. Mycoplasma sangat mengkhawatirkan, karena mengubah metabolisme dan perilaku sel tanpa menyebabkan perubahan yang terlihat dalam kultur [1]. Penelitian mengungkapkan kontaminasi mikoplasma dalam 19% sampel bank sel, dengan beberapa koleksi khusus menunjukkan tingkat setinggi 31% [1].
Pemeriksaan mikoplasma secara teratur menggunakan Teknik Amplifikasi Asam Nukleat (NAT) yang sensitif atau PCR real-time dapat memberikan hasil semi-kuantitatif dalam waktu 2–3 jam [1]. Hoechst 33258 fluorescent staining adalah metode lain, mengungkapkan pola fluoresensi ekstraseluler yang khas [9].
Profiling STR menetapkan sidik jari DNA untuk garis sel, bertindak sebagai dasar untuk mendeteksi kontaminasi silang [9]. Selain itu, genotip SNP menggunakan distribusi Frekuensi Alel B (BAF) dapat mengidentifikasi kontaminasi dari garis sel lain, mendeteksi campuran sel asing pada tingkat 20–25% [8].
Pengamatan mikroskopis adalah alat peringatan dini yang sederhana namun efektif, karena morfologi sel yang abnormal sering kali menandakan masalah kultur [9]. Menerapkan Sistem Manajemen Mutu, seperti ISO 9001:2015, bersama dengan Praktik Metode In Vitro yang Baik (GIVIMP), membantu menjaga kondisi kultur yang terstandarisasi dan dapat direproduksi, mengurangi risiko ketidakstabilan genomik [10].
Bagi produsen daging budidaya yang membutuhkan akses ke peralatan dan bahan pengujian khusus, platform seperti
sbb-itb-ffee270
Strategi Pencegahan untuk Ketidakstabilan Genetik
Mendeteksi ketidakstabilan genetik adalah satu hal; mencegahnya adalah tantangan lain sepenuhnya.Untuk menjaga stabilitas genetik tetap utuh, produsen daging budidaya memerlukan sistem yang dipikirkan dengan matang untuk mencegah garis sel dari penyimpangan sebelum masalah muncul. Dua strategi utama memimpin di sini: perbankan sel terstruktur dan rekayasa genetika yang ditargetkan. Bersama-sama, pendekatan ini secara langsung menangani risiko penyimpangan genetik dan aktivasi onkogen.
Perbankan Sel dan Krio-preservasi
Akumulasi mutasi adalah kekhawatiran nyata, jadi sistem perbankan sel yang andal sangat diperlukan. Standar industri melibatkan sistem dua tingkat: Bank Sel Induk (MCB) dan Bank Sel Kerja (WCB). Pengaturan ini memastikan titik awal yang konsisten untuk produksi. Membatasi jumlah lintasan sangat penting, karena setiap lintasan meningkatkan kemungkinan mutasi. Dengan menyimpan sel dalam nitrogen cair, aktivitas biologis secara efektif dihentikan, mengurangi risiko perubahan genetik selama penyimpanan.
Alih-alih melacak waktu, usia sel diukur dengan penggandaan populasi. Misalnya, bioreaktor produksi 5.000 liter tipikal melibatkan sekitar 30 penggandaan populasi[6]. Untuk menjaga konsistensi genetik, manufaktur komersial membatasi jumlah ini antara 45 dan 60 penggandaan[6].
Metode penyaringan seperti RT-PCR dan qPCR sel tunggal dapat mendeteksi masalah lebih awal, seperti penyambungan mRNA yang tidak biasa atau variabilitas transgen. Garis sel yang menunjukkan variabilitas luas dalam jumlah salinan harus dibuang untuk menghindari masalah di masa depan.
Kontrol kualitas tidak bisa ditawar. Yang mengkhawatirkan, penelitian telah menemukan bahwa hingga 31% garis sel di beberapa bank terkontaminasi dengan mikoplasma[3] . Untuk mencegah hal ini, profiling STR digunakan untuk mengonfirmasi keaslian garis sel sepanjang proses perbankan.Seperti yang disoroti oleh FSA Research and Evidence:
Karena sel yang disimpan adalah bahan awal untuk produk akhir, standar tinggi mungkin diperlukan oleh regulator di masa depan untuk memastikan produk daging yang aman dan berkualitas tinggi[2].
Rekayasa Genetik untuk Stabilitas
Rekayasa genetik memberikan lapisan pertahanan tambahan dengan secara langsung meningkatkan stabilitas garis sel. Teknik seperti integrasi terarah (TI), terutama Recombinase-Mediated Cassette Exchange (RMCE), memungkinkan penyisipan transgen yang tepat ke lokasi genom tertentu. Pendekatan ini menghindari ketidakpastian integrasi acak, di mana efek posisi dan ketidakstabilan jumlah salinan dapat menyebabkan masalah. Meskipun RMCE dalam sel CHO memiliki tingkat efisiensi di bawah 0,1%[12], klon yang dihasilkan lebih dapat diprediksi dan stabil.
Pemilihan sistem ekspresi juga penting. Misalnya, sistem Glutamine Synthetase (GS) biasanya menghasilkan sekitar lima salinan transgen per sel, sedangkan sistem Dihydrofolate Reductase (DHFR) dapat memperbanyak jumlah salinan hingga 1.000[6] . Walaupun jumlah salinan yang lebih tinggi mungkin terdengar menarik, mereka meningkatkan kemungkinan perubahan DNA, menjadikan sistem berbasis GS pilihan yang lebih cerdas untuk stabilitas jangka panjang.
Untuk lebih meminimalkan risiko, mutagenesis spesifik situs dan penyaringan NGS pra-transfeksi sangat penting. Karena sekuensing Sanger memiliki batas deteksi yang lebih tinggi, NGS dapat mendeteksi mutasi plasmid di bawah 0,5%, meningkatkan keberhasilan penyaringan klon hingga lebih dari 90%[5] .
Shuai Wang dan rekan-rekannya dari WuXi Biologics menekankan pentingnya kewaspadaan ini:
Karena optimasi proses tidak dapat memperbaiki mutasi pada tingkat gen, pantau tingkat mutasi pada klon stabil dengan ketat[5].
Bagi produsen yang membutuhkan alat khusus - baik untuk kriopreservasi, rekayasa genetika, atau karakterisasi lini sel -
Mengintegrasikan Pengendalian Kualitas ke dalam Produksi
Menggabungkan pengendalian kualitas ke dalam setiap fase produksi sangat penting. Tanpa sistem yang terstruktur, bahkan lini sel yang terawat baik dapat mengalami perubahan selama ekspansi dan peningkatan skala. Pengendalian kualitas tidak boleh dianggap sebagai pemikiran belakangan - ini harus menjadi bagian sentral dari produksi. Ini dimulai pada tahap scale-up, di mana sistem manajemen yang ketat dan lingkungan yang terkontrol memainkan peran penting.
Kontrol Kualitas Selama Ekspansi dan Scale-Up
Seperti yang dibahas sebelumnya, tes genomik dan kontaminasi sangat penting, terutama selama scale-up. Berpindah dari volume kecil ke ribuan liter memperkenalkan risiko baru, dengan setiap lintasan sel meningkatkan kemungkinan mutasi. Sistem Manajemen Kualitas (QMS) membantu mengelola risiko ini secara efektif. Sebagai contoh, antara tahun 2017 dan 2022, Josep M. Canals dan timnya di Universitas Barcelona menerapkan ISO 9001:2015 QMS untuk menstandarisasi kultur sel punca pluripoten manusia. Analisis retrospektif mereka terhadap data G-banding dan aCGH mengungkapkan pengurangan signifikan dalam aberasi kromosom dibandingkan dengan kondisi pra-adaptasi[10][13]. Canals menyoroti pentingnya pemantauan yang berkelanjutan:
Ketidakstabilan genetik yang ditunjukkan oleh hPSCs dalam kultur membuat penilaian ulang yang sering terhadap integritas genom menjadi persyaratan penting ketika merencanakan untuk menggunakannya dalam eksperimen [10].
Pemeriksaan genom rutin adalah suatu keharusan. Teknik seperti kariotip G-banding dan aCGH mendeteksi perubahan struktural, sementara Next-Generation Sequencing (NGS) mengidentifikasi mutasi pada tingkat di bawah 0,5%[5]. Analisis kurva pertumbuhan juga dapat menandai masalah lebih awal, seperti kontaminasi atau pergeseran genetik[9]. Pemantauan lingkungan menambah lapisan keamanan lain, dengan praktik seperti pengujian settle plate dan pemeriksaan filter HEPA setiap enam bulan memastikan lingkungan produksi tetap stabil dan bebas stres untuk garis sel[4] .
Konsistensi dalam media dan reagen sama pentingnya. Menggunakan media yang didefinisikan bebas serum seperti mTeSR1, bersama dengan reagen yang memiliki Sertifikat Analisis, membantu mengurangi variasi antar batch dan membatasi risiko kontaminasi virus[10][4]. Pemeriksaan morfologi secara teratur - pengamatan mikroskopis sederhana pada kepadatan kultur yang berbeda - dapat menangkap tanda-tanda awal diferensiasi atau stres[9]. Untuk mendapatkan peralatan atau reagen khusus, platform seperti
Uji Fungsional untuk Konsistensi Produk
Sementara pemantauan genomik menjaga proses, uji fungsional memastikan bahwa sel berfungsi sesuai yang diharapkan.Stabilitas genetik saja tidak cukup; sel juga harus mempertahankan kemampuan mereka untuk berfungsi dengan baik di seluruh batch produksi. Dalam daging yang dibudidayakan, ini berarti memastikan bahwa sel punca, seperti sel satelit otot, masih dapat berdiferensiasi menjadi jaringan otot atau lemak matang setelah ekspansi[2]. Uji diferensiasi sangat penting untuk memverifikasi hal ini.
Uji metabolik seperti MTT, LDH, dan Resazurin memberikan wawasan tentang kesehatan dan kelangsungan hidup sel [4][9]. Ini, dikombinasikan dengan profiling Short Tandem Repeat (STR), membantu memastikan bahwa garis sel tetap otentik dan bebas dari kontaminasi silang selama proses produksi[1][9].
Analisis transkripsi adalah langkah penting lainnya.Xiaoyue Chen dan Sam Zhang merekomendasikan:
cDNA daripada sekuensing DNA-genomik direkomendasikan untuk deteksi mutasi guna mengevaluasi risiko pada tingkat transkripsi[5].
Metode ini menawarkan gambaran yang lebih akurat tentang produk akhir, karena mencerminkan bagaimana gen diekspresikan daripada hanya lokasi genomiknya. Dengan memasangkan penyaringan genomik dengan uji fungsional, produsen dapat memastikan bahwa setiap batch memenuhi standar ketat untuk keamanan, kualitas, dan kinerja di setiap tahap produksi.
Kesimpulan
Mempertahankan stabilitas genetik sangat penting untuk memproduksi daging budidaya dengan aman dan konsisten. Francisco J. Molina-Ruiz dan rekan-rekannya dari Laboratorium Sel Punca dan Pengobatan Regeneratif menyoroti risikonya:
Perubahan genetik pada hPSC dapat membahayakan tidak hanya keamanan produk sel berbasis hPSC... tetapi juga menyebabkan kecenderungan diferensiasi heterogen dari bahan awal, profil ekspresi gen yang berubah, dan ketidakefisienan produk sel akhir [10].
Taruhannya signifikan - lebih dari 531 garis sel yang salah diidentifikasi telah dicatat oleh International Cell Line Authentication Committee [1].
Menangani masalah ini memerlukan kerangka kontrol kualitas yang kuat. Ini melibatkan penggabungan metode seperti STR profiling, G-banding karyotyping, aCGH, dan NGS lanjutan [5], bersamaan dengan sistem seperti ISO 9001:2015 untuk menstandarisasi proses dan meminimalkan kelainan kromosom [13].
Faktor ekonomi juga mendorong kebutuhan akan langkah-langkah ini.Genetic drift dapat mengakibatkan sel bermutasi mendapatkan keuntungan pertumbuhan, yang berpotensi merusak seluruh batch produksi [10][11]. Dengan meningkatnya fokus pada sel punca pluripoten manusia, permintaan untuk lini sel yang stabil tidak pernah sebesar ini. Seperti yang dijelaskan oleh Profesor David L. Kaplan dari Tufts University:
Lini sel yang diabadikan umumnya dianggap sebagai persyaratan untuk menghasilkan sejumlah besar jaringan yang dapat dimakan dari bioproses yang stabil dan kuat [14].
Bagi produsen daging budidaya, kontrol kualitas harus tertanam dalam setiap langkah - dari penyaringan plasmid hingga pemantauan produksi skala besar. Dengan menggabungkan pengujian menyeluruh dengan strategi pencegahan, produsen dapat memastikan hasil yang konsisten dan dapat diandalkan.
FAQ
Seberapa sering pengujian stabilitas genetik harus dilakukan selama peningkatan skala?
Pengujian stabilitas genetik adalah langkah penting selama peningkatan skala dan harus dilakukan secara teratur. Seberapa sering pengujian ini dilakukan sangat bergantung pada garis sel spesifik dan proses yang dimaksud. Untuk mengurangi kemungkinan mutasi dan mempertahankan sifat stemness sel, bijaksana untuk menetapkan batas pasase yang diinformasikan oleh analisis genetik.
Tes mana yang terbaik untuk mendeteksi mutasi kecil dan perubahan kromosom besar?
Tes seperti analisis array SNP dan genotyping SNP seluruh genom sangat efisien untuk mendeteksi mutasi kecil, perubahan jumlah salinan, dan aneuploidi. Metode ini sangat berguna untuk mengidentifikasi perubahan kromosom besar dalam garis sel.
Apa cara paling sederhana untuk mencegah drift genetik di antara batch produksi?
Untuk meminimalkan drift genetik, penting untuk melakukan analisis genetik dan fungsional secara teratur pada garis sel dan membatasi jumlah pasase yang mereka jalani. Terapkan praktik seperti membangun bank sel master dan secara rutin memeriksa stabilitas genetik, seperti yang direkomendasikan dalam protokol kontrol kualitas. Langkah-langkah ini penting untuk menjaga konsistensi dan memastikan hasil yang dapat diandalkan di antara batch produksi yang berbeda.











