Sertifikasi ruang bersih sangat penting untuk produksi daging budidaya, memastikan keselamatan dan kepatuhan dengan peraturan Inggris seperti Regulation (EC) 853/2004. Tanpa sertifikasi, fasilitas berisiko kontaminasi, ketidakpatuhan, dan masalah kualitas produk. Berikut adalah gambaran singkat dari prosesnya:
- Mengapa Sertifikasi Penting: Mencegah kontaminasi mikroba, selaras dengan prinsip HACCP, dan memastikan produksi yang konsisten.
- Standar Utama: ISO 14644-1 (kebersihan udara), EU GMP Annex 1 (produksi steril), dan EN 17141 (kontrol mikroba).
-
Langkah-langkah Menuju Sertifikasi:
- Desain dan Bangun: Pasang filter HEPA, sistem aliran udara, dan pertahankan perbedaan tekanan yang tepat.
- Kualifikasi Instalasi (IQ): Verifikasi bahwa ruang bersih sesuai dengan spesifikasi desain.
- Kualifikasi Operasional (OQ): Uji kinerja dalam kondisi terkontrol.
- Kualifikasi Kinerja (PQ): Validasi fungsionalitas selama operasi aktual.
- Monitoring Berkelanjutan: Pemeriksaan rutin untuk partikel, tekanan, suhu, dan kelembaban.
- Kepatuhan Berkelanjutan: Rekualifikasi setiap 6–12 bulan atau setelah perubahan besar.
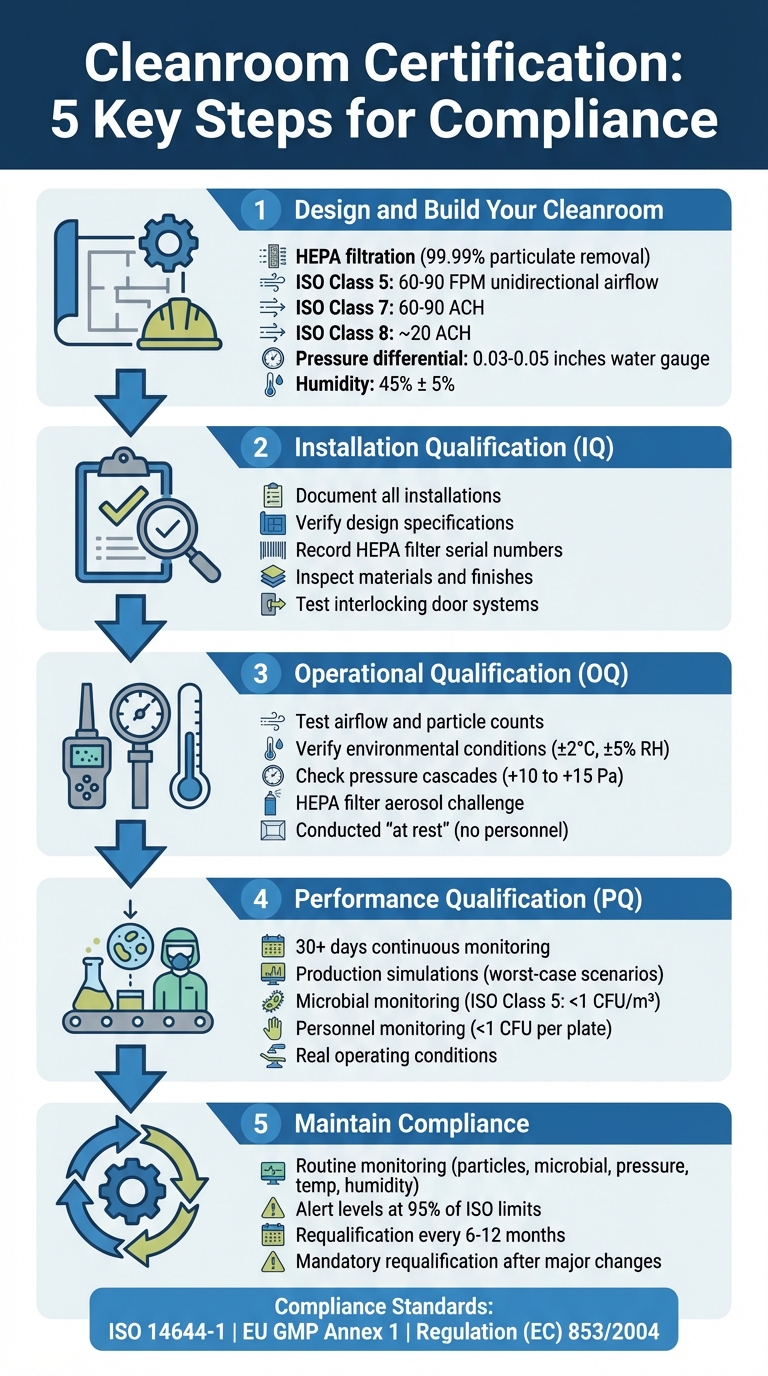
Proses Sertifikasi Ruang Bersih 5 Langkah untuk Fasilitas Daging Budidaya
Desain dan Sertifikasi Ruang Bersih
Langkah 1: Desain dan Bangun Ruang Bersih Anda
Membangun ruang bersih untuk produksi daging budidaya memerlukan perencanaan yang cermat seputar tiga sistem utama: filtrasi HEPA, kontrol lingkungan, dan pemisahan alur kerja. Elemen-elemen ini memastikan kondisi steril dan membantu Anda menghindari modifikasi yang mahal di kemudian hari.Setelah sistem ini terpasang, fokus pada mengoptimalkan kinerjanya selama instalasi.
Persyaratan Filtrasi HEPA dan Aliran Udara
Sistem penanganan udara adalah tulang punggung dari ruang bersih Anda dan menentukan apakah memenuhi klasifikasi ISO yang diperlukan. Filter HEPA menghilangkan 99,99% partikel[5], tetapi efektivitasnya tergantung pada pengiriman udara pada tingkat dan pola tertentu yang disesuaikan untuk setiap zona produksi.
Untuk area Kelas ISO 5 - di mana proses aseptik seperti pemanenan daging terjadi - Anda memerlukan aliran udara searah (laminar) pada 60 hingga 90 kaki per menit (FPM) [5]. Ini melibatkan unit filter kipas yang dipasang di langit-langit (FFU) yang mengarahkan aliran udara melalui ventilasi dinding rendah dengan sudut pelepasan yang sempit.
Di zona Kelas ISO 7 dan 8, desain aliran udara campuran digunakan. Di sini, udara suplai segar bercampur dengan udara internal, memerlukan lebih sedikit perubahan udara per jam (ACH).Zona ISO Kelas 7 memerlukan 60–90 ACH, sedangkan zona ISO Kelas 8 memerlukan sekitar 20 ACH[1][6]. Untuk menghitung ACH, bagi volume udara suplai (per jam) dengan volume ruangan. Ingatlah bahwa langit-langit yang lebih tinggi meningkatkan baik permintaan aliran udara maupun biaya[3].
Diferensial tekanan adalah kunci untuk menjaga kontaminan keluar. Pertahankan diferensial tekanan positif sebesar 0.03–0.05 inci water gauge antara ruang bersih dan area sekitarnya [7]. Namun, jangan melebihi 0.1 inci water gauge di seluruh pintu, karena ini dapat membuatnya sulit dibuka - memerlukan hingga 11 pon gaya pada pintu standar berukuran 3×7 kaki[7].
Setelah pemasangan, uji sistem filtrasi untuk integritas menggunakan tes tantangan aerosol seperti pengujian DOP atau PAO untuk memastikan tidak ada kebocoran atau segel lemah di rumah filter HEPA[1].Studi visualisasi asap juga dapat membantu memverifikasi aliran udara laminar dan memastikan tidak ada turbulensi atau aliran balik di zona sensitif.
Dengan adanya filtrasi, langkah berikutnya adalah memastikan kondisi lingkungan yang konsisten.
Kontrol Lingkungan untuk Produksi
Mempertahankan suhu, kelembaban, dan tekanan yang stabil sangat penting untuk meminimalkan risiko mikroba[9]. Sistem HVAC Anda harus terus-menerus menjaga parameter ini sambil mendukung tingkat perubahan udara yang tinggi yang diperlukan untuk klasifikasi ISO ruang bersih Anda.
Kontrol suhu sangat penting. Sistem harus mengatasi panas dari bioreaktor, pencahayaan, dan personel tanpa mengganggu pola aliran udara. Kelembaban relatif harus tetap pada 45% ± 5%, yang membantu mencegah muatan elektrostatik yang menarik partikel dan menghindari masalah kondensasi. Rentang ini juga memastikan lingkungan kerja yang nyaman bagi staf yang mengenakan gaun[7].
Monitoring parameter lingkungan secara real-time seperti pH dan oksigen terlarut dapat membantu mendeteksi tanda-tanda awal pertumbuhan mikroba[9]. Pemantauan terus-menerus terhadap udara, permukaan, dan air adalah praktik penting lainnya untuk menangkap kontaminasi sebelum meningkat. Selain itu, rancang sistem HVAC Anda untuk waktu pemulihan yang singkat - ini memastikan ruang bersih cepat kembali ke tingkat kebersihan yang ditentukan setelah kejadian kontaminasi, mengurangi waktu henti[1].
Setelah kontrol lingkungan diterapkan, fokuslah pada pengelolaan bagaimana bahan dan orang bergerak melalui ruang untuk meminimalkan risiko kontaminasi.
Mengelola Aliran Material dan Personel
"Pekerja cleanroom adalah sumber kontaminasi terbesar di cleanroom dan semua proses kritis harus diisolasi dari pintu akses personel dan jalur." - Vincent A. Sakraida, Insinyur[7]
Personel adalah risiko kontaminasi terbesar di cleanroom, melepaskan partikel kulit, rambut, dan puing-puing lainnya[7][6]. Untuk mengatasi hal ini, tata letak cleanroom Anda harus secara fisik memisahkan proses kritis dari area lalu lintas tinggi dan titik akses.
Material harus bergerak dalam satu arah - dari zona dengan tingkat lebih rendah ke zona dengan tingkat lebih tinggi - menggunakan proses desinfeksi atau sterilisasi yang telah divalidasi sepanjang jalan[8].Sterilisasi dua ujung, seperti autoklaf pintu ganda atau terowongan depirogenasi, ideal untuk memindahkan barang ke area pemrosesan aseptik tanpa mengorbankan kualitas udara[8].
Ruang udara berfungsi sebagai penyangga antara area dengan tingkat kebersihan yang berbeda. Zona ISO Kelas 7 atau lebih bersih harus mencakup ruang depan untuk mengenakan pakaian, yang mencegah kontaminan luar masuk ke area produksi[6]. Untuk zona Kelas A dan B, sistem pintu pengunci memastikan bahwa hanya satu pintu yang dapat dibuka pada satu waktu[8]. Jika ruang udara terpisah untuk personel dan material tidak memungkinkan, pemisahan berbasis waktu prosedural dapat membantu menghindari pergerakan simultan antara zona[8].
Batasi ruang kritis ke satu titik akses untuk mengurangi risiko kontaminasi silang[7].Jendela observasi atau kamera jarak jauh dapat memungkinkan pengawas untuk memantau aktivitas tanpa memasuki ruang bersih, mengurangi akses yang tidak perlu[8].
Setiap langkah ini memainkan peran penting dalam mencapai sertifikasi ruang bersih dan memastikan fasilitas Anda memenuhi standar ketat yang diperlukan untuk produksi daging budidaya yang aman dan sesuai.
Langkah 2: Selesaikan Kualifikasi Instalasi (IQ)
Setelah konstruksi selesai, langkah berikutnya adalah Kualifikasi Instalasi (IQ). Proses ini memastikan bahwa setiap komponen ruang bersih telah dipasang dengan benar sebelum melanjutkan ke pengujian operasional. Pada dasarnya, IQ bertindak sebagai jembatan antara penyelesaian konstruksi fisik dan memulai penyeimbangan HVAC, mengonfirmasi bahwa semuanya siap untuk fase berikutnya.
"Pemeriksaan Kualifikasi Instalasi (IQ) memastikan bahwa peralatan, komponen, dan pengaturan ruang bersih sesuai dengan spesifikasi pabrikan dan bahwa semuanya telah dipasang dengan benar." - Kjeld Lund, Spesialis Ruang Bersih [11]
IQ berfokus pada keadaan "sebagaimana dibangun" - ketika struktur ruang bersih selesai tetapi peralatan produksi belum dipasang. Tujuan utamanya di sini adalah untuk memastikan bahwa apa yang telah dibangun sesuai dengan desain asli, dengan setiap penyimpangan didokumentasikan dan ditangani dengan benar.
Dokumentasikan Semua Langkah Instalasi
Dokumentasi yang menyeluruh sangat penting selama fase ini. Anda memerlukan catatan as-built yang terperinci, yang mencakup gambar arsitektur yang diperbarui, daftar peralatan HVAC, urutan kontrol, dan diagram pengkabelan listrik. Catatan ini harus mencerminkan bagaimana ruang bersih sebenarnya dibangun, bukan hanya bagaimana direncanakan.
Untuk setiap filter HEPA atau ULPA, catat nomor seri, lokasi tepat, dan tanggal pemasangan. Sangat penting untuk memeriksa filter dari kerusakan selama pengiriman segera setelah pemasangan - karena bahkan kebocoran kecil dapat mengkompromikan integritas ruang bersih. Tandai setiap peralatan dan sensor dengan ID unik yang sesuai dengan daftar peralatan Anda, mempermudah audit dan pemeliharaan di masa depan.
Sertifikat kalibrasi untuk semua instrumen pemantauan juga harus disimpan. Ini termasuk penghitung partikel, sensor tekanan diferensial, probe suhu dan kelembaban, dan perangkat aliran udara. Seperti yang dijelaskan oleh Toni Horsfield dari ISO Cleanroom, "Sertifikat kalibrasi [untuk penghitung partikel] disertakan dalam laporan validasi ruang bersih Anda." [10]
Inspeksi bahan dan hasil akhir sama pentingnya. Verifikasi bahwa panel dinding, lantai, pintu, pass-through, dan sealant memenuhi standar GMP.Permukaan harus tidak mudah mengelupas, rendah VOC, dan disegel dengan baik. Pintu dan jendela harus rata dengan dinding untuk menjaga integritas tekanan.
Simpan log deviasi untuk setiap variasi desain, mencatat penilaian dan tindakan korektif yang diambil. Log ini nantinya akan menjadi bagian dari laporan validasi akhir Anda, mengkonsolidasikan semua temuan dari fase instalasi.
Verifikasi Spesifikasi Desain
Setelah catatan instalasi Anda lengkap, langkah berikutnya adalah memastikan bahwa setiap sistem sesuai dengan desain yang disetujui. Lakukan cross-reference Spesifikasi Kebutuhan Pengguna (URS) dengan instalasi fisik untuk memastikan tidak ada yang terlewatkan selama pengiriman atau perakitan.
Untuk sistem HVAC dan filtrasi, periksa bahwa unit penanganan udara, sambungan saluran, dan posisi diffuser sesuai dengan gambar desain. Pastikan bahwa filter HEPA terpasang dengan benar di dalam rumahnya dan bahwa semua uji tekanan saluran udara telah berhasil diselesaikan. Catat spesifikasi dan lembar data untuk setiap unit filter kipas.
Verifikasi struktural mencakup inspeksi interlock, airlock, dan pass-through untuk memastikan mereka berfungsi sebagaimana mestinya. Uji sistem pintu interlock untuk memastikan bahwa kedua pintu tidak dapat terbuka pada saat yang sama. Periksa bahwa semua segel utuh dan bahwa ruang bersih dapat mempertahankan perbedaan tekanan yang diperlukan.
Jalankan sistem HVAC untuk mencapai kondisi steady-state sebelum melanjutkan ke tahap pengujian berikutnya.
Melakukan IQ dengan presisi sangat penting, karena ini menjadi dasar untuk semua tahap kualifikasi berikutnya. Melewatkan langkah atau terburu-buru dalam dokumentasi dapat menyebabkan komplikasi selama pengujian operasional dan audit regulasi. Dengan menyelesaikan pemeriksaan ini secara menyeluruh, Anda memastikan transisi yang mulus ke kualifikasi operasional.
Langkah 3: Lakukan Kualifikasi Operasional (OQ)
Setelah Kualifikasi Instalasi memastikan bahwa semuanya terpasang dengan benar, langkah berikutnya adalah Kualifikasi Operasional (OQ). Fase ini memastikan ruang bersih Anda beroperasi sesuai yang diharapkan dalam kondisi yang ditentukan. Biasanya, tes ini dilakukan "saat istirahat", artinya sistem HVAC berjalan, tetapi tidak ada staf atau aktivitas produksi yang berlangsung.
"Validasi memberikan bukti objektif bahwa ruang bersih melakukan apa yang dirancang untuk dilakukan: mempertahankan atmosfer yang stabil dan bebas kontaminan baik dalam kondisi statis (saat istirahat) maupun operasional." - Standard Tech [12]
Pengujian OQ sangat penting untuk menunjukkan kepatuhan terhadap standar ISO 14644-1 dan GMP. Untuk fasilitas daging yang dibudidayakan, langkah ini sangat penting karena proses biologis bergantung pada kontrol partikel dan mikroba yang ketat.Untuk memastikan hasil yang akurat, stabilkan ruang bersih selama setidaknya 30 menit sebelum memulai pengujian untuk menghindari jumlah partikel yang menyimpang [12]. Pemeriksaan ini membangun fase instalasi, meletakkan dasar untuk penyempurnaan kontrol lingkungan Anda.
Uji Aliran Udara dan Jumlah Partikel
Penghitungan partikel udara adalah dasar dari klasifikasi ISO. Menggunakan penghitung partikel laser yang terkalibrasi, ukur konsentrasi partikel di udara untuk memastikan kepatuhan dengan kelas ISO yang diperlukan. Untuk ISO Kelas 5, lihat batas partikel yang ditentukan dalam tabel standar.
Jumlah lokasi pengambilan sampel tergantung pada ukuran ruang bersih. ISO 14644-1 memberikan pedoman yang jelas: ruangan yang lebih besar memerlukan lebih banyak titik pengambilan sampel, diatur dalam pola grid [16]. Jika Anda menguji dua hingga sembilan lokasi, Anda perlu menghitung Batas Kepercayaan Atas 95% (UCL) untuk menentukan kepatuhan.Untuk sepuluh atau lebih titik pengambilan sampel, perhitungan ini tidak diperlukan [15].
Pengukuran kecepatan dan volume aliran udara memastikan bahwa tingkat pergantian udara Anda memenuhi spesifikasi desain. Gunakan anemometer untuk mengukur kecepatan di berbagai titik, terutama di dekat area proses kritis, dan konfirmasikan bahwa nilai-nilai ini sesuai dengan target desain Anda.
Studi asap menawarkan cara visual untuk memeriksa arah aliran udara, memastikan bergerak dari zona yang lebih bersih ke yang kurang bersih. Hasilkan asap di dekat pintu, pass-through, dan area rentan lainnya untuk mendeteksi kebocoran atau turbulensi yang dapat mengganggu aliran udara [12]. Meskipun penghitung partikel akurat, studi asap dapat mengungkapkan masalah seperti zona stagnan yang mungkin tidak terdeteksi.
Filter HEPA dan ULPA juga harus divalidasi ulang selama OQ. Gunakan tantangan aerosol untuk memeriksa kebocoran pada filter atau segelnya.Bahkan kesalahan instalasi kecil dapat mengurangi kinerja, jadi selalu lakukan pengujian ulang setelah perawatan atau penggantian filter [12].
Setelah kinerja aliran udara dikonfirmasi, fokus beralih ke kondisi lingkungan yang mempengaruhi kualitas produk dan kenyamanan operator.
Verifikasi Kondisi Lingkungan
Suhu dan kelembaban memainkan peran penting dalam menjaga kualitas produk dan memastikan lingkungan kerja yang nyaman. Untuk fasilitas daging budidaya, target validasi biasanya ±2°C untuk suhu dan ±5% untuk kelembaban relatif [12]. Pemantauan terus-menerus selama setidaknya 24 jam direkomendasikan, karena pemeriksaan sesaat mungkin melewatkan fluktuasi yang dapat mempengaruhi validasi [12].
Ruang bersih untuk daging budidaya biasanya mempertahankan rentang suhu 18–22°C dan kelembaban relatif antara 30–60% [14]. Kondisi ini mendukung proses kultur sel sambil mencegah kondensasi, yang dapat mendorong pertumbuhan mikroba. Gunakan sensor termal yang dikalibrasi dan probe RH yang ditempatkan di seluruh ruang bersih untuk mengidentifikasi variasi kondisi.
Tekanan kaskade adalah faktor kritis lainnya. Ini memastikan bahwa aliran udara bergerak dari area yang lebih bersih ke area yang kurang bersih, mengurangi risiko kontaminasi. Verifikasi perbedaan tekanan - umumnya +10 hingga +15 Pa antara ruangan yang bersebelahan - menggunakan pengukur yang dikalibrasi. Lakukan pengukuran di pintu dan pass-through dalam kondisi steady-state untuk mengonfirmasi hubungan tekanan yang tepat [12].
Pengujian waktu pemulihan mengukur seberapa cepat ruang bersih kembali sesuai setelah kejadian kontaminasi. Perkenalkan sumber partikel yang terkontrol, lalu pantau berapa lama waktu yang dibutuhkan agar jumlah partikel kembali ke baseline.Waktu pemulihan yang lebih cepat menunjukkan desain aliran udara yang lebih baik dan kontrol kontaminasi yang lebih efektif [1].
Untuk menghindari penundaan atau pengujian ulang yang mahal, kalibrasi semua instrumen segera sebelum pengujian OQ. Catat semua detail yang relevan, termasuk tanggal, waktu, lokasi, ID instrumen, dan kondisi lingkungan untuk setiap pengujian. Dokumentasi ini penting untuk laporan validasi Anda dan akan diperlukan selama audit regulasi [12].
sbb-itb-ffee270
Langkah 4: Lakukan Kualifikasi Kinerja (PQ)
Kualifikasi Kinerja (PQ) mengevaluasi kinerja ruang bersih Anda dalam kondisi produksi nyata, dengan peralatan berjalan dan staf yang aktif bekerja [1][12].Membangun pada Kualifikasi Instalasi dan Operasional, PQ memberikan konfirmasi bahwa ruang bersih berfungsi secara konsisten dan andal selama operasi aktual.
"PQ memvalidasi kinerja ruang bersih dalam kondisi operasi aktual, termasuk operasi peralatan dan aktivitas personel." - G-CON [1]
Untuk memastikan pengujian yang menyeluruh, fase PQ harus mencakup setidaknya 30 hari pemantauan terus-menerus. Kerangka waktu yang diperpanjang ini membantu mengidentifikasi variasi, seperti fluktuasi suhu selama siklus produksi atau perubahan kontaminasi mikroba akibat pergerakan staf, yang mungkin terlewatkan oleh pengujian yang lebih singkat. Untuk fasilitas daging yang dibudidayakan, di mana kontrol kontaminasi yang ketat sangat penting, PQ menawarkan bukti terdokumentasi bahwa ruang bersih tetap patuh selama operasi rutin.
Jalankan Simulasi Produksi
Simulasi produksi harus mereplikasi skenario terburuk.Ini mungkin termasuk kapasitas maksimum, operasi simultan dari semua peralatan, dan risiko kontaminasi sementara seperti pembukaan pintu yang sering atau pergerakan intens [1][13]. Pendekatan berbasis risiko, seperti menggunakan Analisis Mode Kegagalan dan Efek (FMEA), dapat membantu mengidentifikasi lokasi pengambilan sampel berdasarkan risiko kontaminasi, aliran material, dan area dengan lalu lintas tinggi [16].
Monitoring mikroba selama simulasi ini sangat penting. Unit pembentuk koloni (CFU) harus dilacak menggunakan metode pengambilan sampel aktif dan pasif [14][17]. Untuk ruang bersih Kelas ISO 5, batas tindakan untuk kontaminasi mikroba umumnya adalah 1 CFU/m³ [14].
Karena manusia adalah sumber partikel terbesar di ruang bersih, pemantauan personel sama pentingnya.Pengambilan sampel ujung jari dengan sarung tangan dapat mengonfirmasi teknik aseptik yang tepat, dengan batas yang dapat diterima kurang dari 1 CFU per pelat [17]. Operator harus diberi pengarahan tentang protokol berpakaian dan pergerakan sebelumnya untuk mencegah lonjakan buatan dalam tingkat kontaminasi [12].
Selain itu, uji seberapa cepat ruang bersih pulih setelah tantangan partikel yang terkontrol. Perkenalkan sumber partikel dan ukur waktu yang dibutuhkan untuk kondisi kembali ke baseline. Proses ini mengevaluasi aliran udara dan efektivitas sistem pengendalian kontaminasi [1][12].
Set Up Environmental Monitoring
Setelah pengujian simulasi, pemantauan lingkungan yang berkelanjutan memastikan kinerja yang konsisten.Sistem ini menyediakan data real-time tentang parameter kritis seperti partikel udara, kontaminasi mikroba, suhu, kelembaban, dan perbedaan tekanan. Ini penting untuk mendeteksi perubahan kinerja sebelum menyebabkan masalah kepatuhan [1]. Untuk produksi daging budidaya, pemantauan berkelanjutan sangat diperlukan.
Selama fase kualifikasi, lakukan pengambilan sampel udara mikroba setiap 1–2 jam di zona kritis untuk mengonfirmasi kontrol kontaminasi yang efektif [14]. Gunakan Tryptic Soy Agar (TSA) untuk mendeteksi bakteri, inkubasi sampel pada suhu 30–35°C selama minimal tiga hari, dan Sabouraud Dextrose Agar (SAB) untuk jamur dan kapang, inkubasi pada suhu 20–25°C selama setidaknya tujuh hari [17]. Hindari penggunaan semprotan aerosol atau disinfektan di dekat pengambil sampel udara selama pengujian.Jika desinfektan rotasi atau alkohol isopropil 70% telah diterapkan, tunggu setidaknya lima menit sebelum memulai pengambilan sampel udara [17].
Tetapkan batas peringatan dan tindakan yang jelas untuk semua parameter yang dipantau. Tingkat peringatan menandakan perlunya investigasi ketika nilai mulai menyimpang, sementara batas tindakan menuntut tindakan korektif segera jika parameter melebihi rentang yang dapat diterima [14]. Simpan catatan terperinci dari setiap pengukuran, termasuk tanggal, waktu, lokasi, detail instrumen, dan kondisi lingkungan. Ini memastikan Anda selalu siap untuk audit dan dapat menunjukkan kepatuhan dengan standar ISO 14644 dan GMP.
Langkah 5: Mempertahankan Kepatuhan Melalui Pemantauan
Setelah Anda menyelesaikan Kualifikasi Kinerja, pekerjaan tidak berhenti di situ. Mempertahankan kepatuhan memerlukan pemantauan terus-menerus dan kualifikasi ulang secara berkala.Sertifikasi ruang bersih bukanlah pencapaian satu kali - ini menuntut upaya konsisten untuk menjaga fasilitas Anda dalam "keadaan terkendali." Untuk fasilitas daging yang dibudidayakan, proses berkelanjutan ini memastikan Anda memenuhi standar regulasi dan operasional, memperluas praktik teliti dari fase kualifikasi ke dalam operasi harian.
Menerapkan Pemantauan Rutin
Untuk memastikan ruang bersih Anda tetap sesuai dengan standar ISO 14644 dan GMP, Anda perlu memantau kontaminan mikroba dan partikel secara teratur. Parameter kunci yang perlu diperhatikan meliputi:
- Jumlah partikel
- Tingkat mikroba
- Tekanan
- Suhu
- Kelembaban
- Aliran udara
Frekuensi pemantauan harus sesuai dengan klasifikasi ruang bersih Anda dan penilaian risiko yang menyeluruh.Sebagai contoh, zona Kelas ISO 5 sering memerlukan pemantauan partikel secara terus-menerus atau setiap jam selama produksi, sementara area yang kurang kritis mungkin hanya memerlukan pemeriksaan harian atau mingguan.
Tetapkan tingkat peringatan pada 95% dari batas ISO untuk menangkap potensi masalah lebih awal. Tingkat ini bertindak sebagai peringatan ketika parameter mulai menyimpang, mendorong investigasi sebelum mereka meningkat. Di sisi lain, batas tindakan menuntut tindakan korektif segera jika parameter melebihi rentang yang dapat diterima [14] .
Bagian penting lainnya dari pemantauan adalah pengambilan sampel ujung jari bersarung tangan (GFS). Metode ini memastikan personel mempertahankan teknik aseptik yang tepat. Kriteria standar biasanya kurang dari 1 CFU per pelat [17]. Melakukan GFS setelah tugas aseptik kritis atau di akhir setiap shift membantu mengidentifikasi dan mengatasi kekurangan dalam teknik lebih awal.
Sementara pemantauan rutin membantu menjaga kontrol harian, kualifikasi ulang memastikan sistem ruang bersih Anda tetap efektif dalam jangka panjang.
Jadwalkan Kualifikasi Ulang
Kualifikasi ulang harus dilakukan setiap 6 hingga 12 bulan. Namun, peristiwa tertentu membuat kualifikasi ulang menjadi wajib, seperti renovasi struktural, pemasangan peralatan baru, penggantian filter HEPA, atau perubahan signifikan pada sistem HVAC [1][14].
Selama kualifikasi ulang, banyak dari tes pada fase Kualifikasi Operasional perlu diulang. Ini termasuk:
- Penghitungan partikel di udara
- Pengujian integritas filter HEPA (membuktikan efisiensi 99,99% untuk partikel ≥0.3 mikron)
- Pengukuran kecepatan aliran udara
- Pemeriksaan perbedaan tekanan
Salah satu pengujian yang sangat penting adalah pengujian waktu pemulihan, yang mengukur seberapa cepat ruang bersih kembali ke tingkat kebersihan target setelah kejadian kontaminasi. Pengujian ini memverifikasi kemampuan sistem HVAC Anda untuk menangani tekanan secara efektif [1].
Simpan Rencana Induk Validasi (VMP) untuk mendokumentasikan semua tahap kualifikasi (IQ, OQ, PQ) dan jadwal re-kualifikasi Anda. Pastikan semua instrumen yang digunakan untuk pengujian - seperti penghitung partikel dan anemometer - dikalibrasi dan memiliki sertifikat yang dapat dilacak ke standar nasional [1] [14]. Ini memastikan akurasi dan keandalan dalam upaya kepatuhan Anda.
Sumberkan Peralatan Cleanroom untuk Kepatuhan
Temukan Pemasok Terverifikasi di Cellbase
Setelah standar operasional dan kinerja cleanroom Anda ditetapkan dan divalidasi, langkah berikutnya adalah mendapatkan peralatan yang tepat untuk menjaga kepatuhan. Untuk produksi daging budidaya, ini berarti bekerja dengan pemasok yang memahami tuntutan unik industri ini.
Pastikan Pengadaan Sesuai GMP
Setelah memverifikasi peralatan, proses pengadaan juga harus memenuhi standar GMP yang ketat.
Selain itu, platform ini memprioritaskan bahan yang memenuhi persyaratan GMP. Misalnya, bahan konstruksi seperti 316L stainless steel dengan permukaan yang dipoles dan tidak mudah terkelupas disorot. Bahan-bahan ini tahan terhadap desinfeksi kimia berulang dan mendukung protokol Cleaning-in-Place (CIP) dan Sterilisation-in-Place (SIP) yang tervalidasi [4]. Dengan memverifikasi kompatibilitas bahan sejak awal, Anda dapat menghindari retrofit yang mahal atau siklus rekuifikasi di kemudian hari. Pendekatan proaktif ini membantu menjaga kepatuhan sambil menghemat waktu dan sumber daya.
Kesimpulan
Poin Penting
Mencapai sertifikasi cleanroom sangat penting untuk menjaga kualitas produk dan memenuhi standar regulasi. Ini dimulai dengan merancang cleanroom yang dilengkapi dengan filtrasi HEPA, aliran udara yang terkontrol, dan aliran material yang efisien. Proses ini dilanjutkan dengan pendekatan kualifikasi tiga tahap: Installation Qualification (IQ), Operational Qualification (OQ), dan Performance Qualification (PQ). Tahap-tahap ini memastikan bahwa semua sistem beroperasi secara efektif dalam kondisi kerja yang sebenarnya.
Sertifikasi tidak berakhir di situ. Pemantauan berkelanjutan terhadap faktor-faktor seperti suhu, kelembaban, tekanan, dan jumlah partikel sangat penting untuk mengidentifikasi masalah kinerja. Revalidasi rutin memastikan kepatuhan dengan ISO 14644-1 dan standar GMP, menciptakan kerangka kerja yang solid untuk perbaikan di masa depan.
Langkah Selanjutnya untuk Fasilitas Anda
Untuk menyelaraskan fasilitas Anda dengan standar ini, pertimbangkan untuk mengembangkan Rencana Induk Validasi (VMP). Rencana ini mengintegrasikan proses kualifikasi dengan kebutuhan operasional harian, membantu Anda tetap di depan tuntutan regulasi [1]. Selain itu, menerapkan sistem manajemen keamanan pangan berbasis HACCP adalah kunci. Setidaknya satu anggota tim harus dilatih hingga Level 4 dalam prinsip-prinsip HACCP untuk memastikan kepatuhan [2].
Untuk kebutuhan peralatan, beralihlah ke
FAQ
Apa manfaat sertifikasi cleanroom untuk produksi daging budidaya?
Sertifikasi cleanroom memainkan peran penting dalam produksi daging budidaya dengan memastikan kepatuhan terhadap standar keselamatan dan lingkungan yang ketat. Cleanroom bersertifikat dirancang untuk meminimalkan risiko kontaminasi dari mikroba dan partikel, menjaga kondisi steril yang penting untuk pembudidayaan sel. Ini tidak hanya melindungi kualitas dan keamanan produk akhir tetapi juga memastikan kepatuhan dengan standar yang diakui secara internasional seperti klasifikasi ISO dan tingkat GMP - persyaratan utama untuk persetujuan regulasi dan penerimaan pasar.
Di luar kepatuhan, sertifikasi meningkatkan keandalan operasional dengan memvalidasi sistem kritis seperti aliran udara, filtrasi, dan pemantauan lingkungan. Sistem-sistem ini bekerja sama untuk mengurangi risiko kontaminasi, memungkinkan produksi yang konsisten dan meningkatkan efisiensi proses secara keseluruhan.Sebuah ruang bersih bersertifikat juga menanamkan kepercayaan di antara para pemangku kepentingan, menyederhanakan inspeksi regulasi, dan mendukung upaya skala dengan menunjukkan kepatuhan terhadap praktik terbaik dalam mengelola lingkungan terkendali.
Seberapa sering ruang bersih harus dikualifikasi ulang untuk memastikan kepatuhan?
Ruang bersih perlu dikualifikasi ulang secara teratur untuk memastikan mereka memenuhi standar industri. Seberapa sering hal ini terjadi tergantung pada beberapa faktor, termasuk klasifikasi ruang bersih, bagaimana penggunaannya, dan temuan dari penilaian risiko atau rencana pemantauan lingkungan.
Biasanya, kualifikasi ulang dilakukan setahun sekali. Namun, lingkungan berisiko tinggi atau situasi yang melibatkan perubahan besar - seperti peningkatan peralatan atau penyesuaian tata letak - mungkin memerlukan pemeriksaan yang lebih sering. Pemantauan kinerja yang berkelanjutan juga penting untuk memverifikasi bahwa aliran udara, filtrasi, dan kontrol lingkungan terus memenuhi standar yang diperlukan.
Faktor lingkungan apa yang perlu dipantau di ruang bersih untuk produksi daging budidaya?
Untuk memastikan kepatuhan dan mengurangi risiko kontaminasi di fasilitas daging budidaya, penting untuk memantau beberapa faktor lingkungan dengan cermat. Ini termasuk jumlah partikel, kontaminasi mikroba, pola aliran udara, perbedaan tekanan udara, temperatur, dan tingkat kelembaban. Pemantauan rutin elemen-elemen ini membantu mempertahankan standar GMP dan menciptakan lingkungan terkendali yang penting untuk produksi.
Dengan mengelola kondisi ini dengan hati-hati, fasilitas dapat melindungi kualitas produk sambil memenuhi kriteria ketat yang diperlukan untuk sertifikasi ruang bersih.











