Protokol validasi memastikan produksi daging budidaya aman, konsisten, dan memenuhi standar regulasi. Tanpa langkah pemanasan untuk membunuh patogen, kesterilan harus dijaga di setiap tahap. Protokol ini berfokus pada:
- Validasi peralatan: Memastikan bioreaktor dan sistem sterilisasi berfungsi dengan benar.
- Validasi bahan: Memverifikasi media pertumbuhan dan input lainnya steril dan berkualitas tinggi.
- Validasi proses: Mempertahankan teknik aseptik dan kontrol lingkungan.
Dengan mengatasi risiko seperti kontaminasi mikroba dan salah identifikasi garis sel, protokol ini membantu produsen memenuhi standar dari organisasi seperti FDA dan EFSA. Perusahaan seperti UPSIDE Foods dan Aleph Farms telah mencapai persetujuan regulasi dengan mengikuti langkah-langkah ini. Alat seperti analisis HACCP, pengujian sterilitas, dan dokumentasi pihak ketiga sangat penting untuk kepatuhan dan kepercayaan konsumen.
Platform seperti
Mitigasi Risiko dalam Produksi Daging Budidaya
Faktor Risiko Utama
Transisi dari penelitian laboratorium ke produksi skala besar membawa beberapa tantangan, dengan tiga risiko yang menonjol. Kekhawatiran yang paling mendesak adalah kontaminasi mikroba yang disebabkan oleh agen adventif. Ini menuntut langkah-langkah sterilitas yang ketat di setiap tahap produksi untuk memastikan keamanan.
Masalah besar lainnya adalah kesalahan identifikasi garis sel. Ini telah menjadi masalah lama dalam penelitian ilmiah, di mana garis sel yang salah label atau terkontaminasi silang telah menyebabkan hasil yang cacat. Dalam konteks daging yang dibudidayakan, kesalahan semacam itu dapat menghasilkan produk yang tidak sesuai dengan spesies atau jenis jaringan yang dimaksudkan, memicu masalah keamanan dan regulasi. Selain itu, hasil yang tidak konsisten selama peningkatan skala kultur sel dapat mengganggu proses manufaktur komersial.
"Untuk kelayakan komersial, daging yang dibudidayakan memerlukan pendekatan yang diinformasikan secara ilmiah untuk mengidentifikasi dan mengelola bahaya dan risiko." – Nature Food [4]
Bagaimana Protokol Validasi Mengelola Risiko
Untuk mengatasi risiko ini, protokol validasi dirancang khusus untuk menangani setiap ancaman. Dengan meminjam dari bioteknologi farmasi, protokol ini menetapkan kerangka kerja kontrol kualitas yang kuat.Sebagai contoh, mereka menggabungkan metode berbasis ICH Q5A untuk secara proaktif mengidentifikasi dan menghilangkan risiko kontaminasi virus. Alih-alih menunggu kontaminasi terjadi, langkah-langkah ini berfokus pada pencegahan melalui karakterisasi garis sel yang mendetail, pembuatan bank sel kelas makanan, dan pemantauan berkelanjutan terhadap titik kontrol kritis.
Kontaminasi mikroba dikelola dengan pengujian sterilitas yang ketat dan pengawasan berkelanjutan. Sementara itu, kesalahan identifikasi garis sel diatasi dengan proses karakterisasi yang menyeluruh dan protokol perbankan yang aman.
Bagian penting dari pendekatan ini adalah penilaian keamanan pra-pasar, yang mendokumentasikan setiap aspek produksi. Perusahaan seperti UPSIDE Foods dan GOOD Meat mencapai persetujuan regulasi penuh di Amerika Serikat pada tahun 2023 dengan menyajikan dokumen keamanan yang mendetail yang mematuhi protokol validasi ini.Demikian pula, Aleph Farms memperoleh persetujuan regulasi pertama di dunia untuk daging sapi yang dibudidayakan pada awal 2024 dengan mengikuti standar dokumentasi yang sebanding [4]. Protokol ini tidak hanya memenuhi otoritas regulasi - seperti FDA, Singapore Food Agency, dan Food Standards Australia New Zealand - tetapi juga memastikan konsistensi dari batch ke batch, yang sangat penting untuk keberhasilan komersial.
Strategi manajemen risiko ini meletakkan dasar untuk komponen validasi yang dibahas di bagian berikutnya.
sbb-itb-ffee270
Praktik Validasi dan Verifikasi untuk Industri Makanan
Komponen Inti dari Protokol Validasi
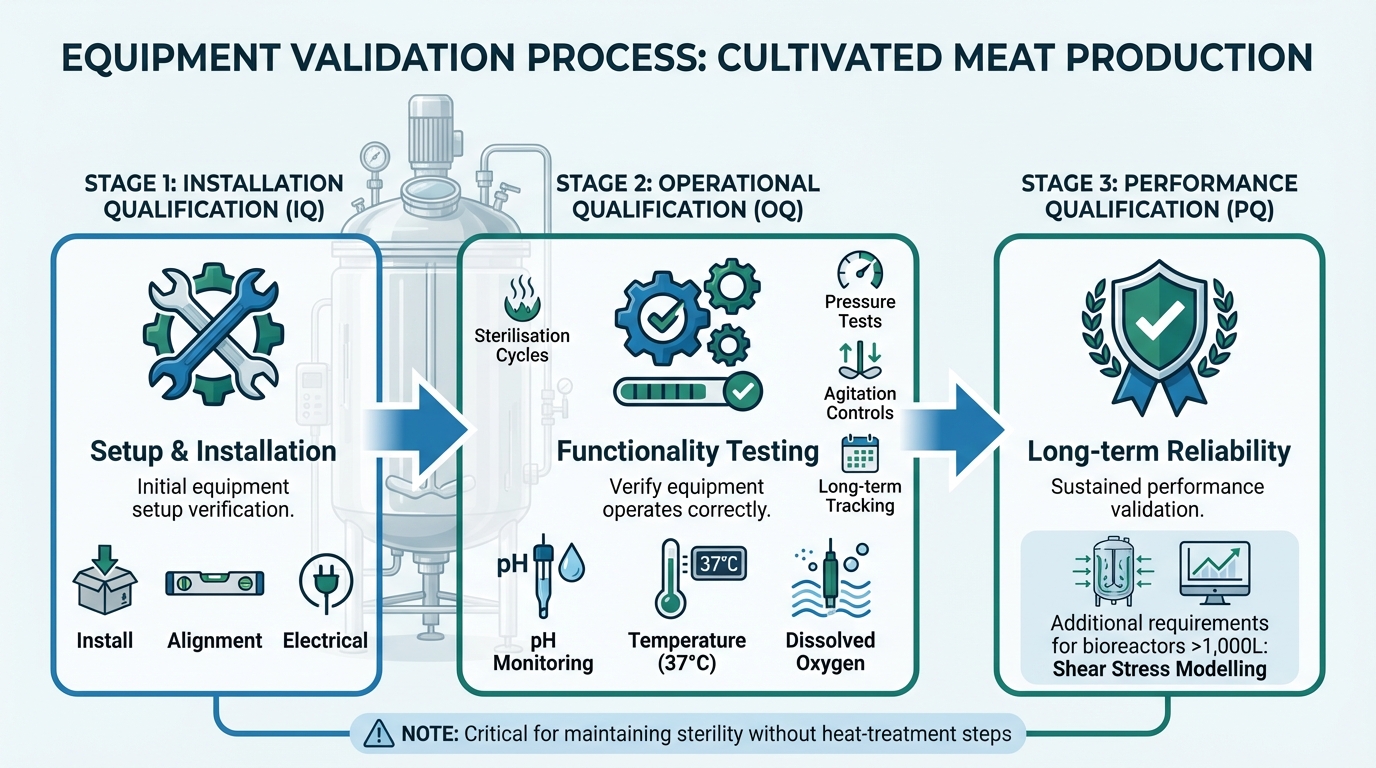
Proses Validasi Peralatan Tiga Tahap untuk Produksi Daging Budidaya
Protokol validasi dalam produksi daging budidaya dibangun di atas tiga area kunci - peralatan, bahan, dan proses - untuk memastikan kesterilan dan konsistensi tanpa langkah pembunuhan tradisional [1]. Komponen-komponen ini membentuk pendekatan terstruktur untuk menjaga produksi bebas kontaminasi.
Validasi Peralatan
Validasi peralatan terjadi dalam tiga tahap: Kualifikasi Instalasi (IQ) untuk pengaturan, Kualifikasi Operasional (OQ) untuk fungsionalitas, dan Kualifikasi Kinerja (PQ) untuk keandalan jangka panjang.Untuk bioreaktor, ini melibatkan validasi siklus sterilisasi, uji tekanan, dan kontrol agitasi. Sensor perlu kalibrasi yang cermat untuk memantau pH, suhu (37°C), dan oksigen terlarut secara real time [2]. Menggunakan alat yang dirancang khusus daripada peralatan farmasi standar dapat meningkatkan akurasi dan keandalan [2].
Permukaan diseka, dan air bilasan diuji baik sebelum maupun sesudah digunakan. Selain itu, siklus sterilisasi, kondisi penyimpanan, sertifikat pemasok, dan tanggal kedaluwarsa harus didokumentasikan dengan teliti [1]. Untuk bioreaktor yang lebih besar (lebih dari 1.000 liter), validasi juga harus menangani pemodelan tegangan geser untuk memastikan bahwa kekuatan mekanis tidak merusak sel mamalia yang halus, langkah penting dalam mencegah kontaminasi, yang tetap menjadi tantangan signifikan [5].
Validasi Bahan
Setelah peralatan divalidasi, bahan yang digunakan dalam proses harus diperiksa untuk kualitas dan konsistensi. Media pertumbuhan, misalnya, dianalisis menggunakan High-Performance Liquid Chromatography (HPLC) dan spektrometri massa untuk mengkonfirmasi profil nutrisinya [3]. Penyaringan residu menggunakan metode sensitif seperti ELISA atau LC-MS/MS untuk mendeteksi antibiotik dan hormon, memastikan mereka tidak mencemari produk akhir [3]. Scaffold diuji untuk kemandulan dan kompatibilitas bahan untuk menghindari pencucian, sementara pengurutan genom memastikan garis sel tetap stabil secara genetik. Catatan keterlacakan juga dipertahankan untuk melacak setiap komponen dalam rantai pasokan media [3].
Pengujian residu antibiotik sangat penting, karena daging yang dibudidayakan tidak memiliki langkah memasak yang biasanya menghilangkan kontaminan.Proses pencucian hilir harus menghilangkan semua antibiotik dan faktor pertumbuhan. Beberapa sampel dari setiap batch diuji terhadap batas residu maksimum (MRLs) menggunakan metode LC-MS/MS yang tervalidasi, dan sertifikat analisis mengonfirmasi bahwa residu berada di bawah tingkat yang dapat dideteksi [3]. Tingkat transparansi ini dan verifikasi pihak ketiga membantu memenuhi standar regulasi dan membangun kepercayaan konsumen.
Validasi Proses
Validasi proses memastikan bahwa alur kerja kultur sel dan bioproses secara konsisten memberikan hasil bebas kontaminasi. Ini melibatkan pengujian kemandulan, studi pemulihan menggunakan organisme indikator, pengujian mikroba, dan pemantauan faktor kunci seperti kondisi kultur sel, kualitas media, dan kinerja bioreaktor [1][2]. Pengambilan sampel diselaraskan dengan fase pertumbuhan dan siklus pemberian makan, berfokus pada area berisiko tinggi seperti persiapan media dan koneksi bioreaktor [1][2].
Uji reproduktibilitas dengan beberapa operator membantu mengidentifikasi potensi ketidakkonsistenan [1]. Studi pemulihan menggunakan organisme indikator untuk menguji sensitivitas deteksi, sementara semua proses terintegrasi dengan HACCP titik kendali kritis. Ini termasuk pengujian mikroba, analisis lipid, dan penilaian masa simpan di setiap tahap untuk memastikan pemrosesan bio yang aman dan konsisten [1][2]. Dokumentasi komprehensif - mencakup pelatihan personel, foto validasi, log penyimpangan, dan tanda tangan tinjauan - menciptakan jejak audit lengkap untuk tujuan regulasi dan jaminan kualitas [1].
Langkah Implementasi untuk Protokol Validasi
Membangun komponen penting dari validasi, berikut adalah cara untuk mengimplementasikan protokol yang efektif langkah demi langkah.
Melakukan Analisis HACCP
Mulailah analisis HACCP dengan membentuk tim ahli yang beragam di berbagai bidang seperti sumber sel, isolasi, proliferasi, pemanenan, keamanan pangan, dan pemeliharaan fasilitas. Untuk memenuhi persyaratan regulasi, pastikan setidaknya satu anggota tim memiliki pelatihan HACCP Level 4. Mulailah dengan mendefinisikan dengan jelas ruang lingkup produk, umur simpan yang diharapkan, kemasan, dan target audiens.
Selanjutnya, rancang diagram alur proses yang menguraikan setiap tahap, dari isolasi sel hingga produk akhir. Sertakan semua input - seperti media kultur dan faktor pertumbuhan - dan output seperti limbah dan produk sampingan. Kategorikan bahaya menjadi empat jenis utama:
- Biologis: Risiko seperti kontaminasi mikroba
- Kimia: Sisa dari antibiotik, faktor pertumbuhan, atau reagen
- Fisik: Potensi fragmen logam, plastik, atau kaca
- Alergenik: Risiko kontak silang dari komponen media
Gunakan pohon keputusan untuk mengidentifikasi Titik Kendali Kritis (CCP) dan tetapkan batas yang dapat diukur (e.g. , suhu, pH, waktu) untuk mengelola bahaya ini secara efektif. Tinjau dan perbarui rencana HACCP setidaknya setiap tahun atau setiap kali ada perubahan pada produk, proses, atau peralatan.
Menyusun Sistem Pemantauan dan Pencegahan
Setelah bahaya dan CCP diidentifikasi, langkah berikutnya adalah membangun sistem pemantauan dan koreksi yang kuat.
Tentukan protokol pemantauan Anda dengan menentukan metode, frekuensi, tanggung jawab, dan jenis data yang akan dicatat. Untuk sistem otomatis, pemantauan terus-menerus harus dilengkapi dengan pemeriksaan peralatan terjadwal. Sebaliknya, sistem manual memerlukan pemeriksaan yang disesuaikan dengan skala dan risiko operasi. Seperti yang dijelaskan oleh Food Standards Agency:
"Pemantauan dapat sesederhana atau sekompleks langkah yang diperlukan. Ini bisa berupa pemeriksaan visual, atau dilakukan melalui penggunaan instrumen pengukuran tertentu" [6].
Tugaskan peran ganda di mana satu orang melakukan pemantauan dan orang lain memverifikasi pemeriksaan. Jika CCP berulang kali gagal, lakukan analisis akar penyebab untuk mengidentifikasi dan menyelesaikan masalah mendasar. Terapkan rencana tindakan korektif tiga tahap untuk memulihkan kontrol, menangani produk yang terpengaruh, dan mencegah masalah serupa di masa depan.Kalibrasi rutin instrumen dan audit berkala sangat penting untuk memastikan sistem pemantauan tetap efektif.
Dokumentasi dan Verifikasi Kepatuhan
Untuk mematuhi peraturan Inggris untuk daging budidaya, pertahankan dokumentasi yang teliti untuk HACCP, SOP, dan catatan pemantauan. Berdasarkan Regulation (EC) 853/2004, daging budidaya diklasifikasikan sebagai Produk Asal Hewan (POAO), yang memerlukan kepatuhan terhadap standar kebersihan tertentu. Atur dokumentasi Anda ke dalam tiga bagian utama:
- Rencana HACCP: Sertakan daftar tim, ruang lingkup, diagram alur proses, dan analisis bahaya.
- Dokumen Kebijakan: Meliputi Prosedur Operasi Standar, kebijakan kebersihan, dan program prasyarat.
- Catatan: Pertahankan log untuk pemantauan, tindakan korektif, hasil tes, dan kalibrasi instrumen.
Gunakan sistem kontrol versi untuk dokumen fisik dan digital untuk memastikan semua staf memiliki akses ke prosedur terbaru. Validasi rencana HACCP sebelum implementasi dan verifikasi efektivitasnya setelahnya. Lakukan pemeriksaan internal setidaknya sekali setahun, terlepas dari adanya masalah. Jika tindakan korektif diambil, dokumentasikan analisis akar penyebab secara menyeluruh. Seperti yang disoroti oleh Badan Standar Makanan:
"Operator bisnis makanan harus menempatkan, menerapkan, dan memelihara prosedur permanen atau prosedur berdasarkan prinsip-prinsip HACCP" [6].
Dokumentasi yang komprehensif tidak hanya memastikan kepatuhan terhadap peraturan tetapi juga mempersiapkan operasi Anda untuk audit. Praktik-praktik ini juga membuka jalan untuk mendapatkan sumber daya yang tervalidasi melalui platform seperti
Menggunakan Cellbase untuk Pengadaan Sumber Daya Validasi
Bagaimana Cellbase Mendukung Validasi
Setelah rencana HACCP dan sistem pemantauan Anda diterapkan, mengamankan peralatan dan bahan yang telah divalidasi menjadi langkah berikutnya. Di sinilah
Yang membedakan
Pemasok di
"Ketika Anda membangun alur kerja kultur sel untuk produksi daging budidaya, persyaratannya berubah. Sertifikasi tingkat makanan. Struktur biaya dioptimalkan untuk produksi komersial, bukan anggaran penelitian" [7].
Pendekatan yang sangat terkurasi ini memastikan kepatuhan sambil merampingkan proses pengadaan.
Keuntungan Pengadaan Melalui Cellbase
Proses pengadaan tradisional sering memperlambat produksi.
Pemasok di
Kesimpulan
Protokol validasi adalah dasar dari produksi daging budidaya dengan aman dan dalam skala besar, menangani risiko biologis, kimia, dan fisik sambil memastikan kepatuhan dengan peraturan Inggris.Seperti yang dijelaskan oleh Food Safety and Inspection Service, "Validasi adalah proses untuk menunjukkan bahwa sistem HACCP yang dirancang dapat mengendalikan bahaya yang teridentifikasi secara memadai untuk menghasilkan produk yang aman" [8] . Tanpa dukungan ilmiah yang menyeluruh dan penerapan praktis, sistem produksi tidak dapat memenuhi standar ketat yang ditetapkan oleh FSA dan FSS.
Untuk menerapkan protokol ini, peralatan, bahan, dan sistem pemantauan yang telah divalidasi sangat penting.
Transisi ke bahan-bahan berkualitas makanan adalah tonggak penting untuk kesuksesan komersial. Dengan daftar yang dipilih dengan cermat oleh
Seiring berjalannya program regulatory sandbox di Inggris hingga Februari 2027, didukung oleh pendanaan pemerintah sebesar £1,6 juta [9], ada peluang unik untuk menetapkan protokol validasi yang kuat.
FAQ
Apa risiko validasi terbesar saat meningkatkan produksi daging budidaya?
Saat meningkatkan produksi daging budidaya, dua tantangan utama menonjol: pengendalian kontaminasi dan konsistensi proses.
Kontaminasi menjadi ancaman yang lebih besar seiring dengan peningkatan skala produksi. Operasi yang lebih besar meningkatkan risiko kontaminasi, yang dapat menyebabkan kegagalan batch yang mahal. Untuk meminimalkan hal ini, menjaga kesterilan, mengkualifikasi bahan baku, dan mengelola kondisi lingkungan sangatlah penting.
Konsistensi dalam proses produksi adalah faktor penting lainnya. Parameter seperti tingkat pH dan kepadatan sel harus tetap dalam batas ketat untuk memastikan produk akhir memenuhi standar kualitas dan regulasi. Membangun protokol yang terperinci dan ketat sangat penting untuk mengelola risiko ini dan mencapai proses produksi yang dapat diskalakan dan andal.
Bagaimana IQ, OQ, dan PQ diterapkan pada bioreaktor dalam daging budidaya?
Dalam produksi daging budidaya, validasi bioreaktor melibatkan tiga langkah penting: Installation Qualification (IQ), Operational Qualification (OQ), dan Performance Qualification (PQ). Masing-masing memainkan peran kunci dalam memastikan operasi yang lancar dan sesuai.
- Installation Qualification (IQ): Langkah ini memverifikasi bahwa bioreaktor dipasang dengan benar, sesuai dengan pedoman pabrikan dan persyaratan regulasi. Ini tentang memastikan fondasi yang kuat sebelum melangkah lebih jauh.
- Operational Qualification (OQ): Setelah dipasang, bioreaktor perlu membuktikan bahwa ia dapat berfungsi sesuai harapan. Ini melibatkan pengujian di bawah kondisi tertentu, seperti menjaga suhu dan tingkat pH yang tepat, untuk memastikan semuanya berfungsi sebagaimana mestinya.
- Kualifikasi Kinerja (PQ): Langkah terakhir adalah tentang konsistensi. Di sini, fokusnya adalah memastikan bioreaktor berfungsi dengan andal selama proses produksi aktual, memenuhi tuntutan manufaktur daging budidaya.
Dengan mengikuti langkah-langkah ini, produsen dapat mengurangi risiko, menjaga kepatuhan, dan menciptakan fondasi yang kuat untuk produksi yang dapat diskalakan dan berkualitas tinggi. Alat seperti
Bukti apa yang diharapkan regulator dalam dokumen keamanan pra-pasar?
Regulator mengharapkan perusahaan untuk memberikan bukti identifikasi bahaya , penilaian risiko, dan penerapan langkah-langkah pengendalian. Ini melibatkan pemeliharaan dokumentasi yang teliti, mencakup segala sesuatu mulai dari detail bahan baku hingga validasi proses dan pengujian keamanan.Catatan yang jelas dan komprehensif tidak hanya menunjukkan kepatuhan terhadap peraturan keselamatan tetapi juga memainkan peran penting dalam mendapatkan persetujuan untuk produk daging budidaya.











