無血清培地のスケーリングは高価ですが、賢い戦略でコストを大幅に削減できます。 主な費用は、FGF-2やTGF-βのような成長因子から来ており、これが培地コストの大部分を占めています。例えば、 Essential 8のような配合では、これらが総価格の98%を占めています。産業規模では、これらのタンパク質の少量でもバッチごとに数千ポンドの費用がかかることがあります。
主なポイントは以下の通りです:
- 成長因子がコストを押し上げる: これらのタンパク質は最も高価な培地成分です。
- 大量購入が助けになる: 大量購入と粉末培地の使用でコストを最大77%削減できます。
- 食品グレード vs 医薬品グレード: 食品グレードの成分は安価ですが、汚染のリスクがあります。
- プロセスの調整で節約: 培地の再利用や配合の最適化で廃棄物と費用を削減します。
Dr. Peter Stogios: 無血清培地のための低コスト成長因子
無血清培地の主なコスト要因
無血清培地は、培養肉生産における変動運用コストの半分以上を占める可能性があり、オペレーションの拡大における重要な課題となっています[1]。しかし、すべての成分がこれらのコストに等しく寄与するわけではありません。最も高価な成分を特定することは、ラボスケールから商業生産に移行するために重要です。
コストの大部分は成長因子と組換えタンパク質から来ています。これらの生物活性分子、例えばFGF-2、TGF-β、インスリン、アルブミン、トランスフェリンは、微量で必要とされますが、高価です。一方で、塩類、アミノ酸、ビタミン、緩衝液などの基礎培地成分は比較的安価です。成分のグレード(医薬品グレード対食品グレード)もコストに影響を与えますが、組換えタンパク質は依然として最も高価な部分です。
成長因子と組換えタンパク質
Good Food Instituteによると、無血清培地のコストは1リットルあたり約£317(約$400)で、通常のプロセスでは生産ごとに数千ポンド相当の培地が必要です[2]。
特定の配合を見てみると、コストの分布が明らかになります。例えば、Essential 8では、FGF-2とTGF-βが総コストの約98%を占めています[1]。Beefy-9では、アルブミン、FGF-2、インスリンが約60%を占めています[1][3]。
Beefy-9の配合を例にとると、FGF-2の基準濃度が40 ng/mLの場合、培地のコストは1リットルあたり£172(約$217)です。FGF-2の濃度を5 ng/mLに減らすと、コストは1リットルあたり£150(約$189)に下がります。大量購入と粉末培地への切り替えで、コストをさらに下げることができます。例えば、大量購入し粉末の基礎培地を使用すると、高濃度のFGF-2の場合は1リットルあたり£59(約$74)、低濃度の場合は1リットルあたり£36(約$46)にコストが下がります[3]。
衛星細胞用の商業用無血清培地は、通常1リットルあたり£159から£397(約$200–500)の範囲です[3]。比較すると、血清を含む培地(BSC-GM)は、非バルク量で購入した場合、1リットルあたり約230ポンド(約1リットルあたり290ドル)のコストがかかります。これは、企業が成長因子の使用を最適化し、細胞性能を犠牲にすることなくバルク割引を確保すれば、血清不使用の製剤が競争力を持ち、場合によってはより安価であることを示しています。
成長因子がコストを支配する一方で、基礎成分のグレードも全体的なコスト効率において重要な役割を果たします。
食品グレード vs 医薬品グレードの成分
成長因子を超えて、基礎成分の品質グレードはコストに大きな影響を与えます。医薬品グレードの成分は、厳格な純度基準を満たすために生産され、厳密なエンドトキシン試験を受け、詳細な認証が付属しており、これらすべてが価格を押し上げます。一方、食品グレードの成分ははるかに安価ですが、品質の一貫性がないリスクがあります。
Spechtによる研究は、コストの違いを強調しています。食品グレードの基礎成分は、1 kgスケールで医薬品グレードのものより約82%安価です[1]。医薬品グレードの成分を食品グレードの代替品に置き換えることで、基礎培地のコストを最大77%削減できます[1]。数千リットルの培地を使用する大規模生産では、食品グレードの材料が必要な性能と安全基準を満たしている限り、かなりのコスト削減が可能です。
しかし、食品グレードの成分を使用するリスクを無視することはできません。例えば、コンドロイチン硫酸とグルコサミンを含む10種類の市販食品サプリメントを調査した研究では、いずれも正確な宣言濃度を含んでいないことが判明しました。すべてのサンプルにケラタン硫酸の汚染が見られ、ほとんどが細胞アッセイで細胞毒性を示しました[1]。これは、バッチ間の変動、予期しない汚染物質、細胞の性能に影響を与えたり、安全性の懸念を引き起こす可能性のあるエンドトキシンの定期的な検査の欠如を含む、食品グレードのサプライチェーンの潜在的な課題を強調しています。
| コンポーネントタイプ | 平均コスト削減 | 純度 & 基準 | リスク & 課題 |
|---|---|---|---|
| 医薬品グレード | ベースライン(高コスト) | 高純度、エンドトキシン検査済み、認証済み | 変動が少ないが、価格が高い |
| 食品グレード | 1 kgスケールで82%安価; 基礎培地コストが77%削減 | 純度が低い; エンドトキシンの定期的な検査なし | バッチの変動、潜在的な汚染物質 (e.g.ケラタン硫酸の細胞毒性) |
培養肉セクターの企業にとって、医薬品グレードと食品グレードの成分を選択する際には、コスト削減と品質保証のバランスを取ることが重要です。多くの企業は、可能な限り食品グレードの基礎成分を使用しつつ、医薬品グレードの組換えタンパク質を使用するハイブリッド戦略を選択しています。このような場合、組成試験や汚染物質分析などの強力な品質管理手段が不可欠です。
大規模なメディアコスト削減方法
血清不使用メディアのコスト削減は、賢いリサイクル技術や大量購入戦略を通じて達成でき、これにより経費を大幅に削減できます。
メディアのリサイクルと廃棄物削減
メディアのリサイクルは、使用済みメディアから貴重な成分を回収することを含みます。超ろ過のような技術は、成長因子、アミノ酸、その他の高価な分子を抽出し、それらを再利用可能にします。この方法は、大規模なバイオリアクターのセットアップで20〜30%のコスト削減につながる可能性があります[1]。
しかし、リサイクルされたメディアには課題もあります。副産物が蓄積したり、pHの変化が起こったり、栄養素が枯渇することがあります。新しいメディアと同様に効果的に機能するためには、厳格なテストが不可欠です。正しく行われれば、企業は細胞の生存率に影響を与えることなく、廃棄物を最大50%削減することができます[1][3]。さらに、リアルタイムの栄養センサー、横流ろ過、最適化された給餌戦略などのツールを使用することで、廃棄物をさらに20〜40%削減することができます[1][5]。
大量購入とサプライヤーネットワーク
大量購入は、リサイクルの取り組みを補完し、メディアコストを削減するもう一つの実証済みの方法です。
大量購入は、1リットルあたりのコストを大幅に下げることができます[3]。このアプローチは規模の経済を活用し、注文サイズが大きくなるにつれて単価を下げます。しかし、大量購入の成功は、品質が損なわれないようにするための強力なサプライヤー関係に依存します。
信頼できるサプライヤーネットワークはここで重要な役割を果たします。彼らは、培養肉生産に特化した競争力のある価格設定と大量購入オプションへのアクセスを提供します。例えば、
sbb-itb-ffee270
プロセスの改善と処方の精緻化
メディアの処方を微調整することで、かなりのコスト削減が可能です。秘密は、成分をランダムに入れ替えて最善を期待するのではなく、細胞の性能を維持しながら処方を体系的にテストし調整することにあります。この方法は、コスト効率と信頼性のある細胞成長の両方を達成するプロトコルの最適化への道を自然に開きます。
難しいのは、コスト削減と生物学的成果の維持の間で適切なバランスを取ることです。濃度を調整することでリットルあたりのコストを削減できますが、これらの節約を細胞収量の効率と比較検討することが重要です。例えば、成分濃度を減らしてメディアコストを下げることは、細胞の成長が損なわれた場合、細胞収量あたりのコストを逆に増加させる可能性があります。調整を行う際は、常に細胞収量あたりのコストに注目してください。
同様に重要なのは、メディアの処理方法を改善することです。例えば、熱に敏感な成長因子に対して、熱滅菌から無菌ろ過に切り替えることで、劣化と廃棄を最小限に抑えることができます。他のステップとしては、塩類や緩衝液を先に溶解し、ビタミンや成長因子を低温で穏やかに混合することで、さらに廃棄を減らすことができます。生産を2段階に分け、まずバルクの基礎メディアを作成し、使用直前に濃縮サプリメントを追加することで、バッチが損なわれた場合の損失を防ぐこともできます[1][3]。これらの調整は、実験計画法(DoE)を用いた体系的なメディア最適化の基盤を築きます。
メディア最適化のための実験計画法 (DoE)
実験計画法 (DoE) は、無限の試行錯誤に頼ることなく、配合を洗練するための構造化された方法を提供します。DoE を使用すると、1つの成分を調整する代わりに、アミノ酸、グルコース、FGF‑2、インスリン、アルブミン濃度などの複数の要因を同時にテストできます。このアプローチにより、これらの成分がどのように相互作用し、成長率、存続率、分化に影響を与えるかが明らかになります[1][4]。
プロセスは通常、分数因子計画やプラケット–バーマン法などのスクリーニング計画から始まり、パフォーマンスに真に影響を与える成分を特定します。これらの主要な要因が特定されると、応答曲面法を使用してより複雑な相互作用を探ります。これにより、コストのかかる成分の使用を削減しながら、細胞のパフォーマンスを維持する配合を特定するのに役立ちます。例えば、濃度の削減と大量調達を組み合わせることで、1リットルあたりのコストを£46–74/Lに引き下げました。これは、血清含有培地と比較して約75%の削減です [3]。DoEを廃棄物削減や大量購入などの以前の戦略と統合することで、全体的な培地コストを効果的に管理できます。
食品グレードの原料を使用する場合、バッチ間での変動が多いため、DoEはさらに価値があります。品質を犠牲にすることなく、変動成分の許容範囲を確立するのに役立ちます。英国のチームにとって、
コスト内訳の例: 無血清培地の配合
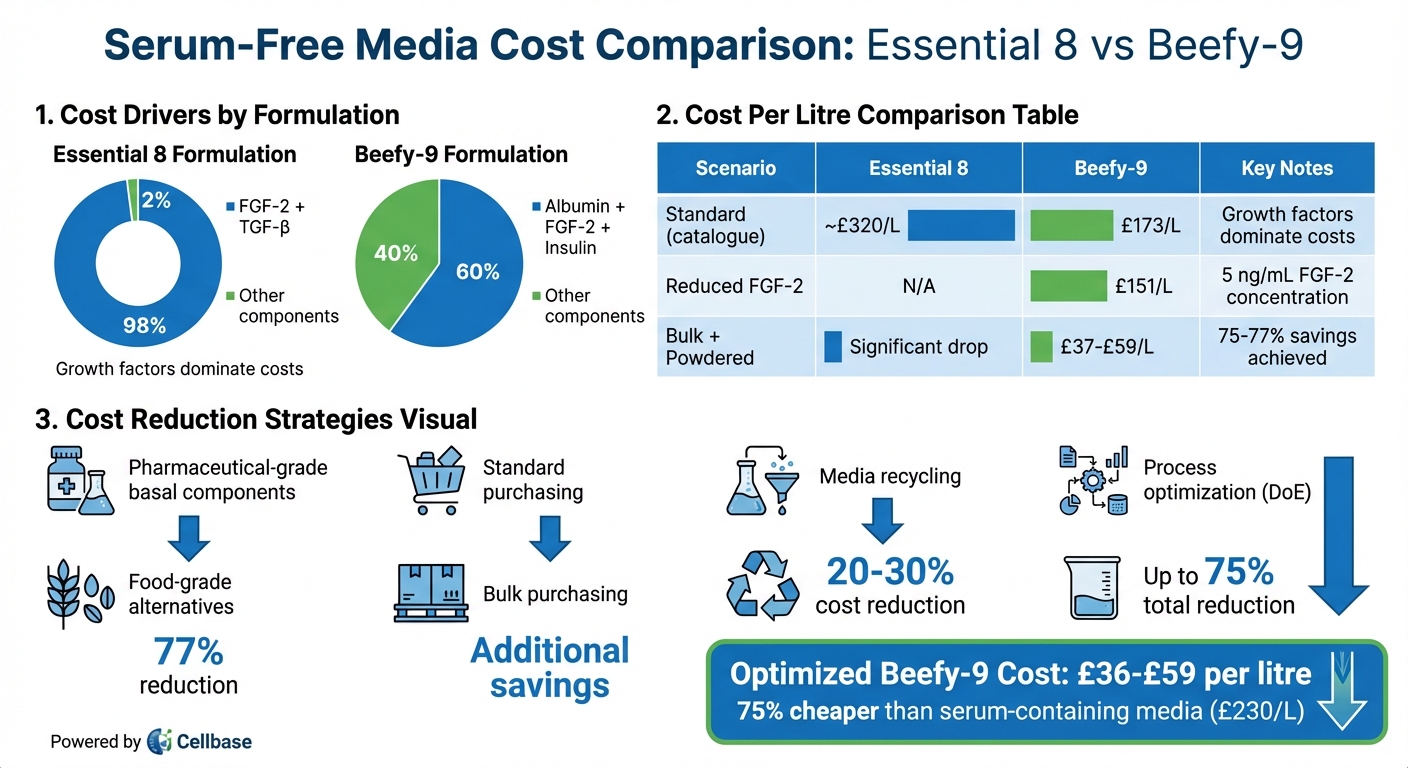
無血清培地のコスト内訳: Essential 8 対 Beefy-9 の配合
コスト比較: Essential 8 対 Beefy-9 メディア
無血清培地の配合のコストダイナミクスを掘り下げ、2つの例、Essential 8 (E8) と Beefy-9 に焦点を当てます。これらの例は、成長因子のコストと調達戦略が培養肉生産に使用される培地の全体的な費用にどのように影響するかを明らかにします。
Essential 8は、多能性幹細胞に一般的に使用され、特定の成長因子がそのコスト構造において支配的であることを示しています。1リットルあたりのコストのほぼ98%がFGF-2とTGF-βから来ています[1]。これは、細胞収量に関連するコスト効率を理解するための優れたケーススタディとなります。
一方で、Beefy-9は、ウシ衛星細胞用に設計された無血清培地であり、異なるコスト内訳を示しています。ここでは、組換えアルブミン、FGF-2、およびインスリンが総コストの約60%を占めています[1][3]。特に、FGF-2の濃度を下げることで、全体の費用を大幅に削減できます。例えば、チームがバルク購入と粉末状の基礎培地を選択した場合、FGF-2のレベルが高いときのBeefy-9のコストは1リットルあたり約£59に下がり、FGF-2のレベルを下げると1リットルあたり£37まで低下します。これは、同様のバルクスケールでの血清含有培地と比較して、驚くべき75%の削減を表しています[3]。
以下の表は、異なる購入および製剤シナリオにおけるリットルあたりのコストの変動をまとめたものです:
| シナリオ | Essential 8 (£/L) | Beefy‑9 (£/L) | 重要な注意点 |
|---|---|---|---|
| 標準(カタログ) | ~320 | 173 | FGF‑2/TGF‑βがE8の98%を占める; アルブミン/FGF‑2/インスリンがBeefy‑9の60%を構成 [1][3] |
| FGF‑2削減 | N/A | 151 | Beefy‑9に5 ng/mLのFGF‑2 [3] |
| バルク/粉末 | 大幅な減少 | 37–59 | バルクおよび食品グレードの代替品で75–77%の節約 [1][3] |
これらの節約は魅力的ですが、トレードオフを考慮することが重要です。Beefy-9のリットルあたりの低コストは、必ずしも全体の生産コストの低下を意味するわけではありません。その細胞成長の遅さは、バイオマス1キログラムあたりの費用を増加させる可能性があります。これは、培養肉の生産において重要な要素であり、最終的な目標は培地の価格だけでなく、バイオマス1キログラムあたりのコストを最適化することです。
英国でコンポーネントを大規模に調達するチームにとって、
影響力のあるアプローチの一つは、医薬品グレードの成分を食品グレードの代替品に置き換えることで、基礎コストを最大77%削減することができます [1]。バルク購入は、リットルあたりの費用を下げることでさらにコストを削減します。メディアのリサイクル、廃棄物の削減、改良された配合方法などの技術によって、材料と労働コストを最小限に抑えることができ、追加の節約が可能です[1]。実験計画法(DoE)を使用することは、チームが高価な成分の最小有効濃度を特定するのに役立つもう一つの効果的なツールです。これにより、細胞の性能を維持しながら高価な成長因子への依存を減らすことができます[1]。
よくある質問
血清フリーメディアで食品グレードの成分を使用する際に、コストと品質のバランスを取る最良の方法は何ですか?
コストを管理しながら品質を犠牲にしないために、企業は厳しい安全性と品質基準を満たす食品グレードの成分を使用することに焦点を当てるべきです。廃棄物を削減し、生産効率を向上させるための調整は、製品性能を維持しながら経費を削減するのにも役立ちます。
信頼できる、検証済みのサプライヤーと協力することは、一貫した品質を確保するための鍵です。
大規模生産における無血清培地のリサイクルのリスクと利点は何ですか?
大規模生産における無血清培地のリサイクルは、 利点と課題の両方を提供します。良い点としては、新しい培地の必要性を減らし、廃棄物を最小限に抑えることでコストを削減し、より持続可能なシステムを作る努力と一致します。これらの利点により、培養肉の生産において魅力的な選択肢となります。
とはいえ、克服すべき課題もあります。リサイクルは、汚染や代謝副産物の蓄積などのリスクを引き起こし、細胞の成長や製品の全体的な品質に悪影響を及ぼす可能性があります。さらに、培地の繰り返し使用は、必須栄養素の枯渇を招き、時間とともにその効果を低下させる可能性があります。これらの落とし穴を避けつつ、その可能性を最大限に活用するためには、強力なプロセス管理と信頼性の高い監視システムの導入が重要です。
実験計画法(DoE)を使用することで、血清不使用培地の開発におけるコストをどのように削減できますか?
実験計画法(DoE)は、パフォーマンスに最も影響を与える要因を特定することで、血清不使用培地の開発におけるコストを賢く削減する方法を提供します。長時間の試行錯誤プロセスに頼る代わりに、研究者はこの方法を使用して、より正確かつ効率的に配合を洗練することができます。
調整を簡素化し、無駄なリソースを削減することで、DoEは材料コストを節約するだけでなく、開発のタイムラインを加速します。これにより、培養肉セクターにおける無血清培地の生産拡大にとって非常に貴重なアプローチとなります。











