- 目的: バイオリアクターが規制および生産基準を満たし、無菌状態、正確な環境制御、食品安全を維持することを保証します。
- 主な特徴: 攪拌槽型バイオリアクターは、牛の筋細胞に適しており、制御されたせん断力とスケーラビリティを提供するために選ばれました。
- 課題: 高密度の細胞を扱うためのバイオリアクターのスケーリングとコスト削減には、材料、滅菌方法、プロセス設計の再考が必要でした。
- 解決策: 食品グレードの材料への切り替え、コスト効果の高い滅菌方法の使用、プロセス最適化のための機械学習の統合により、コストが大幅に削減されました。
- 結果: 生産コストは£437,000/kgから£1.95/kgに低下し、生産性が15倍に向上し、再生可能エネルギーで稼働する場合、温室効果ガス排出量が最大92%削減されました。
この研究は、検証プロトコルとスマートな設計選択が、培養肉を従来の肉と価格の均衡に近づけている方法を概説しています。
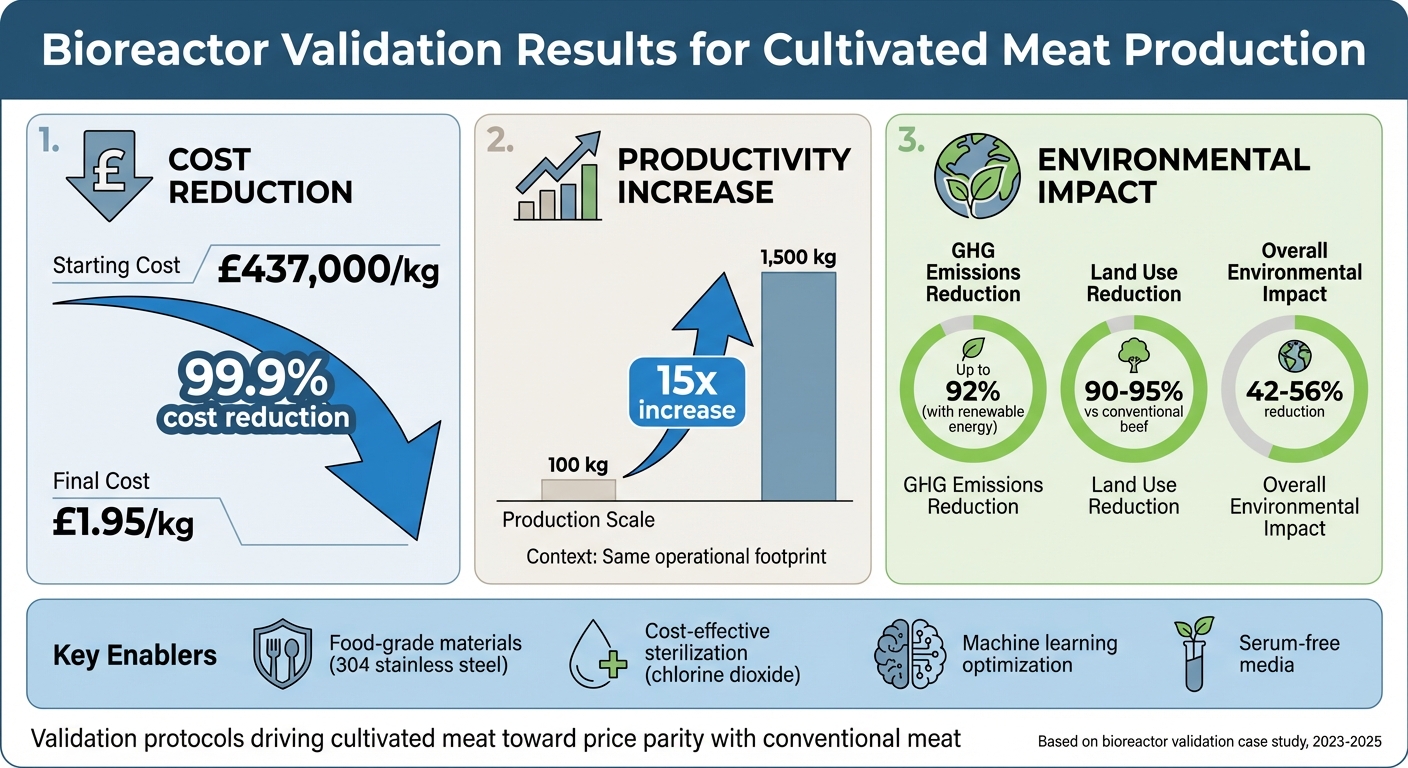
バイオリアクターの検証の影響:培養肉生産におけるコスト削減と環境への利点
バイオリアクター検証のための規制要件
適用される規制基準
培養肉産業において、厳格な規制基準を満たすことは、バイオリアクター検証プロセスの重要な部分です。イギリスでは、食品基準庁(FSA)とスコットランド食品基準庁(FSS)が培養肉を「動物由来製品」(POAO)として分類しています。この分類により、バイオリアクターの運用を含むすべての生産段階で食品安全と衛生規制が適用されることが保証されます。ただし、英国のガイダンス(2025年12月)によれば、これらの製品はPOAOカテゴリーに該当するものの、法的には「肉」としては認められていません。この区別により、特定の従来の動物福祉および微生物学的要件が除外され、英国で必要とされる特定の検証プロトコルが形成されます。
世界的に見て、安全性評価の期間はさまざまです。シンガポールとアメリカ合衆国では通常12か月以内にレビューが完了しますが、欧州連合では平均して約18か月かかります。英国は独自の道を切り開き、2027年2月まで資金提供されるCCPサンドボックスプログラムを実施しています。このイニシアチブにより、規制当局はGourmey, Hoxton Farms, およびMosa Meat, などの企業と直接協力し、データ要件を合理化し、安全性評価を迅速化することができます。
"サンドボックスプログラムは、安全基準を損なうことなく、新興の食品技術に対する障壁を減らすために、規制に関する知識を迅速に取得することを可能にしています。"
– Dr. Thomas Vincent, Deputy Director of Innovation, FSA [3]
管轄区域に関係なく、企業は市場に参入する前に詳細な安全性に関する書類を提出しなければなりません。これらの書類には、生産プロセス、製品の構成、安全性データが記載されています。また、培養肉が従来の肉と栄養的に同等であることを確認しなければならず、マクロおよびミクロン栄養素、アミノ酸および脂肪酸プロファイルの分析を含みます。
検証プロトコル要件
規制基準は、安全で制御された運用を確保するために厳格なバイオリアクターの検証プロトコルを要求します。重要な要素は、危害分析重要管理点 (HACCP) プランの実施です。このフレームワークは、初期の細胞生検から細胞塊の最終収穫に至るまで、生産の各段階でリスクを特定し、軽減します。培養肉生産の新規性を考慮すると、安全性評価はプロセス全体を通じて潜在的な危険を対処する必要があります。
バリデーションプロトコルは、バイオリアクターシステムが生産サイクル中に無菌状態を維持し、微生物汚染を効果的に防止することを証明しなければなりません。さらに、これらのプロトコルは、培養肉のタンパク質が消費者にアレルギー反応を引き起こす可能性があるかどうかを評価する必要があります。
「私たちの新しいガイダンスは、企業がUKの食品規制当局に対して製品の安全性を理解し、正しく示すのを助けるための明確さを提供します。具体的には、このガイダンスは、企業が潜在的なアレルギーリスクを評価し、栄養的に適切であることを確認した上で、販売の認可を受けることを保証します。」
– Dr.トーマス・ヴィンセント、イノベーション副ディレクター、FSA [2]
英国では、検証は市場認可を与えるのではなく、科学的リスク評価のための十分なデータを提供することに焦点を当てています。ニコラ・モラン=フォレスト、GOURMEYの共同創設者 & CEOは、この違いを強調しました:
「グレートブリテンの検証は、私たちの新規食品規制の旅における重要なステップであり、完全なリスク評価に進んでいることを確認し、消費者に製品を提供する一歩手前に来ています。」[4]
バイオリアクターの選択とシステム仕様
選択されたバイオリアクター技術
施設は撹拌槽型バイオリアクター, を選択しました。この選択は、ウシ筋肉前駆細胞. での信頼性のある性能によって導かれました。この決定に影響を与えた主な要因には、細胞の特定のニーズ、望ましい生産規模、全体的なコストの考慮が含まれていました。
牛の筋肉細胞は、付着依存性であるため、培養中の損傷を避けるために0.1 N/m²未満の低せん断力を必要とします。撹拌槽設計はこの要件を満たし、パイロットスケールの実験と商業生産の両方に適応可能であることが証明されました。コストも主要な要因であり、パイロットスケールのユニットは£50,000から£100,000の価格で、製薬業界ではなく培養肉セクターで一般的な予算にアクセス可能です[5][7].
生産規模は商業的な実現可能性を確保するために100リットルから1,000リットルの間の容量を目標としました。モジュラー撹拌槽システムは、質量移動限界を超えずに10倍にスケールアップできる能力があるため、充填層の代替案よりも選ばれました。これらのシステムは、1バッチあたり1–10 kgの培養肉を生産することを目指し、容量1リットルあたり約£200の資本投資をバランスさせています [7][8].
システム設計の特徴
撹拌槽バイオリアクターが選ばれた後、その設計には最適な細胞成長を促進するための高度な機能が組み込まれました。ガス交換システムはマイクロスパージャー技術を採用し、20–100 µmの気泡を供給します。この設定により、37°CでkLa値100–200 h⁻¹を達成し、溶存酸素レベルを30–50%の飽和状態に維持します。CO₂のストリッピングを管理するために、ヘッドスペースエアレーションが膜コンタクターと消泡センサーと組み合わされています[5][6].
効率的な混合のために、バイオリアクターはデュアルラシュトンインペラー, を使用し、50–150 rpmの速度で動作します。これにより、剪断速度が5,000 s⁻¹未満, で均一な混合が保証され、細胞を損傷から保護しながら栄養勾配を10%未満に保ちます。攪拌はPID制御されており、pHと溶存酸素レベルのリアルタイムフィードバックがあり、1日あたり1–5容器体積の灌流速度をサポートします[5][7].
スケーラビリティは設計の重要な焦点でした。バイオリアクターは、異なるスケールにわたって幾何学的類似性を維持し、高さ対直径比2:1に準拠しています。CFD最適化インペラー は線形スケールアップを保証し、パイロットテストでは10リットルから200リットルへのスケーリング時に細胞生存率が95%保持されることが示されました。モジュール設計により、GxPコンプライアンス基準を満たしながら、より大規模な生産システムへの統合が可能です[7] [8].
プロセス分析技術も統合されており、ラマン分光法を特徴とし、pH(6.8–7.2)や乳酸(2 g/L以下に維持)などの重要なパラメータをリアルタイムで監視します。モノクローナル抗体生産から適応された予測モデルは、R²値が0.95以上のグルコースレベルを追跡し、正確なプロセス制御を保証します[5] [6][7].
これらの機能は、細胞培養を強化するだけでなく、英国の規制機関が要求する厳格な検証基準も満たしています。
検証プロトコルの実行
コア検証手順
運用の整合性を確保するために、先進的な設計機能を組み込んだ徹底的な検証プロトコルが実施されました。リアルタイムモニタリングが重要な役割を果たし、プロセス分析技術 (PAT) センサーが各培養ラン中に溶存酸素、pH、CO₂レベルなどの重要なパラメータを継続的に追跡しました[6] . プロセスは、1×10⁵ cells/mLの密度で播種された細胞から始まり、3 g/Lのグルコースを含む培地で1週間培養されました。ラマン分光法を用いて、乳酸とグルコースのレベルを通してモニタリングしました[5].
せん断応力分析により、攪拌力が牛筋細胞の臨界限界である0.1 Paを下回っていることが確認されました。ストレス後のテストでは、細胞の生存率が90%以上であることが示されました[6].
すべての原材料に対する無菌試験が拡大され、特に培地に注意が払われました。サプライヤーは、英国施設の基準に沿った第三者試験によって検証された分析証明書を提供することが求められました。プロトコルには、グラム陰性菌からのエンドトキシンを検出するためのELISA免疫測定法が含まれ、細胞のサイズ、形状、蛍光特性に基づいて汚染物質を特定するためのフローサイトメトリーが含まれていました[9] .
プロセス最適化手法
システムの安定性が確認された後、先進的な分析を使用してプロセスの改良に取り組みました。機械学習アルゴリズムは、継続的なPATデータに基づいて培地の流量と攪拌速度を動的に調整しました。これらのモデルは、実験計画法 (DoE) データセットで訓練され、誘電率測定とバイオマス品質を関連付けることにより、費用対効果の高い給餌戦略を特定しました[6] . このアプローチは、商業生産において一貫した成長率が重要な増殖期において特に効果的でした。
ラマン分光法は、もともとモノクローナル抗体の生産のために開発されましたが、培養肉の用途にうまく適応されました。その分析物特異性により、施設は確立された検証プロトコルを採用しながら、培養サイクル全体を通じてリアルタイムモニタリングに必要な精度を維持することができました[5].
技術的課題と解決策
スケールアップと生産性の問題
バイオリアクターを研究室の設定から商業生産にスケールアップすることは容易ではありませんでした。施設は10〜100 kgの培養肉を生産することを目指しており、この目標を達成するためには10¹²〜10¹³個の細胞が必要でした[11]. しかし、高い細胞密度に到達することは大きな障害となりました。中空糸バイオリアクターは理論的には10⁸から10⁹細胞/mLの密度を達成できるものの[13], 従来のバイオリアクターデザインは培養肉の生産には不十分でした。
GFIリサーチフェローのマット・マクナルティは問題の根本を説明しました。「培養肉に使用されるバイオリアクターは、依然として従来の食品および製薬デザインから大部分が適応されています。これらのデザインは培養肉の生産ニーズに特化しておらず、そのためにこの適合性の欠如による非効率性がコストを押し上げています」[12]. このデザインと目的の不一致は、設備とプロセスの完全な再考を必要としました。
実施されたソリューションとパフォーマンスデータ
これらの課題に対処するため、施設は培養肉生産の特定の要求により密接に一致するように、設備とプロトコルを再構築しました。主な変更点の一つは、医薬品グレードから食品グレードの基準への移行でした。例えば、チームは316ステンレス鋼の容器を304ステンレス鋼の代替品に置き換え、食品安全要件を満たしながら資本コストを大幅に削減しました[12]. さらに、従来の現場蒸気滅菌プロセスを二酸化塩素ガス処理に変更しました。この調整により、代替材料で作られた薄壁の容器を使用することが可能になり、コストをさらに削減しました[12].
コスト削減のもう一つの手段として、培地調製において医薬品グレードの水から「一般に安全と認められている」(GRAS)食品グレードの水に切り替えました[12]. チームはまた、食用のマイクロキャリアと足場を導入し、細胞の剥離問題を解決しただけでなく、食品安全規制にも準拠しました[11].
さらに運用を最適化するために、施設は多重化センサーシステムを導入しました。これらのセンサーはリアルタイムのパフォーマンスデータを提供し、機械学習アプリケーションでプロセスを微調整するために利用できました[12]. これらの変更により、生産コストに劇的な影響があり、£437,000/kgからわずか£1.95/kgに削減されました[10]. この顕著なコスト削減は、生産プロトコルを規制基準に合わせることで、安全性や品質を犠牲にすることなく商業的なスケーラビリティを達成できることを示しています。
sbb-itb-ffee270
検証結果と業界への影響
測定されたパフォーマンスの成果
厳格なテストを通じて、システムは生産性の驚異的な向上を示しました。バブルフリーの連続バイオリアクター技術を使用することで、細胞成長の生産性が15倍, に向上し、同じ運用フットプリント内で生産量が100 kgから1,500 kgに増加しました[16]. 分化段階では、細胞バイオマスを最適化するための調整により128%増加, し、全体的な環境への影響を42–56%. 大幅に削減しました。C2C12からCHO細胞代謝への移行は、環境への影響を削減する上で大きな役割を果たし、再生可能エネルギー源で稼働する場合、最大67%の削減を達成しました[14]. さらに驚くべきことに、再生可能エネルギーの使用により、温室効果ガスの排出が最大 92%削減され、従来の牛肉生産方法と比較して土地利用が90–95%削減されました[15] [16]. これらの結果は、業界全体での広範な採用への道を開きます。
業界慣行への貢献
検証結果は、培養肉生産におけるバイオリアクターデザインと規制遵守の基準を再定義しました。食品グレードの基準が安全性を損なうことなく製薬グレードの基準に効果的に取って代わることができることを示すことにより、このプロセスは業界にとってコスト削減のロードマップを導入しました。例えば、316ステンレス鋼から304ステンレス鋼への切り替え、二酸化塩素による滅菌、GRASに分類された水の使用を組み合わせることで、コンプライアンスを維持しながら資本コストを大幅に削減しました。
技術的な実現可能性を証明するだけでなく、これらの進歩は業界のベンチマークを変えつつあります。経済モデルは、統合された連続処理が10年間で資本および運用コストを55%節約できることを示唆しています[1]. 調達チームにとって、
結論
主な発見
この分析は、賢明な設備選択と運用プロトコルの改善によって、培養肉の生産が商業的成功に向かう方法を強調しています。304ステンレス鋼のような食品グレードの材料を選択することで、安全性とコンプライアンスを確保しながらコストを削減し、より高価な316ステンレス鋼を避けることができます。GOOD Meatの配合が2023年初頭にシンガポール食品庁によって承認されたことにより、血清を使用しない培地への移行は、動物由来の投入物に関連する倫理的および財政的な課題を排除します[15].
特に260,000 Lのエアリフトリアクターでの生産拡大は、コストを約£10.50/kgに引き下げる可能性を示しています。これは、42,000 Lの撹拌タンクリアクターに関連する£24.50/kgのコストと比較して大幅な改善です[17]. しかし、高い細胞密度 - 最大2 × 10⁸ cells/mL - を達成するには、アンモニアや乳酸のような代謝廃棄物を処理するための高度なパーフュージョンシステムが必要です。これらの課題に対処するためには、プロセスの最適化が不可欠であることが証明されています[11]. 調達チームにとって、
将来の展開
コスト効率とプロセス制御が検証された今、焦点は生産経済を再定義することを約束するメガスケールのバイオリアクターに移ります。GOOD Meatが2022年5月に発表した施設は、10基の250,000 Lバイオリアクターを備えており、年間13,700メートルトンの培養チキンとビーフを生産する能力を持っています。これは、パイロットプロジェクトから産業規模の生産への重要な移行を示しています [11][15]. これは、カリフォルニア大学デービス校のPatrick G. Negulescuらによって設定された経済的ベンチマークと一致していますUniversity of California, Davis:
「牛肉と直接競争するためには、CM製品、または少なくとも生産コストを9ドル/kg未満に下げる必要があります」[17]
予測によれば、この目標は達成可能であり、特にメディアコストが引き続き低下し、1リットルあたり0.20ポンド未満を目標としていることからも明らかです。
食用マイクロキャリアや、単一の容器で細胞の拡大と分化を組み合わせるハイブリッドシステムのような革新は、検証プロセスを簡素化し、汚染リスクを低減することが期待されています。このケーススタディで概説されたプロトコルは、企業が事業を拡大する際の再現可能なモデルを提供し、厳格なテストがコスト削減と共存できることを証明しています。これらの検証済みの方法を採用する施設が増えるにつれ、培養肉産業は従来の肉との価格の均衡に近づいています。これに加えて、再生可能エネルギー源によって駆動される場合、温室効果ガス排出量を最大92%削減するなど、顕著な環境上の利点を提供しています[15].
バイオリアクターのまとめ:センサー、モデリング、スケールアップ、代替リアクターデザイン
よくある質問
培養肉のバイオリアクター検証書類において、規制当局はどのような証拠を期待していますか?
規制機関は、システムが定義されたパラメータ内で機能することを確認するために、バイオリアクター検証書類を要求します。これには、一貫したプロセスパフォーマンスと、リアルタイムモニタリングの確保が含まれます。重要な要素として、pHレベル, 溶存酸素 , および温度 . があります。さらに、無菌試験は汚染を防ぐために重要な役割を果たします。ISO 14644-1およびEU GMP Annex 1などの基準の遵守は、微生物管理を維持し、無菌製造慣行を守るために必須です。
攪拌槽型バイオリアクターは、ウシ筋細胞を損傷させずにどのようにスケールアップできますか?
培養肉生産のための攪拌槽型バイオリアクターのスケールアップには、ウシ筋細胞を損傷させる可能性のあるせん断応力 , の管理が含まれます。これに対処するために、計算流体力学(CFD)やスケールダウンモデルなどのツールを使用して流れのパターンを予測します。これらの洞察は、インペラーデザインや攪拌速度の調整を導き、細胞の損傷を減少させるのに役立ちます。
同様に重要なのは、栄養素と酸素の均一な分布を確保することです。高度な監視システムと効果的な混合技術を組み合わせることで、一貫した条件を作り出すことが鍵となります。このアプローチは、局所的なストレスを最小限に抑え、大規模生産全体での細胞の健康をサポートします。
£/kgに最も影響を与えるコスト削減の検証変更は何ですか?
シングルユースバイオリアクターの採用は、£/kgで測定されるコスト削減に顕著な効果があります。これらのシステムは初期の資本投資と労働費を削減しますが、消耗品のコストが高くなります。それに加えて、リアルタイムモニタリングとメディアリサイクル技術の導入は、運用効率を向上させます。これらの進歩はプロセスを合理化するだけでなく、長期的なコスト削減にもつながります。











