Penapisan CRISPR berkapasiti tinggi sedang mengubah sektor daging yang ditanam dengan membolehkan pengubahsuaian genetik yang tepat untuk meningkatkan prestasi garis sel. Berikut adalah apa yang anda perlu tahu:
- Cabaran Utama: Pengeluaran daging yang ditanam memerlukan garis sel yang tumbuh dengan cekap, menahan penuaan, dan membezakan kepada tisu otot dan lemak.
- Peranan CRISPR: Dengan menyasarkan ribuan gen secara serentak, platform ini mengenal pasti suntingan genetik yang meningkatkan pertumbuhan, melambatkan penuaan, dan menyokong pembezaan.
- Penemuan Penting: Kajian telah menunjukkan bahawa menghapuskan gen seperti TP53 dan PTEN dalam sel stem mesenkimal lembu boleh meningkatkan percambahan sehingga 1,000 kali ganda dalam 30 hari dan memanjangkan jangka hayat mereka dari 100 hingga 200 hari.
- Aplikasi: Alat CRISPR seperti skrin knockout, CRISPRi, dan CRISPRa digunakan untuk mengoptimumkan pertumbuhan sel, mengawal ekspresi gen, dan mengimbangi proliferasi dengan pembezaan.
- Alat Industri: Teknik canggih seperti RMCE, RNA-seq, dan platform sel tunggal mengintegrasikan hasil CRISPR dengan data multi-omik, memastikan penambahbaikan yang tepat dan boleh diskalakan.
Untuk jurutera bioproses dan profesional R&D, inovasi ini menangani halangan kritikal dalam penskalakan proses daging yang diternak sambil mengekalkan kualiti dan fungsi sel. Integrasi CRISPR dengan sistem automatik dan sumber yang disesuaikan seperti
Asas CRISPR-Cas9 untuk Skrin Knockout Seluruh Genom
Bagaimana CRISPR-Cas9 Berfungsi dalam Penyuntingan Gen Skala Besar
Sistem CRISPR-Cas9 bergantung pada nuklease Cas9 yang dipasangkan dengan RNA panduan tunggal (sgRNA) untuk menyasarkan urutan DNA tertentu. Setelah sgRNA mengarahkan Cas9 ke lokasi genom yang diingini, enzim tersebut mencipta kerosakan dua untai dalam DNA. Kerosakan ini kebanyakannya dibaiki melalui penyambungan hujung bukan homolog (NHEJ), satu proses yang cenderung kepada ralat yang sering memperkenalkan sisipan atau pemadaman kecil (indel). Indel ini boleh menyebabkan mutasi pergeseran bingkai, secara efektif mengganggu fungsi gen yang disasarkan [1]. Mekanisme tepat ini adalah asas untuk menjalankan skrin knockout seluruh genom, yang penting dalam mengenal pasti pengawal selia kritikal bagi tingkah laku selular.
Untuk saringan berskala besar, penyelidik menggunakan perpustakaan sgRNA yang pelbagai, biasanya dihantar ke dalam populasi sel campuran melalui transduksi lentivirus. Untuk memastikan setiap sel menerima hanya satu perubahan genetik, kadar jangkitan yang rendah (MOI sekitar 0.3) dikekalkan [1]. Dari masa ke masa, sel dengan mutasi yang menguntungkan cenderung untuk berkembang biak lebih berjaya daripada yang lain, satu fenomena yang diperhatikan merentasi pelbagai jenis sel dan keadaan eksperimen.
Kaedah penghantaran alternatif, seperti pertukaran kaset yang dimediasi oleh rekombinase (RMCE), menawarkan ketepatan tambahan dengan menyasarkan "pad pendaratan" genomik tertentu untuk mengurangkan kebolehubahan dalam tapak integrasi. Sebagai contoh, satu kajian menggunakan sel CHO-K1 menggunakan kaedah RMCE tanpa virus untuk menyaring 111,651 gRNA unik merentasi 21,585 gen. Pendekatan ini mengenal pasti gen yang penting untuk kecergasan sel dalam tempoh 16 dan 37 hari [7].
Manfaat Penapisan Seluruh Genom
Penapisan knockout seluruh genom memanfaatkan ketepatan CRISPR-Cas9 untuk menyiasat secara sistematik ribuan gen. Ini membolehkan penyelidik untuk menemui gen yang mempengaruhi kelangsungan hidup sel, pertumbuhan, dan tindak balas terhadap tekanan. Selain faktor genetik, mengoptimumkan fungsionalisasi permukaan adalah kritikal untuk meningkatkan lekatan dan pertumbuhan sel dalam sistem ini. Penjelajahan tanpa bias ini amat relevan kepada pengeluaran daging yang diternak, di mana sel stem mesenkim (yang membentuk kira-kira 25% daripada sumber sel) sering menghadapi cabaran seperti pembiakan terhad dan penuaan awal [1].
sbb-itb-ffee270
Kaedah Penapisan Perpustakaan CRISPR Berkumpulan
Membina Perpustakaan CRISPR Berkumpulan
Perpustakaan CRISPR berkumpulan bermula dengan koleksi RNA panduan tunggal (sgRNA) yang dipilih dengan teliti.Dalam konteks penyelidikan daging yang ditanam, perpustakaan yang disasarkan sering direka untuk memberi tumpuan kepada keluarga gen tertentu, seperti faktor transkripsi atau pengawal selia pembiakan sel. Pendekatan ini membantu mengimbangi kos dengan kebolehan skala sambil mengekalkan fokus pada ciri-ciri yang relevan dengan fenotip yang diingini [1].
Proses ini bermula dengan mensintesis oligonukleotida sebagai satu kumpulan, memperbanyaknya melalui PCR, dan mengklonkan mereka ke dalam vektor penghantaran. Sebagai contoh, perpustakaan khusus lembu yang dibina pada awal 2025 termasuk 3,000 sgRNA yang menyasarkan 603 gen untuk mengenal pasti faktor yang mempengaruhi pengembangan sel stem [1]. Pada skala yang lebih besar, saringan seluruh genom boleh mencapai kerumitan yang jauh lebih tinggi. Satu contoh adalah saringan sel Ovari Hamster Cina (CHO), yang menggunakan 111,651 gRNA unik untuk menyasarkan 21,585 gen [7].
Transduksi lentiviral biasanya digunakan untuk menyampaikan perpustakaan ini pada kadar jangkitan yang rendah (sekitar 0.3), memastikan setiap sel mengalami hanya satu pengubahsuaian genetik [1]. Sebagai alternatif, kaedah bebas virus seperti pertukaran kaset yang dimediasi rekombinase (RMCE) mengintegrasikan perpustakaan gRNA ke dalam "pad pendaratan" genomik yang telah ditentukan dalam garis sel induk. Teknik ini mencapai liputan gRNA 99.9% dengan sedikit penyimpangan [7].
Untuk mengekalkan kebolehpercayaan statistik, penyelidik memastikan liputan tinggi - biasanya 500 hingga 600 sel per sgRNA [1] [7] . Beberapa platform menggunakan sistem Cas9 boleh diinduksi (iCas9), membolehkan kawalan tepat ke atas bila penyuntingan gen berlaku. Sebagai contoh, penyuntingan boleh dicetuskan selepas sel mencapai keadaan tertentu, seperti ketumpatan tinggi atau permulaan penuaan. Kawalan temporal ini amat berguna untuk mengkaji fasa bukan proliferatif, yang penting untuk mengatasi halangan penuaan dengan memilih antara garis sel primer vs diabadikan untuk meningkatkan pengeluaran daging yang ditanam [4] .
Sebaik sahaja perpustakaan dibina, penyelidik beralih kepada ujian saringan yang disasarkan untuk menilai fungsi gen.
Pendekatan Saringan untuk Garis Sel Daging yang Diternak
Selepas membina perpustakaan, penyelidik menilai prestasi sel menggunakan ujian persaingan dan teknik penyusunan fungsional. Kaedah yang digunakan secara meluas ialah ujian percambahan berasaskan persaingan, yang mengenal pasti perubahan genetik yang memberikan pertumbuhan atau ketahanan penuaan - sifat utama untuk mengoptimumkan garis sel untuk daging yang diternak.
Skrin jangka pendek (berlangsung kira-kira 30 hari) mengenal pasti gen yang segera mempengaruhi kitaran sel, manakala skrin jangka panjang (sehingga 200 hari) memberi tumpuan kepada gen yang membantu sel mengatasi penuaan replikasi. Ini adalah cabaran kritikal dalam meningkatkan pengeluaran daging yang diternak [1]. Untuk sifat yang lebih kompleks, seperti peningkatan rembesan protein atau ekspresi penanda tertentu, pengisihan sel diaktifkan pendarfluor (FACS) digunakan. Satu contoh ialah "ujian rembesan penangkapan sejuk", yang mengasingkan populasi sel produktif dengan menangkap protein yang dirembeskan pada permukaan sel sebelum pengisihan [7] [5] .
Pengesahan adalah langkah penting dalam mengesahkan keputusan saringan. Ujian Cellular Fitness (CelFi), sebagai contoh, menjejaki nisbah mutasi di luar rangka kepada mutasi dalam rangka dari semasa ke semasa.Jika sel dengan mutasi di luar rangka hilang dari populasi, ini menunjukkan bahawa gen yang disasarkan adalah penting untuk kecergasan selular [2].
Pada bulan Jun 2025, penyelidik yang diketuai oleh Shijie Ding di Universiti Pertanian Nanjing menggunakan CRISPR/Cas9 untuk mencipta CDKN2A–/– garis sel satelit porcine. Sel-sel yang diubah suai ini mengekalkan percambahan stabil sekurang-kurangnya 15 laluan dalam keadaan bebas serum sambil mengekalkan penanda stemness. Apabila disemai pada perancah 3D yang boleh dimakan berasaskan tumbuhan, mereka membentuk struktur seperti daging dengan tekstur yang diperbaiki, termasuk peningkatan kekenyalan dan kelikatan [8].
"Penemuan ini menunjukkan kegunaan saringan CRISPR untuk mengoptimumkan ciri-ciri sel stem lembu dan menawarkan jalan ke arah pengeluaran daging kultur yang lebih berskala pada masa hadapan." – Komunikasi Biologi [1]
CRISPR-Genetic Screens Berkumpulan dalam Sel Mamalia | Pratonton Protokol
CRISPRi dan CRISPRa untuk Skrin Pengawalan Gen Reversibel
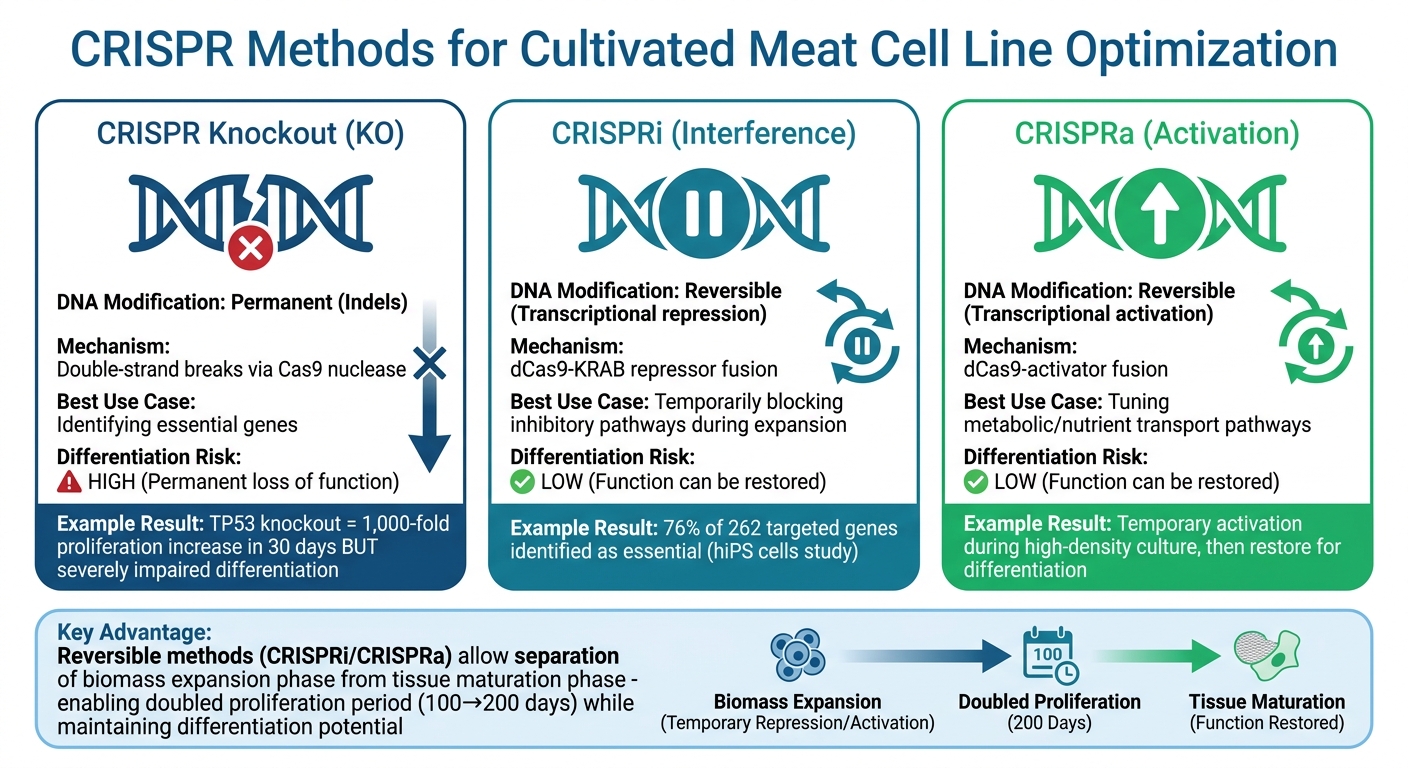
Kaedah Penyuntingan Gen CRISPR untuk Daging Ternakan: Perbandingan Knockout vs CRISPRi/CRISPRa
Menggunakan CRISPRi dan CRISPRa dalam Genomik Fungsional
Apabila berkaitan dengan meningkatkan pengeluaran daging ternakan, gangguan CRISPR (CRISPRi) dan pengaktifan CRISPR (CRISPRa) menyediakan alat yang berkuasa. Teknik-teknik ini menggunakan protein Cas9 yang tidak aktif dipasangkan dengan penekan atau pengaktif, membolehkan penyelidik menyesuaikan ekspresi gen secara sementara tanpa membuat perubahan kekal pada DNA [10].
Kebolehulangan ini amat penting untuk menangani cabaran utama: gen yang mempromosikan pertumbuhan sel yang cepat sering mengganggu peringkat akhir pembezaan menjadi tisu otot atau lemak. Sebagai contoh, menyingkirkan gen TP53 secara kekal dalam sel stem mesenkimal lembu boleh meningkatkan percambahan lebih 1,000 kali ganda dalam hanya 30 hari tetapi menjejaskan keupayaan mereka untuk membezakan [1]. CRISPRi menawarkan penyelesaian yang lebih fleksibel dengan menyekat sementara laluan yang menghalang pembezaan semasa pengembangan biojisim dalam bioreaktor untuk daging yang diternak. Sebaik sahaja sel-sel bersedia untuk pematangan tisu, fungsi gen normal boleh dipulihkan.
Pada Oktober 2025, penyelidik seperti Gabriele Casagrande Raffi dan Roderick L. Beijersbergen dari Netherlands Cancer Institute membangunkan sistem CRISPR yang boleh diinduksi.Pendekatan ini menangguhkan penyuntingan gen sehingga sel mencapai keadaan tertentu - seperti ketumpatan tinggi atau fasa tidak berproliferasi - membantu memelihara daya hidup sel [4].
CRISPRi juga menonjol kerana ketepatannya berbanding dengan gangguan RNA tradisional (RNAi). RNAi sering membawa kepada keputusan yang tidak konsisten dan kesan luar sasaran, manakala CRISPRi memberikan penindasan gen yang lebih boleh dipercayai dan spesifik [2]. Satu lagi kelebihan ialah CRISPRi mengelakkan pencetus ketoksikan berkaitan p53, yang sering disebabkan oleh tindak balas kerosakan DNA. Dalam kajian 2025 yang diketuai oleh Liqin Wang di Sun Yat-sen University Cancer Centre, penyelidik menggunakan sistem KRAB–dCas9 yang boleh diinduksi doxycycline untuk menyaring 262 gen dalam sel stem pluripoten teraruh manusia (sel hiPS). Mereka mendapati bahawa 76% daripada gen berkaitan terjemahan yang disasarkan (200 daripada 262) adalah penting untuk pertumbuhan, menunjukkan keberkesanan sistem ini [10].
Kebolehan untuk menala halus ekspresi gen menjadikan CRISPRi dan CRISPRa alat yang berharga untuk mengimbangi proliferasi dan pembezaan sel dalam penyelidikan genomik fungsional.
Mengadaptasi Skrin Boleh Balik untuk Aplikasi Daging Ternakan
Peraturan gen boleh balik menawarkan penyelesaian kepada cabaran utama dalam pengeluaran daging ternakan. Sebagai contoh, CRISPRa boleh mengaktifkan sementara gen yang terlibat dalam pengangkutan nutrien atau laluan metabolik semasa kultur berketumpatan tinggi. Setelah sel mencapai ketumpatan yang diingini, sistem boleh mengembalikan ekspresi gen ke tahap normal, menyokong pembezaan yang betul ke dalam tisu otot atau lemak.
Sistem boleh aruh juga memungkinkan pemisahan fasa pengembangan biojisim daripada pematangan tisu. CRISPRi boleh menekan gen yang berkaitan dengan penuaan semasa proses pembesaran, secara efektif menggandakan tempoh proliferasi sel lembu dari sekitar 100 hari kepada lebih 200 hari [1]. Setelah mencapai biomassa yang mencukupi, penyelidik boleh memulihkan ekspresi gen normal untuk membolehkan pembezaan. Pendekatan ini amat berguna untuk sel stem mesenkimal, yang cenderung memasuki penuaan awal dalam kultur [1].
"Penyuntingan genetik yang disasarkan bagi kedua-dua proses ini boleh mengoptimumkan kecekapan pengembangan MSC sambil mengekalkan multipotensi dan potensi pembezaan penting mereka, akhirnya memajukan sistem daging kultur yang boleh diskalakan." – Biologi Komunikasi [1]
Jadual di bawah menyoroti perbezaan antara kaedah pengawalan gen yang boleh diterbalikkan dan kekal:
| Ciri | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| Pengubahsuaian DNA | Kekal (Indels) | Boleh diterbalikkan (Transkripsi) |
| Mekanisme | Pecahan dua helai | Gabungan dCas9-effector |
| Kes Penggunaan Terbaik | Mengenal pasti gen penting | Menala laluan metabolik/pertumbuhan |
| Risiko Pembezaan | Tinggi (Kehilangan fungsi kekal) | Rendah (Fungsi boleh dipulihkan) |
Perbandingan ini menggambarkan bagaimana kaedah pengawalan gen yang boleh diterbalikkan boleh disesuaikan untuk memenuhi cabaran khusus dalam membangunkan garis sel untuk pengeluaran daging yang ditanam.
Menggabungkan Skrin CRISPR dengan Panel Sel dan Teknologi Genotip
Menghubungkan Skrin CRISPR dengan Analisis Multi-Omik
Mengintegrasikan multi-omik dan genotip automatik ke dalam skrin CRISPR memperhalusi kegunaannya, terutamanya dalam memajukan pembangunan garis sel daging yang ditanam.
Menggabungkan skrin CRISPR dengan multi-omik, seperti penjujukan RNA, membolehkan penyelidik memetakan kesan penyingkiran gen tertentu pada laluan selular. Ini amat relevan untuk daging yang ditanam, di mana memahami bagaimana sel mengimbangi percambahan dan pembezaan adalah kritikal.
Contohnya, skrin penyingkiran CRISPR berkumpulan yang menyasarkan 600 gen dalam sel stem mesenkim yang berasal dari adiposa lembu, digandingkan dengan RNA-seq, mendedahkan bahawa penyingkiran TP53 dan PTEN melambatkan penuaan.Sel-sel ini mengekalkan profil ekspresi gen yang muda, dengan gen kitaran sel yang dinaikkan, membawa kepada peningkatan 50% dalam kadar penggandaan menjelang hari ke-50 selepas transduksi [1] .
Platform sel tunggal seperti CROP-seq membawa ini lebih jauh dengan secara serentak mengesan kedua-dua perubahan sgRNA dan transkriptomik dalam sel individu [6]. Tahap ketepatan ini amat berharga untuk mengenal pasti pengubahsuaian genetik yang meningkatkan pembezaan otot atau sintesis protein - faktor kritikal untuk mencapai tekstur dan sifat pemakanan yang diingini dalam daging yang dikultur.
Pendekatan menjanjikan lain melibatkan saringan panel sel, di mana gangguan CRISPR diuji merentasi pelbagai garis sel dari pelbagai penderma, tapak anatomi, dan spesies. Sebagai contoh, penyelidik mengesahkan perpustakaan MyoCRISPR-KOLib pada garis myoblast manusia dari tujuh penderma.Menggunakan sistem pemilihan toksin terpisah, mereka mengenal pasti 250 gen yang penting untuk peleburan myoblast. Daripada jumlah ini, 41 gen telah disahkan melalui pangkalan data perubatan untuk memainkan peranan dalam morfologi otot rangka [6] . Pengesahan pelbagai baris ini memastikan bahawa sasaran genetik kekal kukuh merentasi variasi biologi, satu pertimbangan utama untuk meningkatkan pengeluaran daging yang ditanam.
Penemuan ini membuka jalan untuk platform automatik dan boleh diskalakan yang menggabungkan saringan genetik dengan genotip terperinci untuk aplikasi industri.
Automasi dan Skalabiliti dalam Platform Bersepadu
Automasi adalah penting untuk mengendalikan set data dan sampel yang besar yang dihasilkan oleh platform CRISPR dan genotip bersepadu. Sistem RMCE, yang membolehkan penghantaran perpustakaan sgRNA yang bebas virus dan khusus tapak, adalah satu langkah besar ke hadapan. Platform ini memastikan setiap sel menerima satu salinan sgRNA yang konsisten, mengurangkan kebolehubahan.RMCE telah menunjukkan liputan perpustakaan yang tinggi dengan bias yang minimal dalam sel ovari hamster Cina (CHO) [5].
"Platform penyaringan genetik throughput tinggi yang tidak berat sebelah adalah penting untuk pembangunan kilang CHO generasi seterusnya." - Pasukan Penyelidikan Ovari Hamster Cina [5]
Kebolehsuaian ditingkatkan lagi dengan alat pengesahan seperti ujian Cellular Fitness (CelFi). Ujian ini menggunakan penjujukan mendalam yang disasarkan untuk memantau profil indel dari masa ke masa, menjejaki nisbah mutasi dalam bingkai berbanding luar bingkai. Dengan mengaitkan mutasi ini dengan kelebihan atau kekurangan pertumbuhan, penyelidik dapat mengesahkan sasaran genetik dengan cekap dalam garis sel daging yang ditanam [2].
| Teknologi | Kaedah Integrasi | Manfaat Utama untuk Daging Ternak |
|---|---|---|
| RNA-seq / Multi-omik | Menghubungkan hasil CRISPR kepada profil transkriptomik | Memahami bagaimana gen mengawal pertumbuhan dan pembezaan [1][6] |
| Sistem Toksin Terpisah | Menghubungkan peleburan sel kepada pemilihan daya tahan hidup | Pemilihan kuantitatif sel yang mampu atau cacat peleburan [6] |
| Platform RMCE | Integrasi khusus tapak perpustakaan gRNA | Pemeriksaan throughput tinggi, bebas virus dengan bilangan salinan gen yang konsisten [5] |
| CROP-seq | Single-cell CRISPR + RNA-seq | Pengesanan serentak sgRNA dan perubahan transkriptomik [6] |
| CelFi Assay | Penjujukan mendalam terarah bagi indel | Pengesahan pantas sasaran genetik dengan menjejaki perubahan frekuensi alel [2] |
Platform canggih ini memudahkan proses daripada mengenal pasti sasaran genetik kepada mengesahkan kesannya terhadap kecergasan sel. Kecekapan ini menyokong pembangunan garis sel yang cukup kukuh untuk pengeluaran daging yang diternak secara besar-besaran.
Menggunakan Skrin CRISPR untuk Meningkatkan Pertumbuhan dan Proliferasi Garis Sel
Kaedah saringan CRISPR telah menjadi alat yang berkuasa untuk meningkatkan prestasi garis sel, menawarkan manfaat langsung untuk pengeluaran daging yang diternak.
Contoh Peningkatan Garis Sel Berasaskan CRISPR
Skrin CRISPR telah berjaya meningkatkan prestasi garis sel dalam penyelidikan daging yang diternak. Sebagai contoh, skrin knockout berkumpulan yang menyasarkan 600 gen dalam sel stem mesenkima yang berasal dari lemak lembu mengenal pasti TP53 dan PTEN sebagai penghalang utama pertumbuhan. Penghapusan TP53 secara signifikan meningkatkan kelimpahan sel dalam masa 30 hari[1] . Selain itu, sel stem mesenkima lembu yang diedit menunjukkan kadar penggandaan 12% lebih tinggi secara purata [1].
Dengan menyasarkan gen penekan tumor, penyelidik memanjangkan jangka hayat proliferatif sel daripada kira-kira 100 kepada lebih 200 hari, dengan berkesan melepasi had Hayflick. Kelewatan dalam penuaan ini membolehkan pengembangan biojisim dalam jangka masa yang relevan secara industri[1].
Dalam contoh lain, penyelidik dari Universiti Pertanian Nanjing, yang diketuai oleh Shijie Ding, Chunbao Li, dan Guanghong Zhou, menggunakan CRISPR/Cas9 untuk membangunkan CDKN2A−/− garis sel satelit babi. Sel-sel yang direka bentuk ini mengekalkan proliferasi stabil sekurang-kurangnya 18 laluan dalam medium bebas serum 19-komponen tersuai (A19). Mereka juga berjaya disemai ke atas rangka boleh dimakan, mewujudkan struktur seperti daging dengan peningkatan kekenyalan dan kelikatan[8]. Sel-sel mengekalkan lebih 90% daya hidup merentasi pelbagai laluan dalam keadaan bebas serum[8].
"Sel-sel knockout CDKN2A berasaskan CRISPR menyediakan sumber yang boleh diperbaharui bagi progenitor otot, mengurangkan kebergantungan pada biopsi haiwan yang berulang."
Contoh-contoh ini menonjolkan bagaimana saringan CRISPR boleh mengenal pasti pengubahsuaian genetik yang meningkatkan kadar pertumbuhan, melambatkan penuaan selular, dan membolehkan kultur bebas serum - tiga aspek penting untuk meningkatkan pengeluaran daging yang diternak.
Cabaran Penskalaan untuk Garis Sel Dioptimumkan CRISPR
Walaupun garis sel dioptimumkan CRISPR menunjukkan kelebihan yang jelas, penskalaan mereka untuk kegunaan industri menghadirkan cabaran. Peningkatan percambahan sering datang dengan kos pembezaan.Sebagai contoh, TP53 knockouts dalam sel stem mesenkimal lembu telah dikaitkan dengan pengurangan ekspresi gen pembezaan otot, yang boleh menghalang keupayaan mereka untuk matang menjadi tisu yang boleh dimakan[1]. Untuk menangani ini, strategi tambahan, seperti menambah suplemen media atau mengaktifkan faktor transkripsi tertentu, mungkin diperlukan untuk memulihkan pembezaan selepas pengembangan[1].
Satu lagi isu kritikal adalah mengekalkan kestabilan genetik. Variasi dalam bilangan salinan gen (aneuploidy) dan kesan luar sasaran semasa penyuntingan CRISPR boleh membawa kepada keputusan yang tidak konsisten atau positif palsu dalam kajian saringan[2]. Alat seperti ujian Cellular Fitness (CelFi) membantu mengurangkan risiko ini dengan memantau nisbah indel di luar bingkai dari masa ke masa, memastikan bahawa manfaat pertumbuhan yang diperhatikan berkaitan secara langsung dengan suntingan yang dimaksudkan[2].
Halangan ekonomi dan teknikal juga masih ada. Sel stem mesenkim, yang membentuk kira-kira 25% daripada sumber sel dalam industri daging yang ditanam, menghadapi cabaran seperti kos tinggi faktor pertumbuhan, keperluan untuk media bebas serum yang dioptimumkan, dan pembangunan bioreaktor berskala besar (kapasiti 10,000–50,000 L)[1][9][11]. Selain itu, memastikan tekstur yang diingini apabila sel disemai pada perancah 3D terus menjadi tugas yang kompleks[11].
"Keadaan semasa daging yang ditanam menghadapi cabaran yang ketara, termasuk kos yang tinggi, isu kebolehskalaan, dan keperluan untuk kemajuan teknologi yang lebih lanjut."
- Biologi Komunikasi [1]
Mengatasi cabaran ini memerlukan pendekatan menyeluruh yang menggabungkan pengoptimuman genetik dengan kemajuan dalam formulasi media, teknologi bioreaktor, dan protokol pembezaan. Walaupun saringan CRISPR memberikan pandangan genetik yang kritikal, menterjemahkan penemuan ini kepada penyelesaian yang boleh diskalakan akan memerlukan sistem bersepadu dan proses pengesahan yang ketat. Usaha ini penting untuk memindahkan pengeluaran daging yang ditanam dari makmal kepada kebolehlaksanaan komersial.
Bagaimana Cellbase Menyokong Penyelidikan CRISPR dalam Daging Ternakan
Saringan CRISPR telah menunjukkan potensinya, tetapi untuk menskalakannya bagi kegunaan industri memerlukan akses kepada alat dan sumber khusus. Di sinilah
Mengakses Sumber CRISPR Melalui Cellbase
Tidak seperti pembekal farmaseutikal spektrum luas,
Pada November 2025,
"Setiap syarikat daging yang ditanam yang kami temui membuang masa pada masalah perolehan yang sama. Mencari pembekal untuk komponen kritikal bermakna mencari melalui halaman pembekal farmasi yang tidak memahami aplikasi makanan."
- David Bell, Pengasas Cultigen Group [15]
Dengan memusatkan sumber-sumber ini,
Membolehkan Kerjasama dalam Pembangunan Daging Ternak
Platform ini direka untuk menangani permintaan projek komersial berskala besar, seperti yang dijalankan oleh Believer Meats dan Aleph Farms. Usaha ini memerlukan infrastruktur untuk bioreaktor 50,000 liter dan rantaian bekalan pengeluaran yang dioptimumkan, yang
Kesimpulan
Pemeriksaan CRISPR berkapasiti tinggi telah beralih daripada konsep yang menjanjikan kepada alat kritikal dalam memajukan pembangunan daging yang diternak. Kesan teknologi ini dalam mengoptimumkan garis sel tidak dapat dinafikan. Sebagai contoh, penemuan terkini telah menunjukkan bahawa pengubahsuaian genetik boleh menggandakan jangka hayat percambahan sel stem lembu dari 100 kepada 200 hari, mengurangkan populasi sel penuaan dari 60% kepada hanya 10%, dan mencapai peningkatan 1,000 kali ganda dalam kelimpahan sel dalam masa sebulan sahaja [1]. Kemajuan ini menandakan peralihan yang jelas daripada penyelidikan eksperimen kepada aplikasi industri praktikal.
Platform padat dan perpustakaan yang disasarkan sedang menangani beberapa cabaran paling mendesak dalam bidang ini. Sistem mikrofluidik digital kini membolehkan pemeriksaan dengan hanya 3,000 sel setiap keadaan, menjadikannya boleh dilaksanakan untuk bekerja dengan sel haiwan utama yang terhad yang tidak tersedia secara komersial.Sementara itu, perpustakaan fokus seperti MyoCRISPR-KOLib dengan cekap menyasarkan 90% transkrip yang relevan sambil meliputi hanya sepertiga daripada genom [3][6]. Tahap ketepatan dan kecekapan ini adalah kritikal untuk mengatasi kekangan sumber dan meningkatkan pengeluaran.
"Penemuan ini menunjukkan kegunaan saringan CRISPR untuk mengoptimumkan sifat sel stem lembu dan menawarkan jalan ke arah pengeluaran daging yang ditanam lebih berskala pada masa hadapan." [1]
Walaupun dengan kemajuan ini, kejayaan bergantung kepada akses kepada infrastruktur yang betul. Penyelidik memerlukan perpustakaan gRNA khusus spesies, media pertumbuhan yang direka untuk aplikasi makanan, bioreaktor yang serasi, dan alat analisis yang disesuaikan untuk pengeluaran daging yang ditanam dan bukannya penggunaan farmaseutikal. Menangani keperluan ini,
Untuk pasukan yang bekerja untuk merekayasa gelombang seterusnya garis sel daging yang ditanam, alat dan teknologi sudah sedia. Cabaran kini terletak pada pelaksanaan saringan CRISPR yang pantas dan berkesan untuk merealisasikan potensi penuhnya.
Soalan Lazim
Bagaimana anda memilih antara CRISPR knockout, CRISPRi dan CRISPRa untuk saringan?
Pilihan antara sistem ini bergantung pada soalan biologi khusus anda dan hasil yang anda sasarkan:
- CRISPR knockout: Kaedah ini mengganggu fungsi gen sepenuhnya, menjadikannya ideal untuk mengkaji kesan kehilangan atau penyahaktifan gen.
- CRISPRi: Dengan menekan ekspresi gen tanpa memotong DNA, pendekatan ini sangat sesuai untuk menyelidik gen penting atau apabila penindasan yang boleh diterbalikkan diperlukan.
- CRISPRa: Jika anda perlu meningkatkan ekspresi gen, sistem ini adalah pilihan utama. Ia amat berguna untuk meneliti kesan ekspresi berlebihan, seperti mempromosikan percambahan atau pembezaan sel.
Apabila membuat keputusan, ambil kira model selular anda, gen yang anda sasarkan, dan matlamat keseluruhan eksperimen anda.
Bagaimana anda boleh meningkatkan percambahan tanpa merosakkan pembezaan otot atau lemak?
Meningkatkan percambahan sel otot atau lemak sambil mengekalkan keupayaan mereka untuk membezakan adalah cabaran utama dalam pengeluaran daging yang diternak.Satu pendekatan yang menjanjikan melibatkan pengeditan gen berasaskan CRISPR, yang membolehkan manipulasi gen yang tepat untuk meningkatkan pertumbuhan atau memanjangkan jangka hayat sel. Sebagai contoh, menyasarkan myostatin (MSTN) boleh mempromosikan pertumbuhan sel, manakala mengedit CDKN2A membantu sel mengelakkan penuaan.
Walau bagaimanapun, mencapai keseimbangan antara proliferasi dan pembezaan adalah kritikal. Pengurusan yang salah terhadap sasaran tertentu, seperti P53 (TP53), boleh menjejaskan pembezaan, berpotensi menjejaskan kualiti tisu. Untuk menavigasi kerumitan ini, penyaringan CRISPR berkapasiti tinggi adalah penting. Teknik ini mengenal pasti pengawal selia gen yang paling berkesan, membuka jalan untuk pembangunan tisu yang berskala dan sihat dalam pengeluaran daging yang ditanam.
Apa yang diperlukan untuk mengesahkan hasil saringan CRISPR sebelum meningkatkan skala garis sel?
Mengesahkan hasil saringan CRISPR untuk pengeluaran daging yang ditanam memerlukan pendekatan yang sistematik. Pertama, fungsi gen mesti disahkan melalui eksperimen bebas, seperti pemadaman gen, untuk memastikan kesan yang diperhatikan boleh dihasilkan semula. Seterusnya, adalah penting untuk menilai kepentingan biologi gen-gen ini dengan memeriksa kesannya terhadap faktor seperti percambahan sel, daya hidup, dan jangka hayat.
Penilaian keselamatan adalah sama penting untuk menolak kesan luar sasaran atau ketidakstabilan genetik yang boleh menjejaskan proses. Pengesahan fungsi di bawah keadaan yang meniru persekitaran industri, seperti bioreaktor, adalah langkah penting lain. Ini memastikan bahawa suntingan genetik berfungsi seperti yang diharapkan dalam persekitaran pengeluaran berskala besar. Ujian menyeluruh pada setiap peringkat adalah tidak boleh dirunding sebelum mempertimbangkan peningkatan skala.











