Overschakelen van foetaal kalfsserum (FBS) naar serumvrije media (SFM) is cruciaal voor het opschalen van de productie van gekweekt vlees. Afhankelijkheid van FBS creëert uitdagingen zoals hoge kosten, beperkte beschikbaarheid en inconsistente kwaliteit. SFM biedt een veiliger, meer gecontroleerd alternatief, maar het brengt ook hindernissen met zich mee:
- Problemen met celhechting: Myoblasten hebben moeite om zich zonder serum te hechten, wat vaak dure coatings zoals laminine of Matrigel vereist. Geconditioneerde media of specifieke supplementen kunnen de hechting verbeteren.
- Langzamere groeisnelheden: Serumvrije systemen missen essentiële voedingsstoffen, wat leidt tot verminderde proliferatie en ammoniakopbouw. Het toevoegen van groeifactoren en het vervangen van glutamine door alternatieven kan helpen.
- Inconsistente mediaprestaties: Veel commerciële SFM's, geoptimaliseerd voor menselijke cellen, ondersteunen de groei van myoblasten van vee niet effectief. Testen over verschillende soorten en langere perioden met een media optimalisatie ontdekkingskit is cruciaal.
Oplossingen omvatten op maat gemaakte formuleringen, gedeeltelijke mediumvervanging en co-cultuursystemen om serumachtige omstandigheden na te bootsen. Hoewel SFM de prestaties van FBS-systemen kan benaderen, introduceert opschaling naar 3D-bioreactoren complexiteiten zoals adhesie en afvalbeheer. Zorgvuldige monitoring van de celkwaliteit zorgt voor succes in grootschalige productie.
Overschakelen naar SFM gaat niet alleen over betere wetenschap - het wordt een noodzaak nu de prijzen van FBS blijven stijgen. Onderzoekers en producenten moeten zich richten op het optimaliseren van media en het verkrijgen van betrouwbare materialen om de productie van gekweekt vlees levensvatbaar en kosteneffectief te maken.
Plantaardige steigers die serumvrije celadhesie induceren voor gekweekt vlees - Indi Geurs - ISCCM9
sbb-itb-ffee270
Veelvoorkomende problemen in serumvrije media voor myoblasten
Overschakelen van serum-gebaseerde naar serumvrije formuleringen kan verschillende technische uitdagingen met zich meebrengen die workflows verstoren en de kosten verhogen. Deze problemen komen vaak op specifieke manieren naar voren, te beginnen met celhechting.
Verminderde celhechting en overleving
Een van de grootste obstakels is dat myoblasten zich niet goed hechten in serumvrije media. Serum biedt van nature een mix van eiwitten, groeifactoren en lipiden die helpen cellen aan oppervlakken te laten kleven. Zonder deze componenten hebben myoblasten moeite om zich te hechten, wat vaak leidt tot vroege celdood.
Om dit aan te pakken, vertrouwen veel serumvrije systemen op dure coatingmiddelen zoals laminine 511 of Matrigel. Maar zelfs met deze coatings blijven de hechtingsniveaus vaak achter bij wat wordt gezien in serum-gebaseerde culturen. Een studie uit 2024 vond bijvoorbeeld dat standaard serumvrije media slechts 2.210 ± 319 cellen/cm² ondersteunden op ongecoate schalen. Daarentegen verdrievoudigde een geconditioneerd serumvrij medium - aangevuld met uitgescheiden factoren van andere cellijnen - dat cijfer bijna tot 5.985 ± 1.558 cellen/cm² [2].
Een ander probleem is de verhoogde gevoeligheid voor antibiotica. In serumvrije opstellingen kunnen antibiotica zoals Penicilline, Streptomycine en Amfotericine B de proliferatie met maar liefst 62% verminderen, vergeleken met een vermindering van 20-26% in serum-gebaseerde systemen [1]. Zonder de beschermende elementen van serum zijn cellen kwetsbaarder voor stress, wat hun overleving en groei verder belemmert.
Langzamere Celgroei
Zelfs als cellen erin slagen zich te hechten, blijven de groeisnelheden vaak achter.Serum biedt essentiële voedingsstoffen zoals groeifactoren, cytokines, cholesterol en vetzuren - waarvan vele ontbreken of onvoldoende aanwezig zijn in de meeste commerciële serumvrije formuleringen. Dit voedingsgat resulteert in lagere celopbrengsten en langere productietijden.
Een andere complicatie is de ophoping van ammoniak door glutaminemetabolisme. Ammoniak remt de groei en, in serumvrije omstandigheden, waar cellen al onder metabole druk staan, kan deze toxiciteit de uitbreiding ernstig belemmeren. Veel commerciële media zijn oorspronkelijk ontworpen voor menselijke cellen, dus ze voldoen mogelijk niet aan de specifieke voedingsbehoeften van rund- of varkensmyoblasten [1][3].
Gedeeltelijke mediumvervanging, zoals het vervangen van 75% van het medium tijdens het voeden, kan helpen om enkele endogene groeifactoren te behouden.Hoewel dit bescheiden de groeipercentages verbetert, sluit het de kloof tussen serumvrije en serumbased systemen niet volledig [1].
Variabele Prestaties Tussen Commerciële Producten
Niet alle commerciële serumvrije media presteren even goed. In een studie waarin zeven formuleringen werden vergeleken, ondersteunden slechts drie - FBM™, Essential 8™ en TeSR™-E8™ - consistente groei van rundermyoblasten gedurende zes dagen. Andere, zoals StemPro™ en mTeSR1™, ondersteunden groei slechts vier dagen voordat ze stopten, terwijl STEMmacs™ er helemaal niet in slaagde om proliferatie te ondersteunen [1].
Het probleem ligt in het feit dat de meeste commerciële media zijn geoptimaliseerd voor menselijke stamcellen of fibroblasten, niet voor veemyoblasten. Wat goed werkt in biomedisch onderzoek schiet vaak tekort voor de productie van gekweekt vlees. Deze inconsistentie benadrukt de behoefte aan formuleringen die specifiek zijn afgestemd op veemyoblasten. Fabrikantgegevens voor menselijke cellen kunnen niet betrouwbaar voorspellen hoe goed een medium zal presteren met runder- of varkenscellen.
Om het juiste serumvrije medium te vinden, is het cruciaal om uitgebreide tests uit te voeren - idealiter over zes tot tien dagen - om ervoor te zorgen dat het langdurige celuitbreiding ondersteunt in plaats van alleen kortdurende groei.
Vergelijking van Commerciële Serumvrije Media Opties
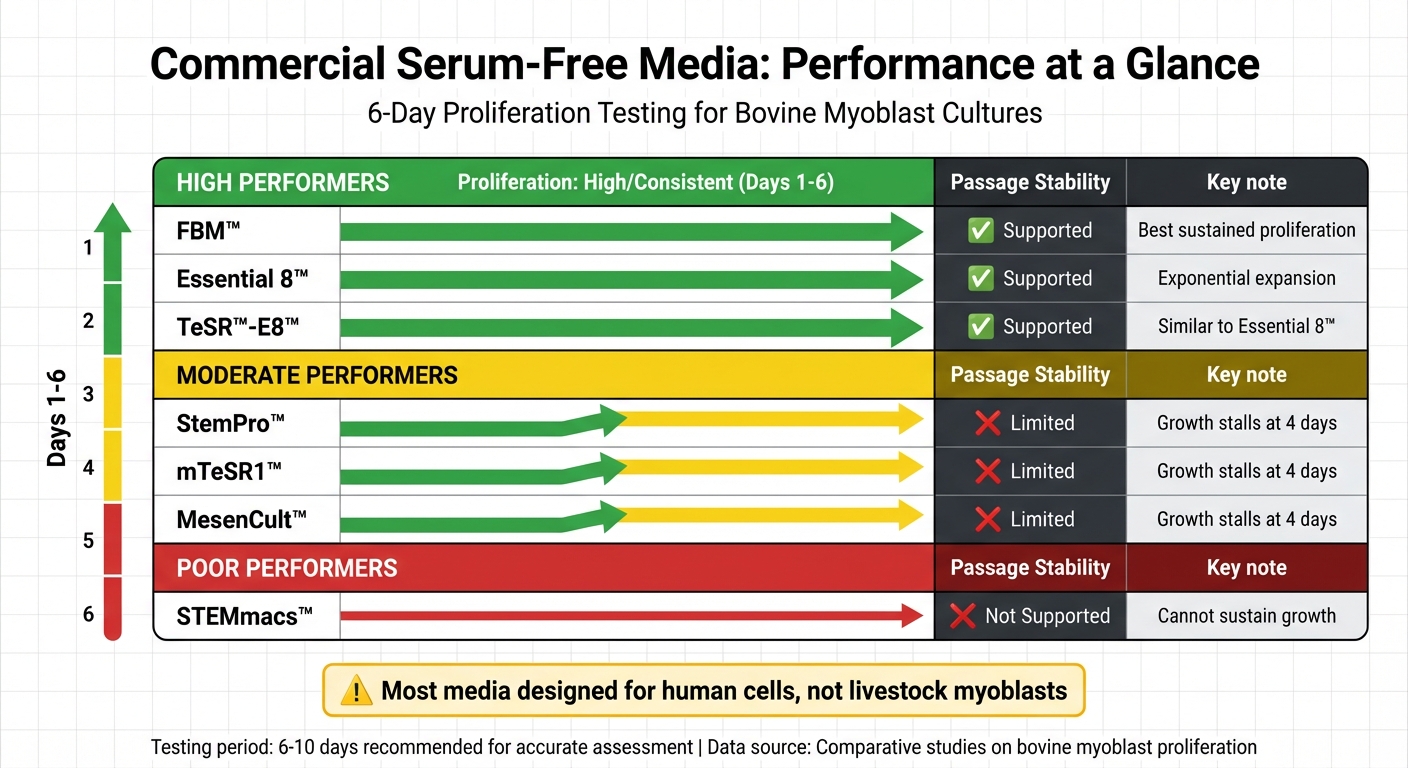
Prestatievergelijking van Commerciële Serumvrije Media voor Runder Myoblast Culturen
Prestatiegegevens voor Veelvoorkomende Media
Als het gaat om serumvrije media voor myoblastculturen, kan de prestatie sterk variëren. Sommige producten, zoals FBM™, Essential 8™, en TeSR™-E8™, ondersteunen consequent de proliferatie van runder myoblasten gedurende zes dagen. Daarentegen stagneren anderen, zoals StemPro™, mTeSR1™, en MesenCult™, vaak al na vier dagen.Ondertussen slaagt STEMmacs™ er niet in om groei te behouden [1].
Hier is een snelle vergelijking van prestatiestatistieken voor deze media:
| Medium | Proliferatie (Dagen 1–6) | Passagestabiliteit | Belangrijkste Observaties |
|---|---|---|---|
| FBM™ | Hoog/Consistent | Ondersteund | Biedt het beste potentieel voor langdurige proliferatie [1] |
| Essential 8™ | Hoog/Consistent | Ondersteund | Ondersteunt exponentiële expansie, hoewel minder dan serum-gebaseerd [1] |
| TeSR™-E8™ | Hoog/Consistent | Ondersteund | Vergelijkbaar met Essential 8™ voor rundermyoblasten [1] |
| StemPro™ | Gemiddeld | Beperkt | Groei stopt na vier dagen [1] |
| mTeSR1™ | Gemiddeld | Beperkt | Groei stopt na vier dagen [1] |
| MesenCult™ | Gemiddeld | Beperkt | Groei stopt na vier dagen [1] |
| STEMmacs™ | Laag/Geen | Niet Ondersteund | Niet in staat om groei van rundermyoblasten te ondersteunen [1] |
Interessant genoeg tonen de meeste media - behalve FBM™ - aanzienlijk lagere celgetallen binnen 24 uur na zaaien in vergelijking met serum-gebaseerde controles. Dit benadrukt het belang van het evalueren van deze statistieken bij het kiezen van een medium, vooral gezien regelgevende trends in groeimedia voor voedselveiligheid.
Hoe kies je het juiste serumvrije medium
Het selecteren van het beste serumvrije medium gaat niet alleen om groeisnelheden; het vereist een balans van verschillende factoren zoals proliferatie, hechting en kosteneffectiviteit. Het testen van media over een periode van zes dagen is cruciaal, aangezien kortere tests misleidende resultaten kunnen geven [1].
Soortspecifiteit is een andere belangrijke overweging. Veel serumvrije opties zijn ontworpen met menselijke cellen in gedachten, wat betekent dat ze mogelijk niet voldoen aan de voedingsbehoeften van myoblasten van vee zoals rund- of varkenscellen. De voedingsbehoeften van verschillende soorten en celstaten kunnen aanzienlijk variëren, dus testen is essentieel [3] .
Coatingvereisten spelen ook een grote rol. Sommige media hebben dure coatings nodig zoals laminine of Matrigel om celadhesie te garanderen. Als uw proces ongecoate oppervlakken of voedselveilige materialen omvat, is het de moeite waard om te testen of het medium hechting kan ondersteunen zonder deze toevoegingen. Geconditioneerde media of formuleringen die zijn afgestemd op ongecoate schalen kunnen een kosteneffectief alternatief zijn [2] .
Een andere kritische factor is het gebruik van antibiotica. Standaard antibioticacocktails, zoals Penicilline/Streptomycine, kunnen de proliferatie van myoblasten met 20–26% verminderen in serumbevattende media en met maar liefst 62% in serumvrije systemen. Het elimineren van antibiotica kan leiden tot aanzienlijk hogere celopbrengsten [1].
Ten slotte, vergeet niet het beheer van metabolisch afval. Ammoniakophoping kan giftig zijn voor culturen, dus het is een goed idee om media aan te vullen met niet-ammoniagenische verbindingen zoals α-ketoglutaraat of pyruvaat. Deze additieven helpen de toxiciteit van ammoniak te verminderen en verlengen de levensduur van culturen [3].
Methode om Serumvrije Myoblastculturen te Verbeteren
Het aanpakken van de uitdagingen van serumvrije myoblastculturen vereist gerichte strategieën. Hier zijn enkele praktische methoden om hun prestaties te verbeteren.
Toevoegen van Belangrijke Supplementen
Het opnemen van specifieke supplementen kan de groei van myoblasten aanzienlijk verbeteren. Een mengsel van FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), en insuline (10 μg/ml) heeft aangetoond de celuitbreiding in basismedia zoals FBM te verbeteren [1] . Deze groeifactoren werken samen om celproliferatie te bevorderen terwijl ze de ongedifferentieerde staat behouden die nodig is voor productie.
Aminozuren en vitamines zijn ook cruciaal. Verbindingen zoals pyridoxamine (Vitamine B6), asparagine, en glutaminezuur spelen een sleutelrol bij het bevorderen van celadhesie en proliferatie, vooral op ongecoate oppervlakken [2] . Deze supplementen helpen de metabole ondersteuning te vervangen die normaal door serum wordt geleverd, en pakken adhesiegerelateerde uitdagingen aan.
"Componentanalyse en validatie-experimenten suggereerden dat pyridoxamine, asparagine en glutaminezuur bijdroegen aan de verwerving van de cultuurfunctie van het ontwikkelde medium." - npj Science of Food [2]
Echter, voorzichtigheid is geboden met lipide-gebaseerde supplementen zoals LipoGro. Hoewel ze groei kunnen stimuleren, kunnen ze ook adipogene differentiatie induceren, waardoor myoblasten vetvacuolen ontwikkelen en hun spiercelidentiteit verliezen [1].
Mediaformuleringen op maat maken
Het aanpassen van mediaformuleringen kan serumvrije culturen optimaliseren met behulp van een groeifactor ontdekkingskit. Een effectieve benadering omvat het gebruik van geconditioneerde media. Media geconditioneerd door co-cultivering van HepG2 (menselijke hepatoma) en NIH/3T3 (muis fibroblast) cellen repliceert het metabolische profiel van de foetale lever. Deze methode bereikt een celdichtheid van 5.985 ± 1.558 cellen/cm² op ongecoate schalen, vergelijkbaar met de 6.722 ± 1.500 cellen/cm² bereikt met serumbevattende media [2] . De interactie tussen deze celtypen bevordert de secretie van serumachtige componenten, wat de groei verbetert.
Een andere kosteneffectieve strategie is gedeeltelijke mediumvervanging. Door slechts 75% van het medium te vervangen in plaats van een volledige verandering, worden endogene groeifactoren die door de cellen worden geproduceerd behouden, wat de groeisnelheden verbetert zonder de noodzaak van extra supplementen [1].
Voorkomen van vroege differentiatie met remmers
Het handhaven van een proliferatieve toestand vereist zorgvuldige controle van differentiatie signalen. Bijvoorbeeld, geconditioneerd medium van HepG2-cellen kan de expressie van de myogene differentiatiemarker Desmin, onderdrukken, waardoor cellen ongedifferentieerd blijven en klaar zijn voor uitbreiding [2].
Bovendien helpt het volgen van markers zoals CD29 (integrine beta-1) en Ki67 ervoor te zorgen dat de formulering effectief is in het handhaven van celproliferatie, waardoor het risico op voortijdige differentiatie wordt verminderd.Deze markers bieden een betrouwbare manier om de cultuurcondities te monitoren en aan te passen voor optimale resultaten.
Schaalvergroting van Serumvrije Myoblast Culturen voor Productie
Overstappen naar 3D Cultuursystemen
Het verschuiven van serumvrije myoblast culturen van platte 2D schalen naar 3D bioreactorsystemen brengt zijn eigen uitdagingen met zich mee, vooral als het gaat om celadhesie. Het coaten van bioreactorcomponenten met dure middelen zoals laminine is niet praktisch voor grootschalige productie. Het gebruik van geconditioneerd medium van HepG2 en NIH/3T3 co-culturen of het verrijken van basismedia met verbindingen zoals pyridoxamine, asparagine en glutaminezuur is echter effectief gebleken. Deze methoden stellen myoblasten in staat om zich te hechten aan ongecoate 3D-skeletten en microcarriers, het aanpakken van de adhesieproblemen zonder toevlucht te nemen tot kostbare coatings [2].
Een andere kritische factor bij schaalvergroting is het beheren van metabolisch afval. Dichte bioreactorculturen kunnen een ophoping van toxisch ammoniak ervaren, wat kan worden vermeden door glutamine te vervangen door niet-ammoniagenische alternatieven zoals α-ketoglutaraat, glutamaat of pyruvaat [3]. Deze aanpassingen zijn essentieel bij het overschakelen naar systemen op grotere schaal en vereisen zorgvuldige kwaliteitscontrole en sensormonitoring om de integriteit van myoblasten tijdens de productie te behouden.
Bevestiging van Celkwaliteit in Aangepaste Culturen
Naarmate culturen worden aangepast voor productie op grotere schaal, is het waarborgen van de kwaliteit van de cellen cruciaal. Technieken zoals transcriptomische, metabolomische en functionele assays worden gebruikt om te verifiëren dat cellen hoge niveaus van CD29 en Ki67 behouden terwijl de expressie van Desmin wordt onderdrukt. Deze markers geven aan dat de cellen in een proliferatieve, ongedifferentieerde staat blijven tijdens het opschalingsproces [2]. Het monitoren van deze indicatoren is bijzonder belangrijk wanneer kostenbesparende maatregelen, zoals het overschakelen naar voedselveilige componenten of het gebruik van gedeeltelijke mediawijzigingen, worden ingevoerd. Deze stap zorgt ervoor dat de overgang van onderzoeks- naar productiesystemen de celkwaliteit niet in gevaar brengt. Het verfijnen van deze parameters is een cruciale stap om de productie van gekweekt vlees schaalbaar en kostenefficiënt te maken.
Serumvrij versus serumbasede kweekprestaties
Wanneer geoptimaliseerd, kunnen serumvrije systemen resultaten bereiken die dicht bij traditionele serumbasede culturen liggen.De onderstaande tabel benadrukt belangrijke statistieken van rundermyoblastculturen die op ongecoate oppervlakken zijn gekweekt:
| Metric | Serum-Based (20% FBS + 10% HS) | Conditioned Serum-Free |
|---|---|---|
| Celadhesie (24u) | ~6,722 cellen/cm² | ~5,985 cellen/cm² |
| Celproliferatie (72u) | ~10,050 cellen/cm² | ~8,998 cellen/cm² |
| CD29 Expressie | Hoog | Hoog |
| Ki67 Expressie | Hoog | Hoog |
| Desmin Expressie | Onderdrukt | Onderdrukt |
Gegevens afkomstig van npj Science of Food [2]
Hoewel serum-gebaseerde systemen nog steeds een klein voordeel hebben in cel dichtheid, levert serumvrije media vergelijkbare resultaten op in adhesiemarkerexpressie en houdt het cellen ongedifferentieerd - belangrijke factoren voor productie. De kloof wordt verder verkleind wanneer specifieke supplementen worden toegevoegd om formuleringen te optimaliseren, waardoor serumvrije systemen een steeds praktischere optie worden voor grootschalige productie van gekweekt vlees.
Conclusie
Het overschakelen van myoblastculturen naar serumvrij medium brengt de nodige uitdagingen met zich mee: vroege hechtingsproblemen, langzamere celgroei en inconsistente resultaten van commerciële producten. Echter, eenvoudige veranderingen - zoals het verwijderen van antibiotica en het kiezen voor gedeeltelijke mediumvervangingen - kunnen de proliferatiesnelheden aanzienlijk verbeteren [1]. Door zorgvuldig media te kiezen en specifieke groeifactoren toe te voegen, kunnen onderzoekers de kloof tussen serumvrije en serumbased systemen qua prestaties dichten. Deze vooruitgangen effenen de weg voor opschaling van de productie.
Het opschalen van serumvrije culturen introduceert echter nieuwe lagen van complexiteit.Overgang van cellen naar 3D-bioreactorsystemen terwijl ze hun fenotype behouden, vereist rigoureuze kwaliteitscontrole. Toch blijkt uit bewijs dat goed geoptimaliseerde serumvrije systemen cel dichtheden kunnen bereiken die vergelijkbaar zijn met die gekweekt in serumbased media. Dit maakt serumvrije methoden steeds praktischer voor commerciële productie van gekweekt vlees.
Het economische argument voor serumvrije media is moeilijk te negeren. Nu de prijzen van FBS blijven stijgen, worden serumbased methoden financieel onwerkbaar [1] . Deze verschuiving gaat niet alleen over technische verbeteringen - het gaat om economisch overleven voor de gekweekte vleesindustrie.
Voor onderzoekers en productieteams die deze overgang maken, is het essentieel om de juiste materialen te vinden. Van chemisch gedefinieerde media tot recombinante groeifactoren, toegang hebben tot betrouwbare voorraden is cruciaal.Dit is waar
Veelgestelde Vragen
Hoe kan ik de hechting van myoblasten verbeteren in serumvrij medium zonder laminine of Matrigel?
Om de hechting van myoblasten in serumvrij medium te verbeteren zonder gebruik van laminine of Matrigel, overweeg het gebruik van geconditioneerd serumvrij medium. Deze aanpak kan adhesie en proliferatie bevorderen, zelfs op niet-gecoate schalen. Een andere optie is om het medium te optimaliseren door componenten toe te voegen zoals FGF2, fetuin, en BSA. Deze aanpassingen kunnen een merkbaar verschil maken in het verbeteren van celhechting en groei, waardoor de noodzaak voor extracellulaire matrixcoatings wordt geëlimineerd.
Wat is de snelste manier om de ophoping van ammoniak in serumvrije myoblastculturen te verminderen?
Om de ophoping van ammoniak in serumvrije myoblastculturen te verminderen, richt u zich op het verbeteren van de mediaformulering. Een benadering is het gebruik van geconditioneerde media die zowel celadhesie als proliferatie bevorderen, terwijl de ammoniakniveaus laag blijven. Bovendien kan het verfijnen van de kweekomstandigheden helpen om de ammoniakproductie te minimaliseren. Dit kan inhouden dat factoren zoals pH, temperatuur of nutriëntconcentraties worden aangepast om beter aan te sluiten bij de metabole behoeften van de cellen.
Hoe valideer ik dat myoblasten ongedifferentieerd blijven na overschakeling naar serumvrije media?
Om ervoor te zorgen dat myoblasten in hun ongedifferentieerde staat blijven wanneer ze worden gekweekt in serumvrije media, is het cruciaal om specifieke markers te volgen. Pax7 is een betrouwbare indicator van ongedifferentieerde myoblasten, terwijl de afwezigheid van differentiatiemarkers zoals myosine zware keten (MHC) bevestigt dat ze nog niet zijn begonnen met differentiëren.
U kunt technieken gebruiken zoals:
- Immunocytochemie: Om eiwitexpressie in cellen te visualiseren.
- Flowcytometrie: Voor het analyseren van markerexpressie in een grote celpopulatie.
- qPCR: Om mRNA-niveaus van belangrijke markers te meten.
Bovendien is het essentieel om de cellen onder een microscoop te observeren. Myoblasten moeten hun karakteristieke uiterlijk behouden en de vorming van multinucleaire myotubes vermijden, wat een duidelijk teken van differentiatie is. Door deze methoden te combineren en regelmatig te monitoren, kunt u ervoor zorgen dat de cellen ongedifferentieerd blijven.











