High-throughput CRISPR-screening transformeert de sector van gekweekt vlees door precieze genetische modificaties mogelijk te maken die de prestaties van cellijnen verbeteren. Dit is wat u moet weten:
- Belangrijkste Uitdaging: De productie van gekweekt vlees vereist cellijnen die efficiënt groeien, veroudering weerstaan en differentiëren in spier- en vetweefsel.
- De Rol van CRISPR: Door duizenden genen tegelijkertijd te targeten, identificeren deze platforms genetische bewerkingen die groei verbeteren, veroudering vertragen en differentiatie ondersteunen.
- Opmerkelijke Bevindingen: Studies hebben aangetoond dat het uitschakelen van genen zoals TP53 en PTEN in boviene mesenchymale stamcellen de proliferatie tot 1.000-voudig kan verhogen in 30 dagen en hun levensduur kan verlengen van 100 tot 200 dagen.
- Toepassingen: CRISPR-tools zoals knockout screens, CRISPRi en CRISPRa worden gebruikt om celgroei te optimaliseren, genexpressie te reguleren en proliferatie in balans te brengen met differentiatie.
- Industrie Tools: Geavanceerde technieken zoals RMCE, RNA-seq en single-cell platforms integreren CRISPR-resultaten met multi-omics data, wat zorgt voor nauwkeurige en schaalbare verbeteringen.
Voor bioprocesingenieurs en R&D-professionals, deze innovaties aanpakken kritieke knelpunten in het opschalen van gekweekte vleesprocessen terwijl de celkwaliteit en functionaliteit behouden blijven. De integratie van CRISPR met geautomatiseerde systemen en op maat gemaakte middelen zoals
CRISPR-Cas9 Grondbeginselen voor Genoom-Wijde Knockout Screens
Hoe CRISPR-Cas9 Werkt in Grootschalige Genbewerking
Het CRISPR-Cas9-systeem is afhankelijk van een Cas9-nuclease gekoppeld aan een single-guide RNA (sgRNA) om specifieke DNA-sequenties te targeten. Zodra de sgRNA Cas9 naar de gewenste genomische locatie leidt, creëert het enzym een dubbelstrengsbreuk in het DNA. Deze breuk wordt voornamelijk gerepareerd via niet-homologe eindverbinding (NHEJ), een foutgevoelig proces dat vaak kleine inserties of deleties (indels) introduceert. Deze indels kunnen frameshift-mutaties veroorzaken, waardoor de functie van het getargete gen effectief wordt verstoord [1]. Dit precieze mechanisme is de basis voor het uitvoeren van genoom-wijde knockout screens, die essentieel zijn voor het identificeren van kritieke regulatoren van cellulair gedrag.
Voor grootschalige screening gebruiken onderzoekers een diverse bibliotheek van sgRNA's, meestal afgeleverd in een gemengde celpopulatie via lentivirale transductie. Om ervoor te zorgen dat elke cel slechts één genetische verandering ontvangt, wordt een lage multipliciteit van infectie (MOI van ongeveer 0,3) gehandhaafd [1]. Na verloop van tijd hebben cellen met voordelige mutaties de neiging om succesvoller te prolifereren dan andere, een fenomeen dat wordt waargenomen in verschillende celtypen en experimentele omstandigheden.
Alternatieve aflevermethoden, zoals recombinase-gemedieerde cassette-uitwisseling (RMCE), bieden extra precisie door specifieke genomische "landingsplaatsen" te targeten om variabiliteit in integratieplaatsen te verminderen. Bijvoorbeeld, een studie met CHO-K1 cellen gebruikte een virusvrije RMCE-methode om 111.651 unieke gRNA's te screenen over 21.585 genen. Deze benadering identificeerde genen die essentieel zijn voor de celconditie over perioden van 16 en 37 dagen [7].
Voordelen van Genoom-Wijde Screening
Genoom-wijde knockout screens maken gebruik van de nauwkeurigheid van CRISPR-Cas9 om systematisch duizenden genen te onderzoeken. Dit stelt onderzoekers in staat om genen te ontdekken die invloed hebben op celoverleving, groei en reacties op stress. Naast genetische factoren is het optimaliseren van oppervlaktefunctionalisatie cruciaal voor het verbeteren van celhechting en groei in deze systemen. Dergelijke onbevooroordeelde verkenning is vooral relevant voor gekweekte vleesproductie, waar mesenchymale stamcellen (die ongeveer 25% van de celbronnen uitmaken) vaak te maken hebben met uitdagingen zoals beperkte proliferatie en vroege veroudering [1].
sbb-itb-ffee270
Gecombineerde CRISPR Bibliotheek Screening Methoden
Het Bouwen van Gecombineerde CRISPR Bibliotheken
Gecombineerde CRISPR bibliotheken beginnen met een zorgvuldig geselecteerde verzameling van single-guide RNA's (sgRNA's).In de context van onderzoek naar gekweekt vlees worden gerichte bibliotheken vaak ontworpen om zich te concentreren op specifieke genfamilies, zoals transcriptiefactoren of regulatoren van celproliferatie. Deze benadering helpt de kosten in balans te brengen met schaalbaarheid, terwijl de focus blijft op eigenschappen die relevant zijn voor het gewenste fenotype [1].
Het proces begint met het synthetiseren van oligonucleotiden als een pool, deze te amplificeren via PCR en ze te kloneren in een afleveringsvector. Bijvoorbeeld, een runderspecifieke bibliotheek die begin 2025 werd geconstrueerd, omvatte 3.000 sgRNA's die 603 genen targetten om factoren te identificeren die de uitbreiding van stamcellen beïnvloeden [1]. Op grotere schaal kunnen genoomwijde screens een veel hogere complexiteit bereiken. Een voorbeeld is een Chinese Hamster Ovarium (CHO) celscreen, die 111.651 unieke gRNA's gebruikte om 21.585 genen te targetten [7].
Lentivirale transductie wordt vaak gebruikt om deze bibliotheken te leveren bij een lage multipliciteit van infectie (ongeveer 0,3), zodat elke cel slechts een enkele genetische modificatie ondergaat [1]. Alternatief integreren virusvrije methoden zoals recombinase-gemedieerde cassette-uitwisseling (RMCE) de gRNA-bibliotheek in vooraf bepaalde genomische "landingsplaatsen" binnen een mastercellijn. Deze techniek bereikt 99,9% gRNA-dekking met minimale vertekening [7].
Om statistische betrouwbaarheid te behouden, zorgen onderzoekers voor een hoge dekking - typisch 500 tot 600 cellen per sgRNA [1] [7] . Sommige platforms gebruiken induceerbare Cas9 (iCas9) systemen, waardoor nauwkeurige controle mogelijk is over wanneer genbewerking plaatsvindt. Bijvoorbeeld, bewerking kan worden geactiveerd nadat cellen een specifieke toestand bereiken, zoals hoge dichtheid of het begin van senescentie. Deze temporele controle is bijzonder nuttig voor het bestuderen van niet-proliferatieve fasen, die cruciaal zijn voor het overwinnen van senescentiebarrières door te kiezen tussen primaire vs geïmmortaliseerde cellijnen voor opschaling van gekweekt vleesproductie [4] .
Zodra de bibliotheek is geconstrueerd, gaan onderzoekers verder met gerichte screeningsassays om de genfunctie te evalueren.
Screeningsbenaderingen voor gekweekte vleescellijnen
Na het bouwen van de bibliotheek beoordelen onderzoekers de celprestaties met behulp van competitieassays en functionele sorteertechnieken. Een veelgebruikte methode is de competitie-gebaseerde proliferatie-assay, die genetische veranderingen identificeert die groei- of senescentieresistentie verlenen - sleutelkenmerken voor het optimaliseren van cellijnen voor gekweekt vlees.
Kortetermijnscreens (ongeveer 30 dagen) identificeren genen die onmiddellijk invloed hebben op de celcyclus, terwijl langetermijnscreens (tot 200 dagen) zich richten op genen die cellen helpen replicatieve senescentie te overwinnen. Dit is een kritieke uitdaging bij het opschalen van de productie van gekweekt vlees [1]. Voor complexere eigenschappen, zoals verbeterde eiwitsecretie of expressie van specifieke markers, wordt fluorescentie-geactiveerde celsortering (FACS) gebruikt. Een voorbeeld is de "cold capture secretion assay", die productieve celpopulaties isoleert door uitgescheiden eiwitten op het celoppervlak te vangen voordat ze worden gesorteerd [7] [5].
Validatie is een cruciale stap bij het bevestigen van screeningresultaten. De Cellular Fitness (CelFi) assay, bijvoorbeeld, volgt de verhouding van out-of-frame tot in-frame mutaties in de tijd.Als cellen met out-of-frame mutaties verdwijnen uit de populatie, suggereert dit dat het gerichte gen essentieel is voor de cellulaire fitheid [2].
In juni 2025 gebruikten onderzoekers onder leiding van Shijie Ding aan de Nanjing Agricultural University CRISPR/Cas9 om CDKN2A–/– porcine satellietcellijnen . te creëren. Deze gemodificeerde cellen behielden stabiele proliferatie gedurende ten minste 15 passages in serumvrije omstandigheden, terwijl ze stamcelmarkers behielden. Wanneer ze werden gezaaid op een plantaardig 3D eetbaar scaffold, vormden ze vleesachtige constructies met verbeterde textuur, waaronder verbeterde kauwbaarheid en gomachtigheid [8].
"Deze bevindingen demonstreren het nut van CRISPR-screening voor het optimaliseren van eigenschappen van rundstamcellen en bieden een pad naar meer schaalbare productie van gekweekt vlees in de toekomst." – Communicatie Biologie [1]
Gecombineerde CRISPR-Genetische Screens in Zoogdiercellen | Protocol Voorbeeld
CRISPRi en CRISPRa voor Omkeerbare Genregulatie Screens
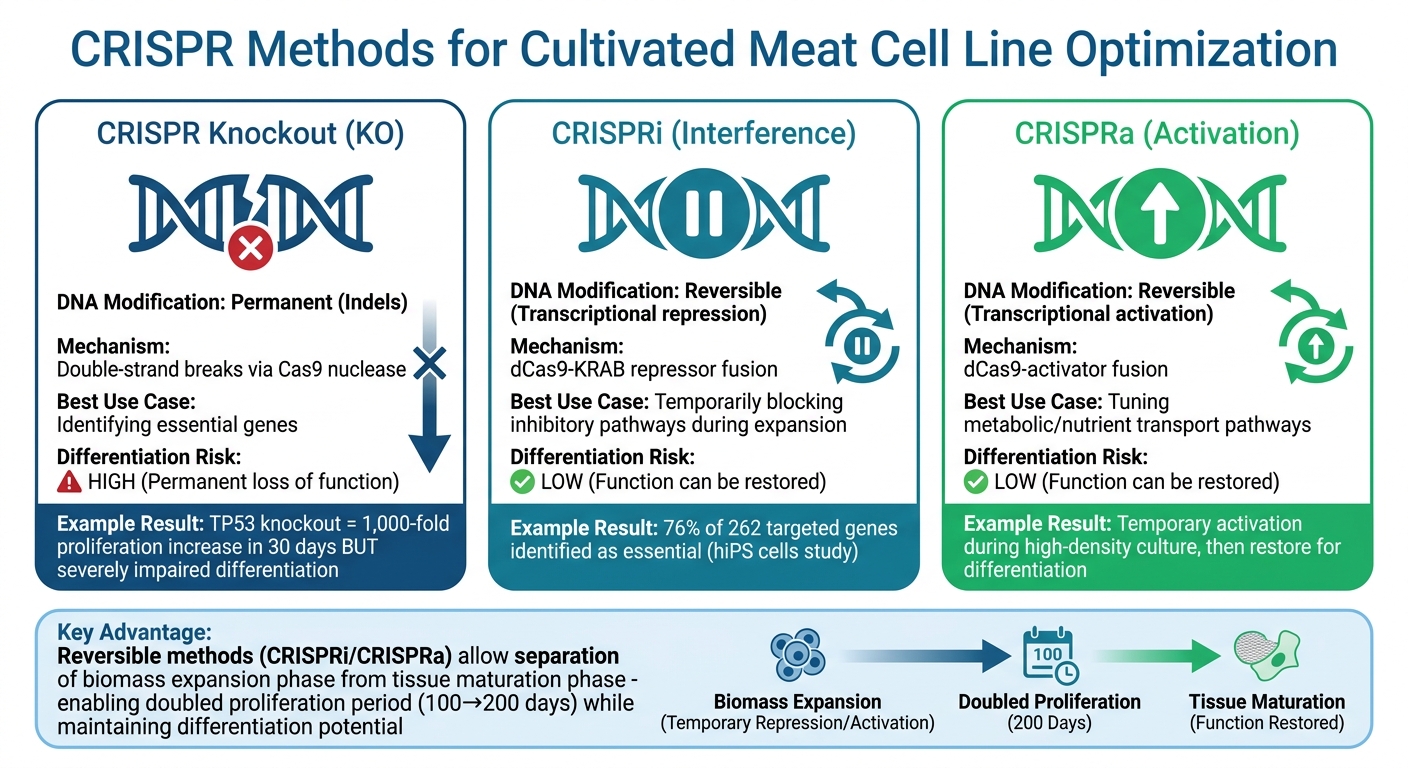
CRISPR Genbewerking Methoden voor Gekweekt Vlees: Knockout vs CRISPRi/CRISPRa Vergelijking
Gebruik van CRISPRi en CRISPRa in Functionele Genomica
Als het gaat om het verbeteren van de productie van gekweekt vlees, bieden CRISPR-interferentie (CRISPRi) en CRISPR-activatie (CRISPRa) krachtige hulpmiddelen. Deze technieken gebruiken een inactief Cas9-eiwit gekoppeld aan repressors of activatoren, waardoor onderzoekers de genexpressie tijdelijk kunnen aanpassen zonder permanente veranderingen aan het DNA aan te brengen [10].
Deze omkeerbaarheid is vooral belangrijk voor het aanpakken van een grote uitdaging: genen die snelle celgroei bevorderen, verstoren vaak de latere stadia van differentiatie in spier- of vetweefsel. Bijvoorbeeld, het permanent uitschakelen van het TP53 gen in runder mesenchymale stamcellen kan de proliferatie meer dan 1.000-voudig verhogen in slechts 30 dagen, maar belemmert hun vermogen om te differentiëren ernstig [1]. CRISPRi biedt een flexibelere oplossing door tijdelijk de paden te blokkeren die differentiatie remmen tijdens biomassa-uitbreiding in bioreactoren voor gekweekt vlees. Zodra de cellen klaar zijn voor weefselrijping, kan de normale genfunctie worden hersteld.
In oktober 2025 ontwikkelden onderzoekers zoals Gabriele Casagrande Raffi en Roderick L. Beijersbergen van het Nederlands Kanker Instituut een induceerbaar CRISPR-systeem.Deze benadering stelt genbewerking uit totdat cellen specifieke toestanden bereiken - zoals hoge dichtheid of een niet-proliferatieve fase - wat helpt om de levensvatbaarheid van cellen te behouden [4].
CRISPRi valt ook op door zijn precisie vergeleken met traditionele RNA-interferentie (RNAi). RNAi leidt vaak tot inconsistente resultaten en off-target effecten, terwijl CRISPRi betrouwbaardere en specifiekere genonderdrukking levert [2]. Een ander voordeel is dat CRISPRi het veroorzaken van p53-gerelateerde toxiciteit vermijdt, wat vaak wordt veroorzaakt door DNA-schade reacties. In een studie uit 2025 onder leiding van Liqin Wang aan Sun Yat-sen University Cancer Centre, gebruikten onderzoekers een doxycycline-induceerbaar KRAB–dCas9-systeem om 262 genen te screenen in humane geïnduceerde pluripotente stamcellen (hiPS-cellen). Ze ontdekten dat 76% van de gerichte translatie-gerelateerde genen (200 van de 262) essentieel waren voor groei, wat de effectiviteit van het systeem aantoont [10].
Deze mogelijkheid om genexpressie fijn af te stemmen maakt CRISPRi en CRISPRa waardevolle hulpmiddelen voor het balanceren van celproliferatie en differentiatie in functioneel genomica onderzoek.
Aanpassen van Reversibele Schermen voor Toepassingen in Gekweekt Vlees
Reversibele genregulatie biedt oplossingen voor belangrijke uitdagingen in de productie van gekweekt vlees. Bijvoorbeeld, CRISPRa kan tijdelijk genen activeren die betrokken zijn bij nutriëntentransport of metabole routes tijdens hoge-dichtheidscultuur. Zodra de cellen de gewenste dichtheid bereiken, kan het systeem de genexpressie terugbrengen naar normale niveaus, wat de juiste differentiatie in spier- of vetweefsel ondersteunt.
Induceerbare systemen maken het ook mogelijk om de fase van biomassa-uitbreiding te scheiden van weefselrijping. CRISPRi kan senescentie-geassocieerde genen onderdrukken tijdens het opschalingsproces, waardoor de proliferatieperiode van runder cellen effectief wordt verdubbeld van ongeveer 100 dagen tot meer dan 200 dagen [1]. Na het bereiken van voldoende biomassa kunnen onderzoekers de normale genexpressie herstellen om differentiatie mogelijk te maken. Deze benadering is bijzonder nuttig voor mesenchymale stamcellen, die de neiging hebben om vroegtijdig in senescentie te gaan in cultuur [1].
"Gerichte genetische bewerking van deze dubbele processen zou de efficiëntie van MSC-uitbreiding kunnen optimaliseren, terwijl hun essentiële multipotentie en differentiatiepotentieel behouden blijven, wat uiteindelijk schaalbare gekweekte vleessystemen bevordert." – Communications Biology [1]
De onderstaande tabel benadrukt de verschillen tussen omkeerbare en permanente genregulatiemethoden:
| Kenmerk | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| DNA-modificatie | Permanent (Indels) | Omkeerbaar (Transcriptioneel) |
| Mechanisme | Dubbelstrengsbreuken | dCas9-effectorfusie |
| Beste gebruiksgeval | Essentiële genen identificeren | Afstemmen van metabolische/groeipaden |
| Differentiatie Risico | Hoog (Permanent functieverlies) | Laag (Functie kan worden hersteld) |
Deze vergelijking illustreert hoe omkeerbare genregulatiemethoden kunnen worden aangepast om te voldoen aan de specifieke uitdagingen van het ontwikkelen van cellijnen voor de productie van gekweekt vlees.
Het combineren van CRISPR-schermen met celpanelen en genotyperingstechnologieën
Het koppelen van CRISPR-schermen aan multi-omics analyse
Het integreren van multi-omics en geautomatiseerde genotypering in CRISPR-schermen verfijnt hun bruikbaarheid, vooral bij het bevorderen van de ontwikkeling van gekweekte vleescellijnen.
Het combineren van CRISPR-schermen met multi-omics, zoals RNA-sequencing, stelt onderzoekers in staat om de effecten van specifieke gen-knockouts op cellulaire routes in kaart te brengen. Dit is vooral relevant voor gekweekt vlees, waar het begrijpen van hoe cellen proliferatie en differentiatie in balans houden cruciaal is.
Een voorbeeld hiervan is een gepoold CRISPR-knockoutscherm dat zich richt op 600 genen in rundvlees afgeleid van mesenchymale stamcellen, gepaard met RNA-seq, onthulde dat het uitschakelen van TP53 en PTEN veroudering vertraagde.Deze cellen behielden een jeugdige genexpressieprofiel, met opgereguleerde celcyclusgenen, wat leidde tot een toename van 50% in verdubbelingssnelheden tegen dag 50 na transductie [1].
Single-cell platforms zoals CROP-seq gaan verder door gelijktijdig zowel sgRNA als transcriptomische veranderingen in individuele cellen te detecteren [6]. Dit niveau van precisie is van onschatbare waarde voor het identificeren van genetische modificaties die spierdifferentiatie of eiwitsynthese verbeteren - kritische factoren voor het bereiken van de gewenste textuur en voedingswaarde in gekweekt vlees.
Een andere veelbelovende benadering omvat celpanelscreening, waarbij CRISPR-verstoringen worden getest op diverse cellijnen van verschillende donoren, anatomische locaties en soorten. Bijvoorbeeld, onderzoekers valideerden de MyoCRISPR-KOLib-bibliotheek op menselijke myoblastlijnen van zeven donoren. Met behulp van een split-toxine selectiesysteem identificeerden ze 250 genen die essentieel zijn voor myoblastfusie. Hiervan werden 41 genen bevestigd via medische databases om een rol te spelen in de morfologie van skeletspieren [6]. Deze multi-lijn validatie zorgt ervoor dat genetische doelen robuust blijven over biologische variaties heen, een belangrijke overweging voor het opschalen van de productie van gekweekt vlees.
Deze inzichten banen de weg voor geautomatiseerde, schaalbare platforms die genetische screens combineren met gedetailleerde genotypering voor industriële toepassingen.
Automatisering en Schaalbaarheid in Geïntegreerde Platforms
Automatisering is essentieel voor het verwerken van de enorme datasets en monsters die worden gegenereerd door geïntegreerde CRISPR- en genotyperingsplatforms. RMCE-systemen, die virusvrije, plaats-specifieke levering van sgRNA-bibliotheken mogelijk maken, zijn een grote stap voorwaarts. Deze platforms zorgen ervoor dat elke cel een enkele, consistente sgRNA-kopie ontvangt, waardoor variabiliteit wordt verminderd.RMCE heeft al aangetoond een hoge bibliotheekdekking te hebben met minimale bias in Chinese hamster-ovarium (CHO) cellen [5].
"Een onbevooroordeeld high-throughput genetisch screeningsplatform is essentieel voor de ontwikkeling van de volgende generatie CHO-fabrieken." - Chinese Hamster Ovarium Onderzoeksteam [5]
Schaalbaarheid wordt verder verbeterd door validatietools zoals de Cellular Fitness (CelFi) assay. Deze assay maakt gebruik van gerichte diepe sequencing om indel-profielen in de loop van de tijd te monitoren, waarbij de verhouding van in-frame versus out-of-frame mutaties wordt gevolgd. Door deze mutaties te correleren met groeivoordelen of -nadelen, kunnen onderzoekers efficiënt genetische doelen verifiëren in gekweekte vleescellijnen [2].
| Technologie | Integratiemethode | Primaire Voordeel voor Gekweekt Vlees |
|---|---|---|
| RNA-seq / Multi-omics | CRISPR-hits koppelen aan transcriptomische profielen | Begrijpen hoe genen groei en differentiatie reguleren[1][6] |
| Split-Toxin Systemen | Cel fusie koppelen aan levensvatbaarheid selectie | Kwantitatieve selectie van fusie-capabele of defecte cellen[6] |
| RMCE Platforms | Site-specifieke integratie van gRNA-bibliotheken | High-throughput, virusvrije screening met consistente gen kopie aantallen[5] |
| CROP-seq | Single-cell CRISPR + RNA-seq | Gelijktijdige detectie van sgRNA en transcriptomische veranderingen [6] |
| CelFi Assay | Gerichte diepe sequencing van indels | Snelle validatie van genetische doelen door het volgen van verschuivingen in allelfrequentie [2] |
Deze geavanceerde platforms stroomlijnen het proces van het identificeren van genetische doelen tot het valideren van hun impact op de cellulaire fitheid. Deze efficiëntie ondersteunt de ontwikkeling van cellijnen die robuust genoeg zijn voor grootschalige productie van gekweekt vlees.
CRISPR-schermen gebruiken om de groei en proliferatie van cellijnen te verbeteren
CRISPR-screeningmethoden zijn een krachtig hulpmiddel geworden voor het verbeteren van de prestaties van cellijnen, met directe voordelen voor de productie van gekweekt vlees.
Voorbeelden van CRISPR-gebaseerde verbeteringen van cellijnen
CRISPR-schermen hebben met succes de prestaties van cellijnen verbeterd in onderzoek naar gekweekt vlees. Bijvoorbeeld, een gecombineerde knockout-screen gericht op 600 genen in mesenchymale stamcellen afgeleid van rundervetweefsel identificeerde TP53 en PTEN als belangrijke groeiremmer. Het uitschakelen van TP53 verhoogde de celabundantie aanzienlijk binnen 30 dagen[1] . Bovendien vertoonden de bewerkte mesenchymale stamcellen van runderen gemiddeld een 12% hogere verdubbelingssnelheid[1] .
Door zich te richten op tumorsuppressorgenen verlengden onderzoekers de proliferatieve levensduur van de cellen van ongeveer 100 tot meer dan 200 dagen, waardoor de Hayflick-limiet effectief werd omzeild. Deze vertraging in veroudering maakt biomassagroei mogelijk over industrieel relevante tijdsbestekken[1].
In een ander voorbeeld gebruikten onderzoekers van de Nanjing Agricultural University, onder leiding van Shijie Ding, Chunbao Li en Guanghong Zhou, CRISPR/Cas9 om CDKN2A−/− varkenssatellietcellijnen te ontwikkelen. Deze gemodificeerde cellen behielden stabiele proliferatie gedurende ten minste 18 passages in een op maat gemaakt 19-componenten serumvrij medium (A19). Ze werden ook succesvol gezaaid op eetbare steigers, waardoor vleesachtige constructies werden gecreëerd met verbeterde kauwbaarheid en gomachtigheid[8]. De cellen behielden meer dan 90% levensvatbaarheid over meerdere passages in serumvrije omstandigheden[8].
"De op CRISPR gebaseerde CDKN2A knockout-cellen bieden een hernieuwbare bron van spierprogenitoren, waardoor de afhankelijkheid van herhaalde dierbiopten wordt verminderd."
Deze voorbeelden benadrukken hoe CRISPR-schermen genetische modificaties kunnen identificeren die groeisnelheden verbeteren, cellulaire veroudering vertragen en serumvrije cultuur mogelijk maken - drie essentiële aspecten voor het opschalen van de productie van gekweekt vlees.
Opschalingsuitdagingen voor CRISPR-geoptimaliseerde cellijnen
Hoewel CRISPR-geoptimaliseerde cellijnen duidelijke voordelen tonen, brengt het opschalen ervan voor industrieel gebruik uitdagingen met zich mee. Verbeterde proliferatie gaat vaak ten koste van differentiatie.Bijvoorbeeld, TP53 knockouts in runder mesenchymale stamcellen zijn geassocieerd met verminderde expressie van spierdifferentiatiegenen, wat hun vermogen om te rijpen tot eetbaar weefsel kan belemmeren[1]. Om dit aan te pakken, kunnen aanvullende strategieën, zoals het toevoegen van mediasupplementen of het activeren van specifieke transcriptiefactoren, nodig zijn om differentiatie na expansie te herstellen[1].
Een ander cruciaal probleem is het behouden van genetische stabiliteit. Variaties in genkopieaantallen (aneuploïdie) en off-target effecten tijdens CRISPR-bewerking kunnen leiden tot inconsistente resultaten of vals-positieven in screeningsstudies[2]. Tools zoals de Cellular Fitness (CelFi) assay helpen deze risico's te verminderen door de verhouding van out-of-frame indels in de tijd te monitoren, waardoor wordt verzekerd dat waargenomen groeivoordelen direct gekoppeld zijn aan de beoogde bewerkingen[2].
Economische en technische barrières blijven ook bestaan. Mesenchymale stamcellen, die ongeveer 25% van de celbronnen in de gekweekte vleesindustrie uitmaken, staan voor uitdagingen zoals de hoge kosten van groeifactoren, de noodzaak voor geoptimaliseerde serumvrije media, en de ontwikkeling van grootschalige bioreactoren (capaciteiten van 10.000–50.000 L)[1][9][11]. Bovendien blijft het waarborgen van de gewenste textuur wanneer cellen op 3D-structuren worden gezaaid een complexe taak[11].
"De huidige staat van gekweekt vlees staat voor aanzienlijke uitdagingen, waaronder hoge kosten, schaalbaarheidsproblemen en de noodzaak voor verdere technologische vooruitgang."
- Communications Biology [1]
Het overwinnen van deze uitdagingen vereist een uitgebreide aanpak die genetische optimalisatie combineert met vooruitgang in mediaformulering, bioreactortechnologie en differentiatieprotocollen. Hoewel CRISPR-schermen kritische genetische inzichten bieden, zal het vertalen van deze bevindingen naar schaalbare oplossingen geïntegreerde systemen en rigoureuze validatieprocessen vereisen. Deze inspanningen zijn van vitaal belang om de productie van gekweekt vlees van het laboratorium naar commerciële levensvatbaarheid te brengen.
Hoe Cellbase Ondersteunt CRISPR Onderzoek in Gekweekt Vlees
CRISPR-screening heeft zijn potentieel al aangetoond, maar het opschalen voor industrieel gebruik vereist toegang tot gespecialiseerde tools en middelen. Hier komt
Toegang tot CRISPR-bronnen via Cellbase
In tegenstelling tot breed-spectrum farmaceutische leveranciers, biedt
In november 2025,
"Elk bedrijf voor gekweekt vlees waarmee we spraken, verspilde tijd aan dezelfde inkoophoofdpijn. Het vinden van leveranciers voor kritieke componenten betekende het doorzoeken van pagina's met farmaceutische leveranciers die geen begrip hadden van voedseltoepassingen."
- David Bell, Oprichter van Cultigen Group [15]
Door deze middelen te centraliseren, versnelt
Het mogelijk maken van samenwerking in de ontwikkeling van gekweekt vlees
Het platform is ontworpen om de eisen van grootschalige commerciële projecten aan te kunnen, zoals die van Believer Meats en Aleph Farms . Deze ondernemingen vereisen infrastructuur voor 50.000-liter bioreactoren en geoptimaliseerde productieketens, die
Conclusie
High-throughput CRISPR-screening is geëvolueerd van een veelbelovend concept naar een cruciaal instrument in de ontwikkeling van gekweekt vlees. De impact van deze technologie op het optimaliseren van cellijnen is onmiskenbaar. Recente doorbraken hebben bijvoorbeeld aangetoond dat genetische modificaties de proliferatielevensduur van runderstamcellen kunnen verdubbelen van 100 tot 200 dagen, de populaties van senescente cellen kunnen verminderen van 60% tot slechts 10%, en een verbluffende 1.000-voudige toename in celrijkdom kunnen bereiken binnen een enkele maand [1]. Deze vooruitgangen markeren een duidelijke verschuiving van experimenteel onderzoek naar praktische industriële toepassingen.
Compacte platforms en gerichte bibliotheken pakken enkele van de meest urgente uitdagingen in het veld aan. Digitale microfluïdische systemen maken nu screening mogelijk met slechts 3.000 cellen per conditie, waardoor het haalbaar is om te werken met beperkte primaire dierlijke cellen die niet commercieel beschikbaar zijn.Ondertussen richten gespecialiseerde bibliotheken zoals MyoCRISPR-KOLib zich efficiënt op 90% van de relevante transcripties terwijl ze slechts een derde van het genoom dekken [3][6]. Dit niveau van precisie en efficiëntie is cruciaal voor het overwinnen van resourcebeperkingen en het opschalen van de productie.
"Deze bevindingen tonen het nut aan van CRISPR-screening voor het optimaliseren van eigenschappen van rundveestamcellen en bieden een pad naar meer schaalbare productie van gekweekt vlees in de toekomst." [1]
Ondanks deze vooruitgangen hangt succes af van toegang tot de juiste infrastructuur. Onderzoekers hebben soortspecifieke gRNA-bibliotheken nodig, groeimedia ontworpen voor voedseltoepassingen, compatibele bioreactoren en analytische hulpmiddelen die zijn afgestemd op de productie van gekweekt vlees in plaats van farmaceutisch gebruik.Het adresseren van deze behoeften,
Voor teams die werken aan het ontwikkelen van de volgende generatie gekweekte vleescellijnen, zijn de tools en technologieën gereed. De uitdaging ligt nu in de snelle en effectieve inzet van CRISPR-screening om het volledige potentieel te realiseren.
Veelgestelde vragen
Hoe kies je tussen CRISPR knockout, CRISPRi en CRISPRa voor een screening?
De keuze tussen deze systemen hangt af van je specifieke biologische vraag en het resultaat dat je wilt bereiken:
- CRISPR knockout: Deze methode verstoort de genfunctie volledig, waardoor het ideaal is voor het bestuderen van de effecten van genverlies of inactivatie.
- CRISPRi: Door genexpressie te onderdrukken zonder het DNA te knippen, is deze benadering zeer geschikt voor het onderzoeken van essentiële genen of wanneer omkeerbare onderdrukking vereist is.
- CRISPRa: Als u genexpressie moet opreguleren, is dit systeem de beste keuze. Het is bijzonder nuttig voor het onderzoeken van de effecten van overexpressie, zoals het bevorderen van celproliferatie of differentiatie.
Bij het beslissen, houd rekening met uw cellulaire model, de genen die u target, en de algemene doelen van uw experiment.
Hoe kunt u proliferatie stimuleren zonder de differentiatie van spier- of vetcellen te schaden?
Het stimuleren van de proliferatie van spier- of vetcellen terwijl hun vermogen om te differentiëren behouden blijft, is een belangrijke uitdaging in de productie van gekweekt vlees.Een veelbelovende benadering omvat CRISPR-gebaseerde genbewerking, die nauwkeurige manipulatie van genen mogelijk maakt om groei te verbeteren of de levensduur van cellen te verlengen. Bijvoorbeeld, het richten op myostatine (MSTN) kan celgroei bevorderen, terwijl het bewerken van CDKN2A cellen helpt om senescentie te omzeilen.
Dat gezegd hebbende, is het bereiken van een balans tussen proliferatie en differentiatie cruciaal. Mismanagement van bepaalde doelen, zoals P53 (TP53), kan differentiatie belemmeren, wat mogelijk de weefselkwaliteit in gevaar brengt. Om deze complexiteiten te navigeren, is high-throughput CRISPR-screening van groot belang. Deze techniek identificeert de meest effectieve genregulatoren, wat de weg vrijmaakt voor schaalbare en gezonde weefselontwikkeling in de productie van gekweekt vlees.
Wat is er nodig om CRISPR-screenhits te valideren voordat een cellijn wordt opgeschaald?
Het valideren van CRISPR-screenhits voor de productie van gekweekt vlees vereist een methodische aanpak. Eerst moet de genfunctie worden bevestigd door middel van onafhankelijke experimenten, zoals gen-knockouts, om ervoor te zorgen dat de waargenomen effecten reproduceerbaar zijn. Vervolgens is het cruciaal om de biologische relevantie van deze genen te evalueren door hun impact op factoren zoals celproliferatie, levensvatbaarheid en levensduur te onderzoeken.
Veiligheidsbeoordelingen zijn even belangrijk om off-target effecten of genetische instabiliteit uit te sluiten die het proces zouden kunnen compromitteren. Functionele validatie onder omstandigheden die industriële omgevingen nabootsen, zoals bioreactoren, is een andere cruciale stap. Dit zorgt ervoor dat de genetische bewerkingen presteren zoals verwacht in grootschalige productieomgevingen. Grondige tests in elke fase zijn ononderhandelbaar voordat opschaling wordt overwogen.











