A estabilidade genética é crítica para a produção de carne cultivada. Sem ela, as linhagens celulares podem sofrer mutações, levando a qualidade inconsistente, riscos de segurança e falhas na produção. A ampliação de milhares para trilhões de células amplifica esses riscos, tornando essenciais sistemas robustos de controle de qualidade. Reguladores como a FDA e a EMA exigem prova de estabilidade antes de aprovar produtos, já que até mesmo pequenas alterações genéticas podem desencadear resultados alérgicos ou prejudiciais.
Os principais desafios incluem a deriva genética, o acúmulo de mutações e a ativação de oncogenes. Esses problemas surgem do prolongado passaging celular, pressões seletivas e estressores ambientais durante a produção. Métodos avançados de teste, como cariotipagem, arrays de SNP e sequenciamento de nova geração (NGS), ajudam a detectar e abordar esses riscos. Estratégias preventivas como o banco de células estruturado e a engenharia genética direcionada protegem ainda mais contra a instabilidade.
Os produtores devem integrar o controle de qualidade em cada etapa da produção - desde o banco de células até biorreatores em larga escala. Ferramentas como perfilamento STR, testes de contaminação e ensaios funcionais garantem consistência e segurança. Plataformas como
Acelerando o Desenvolvimento de Linhas Celulares do DNA ao Banco de Células Mestre - AGC Biologics
Desafios Comuns na Manutenção da Estabilidade Genética
Garantir a estabilidade genética ao longo do ciclo de produção de carne cultivada não é uma tarefa fácil. A escala pura da produção introduz muitas oportunidades para que mudanças genéticas se desenvolvam e se espalhem. Reconhecer esses desafios é fundamental para implementar sistemas eficazes de controle de qualidade.
Deriva Genética e Acumulação de Mutações
A passagem celular estendida é uma fonte importante de instabilidade genômica na produção de carne cultivada. Linhagens celulares imortalizadas, por sua natureza, são propensas a mudanças genômicas, o que pode levar a mutações espontâneas durante o cultivo a longo prazo [6][5]. À medida que as células passam por múltiplas duplicações populacionais, erros na replicação do DNA se acumulam, resultando em populações celulares diversas e, potencialmente, em perda de função. Christopher Frye e Luhong He da BioPharm International destacam essa questão:
Linhagens celulares CHO derivadas clonalmente têm sido frequentemente observadas a divergir, tornando-se uma população heterogênea ao longo de longos períodos de subcultivo [6].
Em ambientes industriais, cerca de 20% das linhas celulares de produção mostram considerável heterogeneidade de transgenes ao longo de gerações sucessivas [6]. Essas mutações podem ocorrer logo no início, durante a replicação do DNA após a transfecção, ou devido a erros quando genes estrangeiros são integrados ao genoma do hospedeiro [5].
Pressões seletivas adicionam outra camada de complexidade. Agentes como antibióticos e marcadores metabólicos (e.g. , MTX) usados para estabilizar linhas celulares podem, na verdade, aumentar as taxas de mutação [6][5]. Em alguns casos, quanto maior a concentração desses agentes, maior a taxa de mutação [6]. Estressores ambientais - como escassez de nutrientes, condições de cultura subótimas durante a ampliação e estresse físico da expansão - podem desestabilizar ainda mais a integridade genética [6][5].
htmlShuai Wang, Diretor de Desenvolvimento de Linhas Celulares na WuXi Biologics, observa:
Os níveis de mutação provavelmente mudarão durante a passagem celular devido à plasticidade genômica das células de ovário de hamster chinês (CHO) [5].
Mudanças epigenéticas também desempenham um papel. Transgenes podem ser parcial ou completamente perdidos ou silenciados durante o processo de cultura, afetando a estabilidade a longo prazo. Essas mutações acumuladas não apenas prejudicam a função celular, mas também aumentam o risco de ativação de oncogenes.
Riscos de Ativação de Oncogenes
A ativação de oncogenes representa uma preocupação crítica de segurança para os produtores de carne cultivada, pois pode comprometer lotes inteiros de produção. A instabilidade genética pode levar à ativação de oncogenes por meio de mecanismos como hipermetilação, que pode resultar em perfis semelhantes a tumores [3][1]. A rápida expansão necessária na produção aumenta ainda mais a probabilidade de acumular essas mutações prejudiciais [5][6].
Este é um desafio bem reconhecido. De acordo com o Consórcio Internacional para Inovação & Qualidade no Desenvolvimento Farmacêutico (IQ), 67% dos entrevistados acreditam que as mutações genéticas representam uma ameaça maior do que a incorporação incorreta de aminoácidos durante a produção [5] . Um caso de maio de 2024 ilustra a gravidade deste problema: a WuXi Biologics descobriu que 43% dos clones de um programa de desenvolvimento de linhagem celular carregavam a mesma mutação pontual genética. A causa raiz? Um nível de variante de 2,1%–2,2% no DNA plasmidial usado durante a transfecção, que não foi detectado pela tradicional sequenciação de Sanger. Para resolver isso, a empresa incorporou a Sequenciação de Próxima Geração (NGS) em seus processos de controle de qualidade para detectar tais variantes precocemente [5].
A detecção precoce de anomalias genéticas é crucial, pois alterações oncogênicas podem comprometer lotes inteiros. O cariótipo padrão de banda G pode identificar subpopulações anormais com apenas 14% de mosaicismo em vinte metáfases celulares [1]. Técnicas mais avançadas, como NGS, podem detectar mutações genéticas em células clonais com uma sensibilidade de 0,5% [5].
A análise de metilação do DNA é outra ferramenta valiosa para avaliar o potencial tumorígeno:
Como os níveis de metilação do DNA e a hipermetilação de certos genes ocorrem na iniciação e progressão do câncer, a análise dos perfis de metilação do DNA pode fornecer informações complementares sobre o potencial tumorígeno das células [3].
O verdadeiro desafio está em implementar sistemas de monitoramento robustos capazes de identificar essas mudanças antes que comprometam a segurança. Para os produtores de carne cultivada, manter a estabilidade genética durante a rápida expansão celular exige medidas avançadas de controle de qualidade. Plataformas especializadas como
Métodos de Teste de Controle de Qualidade
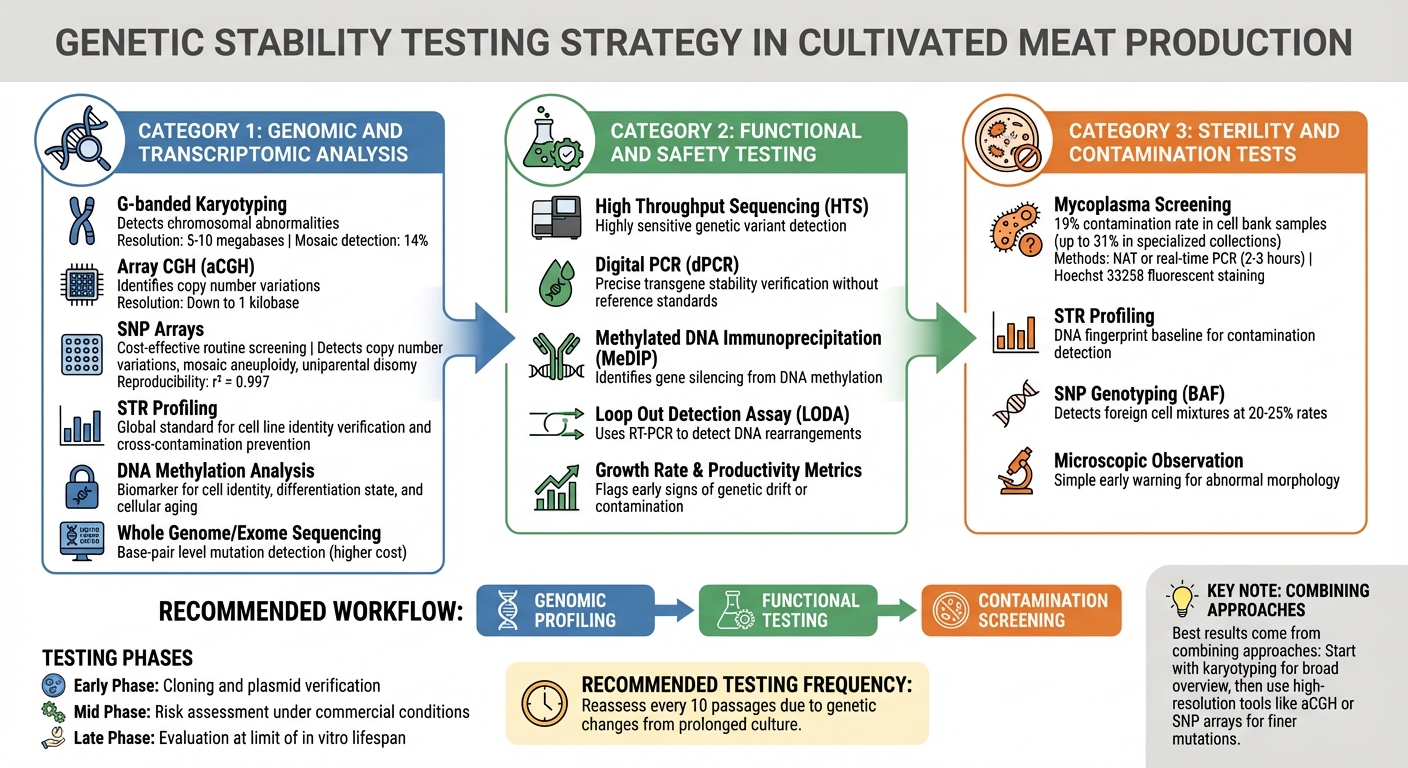
Métodos de Teste de Controle de Qualidade para Estabilidade Genética em Linhagens Celulares de Carne Cultivada
Identificar a instabilidade genética antes que ela impacte a produção requer uma estratégia de teste em várias camadas. Os produtores de carne cultivada dependem de métodos que detectam desde grandes alterações cromossômicas até mutações de base única. A escolha das técnicas depende dos riscos presentes em cada estágio de produção. Essas ferramentas genômicas atuam como o primeiro ponto de verificação, seguidas por avaliações funcionais e de contaminação detalhadas.
Análise Genômica e Transcriptômica
Cariótipo em bandas G é uma ferramenta chave para identificar problemas cromossômicos importantes, como anomalias numéricas e grandes rearranjos estruturais, como translocações. Embora possa detectar níveis de mosaico em torno de 14%, sua resolução é limitada a alterações de 5–10 megabases, o que significa que alterações menores podem passar despercebidas [1] .
Hibridização Genômica Comparativa em Array (aCGH) oferece maior resolução, identificando variações no número de cópias até 1 kilobase. Da mesma forma, arrays de Polimorfismo de Nucleotídeo Único (SNP) fornecem uma opção econômica para triagem de rotina, detectando variações no número de cópias, aneuploidia em mosaico e dissomia uniparental. Estudos de validação mostraram que os arrays SNP são altamente reprodutíveis, com medições de Frequência do Alelo B (BAF) alcançando um impressionante r² = 0.997 [8] [1].
Rocio Aguilar-Quesada do Biobanco do Sistema de Saúde Pública da Andaluzia destaca o valor de combinar métodos:
O cariotipagem continua sendo um ensaio versátil, especialmente quando complementado com testes de alta resolução [1].
O perfil de Repetição Curta em Tandem (STR) é o padrão global para verificar a identidade de linhas celulares e prevenir contaminação cruzada [1] [9]. Enquanto isso, a análise de metilação do DNA serve como um biomarcador para identidade celular, estado de diferenciação e envelhecimento celular [1] . Para detecção de mutações a nível de pares de bases, o sequenciamento do genoma completo ou do exoma é uma opção, embora venha com custos mais altos em comparação com métodos baseados em array [1] .
htmlOs melhores resultados vêm da combinação dessas abordagens. Comece com o cariótipo para uma visão geral ampla, depois use ferramentas de alta resolução como aCGH ou arrays de SNP para capturar mutações mais finas. A reavaliação regular - idealmente a cada 10 passagens - é crítica, pois o cultivo prolongado pode levar a alterações genéticas [10]. Esses insights genômicos são então complementados com ensaios funcionais para garantir um comportamento celular consistente durante toda a produção.
Testes Funcionais e de Segurança
O perfil genômico sozinho não é suficiente. Testes funcionais confirmam que as células mantêm suas características pretendidas durante a expansão. Métricas como taxas de crescimento e produtividade podem sinalizar sinais precoces de deriva genética ou contaminação [9].
Sequenciamento de Alta Vazão (HTS) é altamente sensível para detectar variantes genéticas, enquanto PCR digital (dPCR) verifica precisamente a estabilidade do transgene sem a necessidade de padrões de referência [11]. Christopher Frye e Luhong He da BioPharm International destacam a importância desta etapa:
A linha celular de produção é a base de qualquer bioprocesso e, portanto, a caracterização genética apropriada da linha celular de produção é absolutamente crucial para o sucesso do desenvolvimento do processo [6].
A estabilidade epigenética também é crítica. Imunoprecipitação de DNA Metilado (MeDIP) ajuda a identificar o silenciamento de genes causado pela metilação do DNA, uma razão comum para o declínio da produtividade [7]. Ferramentas como o Loop Out Detection Assay (LODA) usam RT-PCR para detectar rearranjos de DNA, como quando um gene de interesse é deletado enquanto o marcador selecionável permanece [7].
Os testes devem estar alinhados com a fase de produção: testes de fase inicial focam na clonagem e verificação de plasmídeos, testes de fase intermediária avaliam riscos em condições comerciais, e testes de fase final avaliam células no limite de sua vida útil in vitro [6]. Iniciar experimentos com células frescas e de baixa passagem de um banco de células mestre reduz o risco de deriva genética [9].
Testes de Esterilidade e Contaminação
O teste de contaminação é essencial para evitar fatores que possam desestabilizar a genética. Mycoplasma é particularmente preocupante, pois altera o metabolismo e o comportamento celular sem causar mudanças visíveis na cultura [1]. Estudos revelam contaminação por micoplasma em 19% das amostras de bancos de células, com algumas coleções especializadas mostrando taxas de até 31% [1].
O rastreamento regular de micoplasma usando Técnicas Sensíveis de Amplificação de Ácidos Nucleicos (NAT) ou PCR em tempo real pode fornecer resultados semiquantitativos em 2–3 horas [1]. A coloração fluorescente Hoechst 33258 é outro método, revelando padrões característicos de fluorescência extracelular [9].
O perfil STR estabelece uma impressão digital de DNA para linhas celulares, atuando como uma linha de base para detectar contaminação cruzada [9]. Além disso, a genotipagem por SNP usando distribuições de Frequência do Alelo B (BAF) pode identificar contaminação de outras linhas celulares, detectando misturas de células estrangeiras em taxas de 20–25% [8].
A observação microscópica é uma ferramenta de alerta precoce simples, mas eficaz, pois a morfologia celular anormal muitas vezes sinaliza problemas na cultura [9]. A implementação de um Sistema de Gestão da Qualidade, como ISO 9001:2015, junto com as Boas Práticas de Métodos In Vitro (GIVIMP), ajuda a manter condições de cultura padronizadas e reprodutíveis, reduzindo o risco de instabilidade genômica [10].
Para produtores de carne cultivada que precisam de acesso a equipamentos e materiais de teste especializados, plataformas como
sbb-itb-ffee270
Estratégias de Prevenção para Instabilidade Genética
Detectar a instabilidade genética é uma coisa; preveni-la é outro desafio completamente diferente.Para manter a estabilidade genética intacta, os produtores de carne cultivada precisam de sistemas bem planejados que impeçam as linhagens celulares de se desviarem antes que surjam problemas. Duas estratégias principais lideram o caminho aqui: banco de células estruturado e engenharia genética direcionada. Juntas, essas abordagens enfrentam diretamente os riscos de deriva genética e ativação de oncogenes.
Banco de Células e Criopreservação
O acúmulo de mutações é uma preocupação real, por isso um sistema confiável de banco de células é essencial. O padrão da indústria envolve um sistema de dois níveis: um Banco de Células Mestre (MCB) e um Banco de Células de Trabalho (WCB). Essa configuração garante um ponto de partida consistente para a produção. Limitar o número de passagens é crucial, pois cada passagem aumenta a chance de mutações. Ao armazenar células em nitrogênio líquido, a atividade biológica é efetivamente pausada, reduzindo o risco de alterações genéticas durante o armazenamento.
Em vez de rastrear o tempo, a idade celular é medida por dobramentos populacionais. Por exemplo, um biorreator de produção típico de 5.000 litros envolve cerca de 30 dobramentos populacionais[6]. Para manter a consistência genética, a fabricação comercial limita esse número entre 45 e 60 dobramentos[6].
Métodos de triagem como RT-PCR e qPCR de célula única podem detectar problemas precocemente, como emendas incomuns de mRNA ou variabilidade de transgene. Linhagens celulares que mostram grande variabilidade no número de cópias devem ser descartadas para evitar problemas futuros.
O controle de qualidade é inegociável. Alarmantemente, estudos descobriram que até 31% das linhagens celulares em alguns bancos estavam contaminadas com micoplasma [3] . Para evitar isso, o perfil STR é usado para confirmar a autenticidade das linhagens celulares durante todo o processo de armazenamento.Conforme destacado pela Pesquisa e Evidência da FSA:
Como as células armazenadas são o material de partida para o produto final, altos padrões podem ser exigidos por reguladores no futuro para garantir um produto de carne seguro e de alta qualidade[2].
Engenharia Genética para Estabilidade
A engenharia genética fornece outra camada de defesa ao melhorar diretamente a estabilidade da linha celular. Técnicas como integração direcionada (TI), particularmente Troca de Cassete Mediado por Recombinase (RMCE), permitem a inserção precisa de transgenes em locais genômicos específicos. Essa abordagem evita a imprevisibilidade da integração aleatória, onde efeitos de posição e instabilidade do número de cópias podem causar estragos. Embora o RMCE em células CHO tenha taxas de eficiência abaixo de 0,1%[12], os clones resultantes são mais previsíveis e estáveis.
A escolha do sistema de expressão também é importante. Por exemplo, o sistema de Glutamina Sintetase (GS) normalmente resulta em cerca de cinco cópias de transgene por célula, enquanto o sistema de Redutase de Dihidrofolato (DHFR) pode amplificar o número de cópias até 1.000[6] . Embora números de cópias mais altos possam parecer atraentes, eles aumentam a probabilidade de alterações no DNA, tornando os sistemas baseados em GS uma escolha mais inteligente para estabilidade a longo prazo.
Para minimizar ainda mais os riscos, a mutagênese específica de sítio e a triagem NGS pré-transfecção são cruciais. Como o sequenciamento de Sanger tem um limite de detecção mais alto, o NGS pode detectar mutações de plasmídeos abaixo de 0,5%, melhorando o sucesso da triagem de clones para mais de 90%[5] .
Shuai Wang e colegas da WuXi Biologics destacam a importância dessa vigilância:
Como a otimização de processos não pode corrigir mutações a nível genético, monitore rigorosamente os níveis de mutação em clones estáveis[5].
Para produtores que necessitam de ferramentas especializadas - seja para criopreservação, engenharia genética ou caracterização de linhagens celulares -
Integrando Controle de Qualidade na Produção
Incorporar controle de qualidade em cada fase da produção é crucial. Sem um sistema estruturado, mesmo linhagens celulares bem mantidas podem sofrer alterações durante a expansão e aumento de escala. O controle de qualidade não deve ser uma reflexão tardia - deve ser uma parte central da produção. Isso começa na fase de expansão, onde sistemas de gestão rigorosos e ambientes controlados desempenham um papel fundamental.
Controle de Qualidade Durante a Expansão e Escalonamento
Como discutido anteriormente, testes genômicos e de contaminação são vitais, especialmente durante o escalonamento. Passar de pequenos volumes para milhares de litros introduz novos riscos, com cada passagem de célula aumentando a chance de mutações. Um Sistema de Gestão da Qualidade (SGQ) ajuda a gerenciar esses riscos de forma eficaz. Por exemplo, entre 2017 e 2022, Josep M. Canals e sua equipe na Universidade de Barcelona implementaram o SGQ ISO 9001:2015 para padronizar culturas de células-tronco pluripotentes humanas. Sua análise retrospectiva de dados de bandeamento G e aCGH revelou uma redução significativa em aberrações cromossômicas em comparação com as condições pré-adaptação[10] [13] . Os canais destacaram a importância do monitoramento contínuo:
A instabilidade genética mostrada por hPSCs em cultura torna a reavaliação frequente da integridade genômica um requisito essencial ao planejar usá-los para experimentos[10].
O rastreamento genômico de rotina é indispensável. Técnicas como cariotipagem por G-banding e aCGH detectam alterações estruturais, enquanto Next-Generation Sequencing (NGS) identifica mutações em níveis abaixo de 0,5%[5]. A análise da curva de crescimento também pode sinalizar problemas precocemente, como contaminação ou deriva genética[9] . O monitoramento ambiental adiciona outra camada de segurança, com práticas como teste de placa de sedimentação e verificações semestrais de filtros HEPA garantindo que o ambiente de produção permaneça estável e livre de estresse para as linhagens celulares[4].
A consistência em meios e reagentes é igualmente importante. Usar meios definidos e sem soro, como o mTeSR1, juntamente com reagentes com Certificado de Análise, ajuda a reduzir a variação entre lotes e limita o risco de contaminação viral[10][4]. Verificações regulares de morfologia - simples observações microscópicas em diferentes densidades de cultura - podem detectar sinais precoces de diferenciação ou estresse[9]. Para aquisição de equipamentos ou reagentes especializados, plataformas como
Ensaios Funcionais para Consistência do Produto
Enquanto o monitoramento genômico protege o processo, os ensaios funcionais garantem que as células desempenhem conforme o esperado.A estabilidade genética por si só não é suficiente; as células também devem manter sua capacidade de funcionar corretamente em diferentes lotes de produção. Em carne cultivada, isso significa confirmar que células-tronco, como células satélite musculares, ainda podem se diferenciar em tecido muscular ou adiposo maduro após a expansão[2] . Ensaios de diferenciação são essenciais para verificar isso.
Ensaios metabólicos como MTT, LDH e Resazurina fornecem insights sobre a saúde e viabilidade celular[4][9]. Estes, combinados com perfil de Repetição Curta em Tandem (STR), ajudam a confirmar que as linhagens celulares permanecem autênticas e livres de contaminação cruzada durante todo o processo de produção[1][9].
Análise transcricional é outro passo crítico.Xiaoyue Chen e Sam Zhang recomendam:
Recomenda-se o sequenciamento de cDNA em vez de DNA genômico para a detecção de mutações a fim de avaliar os riscos no nível de transcrição[5].
Este método oferece uma imagem mais precisa do produto final, pois reflete como os genes são expressos em vez de apenas suas localizações genômicas. Ao combinar a triagem genômica com ensaios funcionais, os produtores podem garantir que cada lote atenda a padrões rigorosos de segurança, qualidade e desempenho em todas as etapas da produção.
Conclusão
Manter a estabilidade genética é fundamental para produzir carne cultivada de forma segura e consistente. Francisco J. Molina-Ruiz e seus colegas do Laboratório de Células-Tronco e Medicina Regenerativa destacam os riscos:
Mudanças genéticas em hPSCs poderiam comprometer não apenas a segurança dos produtos celulares baseados em hPSC...mas também levam a uma propensão de diferenciação heterogênea do material de partida, perfis de expressão gênica alterados e ineficiência do produto celular final [10].
As apostas são significativas - mais de 531 linhas celulares mal identificadas foram registradas pelo Comitê Internacional de Autenticação de Linhas Celulares [1].
Abordar essas questões requer uma estrutura robusta de controle de qualidade. Isso envolve a combinação de métodos como perfilamento STR, cariotipagem por bandamento G, aCGH e NGS avançado [5], junto com sistemas como ISO 9001:2015 para padronizar processos e minimizar anomalias cromossômicas [13].
Fatores econômicos também impulsionam a necessidade dessas medidas.A deriva genética pode resultar em células mutadas ganhando uma vantagem de crescimento, potencialmente estragando lotes inteiros de produção [10][11]. Com o foco crescente em células-tronco pluripotentes humanas, a demanda por linhas celulares estáveis nunca foi tão alta. Como explica o Professor David L. Kaplan da Universidade Tufts:
Linhas celulares imortalizadas são geralmente consideradas um requisito para a geração de grandes quantidades de tecido comestível a partir de um bioprocesso estável e robusto [14] .
Para os produtores de carne cultivada, o controle de qualidade deve estar embutido em cada etapa - desde a triagem de plasmídeos até o monitoramento da produção em larga escala. Ao combinar testes rigorosos com estratégias preventivas, os produtores podem garantir resultados consistentes e confiáveis.
Perguntas Frequentes
Com que frequência o teste de estabilidade genética deve ser realizado durante a ampliação?
O teste de estabilidade genética é uma etapa crucial durante a ampliação e deve ser realizado regularmente. A frequência desse teste depende em grande parte da linha celular específica e do processo em questão. Para reduzir as chances de mutações e manter a pluripotência das células, é aconselhável estabelecer um limite de passagens com base na análise genética.
Quais testes detectam melhor pequenas mutações e grandes alterações cromossômicas?
Testes como análise de array de SNP e genotipagem de SNP em todo o genoma são e
Qual é a maneira mais simples de prevenir a deriva genética entre lotes de produção?
Para minimizar a deriva genética, é crucial realizar análises genéticas e funcionais regulares das linhagens celulares e restringir o número de passagens que elas sofrem. Implemente práticas como o estabelecimento de bancos de células mestres e a verificação rotineira da estabilidade genética, conforme recomendado nos protocolos de controle de qualidade. Essas medidas são fundamentais para manter a consistência e garantir resultados confiáveis entre diferentes lotes de produção.











