A validação da limpeza garante que os equipamentos de produção em instalações de carne cultivada sejam completamente limpos para remover resíduos como detritos celulares, meios de crescimento e micróbios. É crucial para prevenir a contaminação cruzada, especialmente em configurações de múltiplos produtos.
Pontos principais:
- Por que é importante: Sem a limpeza adequada, resíduos de um lote podem contaminar o próximo. Equipamentos compartilhados, como biorreatores e ferramentas, são áreas de alto risco.
- Padrões Regulamentares: O cumprimento de diretrizes como HACCP, GMP e regulamentos específicos do Reino Unido é obrigatório.
-
Etapas para Validar a Limpeza:
- Escolha os agentes de limpeza adequados (e.g. , alcalinos para proteínas, ácidos para minerais).
- Teste sob condições de "pior caso" (e.g. , resíduos pegajosos ou de alta proteína).
- Use amostragem por swab e defina limites mensuráveis (e.g. , 10 ppm para resíduos químicos).
- Realize três ciclos de limpeza consecutivos para garantir a eficácia.
- Ferramentas de Monitoramento: Swabs de ATP, análise de TOC e placas microbiológicas ajudam a verificar a limpeza.
A validação da limpeza não é apenas sobre segurança - é sobre garantir uma produção consistente e confiável e manter a confiança nos produtos de carne cultivada.
Requisitos Regulatórios e de Biossegurança
Diretrizes Regulatórias Relevantes
No Reino Unido, a carne cultivada está sob a supervisão da Food Standards Agency (FSA) e da Food Standards Scotland (FSS). Essas agências avaliam riscos e estabelecem requisitos para tais produtos dentro do quadro de Alimentos Novos. Além disso, certos produtos podem precisar cumprir com regulamentos de OGM ou PBO.
O cumprimento dessas regulamentações depende de sistemas de garantia de qualidade bem estabelecidos:
- HACCP (Análise de Perigos e Pontos Críticos de Controle): Foca na identificação e controle de perigos microbianos.
- GMP (Boas Práticas de Fabricação): Garante produção consistente e controle de qualidade.
- GCCP (Boas Práticas de Cultura Celular): Aborda o manuseio de linhagens celulares para minimizar riscos de contaminação.
- GHPs (Boas Práticas de Higiene): Abarca padrões operacionais e ambientais gerais.
Os princípios do Codex Alimentarius formam a base para a elaboração de diretrizes específicas da indústria e planos de controle de qualidade, tomando como referência setores como as indústrias clínica e biofarmacêutica.
"Os princípios do Codex e do HACCP fornecem uma base sólida para construir diretrizes específicas e planos de controle de qualidade para este setor, e aprendizados podem ser extraídos da indústria clínica/biotecnológica e adaptados aos novos requisitos alimentares."
– FSA Research and Evidence [1]
Para garantir a confiabilidade, as validações de microbiologia e limpeza devem estar alinhadas com os padrões UKAS. Lições das práticas clínicas e biotecnológicas podem ser adaptadas para a produção de alimentos, abordando os desafios únicos que as instalações de carne cultivada enfrentam.
Riscos de Biossegurança em Plantas Multi-Produto
Instalações que produzem múltiplos produtos de carne cultivada enfrentam preocupações de biossegurança que vão além dos riscos típicos da fabricação de alimentos. Estes incluem:
- Patógenos alimentares tradicionais: Como enterobactérias e vírus animais.
- Contaminantes ocultos: Como micoplasma e micobactérias, que escapam da detecção em meios de cultura, pois não causam turbidez visível e requerem testes especializados.
Esses riscos são particularmente elevados em configurações de equipamentos compartilhados, onde inspeções visuais sozinhas não podem garantir a limpeza. A validação eficaz da limpeza é essencial para eliminar substâncias nocivas, como endotoxinas, exotoxinas e micotoxinas, mesmo em quantidades mínimas.
Técnicas avançadas de monitoramento podem ajudar a mitigar esses riscos. Por exemplo, o monitoramento em linha dos níveis de pH e oxigênio dissolvido pode sinalizar o crescimento microbiano precocemente, indicando possíveis falhas de limpeza ou esterilização. Além disso, o monitoramento ambiental do ar, superfícies e água dentro da instalação pode identificar ameaças de contaminação antes que afetem a produção.
"À medida que a indústria continua a desenvolver e adaptar equipamentos e processos para a produção de CCP, a limpeza, esterilização e outros procedimentos relevantes precisarão de avaliação e validação, e padrões nacionais/internacionais devem ser desenvolvidos."
– Pesquisa e Evidência da FSA [1]
Essas medidas destacam a importância crítica de protocolos rigorosos de limpeza e validação para prevenir a contaminação cruzada e garantir a segurança de cada lote de produção.
sbb-itb-ffee270
Validação de Limpeza em 10 Etapas na Indústria Farmacêutica | Diretriz Completa de Validação de Limpeza
Criando um Protocolo de Validação de Limpeza
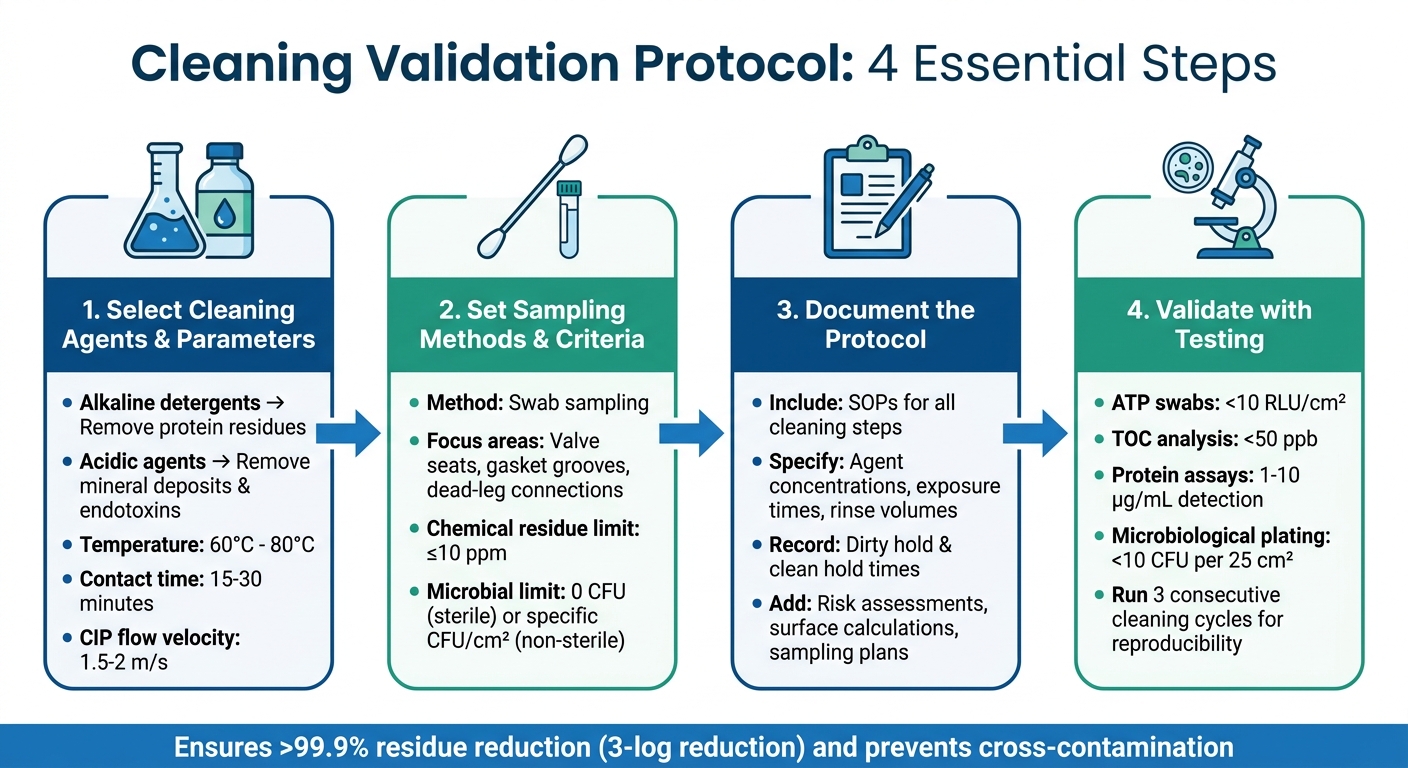
Protocolo de Validação de Limpeza em 4 Etapas para Instalações de Carne Cultivada
Selecionando Agentes de Limpeza e Parâmetros
Escolher os agentes de limpeza corretos depende do tipo de resíduo e dos materiais usados em seu equipamento. Para instalações de carne cultivada, biorreatores de aço inoxidável (geralmente grau 316L) são comuns. Estes requerem detergentes alcalinos para remover resíduos de proteínas, enquanto agentes ácidos são ideais para combater depósitos minerais e endotoxinas. Para maximizar a eficácia dos detergentes sem danificar vedações ou juntas, mantenha as temperaturas de limpeza entre 60°C e 80°C.
Permita que os agentes de limpeza permaneçam em contato por 15–30 minutos, especialmente em áreas complicadas como lâminas do impulsor e portas de sensores . Para sistemas de limpeza no local (CIP), garanta uma velocidade de fluxo de 1,5–2 m/s para remover efetivamente o biofilme. Esses parâmetros devem ser meticulosamente documentados, pois formam a espinha dorsal do seu estudo de validação.
Definindo Métodos de Amostragem e Critérios de Aceitação
A amostragem por swab é o método preferido para detectar resíduos nas superfícies dos equipamentos. Concentre-se em áreas que são mais difíceis de limpar, como assentos de válvulas, ranhuras de juntas e conexões de pernas mortas. Esses pontos fornecem um teste robusto de quão eficaz é o seu processo de limpeza.
Os critérios de aceitação devem ser fundamentados em evidências científicas. Para resíduos químicos, um limite de 10 ppm é amplamente reconhecido, representando 1/1000 de uma dose terapêutica ou um nível toxicologicamente seguro.Para a carga microbiana, produtos estéreis exigem uma ausência completa de organismos viáveis, enquanto produtos não estéreis podem permitir contagens específicas de unidades formadoras de colônias (UFC) por centímetro quadrado. Ao definir limites de resíduos, considere a área total da superfície do equipamento e leve em conta os cenários de produtos mais desafiadores.
"Um protocolo de validação de limpeza é um plano detalhado que descreve todas as atividades de validação. Ele compreende um objetivo específico de validação e o agrupamento de produtos e equipamentos a serem validados." – Kazi, Especialista em GMP [3]
Todos os métodos de amostragem e critérios de aceitação devem ser rigorosamente registrados no protocolo.
Documentando o Protocolo
Uma vez estabelecidos os parâmetros de limpeza e métodos de amostragem, compile o processo completo de limpeza em um protocolo detalhado. Esta documentação deve aderir tanto aos padrões regulatórios quanto aos de biossegurança.Inclua procedimentos operacionais padrão (SOPs) que descrevam cada etapa do processo de limpeza, desde o pré-enxágue inicial até a inspeção final. Especifique as concentrações dos agentes de limpeza, tempos de exposição, volumes de enxágue, verificações de validação e as durações para os tempos de "dirty hold" e "clean hold" .
Além disso, inclua avaliações de risco, cálculos de área de superfície, planos de amostragem e validações para métodos analíticos. O relatório final de validação, uma vez aprovado pela administração, confirmará se o seu processo de limpeza atende a todos os critérios exigidos e está em conformidade com as regulamentações [3] .
Realizando Estudos de Validação
Escolhendo Cenários de Pior Caso
Identificar os desafios de limpeza mais difíceis é fundamental para provar que seu processo de limpeza funciona efetivamente.Em instalações de carne cultivada, resíduos como meios de crescimento ricos em proteínas ou andaimes de carne cultivada pegajosos que aderem às paredes do biorreator estão entre os mais difíceis de remover.
Comece classificando seus produtos com base em fatores como solubilidade, viscosidade, teor de proteína e quanto tempo permanecem em contato com as superfícies. Por exemplo, meios de crescimento com uma concentração de proteína de 20% que foram usados por 72 horas aumentam o risco de desnaturação e formação de biofilme [4][5]. Preste atenção especial a equipamentos com designs intrincados - como lâminas de impulsor, assentos de válvula e portas de sensores - pois essas áreas são notoriamente difíceis de limpar. Cenários de teste, como um meio rico em gordura versus um meio rico em açúcar, também podem ajudar a cobrir o espectro de produtos que você manuseia [6][7].
Depois de definir os piores cenários, concentre-se em validar o processo repetindo os ciclos de limpeza.
Realizando Ciclos de Limpeza Consecutivos
Realizar três ciclos de limpeza consecutivos é uma maneira eficaz de confirmar tanto a reprodutibilidade quanto a eficiência. Esta abordagem imita configurações reais de produção, garantindo que nenhum resíduo seja transportado entre os lotes - especialmente crítico ao mudar de meios contendo alérgenos.
Para começar, suje o equipamento com o produto identificado como pior caso (e.g. , 10% de meio de crescimento em um biorreator). Em seguida, execute um ciclo de limpeza completo de acordo com seu protocolo, amostrando tanto antes quanto depois da limpeza. Repita este processo mais duas vezes sem sujar novamente o equipamento. Os dados mostram que, até o terceiro ciclo, os níveis de resíduo para solos de proteína são reduzidos em mais de 99,9% (uma redução de 3-log) [4][8]. Os testes em planta piloto mostraram consistentemente que os níveis de ATP caem abaixo de 10 RLU/cm² após ciclos consecutivos [5][9].
Depois de confirmar resultados de limpeza consistentes, utilize uma variedade de métodos de detecção de resíduos para validação completa.
Métodos de Teste para Detecção de Resíduos
Para garantir a biossegurança e atender aos padrões regulatórios, combine múltiplos métodos de detecção de resíduos. Swabs de ATP são um bom ponto de partida, oferecendo triagem rápida para resíduos orgânicos e micróbios, com limites de detecção tão baixos quanto 100 RLU (equivalente a menos de 1.000 UFC/cm²). A análise de carbono orgânico total (TOC) é outra ferramenta essencial, medindo resíduos orgânicos de meios de crescimento com limites aceitáveis tipicamente definidos abaixo de 50 partes por bilhão.Para a detecção específica de proteínas - crítica na produção de carne cultivada - ensaios como Bradford ou BCA podem identificar resíduos em concentrações tão baixas quanto 1–10 µg/mL [6][7].
A placa microbiológica adiciona outra camada de precisão ao identificar células viáveis que permanecem após a limpeza. Use placas de contato ou swabs em superfícies limpas, incubando amostras a 30–35°C por 48–72 horas em ágar de soja tripticase. Produtos estéreis geralmente requerem menos de 10 UFC por 25 cm². Pesquisas conduzidas em superfícies de aço inoxidável demonstraram menos de 1 UFC após três ciclos de limpeza [8][10]. Para aplicações de carne cultivada, combine swabs de ATP para verificações rápidas com métodos avançados como HPLC-MS para detectar alérgenos traço, como soro fetal bovino, em níveis tão baixos quanto 0,1 ppm [6][7].
Para orientação sobre equipamentos de teste compatíveis com GMP, consulte
Fonte de Equipamentos de Validação de Limpeza via Cellbase
Depois de configurar métodos eficazes de detecção de resíduos, o próximo passo é garantir que você tenha o equipamento certo para manter seus processos de validação de limpeza.
Equipamentos e Suprimentos Compatíveis com GMP para Validação
Ao adquirir swabs, peça aos fornecedores dados de recuperação para confirmar sua eficácia.A orientação do Health Canada [2] enfatiza que os processos de limpeza devem aderir aos princípios de Gestão de Risco de Qualidade. Para atender a esses padrões, certifique-se de que suas ferramentas de amostragem tenham sido validadas por meio de estudos de recuperação. Além disso, verifique se a sensibilidade de suas ferramentas de detecção de resíduos corresponde aos Limites de Exposição Baseados na Saúde (HBEL) que você calculou.
Concentre-se em fornecedores em
Soluções para Instalações de Carne Cultivada Multi-Produto
Instalações multi-produto enfrentam desafios únicos, particularmente o risco de contaminação cruzada ao alternar entre linhas celulares ou meios que possam conter alérgenos.
Se você depende de sistemas CIP automatizados, procure equipamentos que rastreiem parâmetros críticos de limpeza, como temperatura, pressão e taxa de fluxo. A Health Canada destaca que "O HBEL, como o PDE ou TTC, pode então ser usado na identificação de riscos e justificativa dos limites máximos seguros de transporte para o próximo produto" [2]. O equipamento CIP disponível através de
Conclusão
A validação de limpeza desempenha um papel crucial na garantia da segurança e confiabilidade da produção de carne cultivada de múltiplos produtos. Vai além de atender aos requisitos regulatórios - é um investimento na manutenção de padrões de segurança, eficiência operacional e confiança do consumidor. Ao validar minuciosamente que os processos de limpeza eliminam a contaminação cruzada de produtos e riscos de biossegurança, as instalações não apenas cumprem as normas, mas também minimizam as chances de recalls custosos ou interrupções operacionais, enquanto reforçam a confiança nos produtos de carne cultivada.
A chave para uma validação de limpeza eficaz está em estabelecer metas claras e mensuráveis que estejam alinhadas com as expectativas regulatórias.Por exemplo, substituir objetivos vagos por metas específicas - como definir taxas aceitáveis de remoção de resíduos - garante responsabilidade e melhora os resultados de produção. Essa abordagem não apenas satisfaz as exigências regulatórias, mas também fornece uma estrutura sólida para as medidas práticas delineadas anteriormente.
A consistência é vital. Realize revisões trimestrais para avaliar a eficácia dos protocolos de limpeza e faça ajustes com base nos dados de desempenho. Use os indicadores principais e de atraso recomendados para acompanhar o progresso e atualize a documentação regularmente à medida que surgirem novos insights ou mudanças regulatórias [4].
Perguntas Frequentes
Como defino limites de resíduos para cada troca de produto?
Para estabelecer limites de resíduos, comece com uma avaliação de risco completa para identificar resíduos críticos que possam representar uma preocupação. Utilize técnicas analíticas avançadas como HPLC (Cromatografia Líquida de Alta Eficiência) ou análise de TOC (Carbono Orgânico Total) durante o processo de validação para medir os níveis de resíduos com precisão.
Depois de coletar dados das execuções de limpeza, empregue métodos estatísticos - como calcular a média mais 2 ou 3 desvios padrão - para determinar limites aceitáveis. Esses cálculos ajudam a definir limites que são seguros e em conformidade com os padrões da indústria.
É essencial revisar e refinar regularmente esses limites. O monitoramento contínuo e a validação garantem que os limites de resíduos permaneçam eficazes e alinhados com os requisitos de segurança no campo em constante evolução da produção de carne cultivada.
Qual é a melhor maneira de escolher um solo de "pior caso" em uma planta de múltiplos produtos?
Ao escolher um solo de "pior caso" em uma instalação de carne cultivada de múltiplos produtos, concentre-se no resíduo que é mais difícil de limpar ou que apresenta o maior risco de contaminação cruzada. Isso pode incluir certas proteínas, gorduras ou componentes do meio. Ao testar métodos de limpeza nesse resíduo desafiador, você pode confirmar que o processo é suficientemente completo para gerenciar todos os outros resíduos, garantindo uma descontaminação eficaz em toda a planta.
Quando devo revalidar a limpeza após uma mudança de processo ou receita?
Revalidar a limpeza torna-se essencial sempre que houver mudanças nos processos, materiais ou equipamentos que possam afetar a eficiência do protocolo de limpeza ou introduzir novos resíduos. Este passo garante que resíduos como proteínas, gorduras ou detritos celulares sejam removidos de forma eficaz, reduzindo o risco de contaminação.Além disso, a revalidação regular deve fazer parte dos procedimentos de rotina para manter a conformidade e os padrões de biossegurança nas instalações de produção de carne cultivada.











