Fetal bovine serum (FBS) yerine serum-free media (SFM) kullanmak, kültive edilmiş et üretimini ölçeklendirmek için kritiktir. FBS bağımlılığı, yüksek maliyetler, sınırlı tedarik ve tutarsız kalite gibi zorluklar yaratır. SFM, daha güvenli ve kontrollü bir alternatif sunar, ancak bazı engellerle birlikte gelir:
- Hücre Yapışma Sorunları: Myoblastlar, serum olmadan yapışmakta zorlanır ve genellikle laminin veya Matrigel gibi pahalı kaplamalar gerektirir. Koşullandırılmış medya veya belirli takviyeler yapışmayı iyileştirebilir.
- Daha Yavaş Büyüme Oranları: Serum-free sistemler, temel besin maddelerinden yoksundur, bu da azalmış çoğalma ve amonyak birikimine yol açar. Büyüme faktörleri eklemek ve glutamini alternatiflerle değiştirmek yardımcı olabilir.
- Tutarsız Medya Performansı: Birçok ticari SFM, insan hücreleri için optimize edilmiştir ve hayvan myoblast büyümesini etkili bir şekilde destekleyemez. Türler arasında ve daha uzun süreler boyunca medya optimizasyon keşif kiti ile test yapmak çok önemlidir.
Çözümler, özel formülasyonlar, kısmi ortam değişimi ve serum benzeri koşulları taklit etmek için ortak kültür sistemlerini içerir. SFM, FBS sistemlerinin performansına yaklaşabilse de, 3D biyoreaktörlere ölçeklendirme, yapışma ve atık yönetimi gibi karmaşıklıkları beraberinde getirir. Hücre kalitesinin dikkatli izlenmesi, büyük ölçekli üretimde başarıyı garanti eder.
SFM'ye geçiş sadece daha iyi bilimle ilgili değil - FBS fiyatları yükselmeye devam ettikçe bir gereklilik haline geliyor. Araştırmacılar ve üreticiler, kültive edilmiş et üretimini uygulanabilir ve maliyet açısından etkili hale getirmek için ortamı optimize etmeye ve güvenilir malzemeler temin etmeye odaklanmalıdır.
Serum içermeyen hücre yapışmasını indükleyen bitki bazlı iskeleler - Indi Geurs - ISCCM9
sbb-itb-ffee270
Myoblastlar için Serum İçermeyen Medyada Yaygın Sorunlar
Serum bazlı formülasyonlardan serum içermeyen formülasyonlara geçiş, iş akışlarını aksatan ve maliyetleri artıran çeşitli teknik zorluklar sunabilir. Bu sorunlar genellikle hücre yapışmasıyla başlayarak belirli şekillerde ortaya çıkar.
Azalmış Hücre Yapışması ve Hayatta Kalma
En büyük engellerden biri, myoblastların serum içermeyen medyada iyi yapışmamasıdır. Serum, hücrelerin yüzeylere yapışmasına yardımcı olan proteinler, büyüme faktörleri ve lipidlerin doğal bir karışımını sağlar. Bu bileşenler olmadan, myoblastlar yapışmakta zorlanır ve bu genellikle erken hücre ölümüne yol açar.
Bunu çözmek için, birçok serum içermeyen sistem pahalı kaplama ajanlarına, örneğin laminin 511 veya Matrigel. Ancak bu kaplamalarla bile, bağlanma seviyeleri genellikle serum bazlı kültürlerde görülenin gerisinde kalır. Örneğin, 2024 yılında yapılan bir çalışma, standart serumsuz medyanın kaplanmamış tabaklarda sadece 2,210 ± 319 hücre/cm² desteklediğini bulmuştur. Buna karşılık, diğer hücre hatlarından salgılanan faktörlerle takviye edilmiş bir şartlandırılmış serumsuz ortam, bu rakamı neredeyse üç katına çıkararak 5,985 ± 1,558 hücre/cm²'ye ulaştırmıştır [2].
Başka bir sorun ise antibiyotiklere karşı artan hassasiyettir. Serumsuz düzeneklerde, Penisilin, Streptomisin ve Amfoterisin B gibi antibiyotikler, serum bazlı sistemlere kıyasla çoğalmayı %62'ye kadar azaltabilir, bu oran serum bazlı sistemlerde %20–26 azalmadır [1]. Serumun koruyucu unsurları olmadan, hücreler strese karşı daha savunmasız hale gelir, bu da hayatta kalmalarını ve büyümelerini daha da engeller.
Daha Yavaş Hücre Büyümesi
Hücreler bağlanmayı başarsa bile, büyüme oranları genellikle geride kalır. Serum, büyüme faktörleri, sitokinler, kolesterol ve yağ asitleri gibi temel besin maddelerini sağlar - bunların çoğu, çoğu ticari serumsuz formülasyonlarda. eksik veya yetersizdir. Bu beslenme açığı, daha düşük hücre verimi ve daha uzun üretim süreleri ile sonuçlanır.
Başka bir komplikasyon, glutamin metabolizmasından kaynaklanan amonyak birikimidir. Amonyak büyümeyi engeller ve serumsuz koşullarda, hücreler zaten metabolik stres altındayken, bu toksisite genişlemeyi ciddi şekilde engelleyebilir. Birçok ticari ortam başlangıçta insan hücreleri için tasarlandığından, sığır veya domuz miyoblastlarının özel beslenme ihtiyaçlarını karşılamayabilir [1][3].
Besleme sırasında ortamın %75'ini değiştirmek gibi kısmi ortam değişimi, bazı endojen büyüme faktörlerini korumaya yardımcı olabilir.Bu mütevazı bir şekilde büyüme oranlarını iyileştirirken, serum içermeyen ve serum bazlı sistemler arasındaki farkı tamamen kapatmaz [1].
Ticari Ürünlerde Değişken Performans
Tüm ticari serum içermeyen medyalar eşit performans göstermez. Yedi formülasyonun karşılaştırıldığı bir çalışmada, yalnızca üçü - FBM™, Essential 8™ ve TeSR™-E8™ - altı gün boyunca tutarlı sığır miyoblast büyümesini destekledi. StemPro™ ve mTeSR1™ gibi diğerleri, büyümeyi dört gün boyunca destekledikten sonra dururken, STEMmacs™ tamamen çoğalmayı sürdüremedi [1].
Problem, çoğu ticari medyanın insan kök hücreleri veya fibroblastlar için optimize edilmiş olması, hayvan miyoblastları için değil. Biyomedikal araştırmalarda iyi çalışan şeyler, kültive edilmiş et üretiminde genellikle yetersiz kalır. Bu tutarsızlık, özellikle hayvan miyoblastlarına yönelik formülasyonlara olan ihtiyacı vurgular.İnsan hücreleri için üretici verileri, bir ortamın sığır veya domuz hücreleriyle ne kadar iyi performans göstereceğini güvenilir bir şekilde tahmin edemez.
Doğru serumsuz ortamı bulmak için, uzun süreli testler yapmak çok önemlidir - ideal olarak altı ila on gün boyunca - bu, sadece kısa vadeli büyümeyi değil, sürdürülebilir hücre genişlemesini desteklediğinden emin olmak için.
Ticari Serumsuz Ortam Seçeneklerini Karşılaştırma
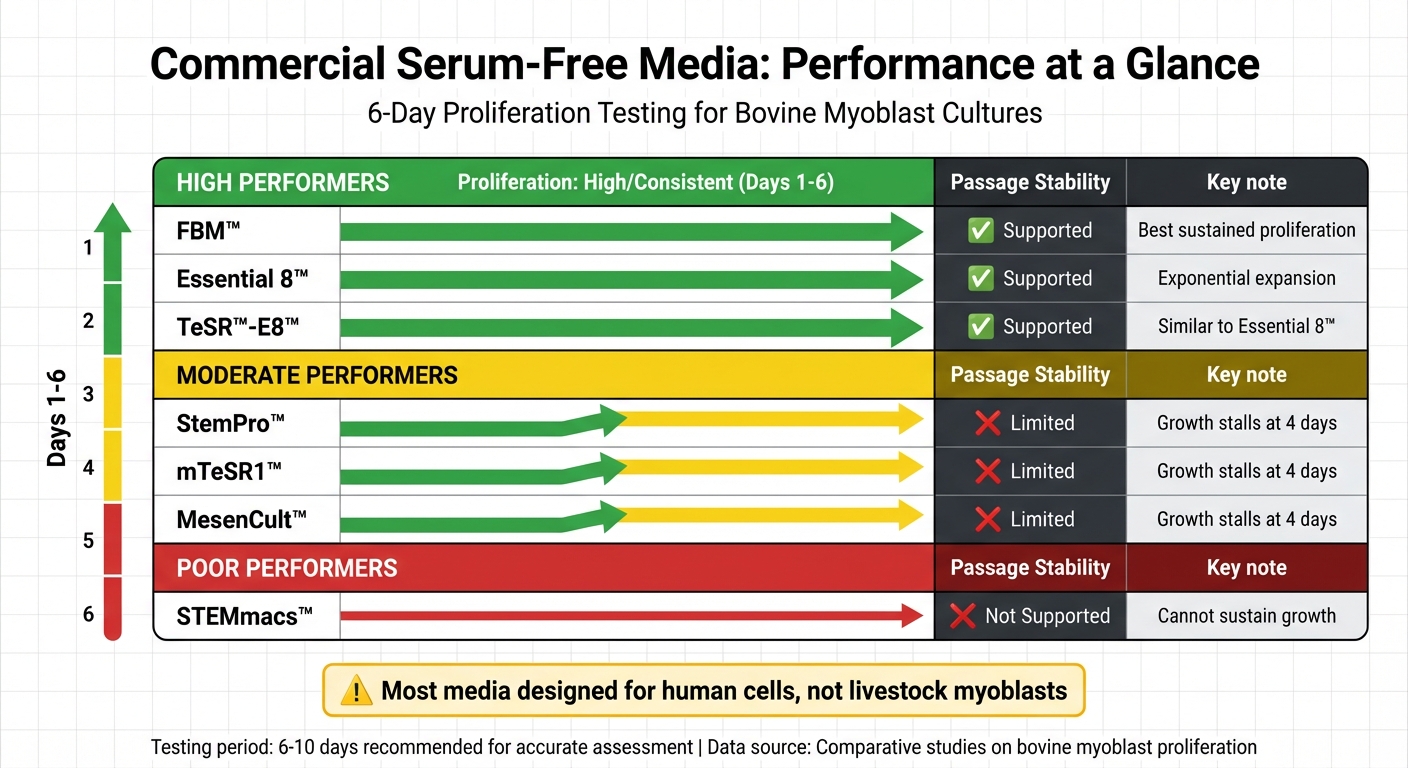
Sığır Miyoblast Kültürleri için Ticari Serumsuz Ortamların Performans Karşılaştırması
Yaygın Ortamlar için Performans Verileri
Miyoblast kültürleri için serumsuz ortam söz konusu olduğunda, performans büyük ölçüde değişebilir. FBM™, Essential 8™, ve TeSR™-E8™, gibi bazı ürünler, altı gün boyunca sığır miyoblast proliferasyonunu sürekli olarak destekler. Buna karşılık, StemPro™, mTeSR1™, ve MesenCult™, gibi diğerleri sadece dört gün sonra durma eğilimindedir.Bu arada, STEMmacs™ büyümeyi tamamen sürdüremiyor [1].
htmlİşte bu medyaların performans metriklerinin hızlı bir karşılaştırması:
| Ortam | Çoğalma (Gün 1–6) | Geçiş Kararlılığı | Ana Gözlemler |
|---|---|---|---|
| FBM™ | Yüksek/Tutarlı | Desteklenmiş | Sürdürülebilir çoğalma için en iyi potansiyeli sunar [1] |
| Essential 8™ | Yüksek/Tutarlı | Desteklenmiş | Serum bazlıdan daha az olsa da üstel genişlemeyi destekler [1] |
| TeSR™-E8™ | Yüksek/Tutarlı | Desteklenmiş | Esansiyel 8™ ile sığır miyoblastları için benzer [1] |
| StemPro™ | Orta | Sınırlı | Büyüme dört gün sonra durur [1] |
| mTeSR1™ | Orta | Sınırlı | Büyüme dört gün sonra durur [1] |
| MesenCult™ | Orta | Sınırlı | Büyüme dört gün sonra durur [1] |
| STEMmacs™ | Düşük/Yok | Desteklenmiyor | Sığır miyoblast büyümesini sürdüremiyor [1] |
İlginç bir şekilde, FBM™ hariç çoğu ortam, serum bazlı kontrollerle karşılaştırıldığında ekimden sonraki 24 saat içinde önemli ölçüde daha düşük hücre sayıları gösterir.Bu, özellikle gıda güvenliği için büyüme ortamlarındaki düzenleyici eğilimler göz önüne alındığında, bir ortam seçerken bu metriklerin değerlendirilmesinin önemini vurgulamaktadır.
Doğru Serumsuz Ortam Nasıl Seçilir
En iyi serumsuz ortamı seçmek sadece büyüme oranlarıyla ilgili değildir; çoğalma, yapışma ve maliyet etkinliği gibi birkaç faktörün dengelenmesini gerektirir. Altı günlük bir süre boyunca ortamların test edilmesi çok önemlidir, çünkü daha kısa testler yanıltıcı sonuçlar verebilir [1].
Tür özgüllüğü başka bir önemli husustur. Birçok serumsuz seçenek insan hücreleri düşünülerek tasarlanmıştır, bu da sığır veya domuz hücreleri gibi hayvan miyoblastlarının besin taleplerini karşılamayabileceği anlamına gelir. Farklı türlerin ve hücre durumlarının besin ihtiyaçları önemli ölçüde değişebilir, bu yüzden test etmek esastır [3].
Kaplama gereksinimleri de büyük bir rol oynar. Bazı ortamlar, hücre yapışmasını sağlamak için laminin veya Matrigel gibi pahalı kaplamalara ihtiyaç duyar. Süreciniz kaplanmamış yüzeyler veya gıda sınıfı malzemeler içeriyorsa, ortamın bu katkı maddeleri olmadan yapışmayı destekleyip destekleyemeyeceğini test etmek faydalı olabilir. Kaplanmamış kaplar için özel olarak hazırlanmış şartlandırılmış ortamlar veya formülasyonlar, maliyet açısından etkili bir alternatif olabilir [2] .
Diğer bir kritik faktör ise antibiyotik kullanımı. Penisilin/Streptomisin gibi standart antibiyotik kokteylleri, serum içeren ortamlarda miyoblast proliferasyonunu %20–26 oranında ve serum içermeyen sistemlerde %62'ye kadar azaltabilir. Antibiyotikleri ortadan kaldırmak, önemli ölçüde daha yüksek hücre verimlerine yol açabilir [1].
Son olarak, metabolik atık yönetimini. göz ardı etmeyinAmonyak birikimi kültürler için toksik olabilir, bu nedenle medyayı α-ketoglutarat veya piruvat gibi amonyak üretmeyen bileşiklerle takviye etmek iyi bir fikirdir. Bu katkı maddeleri amonyak toksisitesini azaltmaya ve kültürlerin ömrünü uzatmaya yardımcı olur [3].
Serum İçermeyen Miyoblast Kültürlerini İyileştirme Yöntemleri
Serum içermeyen miyoblast kültürlerinin zorluklarını ele almak hedefe yönelik stratejiler gerektirir. İşte performanslarını artırmak için bazı pratik yöntemler.
Anahtar Takviyelerin Eklenmesi
Belirli takviyelerin eklenmesi miyoblast büyümesini önemli ölçüde iyileştirebilir. FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), ve insülin (10 μg/ml) karışımının FBM gibi bazal medyada hücre genişlemesini artırdığı gösterilmiştir [1] . Bu büyüme faktörleri, üretim için gerekli olan farklılaşmamış durumu korurken hücre çoğalmasını teşvik etmek için birlikte çalışır.
Amino asitler ve vitaminler de çok önemlidir. Piridoksamin (Vitamin B6), asparajin, ve glutamik asit gibi bileşikler, özellikle kaplanmamış yüzeylerde hücre yapışmasını ve çoğalmasını teşvik etmede önemli bir rol oynar [2] . Bu takviyeler, yapışma ile ilgili zorlukları ele alarak genellikle serum tarafından sağlanan metabolik desteği değiştirmeye yardımcı olur.
"Bileşen analizi ve doğrulama deneyleri, piridoksamin, asparajin ve glutamik asidin geliştirilen ortamın kültür fonksiyonunun kazanılmasına katkıda bulunduğunu öne sürdü." - npj Science of Food [2]
Ancak, LipoGro. gibi lipid bazlı takviyelerle dikkatli olunması gerekir.Büyümeyi teşvik edebilirken, aynı zamanda adipogenik farklılaşmayı da tetikleyebilirler, bu da miyoblastların yağ vakuolleri geliştirmesine ve kas hücresi kimliğini kaybetmesine neden olabilir [1].
Medya Formülasyonlarını Özelleştirme
Medya formülasyonlarını özelleştirmek, büyüme faktörü keşif kiti. kullanarak serum içermeyen kültürleri optimize edebilir. Etkili bir yaklaşım, koşullandırılmış medya. kullanmayı içerir. HepG2 (insan hepatoma) ve NIH/3T3 (fare fibroblast) hücrelerinin birlikte kültürlenmesiyle koşullandırılmış medya, fetal karaciğerin metabolik profilini taklit eder. Bu yöntem, kaplanmamış tabaklarda 5,985 ± 1,558 hücre/cm² hücre yoğunluğuna ulaşır, bu da serum içeren medya ile elde edilen 6,722 ± 1,500 hücre/cm² ile karşılaştırılabilir [2] . Bu hücre tipleri arasındaki etkileşim, büyümeyi artıran serum benzeri bileşenlerin salgılanmasını teşvik eder.
Diğer maliyet-etkin strateji kısmi ortam değişimi. Ortamın tamamını değiştirmek yerine sadece %75'ini değiştirerek, hücreler tarafından üretilen endojen büyüme faktörleri korunur, bu da ek takviyelere ihtiyaç duymadan büyüme oranlarını iyileştirir [1].
İnhibitörlerle Erken Farklılaşmayı Önleme
Proliferatif bir durumu sürdürmek, farklılaşma sinyallerinin dikkatli kontrolünü gerektirir. Örneğin, HepG2 hücrelerinden elde edilen şartlandırılmış ortam, miyojenik farklılaşma belirteci Desmin, ifadesini baskılayarak hücrelerin farklılaşmamış ve genişlemeye hazır kalmasını sağlar [2].
Ayrıca, CD29 (integrin beta-1) ve Ki67 gibi belirteçlerin izlenmesi, formülasyonun hücre proliferasyonunu sürdürmede etkili olduğunu ve erken farklılaşma riskini azalttığını garanti etmeye yardımcı olur. Bu işaretleyiciler, en iyi sonuçlar için kültür koşullarını izlemek ve ayarlamak için güvenilir bir yol sağlar.
Serumsuz Miyoblast Kültürlerini Üretim İçin Ölçeklendirme
3D Kültür Sistemlerine Geçiş
Serumsuz miyoblast kültürlerini düz 2D tabaklardan 3D biyoreaktör sistemlerine kaydırmak, özellikle hücre yapışması söz konusu olduğunda kendi zorluklarını beraberinde getirir. Laminin gibi pahalı ajanlarla biyoreaktör bileşenlerini kaplamak, büyük ölçekli üretim için pratik değildir. Ancak, HepG2 ve NIH/3T3 ortak kültürlerinden elde edilen şartlandırılmış medyayı kullanmak veya bazal medyayı pridoksamin, asparajin ve glutamik asit gibi bileşiklerle zenginleştirmek etkili olmuştur. Bu yöntemler, miyoblastların kaplanmamış 3D iskelelere ve mikro taşıyıcılara, yapışma sorunlarını pahalı kaplamalara başvurmadan çözmelerini sağlar [2].
Ölçeklendirmede bir diğer kritik faktör ise metabolik atık yönetimidir.Yoğun biyoreaktör kültürleri, toksik amonyak birikimi yaşayabilir, bu da glutaminin α-ketoglutarat, glutamat veya piruvat gibi amonyak üretmeyen alternatiflerle değiştirilmesiyle önlenebilir [3]. Bu ayarlamalar, küçük ölçekli sistemlerin ötesine geçerken gereklidir ve üretim sırasında miyoblastların bütünlüğünü korumak için dikkatli kalite kontrol ve sensör izleme gerektirir.
Adapted Kültürlerde Hücre Kalitesinin Onaylanması
Kültürler daha büyük ölçekli üretim için adapte edilirken, hücrelerin kalitesini sağlamak çok önemlidir. Transkriptomik, metabolomik ve fonksiyonel testler gibi teknikler, hücrelerin CD29 ve Ki67 seviyelerini yüksek tutarken Desmin ekspresyonunu baskıladığını doğrulamak için kullanılır. Bu belirteçler, hücrelerin ölçeklendirme süreci sırasında proliferatif, farklılaşmamış bir durumda kaldığını gösterir [2]. Bu göstergelerin izlenmesi, gıda sınıfı bileşenlere geçiş yapmak veya kısmi medya değişiklikleri kullanmak gibi maliyet tasarrufu önlemleri uygulandığında özellikle önemlidir. Bu adım, araştırma sınıfından üretim sınıfı sistemlere geçişin hücre kalitesini tehlikeye atmamasını sağlar. Bu parametrelerin ince ayarı, kültive edilmiş et üretimini ölçeklenebilir ve maliyet açısından verimli hale getirmek için kritik bir adımdır.
Serum İçermeyen ve Serum Bazlı Kültür Performansı
Optimum hale getirildiğinde, serum içermeyen sistemler geleneksel serum bazlı kültürlere yakın sonuçlar elde edebilir.Aşağıdaki tablo, kaplanmamış yüzeylerde yetiştirilen sığır miyoblast kültürlerinden elde edilen temel metrikleri vurgulamaktadır:
| Metrik | Serum Bazlı (20% FBS + 10% HS) | Koşullandırılmış Serumsuz |
|---|---|---|
| Hücre Yapışması (24s) | ~6,722 hücre/cm² | ~5,985 hücre/cm² |
| Hücre Proliferasyonu (72s) | ~10,050 hücre/cm² | ~8,998 hücre/cm² |
| CD29 İfadesi | Yüksek | Yüksek |
| Ki67 İfadesi | Yüksek | Yüksek |
| Desmin İfadesi | Baskılanmış | Baskılanmış |
Veriler npj Science of Food'dan alınmıştır [2]
Serum bazlı sistemler hala hücre yoğunluğunda hafif bir avantaja sahipken, serum içermeyen ortamlar yapışma belirteci ifadesinde benzer sonuçlar verir ve hücreleri farklılaşmamış halde tutar - üretim için önemli faktörler.Aradaki fark, formülasyonları optimize etmek için belirli takviyeler eklendiğinde daha da daralır ve bu da serum içermeyen sistemleri büyük ölçekli kültive edilmiş et üretimi için giderek daha pratik bir seçenek haline getirir.
Sonuç
Myoblast kültürlerini serum içermeyen ortama geçirmek, erken yapışma sorunları, daha yavaş hücre büyümesi ve ticari ürünlerden tutarsız sonuçlar gibi zorluklarla birlikte gelir. Ancak, antibiyotikleri çıkarmak ve kısmi ortam değişimlerini tercih etmek gibi basit değişiklikler, çoğalma oranlarını önemli ölçüde artırabilir [1]. Medya dikkatlice seçilerek ve belirli büyüme faktörleri eklenerek, araştırmacılar performans açısından serum içermeyen ve serum bazlı sistemler arasındaki farkı kapatabilir. Bu gelişmeler, üretimin ölçeklendirilmesinin önünü açar.
Ancak, serum içermeyen kültürlerin ölçeklendirilmesi, yeni karmaşıklık katmanları getirir. Hücreleri 3D biyoreaktör sistemlerine geçirirken fenotiplerini korumalarını sağlamak titiz bir kalite kontrolü gerektirir. Yine de, iyi optimize edilmiş serumsuz sistemlerin, serum bazlı medyada yetiştirilenlere benzer hücre yoğunluklarına ulaşabileceğine dair kanıtlar vardır. Bu, serumsuz yöntemleri ticari kültür et üretimi için giderek daha pratik hale getiriyor.
Serumsuz medyanın ekonomik argümanı göz ardı edilemez. FBS fiyatlarının artmaya devam etmesiyle, serum bazlı yöntemler finansal olarak uygulanamaz hale geliyor [1]. Bu değişim sadece teknik iyileştirmelerle ilgili değil - kültür et endüstrisi için ekonomik hayatta kalma meselesi.
Bu geçişi yapan araştırmacılar ve üretim ekipleri için doğru malzemeleri temin etmek esastır. Kimyasal olarak tanımlanmış medyadan rekombinant büyüme faktörlerine, güvenilir tedariklere erişim sağlamak anahtardır. Bu,
SSS
Laminin veya Matrigel olmadan serumsuz medyada miyoblast bağlanmasını nasıl geliştirebilirim?
Laminin veya Matrigel kullanmadan serumsuz medyada miyoblast bağlanmasını geliştirmek için, koşullandırılmış serumsuz ortam. kullanmayı düşünün. Bu yaklaşım, kaplanmamış tabaklarda bile yapışmayı ve çoğalmayı teşvik edebilir. Diğer bir seçenek, FGF2, fetuin, ve BSA. gibi bileşenler ekleyerek ortamı optimize etmektir. Bu ayarlamalar, hücre bağlanmasını ve büyümesini artırmada belirgin bir fark yaratabilir ve ekstraselüler matris kaplamalarına olan ihtiyacı ortadan kaldırabilir.
Serum içermeyen miyoblast kültürlerinde amonyak birikimini azaltmanın en hızlı yolu nedir?
Serum içermeyen miyoblast kültürlerinde amonyak birikimini azaltmak için, medya formülasyonunu iyileştirmeye odaklanın. Bir yaklaşım, hem hücre yapışmasını hem de çoğalmasını teşvik ederken amonyak seviyelerini düşük tutan şartlandırılmış medya kullanmaktır. Ayrıca, kültür koşullarını iyileştirmek amonyak üretimini en aza indirmeye yardımcı olabilir. Bu, hücrelerin metabolik ihtiyaçlarına daha iyi uyum sağlamak için pH, sıcaklık veya besin konsantrasyonları gibi faktörleri ayarlamayı içerebilir.
Serum içermeyen medyaya geçtikten sonra miyoblastların farklılaşmamış kaldığını nasıl doğrularım?
Serum içermeyen medyada kültürlendiğinde miyoblastların farklılaşmamış durumda kalmasını sağlamak için, belirli belirteçleri izlemek önemlidir.Pax7, farklılaşmamış miyoblastların güvenilir bir göstergesidir, miyozin ağır zinciri (MHC) gibi farklılaşma belirteçlerinin yokluğu ise farklılaşmaya başlamadıklarını doğrular.
Şu teknikleri kullanabilirsiniz:
- İmmünositokimya: Hücrelerdeki protein ifadesini görselleştirmek için.
- Akış sitometrisi: Geniş bir hücre popülasyonunda belirteç ifadesini analiz etmek için.
- qPCR: Anahtar belirteçlerin mRNA seviyelerini ölçmek için.
Ayrıca, hücreleri mikroskop altında gözlemlemek esastır. Miyoblastlar, farklılaşmanın açık bir işareti olan çok çekirdekli miyotüplerin oluşumundan kaçınarak, karakteristik görünümlerini korumalıdır. Bu yöntemleri birleştirerek ve düzenli olarak izleyerek, hücrelerin farklılaşmamış kalmasını sağlayabilirsiniz.











