High-throughput CRISPR-Screening revolutioniert den Bereich des kultivierten Fleisches, indem es präzise genetische Modifikationen ermöglicht, um die Leistung von Zelllinien zu verbessern. Hier ist, was Sie wissen müssen:
- Hauptherausforderung: Die Produktion von kultiviertem Fleisch erfordert Zelllinien, die effizient wachsen, dem Altern widerstehen und sich in Muskel- und Fettgewebe differenzieren.
- Rolle von CRISPR: Durch das gleichzeitige Anvisieren von Tausenden von Genen identifizieren diese Plattformen genetische Veränderungen, die das Wachstum verbessern, die Seneszenz verzögern und die Differenzierung unterstützen.
- Bemerkenswerte Ergebnisse: Studien haben gezeigt, dass das Ausschalten von Genen wie TP53 und PTEN in bovinen mesenchymalen Stammzellen die Proliferation innerhalb von 30 Tagen um das 1.000-fache steigern und ihre Lebensdauer von 100 auf 200 Tage verlängern kann.
- Anwendungen: CRISPR-Tools wie Knockout-Screens, CRISPRi und CRISPRa werden verwendet, um das Zellwachstum zu optimieren, die Genexpression zu regulieren und die Proliferation mit der Differenzierung in Einklang zu bringen.
- Industrielle Werkzeuge: Fortschrittliche Techniken wie RMCE, RNA-seq und Single-Cell-Plattformen integrieren CRISPR-Ergebnisse mit Multi-Omics-Daten und gewährleisten präzise und skalierbare Verbesserungen.
Für Bioprozessingenieure und F&E-Profis adressieren diese Innovationen kritische Engpässe bei der Skalierung von kultivierten Fleischprozessen, während die Zellqualität und Funktionalität erhalten bleibt. Die Integration von CRISPR mit automatisierten Systemen und maßgeschneiderten Ressourcen wie
CRISPR-Cas9 Grundlagen für genomweite Knockout-Screens
Wie CRISPR-Cas9 in der großflächigen Genbearbeitung funktioniert
Das CRISPR-Cas9-System basiert auf einer Cas9-Nuklease, die mit einer Einzelstrang-RNA (sgRNA) gepaart ist, um spezifische DNA-Sequenzen zu zielen. Sobald die sgRNA Cas9 an den gewünschten genomischen Ort leitet, erzeugt das Enzym einen Doppelstrangbruch in der DNA. Dieser Bruch wird überwiegend durch nicht-homologes End-Joining (NHEJ) repariert, ein fehleranfälliger Prozess, der oft kleine Insertionen oder Deletionen (Indels) einführt. Diese Indels können Frameshift-Mutationen verursachen, die die Funktion des Zielgens effektiv stören [1]. Dieser präzise Mechanismus ist die Grundlage für die Durchführung von genomweiten Knockout-Screens, die entscheidend für die Identifizierung kritischer Regulatoren des Zellverhaltens sind.
Für groß angelegte Screenings verwenden Forscher eine vielfältige Bibliothek von sgRNAs, die typischerweise durch lentivirale Transduktion in eine gemischte Zellpopulation eingebracht werden. Um sicherzustellen, dass jede Zelle nur eine genetische Veränderung erhält, wird eine niedrige Infektionsrate (MOI von etwa 0,3) beibehalten [1]. Im Laufe der Zeit neigen Zellen mit vorteilhaften Mutationen dazu, erfolgreicher zu proliferieren als andere, ein Phänomen, das in einer Vielzahl von Zelltypen und experimentellen Bedingungen beobachtet wird.
Alternative Liefermethoden, wie der rekombinase-vermittelte Kassettenaustausch (RMCE), bieten zusätzliche Präzision, indem sie spezifische genomische "Landeplätze" anvisieren, um die Variabilität der Integrationsstellen zu reduzieren. Zum Beispiel verwendete eine Studie mit CHO-K1-Zellen eine virusfreie RMCE-Methode, um 111.651 einzigartige gRNAs über 21.585 Gene zu screenen. Dieser Ansatz identifizierte Gene, die für die Zellfitness über Zeiträume von 16 und 37 Tagen essentiell sind [7].
Vorteile des genomweiten Screenings
Genomweite Knockout-Screens nutzen die Genauigkeit von CRISPR-Cas9, um systematisch Tausende von Genen zu untersuchen. Dies ermöglicht es Forschern, Gene zu entdecken, die das Überleben, das Wachstum und die Reaktionen von Zellen auf Stress beeinflussen. Neben genetischen Faktoren ist die Optimierung der Oberflächenfunktionalisierung entscheidend für die Verbesserung der Zellanhaftung und des Wachstums in diesen Systemen. Solche unvoreingenommenen Erkundungen sind besonders relevant für die Produktion von kultiviertem Fleisch , , wo mesenchymale Stammzellen (die etwa 25% der Zellquellen ausmachen) oft Herausforderungen wie begrenzte Proliferation und frühe Seneszenz gegenüberstehen [1].
sbb-itb-ffee270
Methoden des gepoolten CRISPR-Bibliotheksscreenings
Erstellung gepoolter CRISPR-Bibliotheken
Gepoolte CRISPR-Bibliotheken beginnen mit einer sorgfältig ausgewählten Sammlung von Einzel-Leit-RNAs (sgRNAs).Im Kontext der Forschung zu kultiviertem Fleisch werden gezielte Bibliotheken oft so entworfen, dass sie sich auf spezifische Genfamilien konzentrieren, wie z.B. Transkriptionsfaktoren oder Regulatoren der Zellproliferation. Dieser Ansatz hilft, die Kosten mit der Skalierbarkeit in Einklang zu bringen, während der Fokus auf Merkmalen liegt, die für den gewünschten Phänotyp relevant sind [1].
Der Prozess beginnt mit der Synthese von Oligonukleotiden als Pool, deren Amplifikation mittels PCR und dem Klonieren in einen Liefervektor. Zum Beispiel umfasste eine spezifische Bibliothek für Rinder, die Anfang 2025 konstruiert wurde, 3.000 sgRNAs, die auf 603 Gene abzielen, um Faktoren zu identifizieren, die die Expansion von Stammzellen beeinflussen [1]. In größerem Maßstab können genomweite Screens eine viel höhere Komplexität erreichen. Ein Beispiel ist ein Screen von Chinesischen Hamster-Ovarien (CHO)-Zellen, der 111.651 einzigartige gRNAs verwendete, um 21.585 Gene zu zielen [7].
Lentivirale Transduktion wird häufig verwendet, um diese Bibliotheken bei einer niedrigen Infektionsrate (ungefähr 0,3) zu liefern, wodurch sichergestellt wird, dass jede Zelle nur eine einzige genetische Modifikation durchläuft [1]. Alternativ integrieren virusfreie Methoden wie der rekombinasevermittelte Kassettenaustausch (RMCE) die gRNA-Bibliothek in vorbestimmte genomische "Landeplätze" innerhalb einer Master-Zelllinie. Diese Technik erreicht 99,9% gRNA-Abdeckung mit minimaler Verzerrung [7].
Um die statistische Zuverlässigkeit zu gewährleisten, sorgen Forscher für eine hohe Abdeckung - typischerweise 500 bis 600 Zellen pro sgRNA [1] [7] . Einige Plattformen verwenden induzierbare Cas9 (iCas9)-Systeme, die eine präzise Kontrolle darüber ermöglichen, wann die Genbearbeitung erfolgt. Zum Beispiel kann die Bearbeitung ausgelöst werden, nachdem die Zellen einen bestimmten Zustand erreicht haben, wie z.B. hohe Dichte oder der Beginn der Seneszenz.Diese zeitliche Kontrolle ist besonders nützlich für das Studium nicht-proliferativer Phasen, die entscheidend sind, um Seneszenzbarrieren zu überwinden, indem zwischen primären und immortalisierten Zelllinien für die Skalierung der Produktion von kultiviertem Fleisch gewählt wird [4] .
Sobald die Bibliothek erstellt ist, gehen die Forscher zu gezielten Screening-Assays über, um die Genfunktion zu bewerten.
Screening-Ansätze für kultivierte Fleischzelllinien
Nach dem Aufbau der Bibliothek bewerten die Forscher die Zellleistung mithilfe von Wettbewerbsassays und funktionellen Sortiertechniken. Eine weit verbreitete Methode ist der wettbewerbsbasierte Proliferationsassay, der genetische Veränderungen identifiziert, die Wachstum oder Seneszenzresistenz verleihen - Schlüsselmerkmale zur Optimierung von Zelllinien für kultiviertes Fleisch.
Kurzfristige Screens (etwa 30 Tage) identifizieren Gene, die den Zellzyklus sofort beeinflussen, während langfristige Screens (bis zu 200 Tage) sich auf Gene konzentrieren, die Zellen helfen, die replikative Seneszenz zu überwinden. Dies ist eine kritische Herausforderung bei der Skalierung der Produktion von kultiviertem Fleisch [1]. Für komplexere Merkmale, wie verbesserte Proteinausscheidung oder Expression spezifischer Marker, wird die Durchflusszytometrie (FACS) eingesetzt. Ein Beispiel ist der "Cold Capture Secretion Assay", der produktive Zellpopulationen isoliert, indem er sezernierte Proteine auf der Zelloberfläche einfängt, bevor sortiert wird [7] [5] .
Die Validierung ist ein entscheidender Schritt zur Bestätigung der Screening-Ergebnisse. Der Cellular Fitness (CelFi) Assay verfolgt beispielsweise das Verhältnis von Out-of-Frame- zu In-Frame-Mutationen über die Zeit.Wenn Zellen mit Out-of-Frame-Mutationen aus der Population verschwinden, deutet dies darauf hin, dass das Zielgen für die zelluläre Fitness essentiell ist [2].
Im Juni 2025 nutzten Forscher unter der Leitung von Shijie Ding an der Nanjing Agricultural University CRISPR/Cas9, um CDKN2A–/– porcine Satellitenzelllinien. zu erstellen. Diese modifizierten Zellen behielten eine stabile Proliferation für mindestens 15 Passagen unter serumfreien Bedingungen bei, während sie Stammzellmarker beibehielten. Als sie auf ein pflanzenbasiertes 3D-essbares Gerüst ausgesät wurden, bildeten sie fleischähnliche Konstrukte mit verbesserter Textur, einschließlich erhöhter Kaubarkeit und Gummigkeit [8].
"Diese Ergebnisse demonstrieren den Nutzen des CRISPR-Screenings zur Optimierung von Rinderstammzellmerkmalen und bieten einen Weg zu einer skalierbareren Produktion von kultiviertem Fleisch in der Zukunft." – Communications Biology [1]
Pooled CRISPR-Genetische Screens in Säugetierzellen | Protokollvorschau
CRISPRi und CRISPRa für reversible Genregulations-Screens
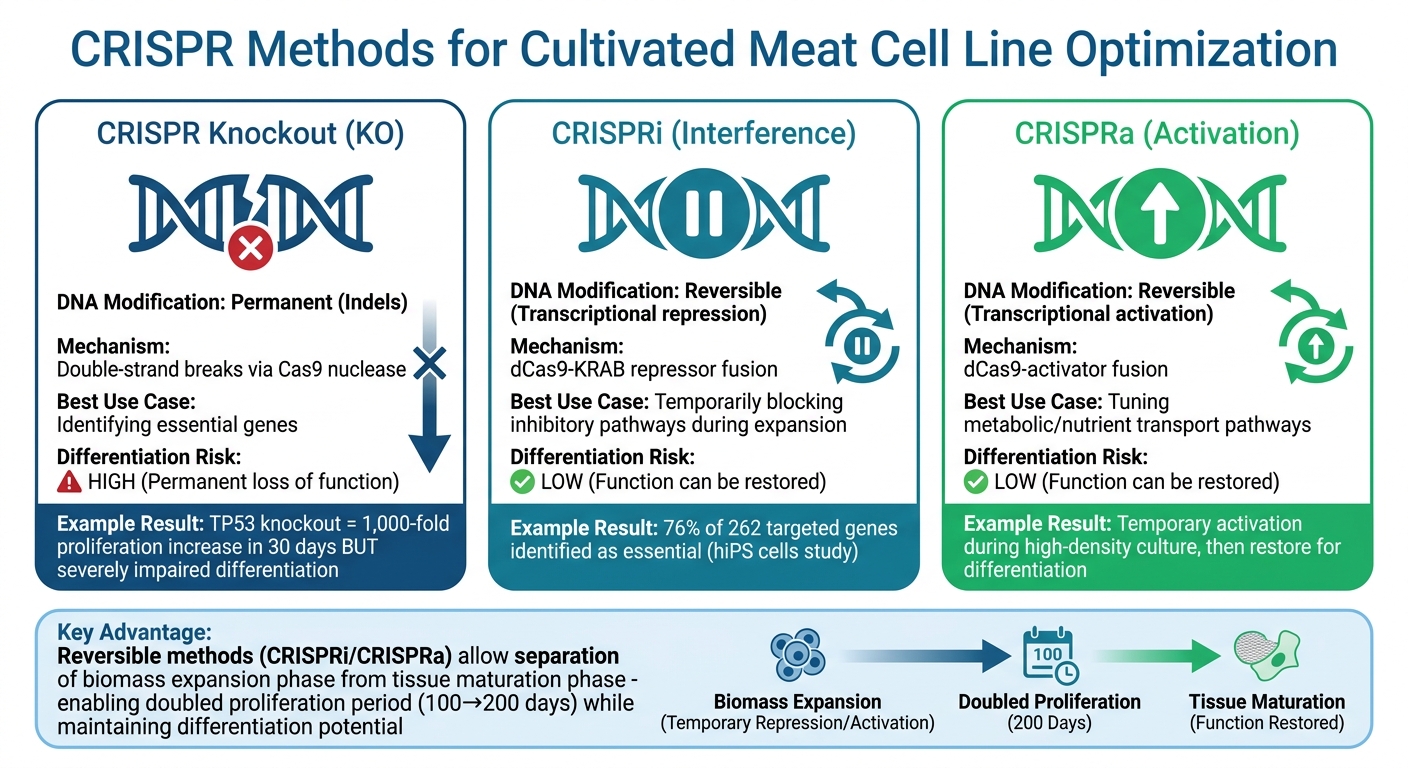
CRISPR-Geneditierungsmethoden für kultiviertes Fleisch: Vergleich von Knockout vs CRISPRi/CRISPRa
Verwendung von CRISPRi und CRISPRa in der funktionellen Genomik
Wenn es darum geht, die Produktion von kultiviertem Fleisch zu verbessern, bieten CRISPR-Interferenz (CRISPRi) und CRISPR-Aktivierung (CRISPRa) leistungsstarke Werkzeuge. Diese Techniken verwenden ein inaktives Cas9-Protein, das mit Repressoren oder Aktivatoren gepaart ist, sodass Forscher die Genexpression vorübergehend anpassen können, ohne dauerhafte Änderungen an der DNA vorzunehmen [10].
Diese Reversibilität ist besonders wichtig, um eine große Herausforderung anzugehen: Gene, die schnelles Zellwachstum fördern, stören oft die späteren Stadien der Differenzierung in Muskel- oder Fettgewebe. Zum Beispiel kann das permanente Ausschalten des TP53-Gens in bovinen mesenchymalen Stammzellen die Proliferation in nur 30 Tagen um das 1.000-fache erhöhen, beeinträchtigt jedoch stark ihre Fähigkeit zur Differenzierung [1]. CRISPRi bietet eine flexiblere Lösung, indem es vorübergehend Wege blockiert, die die Differenzierung während der Biomasseexpansion in Bioreaktoren für kultiviertes Fleisch hemmen. Sobald die Zellen für die Gewebereifung bereit sind, kann die normale Genfunktion wiederhergestellt werden.
Im Oktober 2025 entwickelten Forscher wie Gabriele Casagrande Raffi und Roderick L. Beijersbergen vom Netherlands Cancer Institute ein induzierbares CRISPR-System.Dieser Ansatz verzögert die Genbearbeitung, bis die Zellen bestimmte Zustände erreichen - wie hohe Dichte oder eine nicht-proliferative Phase - und hilft, die Zellviabilität zu erhalten [4].
CRISPRi zeichnet sich auch durch seine Präzision im Vergleich zur traditionellen RNA-Interferenz (RNAi) aus. RNAi führt oft zu inkonsistenten Ergebnissen und Off-Target-Effekten, während CRISPRi eine zuverlässigere und spezifischere Genunterdrückung liefert [2]. Ein weiterer Vorteil ist, dass CRISPRi die Auslösung von p53-bezogener Toxizität vermeidet, die oft durch DNA-Schadensantworten verursacht wird. In einer Studie von 2025, geleitet von Liqin Wang am Sun Yat-sen University Cancer Centre, verwendeten Forscher ein doxycyclin-induzierbares KRAB–dCas9-System, um 262 Gene in menschlichen induzierten pluripotenten Stammzellen (hiPS-Zellen) zu screenen. Sie fanden heraus, dass 76% der gezielten translationsbezogenen Gene (200 von 262) für das Wachstum essentiell waren, was die Effektivität des Systems demonstriert [10].
Diese Fähigkeit, die Genexpression fein abzustimmen, macht CRISPRi und CRISPRa zu wertvollen Werkzeugen, um Zellproliferation und Differenzierung in der funktionellen Genomforschung auszugleichen.
Anpassung reversibler Screens für Anwendungen in kultiviertem Fleisch
Reversible Genregulation bietet Lösungen für zentrale Herausforderungen in der Produktion von kultiviertem Fleisch. Zum Beispiel kann CRISPRa vorübergehend Gene aktivieren, die am Nährstofftransport oder an Stoffwechselwegen während der Hochdichtekultur beteiligt sind. Sobald die Zellen die gewünschte Dichte erreicht haben, kann das System die Genexpression auf normale Werte zurückführen, um die richtige Differenzierung in Muskel- oder Fettgewebe zu unterstützen.
Induzierbare Systeme ermöglichen es auch, die Phase der Biomasseexpansion von der Gewebereifung zu trennen. CRISPRi kann seneszenzassoziierte Gene während des Hochskalierungsprozesses unterdrücken und so die Proliferationsperiode von Rinderzellen effektiv von etwa 100 Tagen auf über 200 Tage verdoppeln [1]. Nach Erreichen ausreichender Biomasse können Forscher die normale Genexpression wiederherstellen, um die Differenzierung zu ermöglichen. Dieser Ansatz ist besonders nützlich für mesenchymale Stammzellen, die in der Kultur dazu neigen, frühzeitig in die Seneszenz einzutreten [1].
"Gezielte genetische Bearbeitung dieser beiden Prozesse könnte die Effizienz der MSC-Expansion optimieren, während ihre wesentliche Multipotenz und Differenzierungspotential erhalten bleiben, was letztendlich skalierbare kultivierte Fleischsysteme voranbringt." – Kommunikationsbiologie [1]
Die folgende Tabelle hebt die Unterschiede zwischen reversiblen und permanenten Genregulationsmethoden hervor:
| Merkmal | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| DNA-Modifikation | Permanent (Indels) | Reversibel (Transkriptional) |
| Mechanismus | Doppelstrangbrüche | dCas9-Effektor-Fusion |
| Beste Anwendungsfall | Identifizierung essentieller Gene | Abstimmung von Stoffwechsel-/Wachstumspfaden |
| Differenzierungsrisiko | Hoch (Permanenter Funktionsverlust) | Niedrig (Funktion kann wiederhergestellt werden) |
Dieser Vergleich veranschaulicht, wie reversible Genregulationsmethoden angepasst werden können, um den spezifischen Herausforderungen bei der Entwicklung von Zelllinien für die Produktion von kultiviertem Fleisch gerecht zu werden.
Kombinieren von CRISPR-Screens mit Zellpanel- und Genotypisierungstechnologien
Verknüpfung von CRISPR-Screens mit Multi-Omics-Analyse
Die Integration von Multi-Omics und automatisierter Genotypisierung in CRISPR-Screens verfeinert deren Nutzen, insbesondere bei der Entwicklung von Zelllinien für kultiviertes Fleisch.
Die Kombination von CRISPR-Screens mit Multi-Omics, wie z.B. RNA-Sequenzierung, ermöglicht es Forschern, die Auswirkungen spezifischer Gen-Knockouts auf zelluläre Signalwege zu kartieren. Dies ist besonders relevant für kultiviertes Fleisch, wo das Verständnis, wie Zellen Proliferation und Differenzierung ausbalancieren, entscheidend ist.
Zum Beispiel deckte ein gepoolter CRISPR-Knockout-Screen, der auf 600 Gene in aus Rinderfett gewonnene mesenchymale Stammzellen, abzielte und mit RNA-seq kombiniert wurde, auf, dass das Ausschalten von TP53 und PTEN die Seneszenz verzögerte.Diese Zellen behielten ein jugendliches Genexpressionsprofil bei, mit hochregulierten Zellzyklusgenen, was zu einer 50%igen Erhöhung der Verdopplungsrate bis Tag 50 nach der Transduktion führte [1] .
Einzelzellplattformen wie CROP-seq gehen noch einen Schritt weiter, indem sie gleichzeitig sowohl sgRNA als auch transkriptomische Veränderungen in einzelnen Zellen nachweisen [6]. Dieses Maß an Präzision ist von unschätzbarem Wert, um genetische Modifikationen zu identifizieren, die die Muskeldifferenzierung oder Proteinsynthese verbessern - kritische Faktoren für das Erreichen der gewünschten Textur und Nährwerteigenschaften in kultiviertem Fleisch.
Ein weiterer vielversprechender Ansatz beinhaltet das Screening von Zellpanelen, bei dem CRISPR-Störungen über verschiedene Zelllinien von verschiedenen Spendern, anatomischen Standorten und Spezies getestet werden. Zum Beispiel validierten Forscher die MyoCRISPR-KOLib-Bibliothek an menschlichen Myoblastenlinien von sieben Spendern. Mithilfe eines Split-Toxin-Auswahlsystems identifizierten sie 250 Gene, die für die Myoblastenfusion essentiell sind. Von diesen wurden 41 Gene durch medizinische Datenbanken bestätigt, eine Rolle in der Morphologie der Skelettmuskulatur zu spielen [6] . Diese mehrstufige Validierung stellt sicher, dass genetische Ziele über biologische Variationen hinweg robust bleiben, ein wichtiger Aspekt für die Skalierung der Produktion von kultiviertem Fleisch.
Diese Erkenntnisse ebnen den Weg für automatisierte, skalierbare Plattformen, die genetische Screens mit detaillierter Genotypisierung für industrielle Anwendungen kombinieren.
Automatisierung und Skalierbarkeit in integrierten Plattformen
Automatisierung ist entscheidend für die Handhabung der umfangreichen Datensätze und Proben, die von integrierten CRISPR- und Genotypisierungsplattformen erzeugt werden. RMCE-Systeme, die eine virusfreie, ortsspezifische Lieferung von sgRNA-Bibliotheken ermöglichen, sind ein bedeutender Fortschritt. Diese Plattformen stellen sicher, dass jede Zelle eine einzelne, konsistente sgRNA-Kopie erhält, was die Variabilität reduziert.RMCE hat bereits eine hohe Bibliotheksabdeckung mit minimalem Bias in chinesischen Hamster-Ovarien (CHO)-Zellen demonstriert [5].
"Eine unvoreingenommene Hochdurchsatz-Gen-Screening-Plattform ist entscheidend für die Entwicklung der nächsten Generation von CHO-Fabriken." - Chinesisches Hamster-Ovarien-Forschungsteam [5]
Die Skalierbarkeit wird weiter durch Validierungstools wie den Cellular Fitness (CelFi)-Assay verbessert. Dieser Assay verwendet gezielte Tiefensequenzierung, um Indel-Profile im Laufe der Zeit zu überwachen und das Verhältnis von In-Frame- zu Out-of-Frame-Mutationen zu verfolgen. Durch die Korrelation dieser Mutationen mit Wachstums-Vorteilen oder -Nachteilen können Forscher genetische Ziele in kultivierten Fleischzelllinien effizient verifizieren [2].
| Technologie | Integrationsmethode | Hauptvorteil für kultiviertes Fleisch |
|---|---|---|
| RNA-seq / Multi-Omics | Verknüpfung von CRISPR-Treffern mit transkriptomischen Profilen | Verständnis, wie Gene Wachstum und Differenzierung regulieren[1][6] |
| Split-Toxin-Systeme | Verknüpfung von Zellfusion mit Lebensfähigkeit | Quantitative Auswahl von fusionsfähigen oder defekten Zellen[6] |
| RMCE-Plattformen | Standortspezifische Integration von gRNA-Bibliotheken | Hochdurchsatz-, virenfreies Screening mit konsistenten Genkopienzahlen[5] |
| CROP-seq | Einzelzell-CRISPR + RNA-seq | Gleichzeitige Erkennung von sgRNA und transkriptomischen Veränderungen [6] |
| CelFi Assay | Zielgerichtete Tiefensequenzierung von Indels | Schnelle Validierung genetischer Ziele durch Verfolgung von Allelfrequenzverschiebungen [2] |
Diese fortschrittlichen Plattformen rationalisieren den Prozess von der Identifizierung genetischer Ziele bis zur Validierung ihrer Auswirkungen auf die Zellfitness. Diese Effizienz unterstützt die Entwicklung von Zelllinien, die robust genug für die großflächige Produktion von kultiviertem Fleisch sind.
Verwendung von CRISPR-Screens zur Verbesserung des Zelllinienwachstums und der Proliferation
CRISPR-Screening-Methoden sind zu einem leistungsstarken Werkzeug zur Verbesserung der Zelllinienleistung geworden und bieten direkte Vorteile für die Produktion von kultiviertem Fleisch.
Beispiele für CRISPR-basierte Verbesserungen von Zelllinien
CRISPR-Screens haben die Leistung von Zelllinien in der Forschung zu kultiviertem Fleisch erfolgreich verbessert. Zum Beispiel identifizierte ein gepoolter Knockout-Screen, der auf 600 Gene in aus Rinderfett gewonnenen mesenchymalen Stammzellen abzielte, TP53 und PTEN als wichtige Wachstumsinhibitoren. Das Ausschalten von TP53 erhöhte die Zellanzahl innerhalb von 30 Tagen signifikant[1] . Zusätzlich zeigten die bearbeiteten bovinen mesenchymalen Stammzellen eine durchschnittlich 12% höhere Verdopplungsrate [1].
Durch die gezielte Beeinflussung von Tumorsuppressorgenen verlängerten Forscher die proliferative Lebensdauer der Zellen von etwa 100 auf über 200 Tage und umgingen damit effektiv das Hayflick-Limit. Diese Verzögerung der Seneszenz ermöglicht eine Biomasseausdehnung über industriell relevante Zeiträume[1].
In einem weiteren Beispiel entwickelten Forscher der Nanjing Agricultural University unter der Leitung von Shijie Ding, Chunbao Li und Guanghong Zhou mithilfe von CRISPR/Cas9 CDKN2A−/− porcine Satellitenzelllinien. Diese entwickelten Zellen behielten eine stabile Proliferation für mindestens 18 Passagen in einem maßgeschneiderten 19-Komponenten-serumfreien Medium (A19) bei. Sie wurden auch erfolgreich auf essbaren Gerüsten, angesiedelt und schufen fleischähnliche Konstrukte mit verbesserter Kaubarkeit und Gummigkeit[8]. Die Zellen behielten über 90% Lebensfähigkeit über mehrere Passagen in serumfreien Bedingungen bei[8].
"Die auf CRISPR basierenden CDKN2A-Knockout-Zellen bieten eine erneuerbare Quelle von Muskelvorläuferzellen und reduzieren die Abhängigkeit von wiederholten Tierbiopsien."
Diese Beispiele zeigen, wie CRISPR-Screens genetische Modifikationen identifizieren können, die Wachstumsraten verbessern, die zelluläre Alterung verzögern und eine serumfreie Kultur ermöglichen - drei wesentliche Aspekte für die Skalierung der Produktion von kultiviertem Fleisch.
Skalierungsherausforderungen für CRISPR-optimierte Zelllinien
Obwohl CRISPR-optimierte Zelllinien klare Vorteile zeigen, stellt die Skalierung für den industriellen Einsatz Herausforderungen dar. Eine verbesserte Proliferation geht oft auf Kosten der Differenzierung.Zum Beispiel wurden TP53-Knockouts in bovinen mesenchymalen Stammzellen mit einer reduzierten Expression von Muskel-Differenzierungsgenen in Verbindung gebracht, was ihre Fähigkeit, sich zu essbarem Gewebe zu entwickeln, beeinträchtigen kann[1]. Um dies zu beheben, können zusätzliche Strategien erforderlich sein, wie das Hinzufügen von Medienzusätzen oder die Aktivierung spezifischer Transkriptionsfaktoren, um die Differenzierung nach der Expansion wiederherzustellen[1].
Ein weiteres kritisches Problem ist die Aufrechterhaltung der genetischen Stabilität. Variationen in der Genkopienzahl (Aneuploidie) und Off-Target-Effekte während der CRISPR-Bearbeitung können zu inkonsistenten Ergebnissen oder falsch-positiven Ergebnissen in Screening-Studien führen[2]. Tools wie der Cellular Fitness (CelFi)-Assay helfen, diese Risiken zu mindern, indem sie das Verhältnis von Out-of-Frame-Indels im Laufe der Zeit überwachen und sicherstellen, dass beobachtete Wachstumsgewinne direkt mit den beabsichtigten Bearbeitungen verbunden sind[2].
Wirtschaftliche und technische Barrieren bestehen weiterhin. Mesenchymale Stammzellen, die etwa 25 % der Zellquellen in der kultivierten Fleischindustrie ausmachen, stehen vor Herausforderungen wie den hohen Kosten für Wachstumsfaktoren, der Notwendigkeit optimierter serumfreier Medien, und der Entwicklung von großtechnischen Bioreaktoren (Kapazitäten von 10.000–50.000 L)[1][9][11]. Zusätzlich bleibt die Sicherstellung der gewünschten Textur, wenn Zellen auf 3D-Gerüste ausgesät werden, eine komplexe Aufgabe[11].
"Der aktuelle Stand von kultiviertem Fleisch steht vor erheblichen Herausforderungen, einschließlich hoher Kosten, Skalierbarkeitsproblemen und der Notwendigkeit weiterer technologischer Fortschritte."
- Communications Biology [1]
Die Überwindung dieser Herausforderungen erfordert einen umfassenden Ansatz, der genetische Optimierung mit Fortschritten in der Medienformulierung, Bioreaktortechnologie und Differenzierungsprotokollen kombiniert. Während CRISPR-Screens entscheidende genetische Einblicke bieten, wird die Umsetzung dieser Erkenntnisse in skalierbare Lösungen integrierte Systeme und rigorose Validierungsprozesse erfordern. Diese Bemühungen sind entscheidend, um die Produktion von kultiviertem Fleisch vom Labor zur kommerziellen Rentabilität zu bringen.
Wie Cellbase die CRISPR-Forschung in kultiviertem Fleisch unterstützt
CRISPR-Screening hat bereits sein Potenzial gezeigt, aber die Skalierung für den industriellen Einsatz erfordert Zugang zu spezialisierten Werkzeugen und Ressourcen. Hier kommt
Zugriff auf CRISPR-Ressourcen durch Cellbase
Im Gegensatz zu breit gefächerten Pharma-Lieferanten bietet
Im November 2025 ging
"Jedes Unternehmen für kultiviertes Fleisch, mit dem wir gesprochen haben, verschwendete Zeit mit demselben Beschaffungsproblem. Lieferanten für kritische Komponenten zu finden, bedeutete, sich durch Seiten von Pharma-Lieferanten zu googeln, die keine Ahnung von Lebensmittelanwendungen hatten."
- David Bell, Gründer der Cultigen Group [15]
Durch die Zentralisierung dieser Ressourcen beschleunigt
Förderung der Zusammenarbeit in der Entwicklung von kultiviertem Fleisch
Die Plattform ist darauf ausgelegt, die Anforderungen von groß angelegten kommerziellen Projekten zu bewältigen, wie sie von Believer Meats und Aleph Farms. Diese Unternehmungen erfordern Infrastruktur für 50.000-Liter-Bioreaktoren und optimierte Produktionslieferketten, die
Fazit
Das Hochdurchsatz-CRISPR-Screening hat sich von einem vielversprechenden Konzept zu einem entscheidenden Werkzeug in der Entwicklung von kultiviertem Fleisch entwickelt. Der Einfluss dieser Technologie auf die Optimierung von Zelllinien ist unbestreitbar. Jüngste Durchbrüche haben gezeigt, dass genetische Modifikationen die Proliferationslebensdauer von bovinen Stammzellen von 100 auf 200 Tage verdoppeln, seneszente Zellpopulationen von 60 % auf nur 10 % reduzieren und eine erstaunliche 1.000-fache Zunahme der Zellmenge innerhalb eines Monats erreichen können [1]. Diese Fortschritte markieren einen klaren Übergang von experimenteller Forschung zu praktischen industriellen Anwendungen.
Kompakte Plattformen und gezielte Bibliotheken adressieren einige der dringendsten Herausforderungen in diesem Bereich. Digitale mikrofluidische Systeme ermöglichen jetzt das Screening mit nur 3.000 Zellen pro Bedingung, was es machbar macht, mit begrenzten primären Tierzellen zu arbeiten, die kommerziell nicht verfügbar sind.In der Zwischenzeit zielen fokussierte Bibliotheken wie MyoCRISPR-KOLib effizient auf 90 % der relevanten Transkripte ab, während sie nur ein Drittel des Genoms abdecken [3][6]. Dieses Maß an Präzision und Effizienz ist entscheidend, um Ressourcenbeschränkungen zu überwinden und die Produktion zu skalieren.
"Diese Ergebnisse zeigen den Nutzen von CRISPR-Screening zur Optimierung von Rinderstammzellmerkmalen und bieten einen Weg zu einer skalierbareren Produktion von kultiviertem Fleisch in der Zukunft." [1]
Trotz dieser Fortschritte hängt der Erfolg vom Zugang zur richtigen Infrastruktur ab. Forscher benötigen artspezifische gRNA-Bibliotheken, Wachstumsmedien, die für Lebensmittelanwendungen entwickelt wurden, kompatible Bioreaktoren und analytische Werkzeuge, die auf die Produktion von kultiviertem Fleisch und nicht auf die pharmazeutische Nutzung zugeschnitten sind.Die Bedürfnisse ansprechend,
Für Teams, die daran arbeiten, die nächste Welle von kultivierten Fleischzelllinien zu entwickeln, stehen die Werkzeuge und Technologien bereit. Die Herausforderung liegt nun in der schnellen und effektiven Umsetzung des CRISPR-Screenings, um sein volles Potenzial auszuschöpfen.
FAQs
Wie wählt man zwischen CRISPR-Knockout, CRISPRi und CRISPRa für ein Screening aus?
Die Wahl zwischen diesen Systemen hängt von Ihrer spezifischen biologischen Fragestellung und dem angestrebten Ergebnis ab:
- CRISPR-Knockout: Diese Methode unterbricht die Genfunktion vollständig und ist ideal, um die Auswirkungen von Genverlust oder -inaktivierung zu untersuchen.
- CRISPRi: Durch die Unterdrückung der Genexpression ohne das Schneiden der DNA ist dieser Ansatz gut geeignet, um essentielle Gene zu untersuchen oder wenn eine reversible Unterdrückung erforderlich ist.
- CRISPRa: Wenn Sie die Genexpression hochregulieren müssen, ist dieses System die erste Wahl. Es ist besonders nützlich, um die Auswirkungen von Überexpression zu untersuchen, wie z.B. die Förderung der Zellproliferation oder Differenzierung.
Bei der Entscheidung sollten Sie Ihr Zellmodell, die Gene, die Sie anvisieren, und die Gesamtziele Ihres Experiments berücksichtigen.
Wie können Sie die Proliferation steigern, ohne die Differenzierung von Muskel- oder Fettzellen zu beeinträchtigen?
Die Steigerung der Proliferation von Muskel- oder Fettzellen bei gleichzeitiger Erhaltung ihrer Differenzierungsfähigkeit ist eine zentrale Herausforderung in der Produktion von kultiviertem Fleisch.Eine vielversprechende Methode beinhaltet CRISPR-basierte Genbearbeitung, , die eine präzise Manipulation von Genen ermöglicht, um das Wachstum zu verbessern oder die Lebensdauer von Zellen zu verlängern. Zum Beispiel kann das Anvisieren von Myostatin (MSTN) das Zellwachstum fördern, während die Bearbeitung von CDKN2A den Zellen hilft, die Seneszenz zu umgehen.
Dennoch ist es entscheidend, ein Gleichgewicht zwischen Proliferation und Differenzierung zu erreichen. Eine Fehlverwaltung bestimmter Ziele, wie P53 (TP53), , könnte die Differenzierung beeinträchtigen und möglicherweise die Gewebequalität gefährden. Um diese Komplexitäten zu bewältigen, ist High-Throughput-CRISPR-Screening von entscheidender Bedeutung. Diese Technik identifiziert die effektivsten Genregulatoren und ebnet den Weg für eine skalierbare und gesunde Gewebeentwicklung in der Produktion von kultiviertem Fleisch.
Was wird benötigt, um CRISPR-Screen-Treffer zu validieren, bevor eine Zelllinie skaliert wird?
Die Validierung von CRISPR-Screen-Treffern für die Produktion von kultiviertem Fleisch erfordert einen methodischen Ansatz. Zuerst muss die Genfunktion durch unabhängige Experimente, wie Gen-Knockouts, bestätigt werden, um sicherzustellen, dass die beobachteten Effekte reproduzierbar sind. Als nächstes ist es entscheidend, die biologische Relevanz dieser Gene zu bewerten, indem ihr Einfluss auf Faktoren wie Zellproliferation, Lebensfähigkeit und Langlebigkeit untersucht wird.
Sicherheitsbewertungen sind ebenso wichtig, um Off-Target-Effekte oder genetische Instabilität auszuschließen, die den Prozess gefährden könnten. Die funktionale Validierung unter Bedingungen, die industrielle Umgebungen wie Bioreaktoren nachahmen, ist ein weiterer kritischer Schritt. Dies stellt sicher, dass die genetischen Änderungen in großtechnischen Produktionsumgebungen wie erwartet funktionieren. Gründliche Tests in jeder Phase sind unverzichtbar, bevor eine Skalierung in Betracht gezogen wird.











