Die Prozessanalytik-Technologie (PAT) integriert die Echtzeit-Qualitätsüberwachung in Fertigungsprozesse, verbessert die Konsistenz und reduziert Abfall. Sie ist besonders nützlich in der Produktion von kultiviertem Fleisch, wo die präzise Kontrolle von Faktoren wie pH-Wert, Sauerstoff und Nährstoffen entscheidend ist. PAT kombiniert Inline-Sensoren, Chemometrie und automatisierte Systeme, um die Produktqualität zu gewährleisten und gleichzeitig die behördlichen Standards zu erfüllen.
Wichtige Schritte zur Implementierung von PAT:
- Identifizieren Sie kritische Prozessparameter (CPPs): Konzentrieren Sie sich auf Faktoren wie Temperatur, gelösten Sauerstoff, pH-Wert und Glukose.
- Wählen Sie Überwachungswerkzeuge: Verwenden Sie Inline-Sensoren (e.g., Raman-Spektroskopie) für Echtzeitdaten.
- Integrieren Sie PAT-Systeme: Verbinden Sie Sensoren mit Bioreaktoren für eine automatisierte Rückkopplungssteuerung.
- Entwickeln Sie prädiktive Modelle: Verwenden Sie Datenanalysen zur Prozessoptimierung.
- Sicherstellung der Einhaltung: Befolgen Sie GMP, ISO 17025 und andere regulatorische Richtlinien.
Plattformen wie
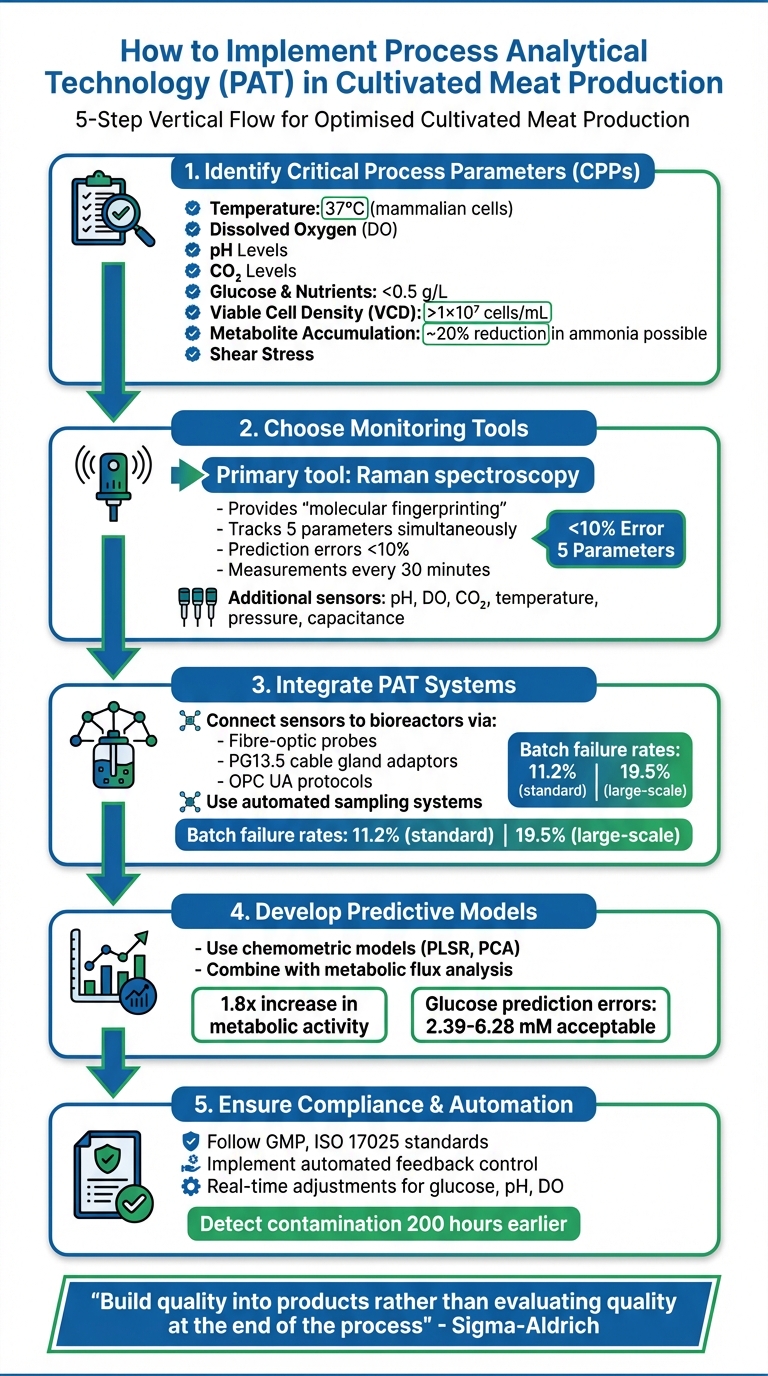
5-Schritte-Prozess zur Implementierung von PAT in der Produktion von kultiviertem Fleisch
Diskussion mit Experten für Bioprozessierung I - PAT-Implementierung
Identifizierung kritischer Prozessparameter (CPPs)
Um den Erfolg in der Produktion von kultiviertem Fleisch sicherzustellen, ist es wichtig, die kritischen Prozessparameter (CPPs) zu identifizieren, die die Zellviabilität, den Biomasseertrag und die Produktqualität beeinflussen. Eine Fehlverwaltung dieser Parameter kann ganze Produktionsläufe gefährden.
Wichtige Parameter zur Überwachung
Temperatur ist ein Schlüsselfaktor. Säugetierzellen gedeihen bei etwa 37°C, während Fisch- und Insektenzellen viel kühlere Umgebungen benötigen, um eine optimale Stoffwechselaktivität aufrechtzuerhalten [2].
Gelöster Sauerstoff (DO) ist ein weiteres kritisches Element für den aeroben Stoffwechsel. Mit zunehmendem Produktionsmaßstab wird die Sicherstellung eines ausreichenden Sauerstofftransfers immer herausfordernder [2]. Ohne genügend Sauerstoff können die Zellen auf anaeroben Stoffwechsel umschalten, was zu einer Milchsäureansammlung führen kann, die das Wachstum behindert.
pH-Werte sind ein Fenster in den Stoffwechselzustand der Kultur. Jegliche Schwankungen können die Enzymaktivität stören, die Zellgesundheit beeinträchtigen und die Eigenschaften des Produkts beeinflussen, wie z.B. Textur und Wasserhaltekapazität [2][3].
Kohlendioxid (CO₂)-Werte müssen sorgfältig verwaltet werden, insbesondere bei groß angelegten Operationen. Tierzellen sind besonders empfindlich gegenüber erhöhten CO₂-Werten, was eine ständige Überwachung unerlässlich macht [2].
Glukose und Nährstoffe sind die Hauptenergiequellen für Zellen. Wenn die Glukosewerte zu niedrig fallen, können die Zellen verhungern, was zum Tod oder zu vorzeitiger Differenzierung führen kann [2]. Niedrige Glukosekonzentrationen (e.g., unter 0,5 g/L) können einen ineffizienten Stoffwechsel verhindern und die Laktatansammlung reduzieren [4].
Lebensfähige Zelldichte (VCD) hilft, die Wachstumsphasen der Kultur - Lag, Log und Stationär - zu verfolgen, um den besten Erntezeitpunkt zu bestimmen [2]. Für kultiviertes Fleisch werden hohe Zelldichten oft als über 1×10⁷ Zellen/mL angesehen [2].
Metabolitenakkumulation - wie Ammoniak und Milchsäure - kann das Wachstum behindern und die Zellviabilität verringern. Die Überwachung und Kontrolle dieser toxischen Nebenprodukte ist entscheidend. Zum Beispiel erreichte eine Methode eine 20%ige Reduzierung der toxischen Ammoniakwerte [2].
Schubspannung, verursacht durch Rührer oder Gasblasen, stellt eine einzigartige Herausforderung dar. Im Gegensatz zu mikrobiellen Zellen fehlt tierischen Zellen eine schützende Zellwand, was sie anfälliger für Schäden macht. Tolerierbare Stressniveaus variieren je nach Spezies und müssen für jede Zelllinie fein abgestimmt werden [2].
Diese Parameter bilden die Grundlage für die Optimierung der Produktion von kultiviertem Fleisch.
Parameter Spezifisch für Kultiviertes Fleisch
Während die oben genannten Faktoren allgemein gelten, bringt die Produktion von kultiviertem Fleisch einzigartige Herausforderungen mit sich, die besondere Aufmerksamkeit erfordern.
CO₂-Empfindlichkeit ist besonders wichtig. Tierzellen, die in der Lebensmittelproduktion verwendet werden, sind im Vergleich zu mikrobiellen Zellen anfälliger für CO₂-Hemmung, was diesen Parameter zu einem kritischen Faktor macht, der verwaltet werden muss [2].
Hochskalierung der Produktion bringt neue Prioritäten mit sich. In der Biopharmaindustrie erreichen Bioreaktoren typischerweise ein Maximum von 20.000 L für hochwertige Produkte. Allerdings wird kultiviertes Fleisch deutlich größere Volumina benötigen, um wirtschaftlich rentabel zu bleiben. Um dies ins rechte Licht zu rücken: Der größte jemals gebaute mikrobielle Bioreaktor fasst 1.500.000 L - ein Maßstab, den die Produktion von kultiviertem Fleisch eines Tages erreichen könnte [2].
Thermisches Management variiert je nach Spezies. Nicht-mammalische Zellen erfordern völlig unterschiedliche Heiz- und Kühlsysteme, was die Temperaturkontrolle hochgradig spezies-spezifisch macht [2]. Diese Variabilität erfordert flexible Process Analytical Technology (PAT)-Systeme.
Schließlich kann die Beschaffung der richtigen Überwachungsausrüstung für diese Parameter schwierig sein. Plattformen wie
Das Beherrschen dieser CPPs ist ein notwendiger Schritt, bevor Echtzeit-Kontrollsysteme durch PAT-Tools implementiert werden.
Auswahl und Integration von PAT-Tools
Sobald Sie die kritischen Prozessparameter identifiziert haben, besteht der nächste Schritt darin, Sensoren auszuwählen, die Ihren Anforderungen entsprechen - insbesondere in Bezug darauf, wo Messungen vorgenommen werden und wie schnell sie reagieren. Inline-Überwachung sticht hier hervor. Da die Sensoren innerhalb des Prozessstroms bleiben, bieten sie die schnellsten und dynamischsten Echtzeiteinblicke im Vergleich zu At-Line- oder Off-Line-Methoden [6]. Für Parameter wie pH oder gelösten Sauerstoff, die sofortiges Feedback erfordern, beseitigen Inline-Sensoren Verzögerungen, die durch Probenahme verursacht werden.
Auswahl von Sensoren und Technologien
Ein herausragendes Werkzeug in diesem Bereich ist die Raman-Spektroskopie, eine bevorzugte Wahl für die Produktion von kultiviertem Fleisch. Ihre Fähigkeit, "molekulare Fingerabdrücke" zu liefern, macht sie besonders effektiv bei der Identifizierung organischer Moleküle wie Glukose und Laktat, während sie von Wasser unbeeinflusst bleibt [6][7]. Eine Studie von Merck/Sigma-Aldrich im Januar 2026 hob die Effektivität des ProCellics™ Raman Analysators und der Bio4C® PAT Raman Software hervor. Dieses System überwachte eine CHO-Zellkultur in einem 3L wasserummantelten Bioreaktor und nahm alle 30 Minuten Messungen vor. Bemerkenswert ist, dass es fünf Parameter gleichzeitig verfolgte und während eines Zelldilutionsereignisses am sechsten Tag genau zwischen der Gesamt- und der lebensfähigen Zelldichte unterschied, mit einer Fehlermarge von unter 10% [11].
"Raman ist zu einem bevorzugten PAT für die Überwachung und Steuerung von Upstream-Bioprozessen geworden, da es eine fortschrittliche Prozesssteuerung erleichtert und eine konsistente Prozessqualität ermöglicht." - Karen A Esmonde-White, Endress+Hauser [8]
Die Raman-Spektroskopie ist nicht nur präzise; sie sagt die Konzentrationen wichtiger Metaboliten mit Fehlern unter 10 % voraus [7][11]. Aber Raman allein reicht nicht aus. Sie benötigen auch Standard-Bioreaktorsensoren für pH, gelösten Sauerstoff, CO₂, Temperatur, Druck und Kapazität [10][6]. Um die Abläufe zu optimieren und das Kontaminationsrisiko zu verringern - insbesondere da die Fehlerraten bei Chargen in der Produktion von kultiviertem Fleisch bei etwa 11,2 % liegen und in größeren Maßstäben auf 19,5 % steigen - sind automatisierte Probensysteme unverzichtbar [5].
Bei der Auswahl von Sensoren stellen Sie sicher, dass sie mit Multivariate Data Analysis (MVDA) und Design of Experiments (DOE) Software [1] kompatibel sind. Diese Kompatibilität stellt sicher, dass die Werkzeuge vom kleinen F&E-Bioreaktor bis zur kommerziellen Produktion im großen Maßstab skalierbar sind [1].
Integration von PAT-Tools in Bioreaktorsysteme
Moderne Bioreaktorsysteme vereinfachen die Integration von PAT-Tools. Nicht-destruktive, Inline-Messungen werden durch den Einsatz von faseroptischen Sonden ermöglicht, die über standardisierte PG13.5 Kabelverschraubungsadapter montiert werden. Diese Sonden verbinden sich nahtlos mit Bioreaktorsystemen über OPC UA Protokolle [8][9][11][1].
Auf der Datenseite verarbeiten Plattformen wie Bio4C® PAT Raman Software oder BioPAT® MFCS Sensordaten in umsetzbare Erkenntnisse für die Echtzeitsteuerung [10][11]. Diese Systeme verwenden fortschrittliche Werkzeuge wie Hauptkomponentenanalyse (PCA) und Partielle Kleinste-Quadrate (PLS), um komplexe Spektraldaten in aussagekräftige Prozessparameter umzuwandeln [9].
"Der Einsatz der Raman-Technologie... ermöglicht ein umfassendes Prozessverständnis und -kontrolle in der biopharmazeutischen Herstellung, sodass Benutzer mit Zuversicht die richtigen Entscheidungen treffen können." - Merck/Sigma-Aldrich [11]
Beim Aufbau von Raman-Modellen helfen Techniken wie Analyten-Spiking - bei denen bekannte Konzentrationen von Analyten hinzugefügt werden - Korrelationen zwischen Verbindungen zu durchbrechen, um sicherzustellen, dass das Modell nicht auf indirekte Trends angewiesen ist [1]. Die Einbeziehung eines breiten Spektrums von Prozessbedingungen mit DOE stellt sicher, dass Modelle robust genug sind, um kommerzielle Variationen zu bewältigen [1].
Nachdem die Integrationsherausforderungen gelöst sind, besteht die nächste Aufgabe darin, die richtige PAT-Ausrüstung zu beschaffen.
Beschaffung von PAT-Ausrüstung für kultiviertes Fleisch
Die richtigen Werkzeuge für die Echtzeitüberwachung in der Produktion von kultiviertem Fleisch zu finden, kann schwierig sein. Glücklicherweise vereinfachen Plattformen wie
Da Wachstumsmedien oft über 50% der Produktionskosten ausmachen [5], ist die Beschaffung effektiver Überwachungsgeräte zur Optimierung des Nährstoffverbrauchs nicht nur praktisch, sondern auch wirtschaftlich klug.
sbb-itb-ffee270
Erstellung prädiktiver Modelle zur Prozessoptimierung
Sobald Sie PAT-Tools implementiert haben, besteht der nächste Schritt darin, prädiktive Modelle zu verwenden, um Variablen zu schätzen, die schwer direkt zu messen sind, wie Zellviabilität und Metabolitspiegel [12]. Durch die Analyse von Spektraldaten können Sie eine schnellere und intelligentere Prozesssteuerung erreichen. Die Herausforderung besteht darin, diese Daten in zuverlässige prädiktive Modelle zu transformieren.
Entwicklung chemometrischer Modelle
Partial Least Squares Regression (PLSR) ist ein guter Ausgangspunkt, um mit den überlappenden und verrauschten Signalen umzugehen, die häufig in der Produktion von kultiviertem Fleisch auftreten [7][13]. Um Raman-Spektren zu verfeinern, die 1.000–3.000 Variablen pro Messung enthalten können [7], verarbeiten Sie die Daten vor, indem Sie Ableitungsberechnungen verwenden. Dies hilft, Rauschen zu reduzieren, während kritische Spitzen erhalten bleiben. Seien Sie jedoch vorsichtig, die Daten nicht zu stark zu glätten, da dies die Signale löschen könnte, auf die Ihr Modell angewiesen ist.
Die Auswahl der Variablen ist ebenso wichtig. Die Hauptkomponentenanalyse (PCA) kann helfen, die spektralen Bereiche zu identifizieren, die am stärksten mit Ihrem Zielparameter verbunden sind. Eine Studie aus dem Jahr 2018 zeigte beispielsweise, dass die achte Hauptkomponente (PC8) stark mit der Glukosekonzentration korreliert war. Die Forscher nutzten diese Erkenntnis, um ihr PLSR-Modell zu optimieren [7]. Dieser fokussierte Ansatz reduziert das Risiko der Überanpassung und stellt sicher, dass sich das Modell auf aussagekräftige Daten konzentriert.
Für die Produktion von kultiviertem Fleisch kann die Kombination von datengetriebenen Modellen mit mechanistischen Modellen, wie der Flussbilanzanalyse (FBA), besonders effektiv sein. Im Jahr 2023 nutzte Oxford Biomedica ein refraktometriebasiertes PAT-System (das Ranger-System), um HEK293T-Zellkulturen zu überwachen.Durch die Integration von Echtzeitdaten mit der metabolischen Flussanalyse entdeckten sie, wie der pH-Wert direkt die intrazellulären Sauerstoffwerte und die Stoffwechselaktivität beeinflusste. Diese hybride Strategie führte zur Entwicklung eines pH-Betriebsplans, der die Stoffwechselaktivität im Vergleich zu nicht optimierten Prozessen um das 1,8-fache steigerte [12][14].
Sobald Ihr Modell erstellt ist, besteht der nächste Schritt darin, sicherzustellen, dass es unter realen Betriebsbedingungen genau und zuverlässig funktioniert.
Validierung von Modellen für den Produktionseinsatz
Der wahre Test eines Modells liegt in seiner Validierung. Beginnen Sie damit, es gegen einen unabhängigen Datensatz zu evaluieren - Daten, die nicht Teil der Trainingsphase waren. Verwenden Sie Metriken wie den Root Mean Square Error of Prediction (RMSEP), um die Genauigkeit zu messen. Für die Glukoseüberwachung in kultivierten Fleischprozessen reichen die Vorhersagefehler von 2,39 mM bis 6.28 mM sind typischerweise für die Echtzeit-Automatisierungskontrolle akzeptabel [7].
Skalierbarkeit ist ein weiterer Schlüsselfaktor. Ihr Modell muss konsistente Ergebnisse liefern, egal ob es in einem kleinen F&E-Bioreaktor oder in einem großen kommerziellen System angewendet wird. Eine Studie aus dem Jahr 2018 zeigte, dass ein PLSR-Modell seine Vorhersagegenauigkeit beibehielt, als es von einem 10 L auf ein 100 L System skaliert wurde [7].
Testen Sie schließlich das Modell unter dynamischen Bedingungen durch "Parameter Probing". Dies beinhaltet das Anpassen von Variablen wie pH oder gelöstem Sauerstoff, um zu überprüfen, ob das Modell Änderungen genau verfolgt [14]. Oxford Biomedica verwendete diese Methode, um ein autonomes pH-Kontrollsystem zu validieren [12]. Führen Sie danach geschlossene Regelkreistests durch, um zu bestätigen, dass das PAT-System die Parameter innerhalb des gewünschten Bereichs halten kann [14].
Implementierung der Echtzeit-Prozesssteuerung
Die Echtzeit-Prozesssteuerung geht einen Schritt weiter als prädiktive Modelle, indem sie kontinuierliche Daten nutzt, um eine optimale Leistung aufrechtzuerhalten. Durch die Umwandlung von Live-Sensordaten in automatisierte Anpassungen stellen diese Systeme sicher, dass wichtige Bedingungen wie Nährstoffgehalt, pH-Wert und gelöster Sauerstoff konstant reguliert werden - ohne manuelles Eingreifen. Dies reduziert nicht nur die Arbeitskosten und menschliche Fehler, sondern garantiert auch eine gleichbleibendere Produktqualität. Für die Produktion von kultiviertem Fleisch ist eine solche Automatisierung ein Wendepunkt bei der Erreichung der Echtzeit-Prozessoptimierung.
Um dies zu ermöglichen, ist es entscheidend, kritische Prozessparameter (CPPs) direkt zu messen und diese Signale in Ihr Steuerungssystem einzuspeisen.Dan Kopec, ein PAT-Experte bei Sartorius Stedim Biotech, hebt die Bedeutung dieses Ansatzes hervor:
Der beste Weg, einen kritischen Prozessparameter (CPP) zu kontrollieren, besteht darin, diesen spezifischen Parameter zu messen, das Live-Signal in Ihr Steuerungssystem zu integrieren und einen intelligenten Feedback-Algorithmus für einen automatisierten Regelkreis anzuwenden.[4]
Diese Regelkreise vergleichen Echtzeit-Sensorwerte mit vordefinierten Sollwerten. Mithilfe von PID-Algorithmen passen sie automatisch kritische Parameter wie Nährstoffzufuhr, pH-Wert und gelösten Sauerstoff an, um einen reibungslosen Ablauf zu gewährleisten.
Zum Beispiel liefern in der Produktion von kultiviertem Fleisch In-situ-Sensoren nahezu sofortige Messungen. Kapazitätssensoren können beispielsweise das Volumen lebensfähiger Zellen verfolgen, indem sie Zellen als Mikrokondensatoren innerhalb eines Hochfrequenzfeldes behandeln. Diese Daten können dann automatisierte Zellblutungssteuerungen in kontinuierlichen Perfusionsprozessen auslösen, um eine gleichmäßige Zelldichte aufrechtzuerhalten.[4]
Einrichten von Rückkopplungssteuerungssystemen
In der Produktion von kultiviertem Fleisch beeinflussen Parameter wie Glukose, pH-Wert und gelöster Sauerstoff direkt das Zellwachstum und die metabolische Effizienz. Es ist besonders wichtig, die Glukosespiegel niedrig zu halten (etwa 0,1–0,5 g/L), um die Ansammlung von Laktat zu verhindern.[4] Um dies zu adressieren, hat Sartorius Stedim Biotech das BioPAT Trace System entwickelt. Diese Technologie verwendet enzymatische Biosensoren und eine Dialysemembran mit einer 10 kDa Membran, um Glukosemessungen so häufig wie einmal pro Minute bereitzustellen - ohne Volumenverlust. Dies gewährleistet eine hohe Zelldichte in Perfusionsbioreaktoren.[4]
Die Automatisierung der pH-Steuerung kann ebenfalls zu erheblichen Verbesserungen führen.In einer Studie verwendeten Forscher von Oxford Biomedica und WattBE Innovations das Ranger Refractive Index (RI) PAT-System, um HEK293T-Zellkulturen zu überwachen. Durch die Entwicklung eines 'Metabolic Rate Index' (MRI) und die Anpassung der pH-Sollwerte erreichten sie eine 1,8-fache Steigerung der Stoffwechselaktivität. Diese Technik, oft als "Parameter Probing" bezeichnet, beinhaltet das Anpassen von Variablen, um Systemreaktionen zu beobachten und Betriebsbedingungen zu verfeinern.[12]
Um die Zuverlässigkeit weiter zu verbessern, können virtuelle Sensoren als Backup für Hardware-Sensoren fungieren. Beispielsweise könnte ein virtueller Sensor, der auf Kapazitätsmessungen basiert, Glukosedaten von einer Raman-Sonde gegenprüfen. Diese Redundanz hilft, Sensorabweichungen oder -ausfälle zu erkennen, bevor sie den Prozess stören - ein besonders nützliches Sicherheitsnetz bei hoher Prozessvariabilität.
Beispiele für Echtzeit-Automatisierung in kultiviertem Fleisch
Echtzeit-Kontrollstrategien haben bereits in verschiedenen Anwendungen beeindruckende Ergebnisse geliefert. Zum Beispiel arbeitete Sartorius Stedim Biotech mit dem GSK Medicine Research Centre zusammen, um die BioPAT-Plattform für automatisierte geschlossene Kreislauffütterung in CHO-Zellkulturen zu nutzen. Dies eliminierte manuelle Probenahmen und gewährleistete eine stetige Nährstoffversorgung.[4]
In einem weiteren Beispiel integrierte Oxford Biomedica das Ranger RI-System mit der Analyse des Stoffwechselflusses, um eine autonome pH-Kontrollstrategie zu entwickeln. Dieses System passte sich dem Stoffwechselzustand der Zellen an und erkannte mikrobielle Kontaminationen bis zu 200 Stunden früher als herkömmliche Methoden, was das Potenzial der Echtzeitüberwachung zur Vermeidung kostspieliger Chargenausfälle verdeutlicht.[12]
Plattformen wie
Wie Kopec treffend zusammenfasst:
Automatisierung und Echtzeitüberwachung sollten Prozesse mit Qualitäts- und Ertragssteigerungen sowie Reduzierungen der Arbeitskosten, Risiken und Abfälle verbessern. [4]
Um zu beginnen, konzentrieren Sie sich auf die kritischsten Parameter - typischerweise Glukose, pH-Wert und gelöster Sauerstoff - und erweitern Sie die Automatisierung schrittweise, während Sie ein tieferes Verständnis Ihres Prozesses gewinnen. Dieser schrittweise Ansatz ist entscheidend für die Optimierung der Produktion von kultiviertem Fleisch durch Echtzeitkontrolle.
Fazit: Schritte zur PAT-Implementierung
Die Einführung der Prozessanalysentechnologie (PAT) in die Produktion von kultiviertem Fleisch erfordert einen klaren und methodischen Ansatz.Beginnen Sie mit der Identifizierung Ihrer Kritischen Prozessparameter (CPPs) - dazu könnten Glukosespiegel, pH-Wert und gelöster Sauerstoff gehören, die alle einen direkten Einfluss auf die Produktqualität haben. Sobald diese definiert sind, wählen Sie PAT-Tools wie Raman-Spektroskopie oder Kapazitätssensoren, um eine Echtzeitüberwachung zu ermöglichen.
Der nächste Schritt besteht darin, diese Sensoren in Ihre Bioreaktorsysteme zu integrieren und prädiktive Modelle zu erstellen, um die gesammelten Daten zu interpretieren. Priorisieren Sie In-Line-Überwachung wann immer möglich, da dies Verzögerungen eliminiert und das Risiko einer Kontamination während des Prozesses verringert.
Automatisierte Rückmeldesysteme spielen hier eine entscheidende Rolle, indem sie Rohdaten in sofortige, umsetzbare Anpassungen umwandeln. Wie Sigma-Aldrich treffend formuliert:
Ein Hauptziel von PAT ist es, Qualität in Produkte einzubauen, anstatt die Qualität am Ende des Prozesses zu bewerten.[6]
Dieser proaktive Ansatz reduziert nicht nur die Arbeitskosten, sondern stellt auch eine gleichbleibende Produktqualität sicher und verringert gleichzeitig Abfall.
Sobald automatisierte Feedback-Systeme in Betrieb sind, sollte der nächste Fokus auf der Beschaffung der richtigen PAT-Ausrüstung liegen. Zuverlässige Ausrüstung ist entscheidend für den Erfolg, und Plattformen wie
Mit zunehmendem Verständnis des Prozesses erweitern Sie schrittweise die Automatisierung, um eine skalierbare und konsistente Produktion zu erreichen und gleichzeitig die regulatorischen Standards zu erfüllen.Indem Sie diese Schritte befolgen, kann die Implementierung von PAT zum Rückgrat eines effizienteren und zuverlässigeren Produktionsprozesses für kultiviertes Fleisch werden.
FAQs
Welche Vorteile bietet die Verwendung von Process Analytical Technology (PAT) in der Produktion von kultiviertem Fleisch?
Die Process Analytical Technology (PAT) spielt eine Schlüsselrolle bei der Verbesserung sowohl der Prozesskontrolle als auch der Produktkonsistenz in der Produktion von kultiviertem Fleisch. Mit Echtzeitüberwachung von entscheidenden Faktoren wie Temperatur, pH-Werten und gelöstem Sauerstoff stellt PAT optimale Wachstumsbedingungen für Zellen sicher und minimiert gleichzeitig die Wahrscheinlichkeit unerwarteter Prozessprobleme. Das Ergebnis? Höhere Erträge, gleichbleibende Qualität und reduzierte Produktionskosten.
Ein weiterer Vorteil von PAT ist, wie es ein Quality-by-Design (QbD) Rahmenwerk unterstützt.Durch die direkte Verbindung analytischer Daten mit den spezifischen Qualitätsmerkmalen des Produkts wird die Abhängigkeit von traditionellen Endpunkt-Testmethoden verringert. Dieser Ansatz beschleunigt nicht nur die Validierungsprozesse, sondern ermöglicht auch datengetriebene Entscheidungen, die die Reproduzierbarkeit verbessern und vorausschauende Kontrollstrategien erlauben.
Für Unternehmen im Bereich kultiviertes Fleisch erleichtern Plattformen wie
Wie verbessert die Raman-Spektroskopie die Echtzeitüberwachung in PAT-Systemen für die Produktion von kultiviertem Fleisch?
Die Raman-Spektroskopie spielt eine entscheidende Rolle bei der Echtzeitüberwachung innerhalb von PAT (Process Analytical Technology)-Systemen, indem sie schnelle, nicht-invasive Inline-Messungen wichtiger Prozessparameter liefert. Dies hilft, einen strafferen Prozessablauf zu gewährleisten und eine gleichbleibende Produktqualität sicherzustellen.
Eine seiner herausragenden Eigenschaften ist die Fähigkeit, mehrere Moleküle gleichzeitig zu erkennen. Zum Beispiel kann es Glukose-, Laktat- und Ammoniumwerte überwachen und gleichzeitig die Zellviabilität und Produkteigenschaften bewerten - alles in einer einzigen Messung. Moderne Raman-Sonden sind so konzipiert, dass sie direkt in Bioreaktorströme installiert werden können, was eine kontinuierliche Datenerfassung ohne Probenentnahme ermöglicht.
Ein weiterer Vorteil ist die Unterstützung von automatisierter Rückkopplungssteuerung. Durch die Bereitstellung von Echtzeitdaten ermöglicht die Raman-Spektroskopie präzise Anpassungen der Nährstoffzufuhr, um optimale Produktionsbedingungen aufrechtzuerhalten. Ihre Flexibilität bei der Skalierung und Übertragung von Modellen auf verschiedene Reaktorgrößen erhöht ihre Nützlichkeit in der Produktion von kultiviertem Fleisch, steigert die Effizienz und minimiert das Fehlerrisiko.
Was sind die wichtigsten Herausforderungen bei der Skalierung der Prozessanalysentechnologie (PAT) für die Produktion von kultiviertem Fleisch?
Die Skalierung von PAT (Prozessanalysentechnologie) für die großtechnische Produktion von kultiviertem Fleisch bringt einige Herausforderungen mit sich, die eine sorgfältige Planung und Ausführung erfordern. Ein zentrales Problem liegt in der Verwaltung und Integration der enormen Datenmengen, die von PAT-Instrumenten erzeugt werden. Mit zunehmender Produktion wird die Aufrechterhaltung der Datengenauigkeit bei gleichzeitiger reibungsloser Integration in Kontrollsysteme zu einer komplexeren Aufgabe.
Ein weiteres bedeutendes Hindernis ist die Leistung der Sensoren in industriellen Bioreaktoren. Sensoren, die in kleineren Anlagen gut funktionieren, stoßen in größeren Systemen oft auf Herausforderungen, bei denen Faktoren wie Scherkräfte und Temperaturschwankungen die Genauigkeit der Echtzeitmessungen beeinträchtigen können.
Es gibt auch das Problem der Beschaffung spezialisierter Ausrüstung, die auf die einzigartigen Anforderungen der Produktion von kultiviertem Fleisch zugeschnitten ist. Plattformen wie
Die frühzeitige Bewältigung dieser Herausforderungen - durch die Auswahl zuverlässiger Sensoren, den Aufbau skalierbarer Datensysteme und die strategische Planung der Beschaffung - kann Unternehmen helfen, den Übergang zur kommerziellen Produktion effizienter zu gestalten.











