Las pruebas de esterilidad son críticas para la producción de carne cultivada, donde incluso una contaminación menor puede llevar a fallos costosos en los lotes. Este proceso asegura que no haya microorganismos dañinos que interrumpan las operaciones del biorreactor, protegiendo tanto la calidad del producto como la viabilidad financiera. Con tasas de contaminación que promedian el 11.2% - y que aumentan al 19.5% para la producción a gran escala - los productores enfrentan desafíos significativos para mantener ambientes estériles.
Puntos clave incluyen:
- Principales Fuentes de Contaminación: El personal, las materias primas y las operaciones del biorreactor son puntos de entrada comunes para los microbios.
- Métodos de Prueba: La filtración por membrana para grandes volúmenes, la inoculación directa para muestras más pequeñas y las pruebas de carga microbiana durante la producción son ampliamente utilizadas.
- Monitoreo en Tiempo Real: Herramientas como los sensores de oxígeno disuelto y el análisis de gases residuales permiten la detección temprana de actividad microbiana.
- Tecnologías Emergentes: La monitorización impulsada por IA, la esterilización con plasma frío y los sistemas de imagen automatizados ofrecen una gestión de la contaminación más rápida y precisa.
Para los productores de carne cultivada, combinar pruebas de esterilidad tradicionales con soluciones de monitoreo avanzadas es esencial para reducir riesgos y mejorar la eficiencia de producción.
Rocker Discover - ¿Cómo realizar una prueba de esterilidad?
sbb-itb-ffee270
Fuentes de Contaminación en Sistemas de Biorreactores
Para prevenir fallos en lotes en sistemas de biorreactores, es crucial identificar de dónde proviene la contaminación. Los contaminantes generalmente se dividen en tres categorías principales: microbiana, particulada y endotoxina. Cada tipo presenta desafíos únicos para la producción de carne cultivada, por lo que es esencial desarrollar estrategias preventivas específicas.
El personal es la fuente principal de contaminación, a menudo introduciendo contaminantes a través de la descamación de la piel, el uso inadecuado de vestimenta o una higiene de manos deficiente [4][7]. Incluso con protocolos estrictos, movimientos simples pueden interrumpir el flujo de aire, llevando a turbulencias o áreas estancadas donde los contaminantes pueden acumularse [4][9]. La U.S. La Administración de Alimentos y Medicamentos destaca los riesgos involucrados, afirmando, "cualquier manipulación manual o mecánica del medicamento esterilizado, componentes, contenedores o cierres antes o durante el ensamblaje aséptico plantea el riesgo de contaminación y, por lo tanto, requiere un control cuidadoso" [4].
Los factores ambientales también juegan un papel significativo.Por ejemplo, no mantener una presión positiva de 10–15 Pascales puede permitir que el aire no filtrado entre en zonas estériles [3][4]. Además, problemas como las ineficiencias de los filtros HEPA - donde la retención de partículas cae por debajo del 99.97% - o los filtros de gas comprimido comprometidos pueden comprometer rápidamente la esterilidad [4].
Contaminación de Materias Primas y Líneas Celulares
Las materias primas que ingresan al sistema de biorreactor son un gran riesgo de contaminación. Ingredientes no verificados, componentes de medios de crecimiento y líneas celulares (disponibles a través de mercados B2B especializados) pueden introducir patógenos oportunistas [2]. El entorno rico en nutrientes de los medios de cultivo celular es particularmente susceptible a la contaminación, lo que hace que los procesos de carne cultivada sean más vulnerables en comparación con los bioprocesos microbianos [8].
Los ingredientes sensibles al calor que no pueden someterse a autoclave son especialmente riesgosos, ya que requieren métodos de esterilización alternativos como la filtración [1][8]. Además, el proceso de inoculación en sí mismo conlleva riesgos inherentes. Incluso cuando las membranas se desinfectan con alcohol o los procedimientos se realizan cerca de una llama abierta, no hay garantía absoluta contra la contaminación durante la introducción de líneas celulares [8]. Estos riesgos subrayan la importancia de una verificación exhaustiva de las materias primas antes de ser introducidas en el sistema.
Riesgos Operacionales del Biorreactor
Las operaciones diarias dentro de los biorreactores presentan numerosas oportunidades de contaminación. El muestreo manual es particularmente de alto riesgo, ya que cada punto de acceso aumenta la posibilidad de introducir contaminantes [1].Problemas como sellos comprometidos, juntas tóricas dañadas o cierres no esterilizados aumentan aún más el riesgo [4][8]. Además, transferir materiales de áreas de menor clasificación a zonas de mayor clasificación sin la adecuada descontaminación es otra vulnerabilidad crítica [7].
Mantener controles ambientales estrictos es innegociable. Las diferencias de presión entre las áreas de salas limpias deben ser monitoreadas continuamente, y cualquier cambio inusual debe ser investigado de inmediato [4]. En áreas críticas de Clase 100 (ISO 5), los conteos de partículas para tamaños ≥0.5 μm deben permanecer por debajo de 3,520 partículas por metro cúbico durante las operaciones [4].Además, la aerosolización de desinfectantes o alcohol isopropílico al 70% cerca de muestreadores de aire puede aumentar las lecturas de partículas, mientras que el condensado en los filtros de gas puede causar obstrucciones o fomentar el crecimiento microbiano [4][7].
Estos riesgos operativos destacan la importancia de implementar métodos rigurosos de prueba de esterilidad para proteger los procesos de biorreactores.
Métodos de Prueba de Esterilidad para Biorreactores
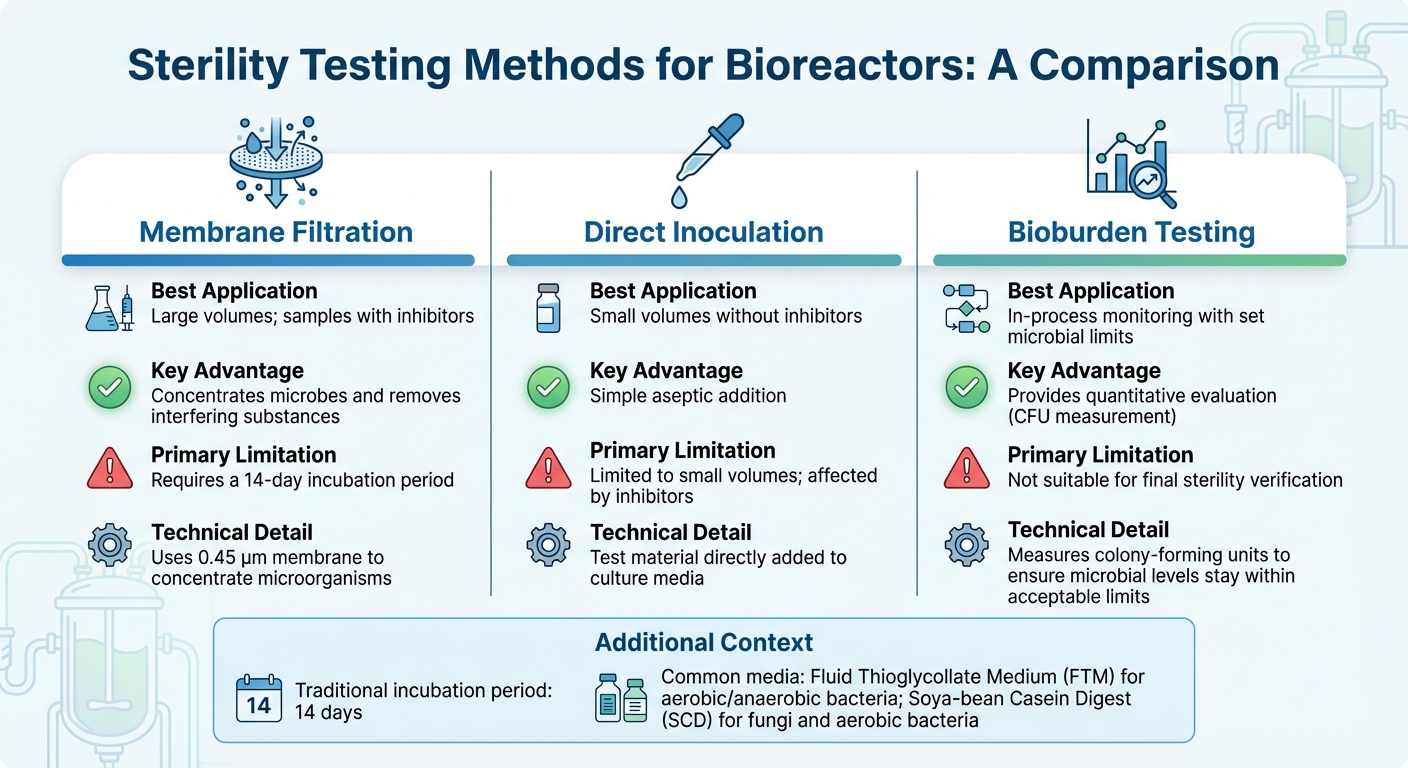
Comparación de Métodos de Prueba de Esterilidad para Biorreactores
La selección del método de prueba de esterilidad adecuado para biorreactores depende de factores como el tamaño del biorreactor, la etapa de producción y los desafíos de escalado, y la composición de la muestra, especialmente cuando hay inhibidores presentes. Para la mayoría de las aplicaciones industriales, la filtración por membrana es el método preferido [3].Mientras tanto, las técnicas moleculares como la PCR ofrecen una detección más rápida de contaminantes específicos. A continuación, exploraremos métodos adaptados a la producción de carne cultivada, abordando los desafíos únicos de las pruebas de muestras grandes y pequeñas.
Para muestras de gran volumen, comunes en biorreactores a escala industrial, la filtración por membrana emplea una membrana de 0.45 µm para concentrar microorganismos, mejorando la sensibilidad de detección [10]. Este método es particularmente efectivo para muestras que contienen antibióticos, ya que el enjuague puede eliminar inhibidores antes de la incubación. Por otro lado, la inoculación directa, donde el material de prueba se agrega directamente al medio de cultivo, funciona mejor para volúmenes de muestra más pequeños pero tiene dificultades para manejar sustancias inhibitorias. Después de concentrar las muestras y eliminar los inhibidores, la incubación y validación aseguran la precisión de los resultados.
Las pruebas de esterilidad tradicionales dependen de un período de incubación de 14 días para confirmar visualmente el crecimiento microbiano [3]. Los medios comúnmente utilizados incluyen Medio de Tioglicolato Fluido (FTM) para bacterias aeróbicas y anaeróbicas, y Digestión de Caseína de Soya (SCD) para hongos y bacterias aeróbicas. Antes de realizar cualquier prueba de esterilidad, es crucial validar que el producto no inhibe el crecimiento microbiano mediante pruebas de bacteriostasis y fungistasis.
Para el monitoreo continuo de procesos, las pruebas cuantitativas de carga microbiana ofrecen una solución más práctica que las pruebas de esterilidad binarias, particularmente en la producción de carne cultivada. A diferencia de las pruebas de esterilidad que proporcionan un simple resultado de aprobado/reprobado, las pruebas de carga microbiana miden las unidades formadoras de colonias (UFC) para asegurar que los niveles microbianos se mantengan dentro de límites aceptables. Este método se alinea con los estándares emergentes de grado alimenticio, logrando un equilibrio entre los estrictos controles farmacéuticos y las realidades económicas de la producción de alimentos a gran escala.
Para suministros de pruebas de esterilidad y soluciones de biorreactores, los profesionales de la carne cultivada pueden recurrir a proveedores de confianza como
| Método | Mejor Aplicación | Ventaja Clave | Limitación Principal |
|---|---|---|---|
| Filtración por Membrana | Grandes volúmenes; muestras con inhibidores | Concentra microbios y elimina sustancias interferentes[3] | Requiere un período de incubación de 14 días[3] |
| Inoculación Directa | Pequeños volúmenes sin inhibidores | Adición aséptica simple | Limitado a pequeños volúmenes; afectado por inhibidores[3] |
| Prueba de Biocarga | Monitoreo en proceso con límites microbianos establecidos | Proporciona una evaluación cuantitativa | No apto para la verificación final de esterilidad [3] |
Monitoreo en Tiempo Real y Garantía de Esterilidad
Confiar en las pruebas de esterilidad tradicionales de 14 días conlleva el riesgo de perder lotes enteros si la contaminación se descubre demasiado tarde.El monitoreo en tiempo real ofrece una solución proactiva al vigilar los parámetros críticos del proceso a medida que ocurren. Esto permite una acción inmediata si algo sale mal. En la producción de carne cultivada, donde las corridas de biorreactores duran semanas y se utilizan medios de crecimiento costosos, la detección temprana de la contaminación puede ahorrar miles de libras y evitar retrasos en la producción. Al combinar datos en tiempo real con pruebas de esterilidad convencionales, los productores pueden cerrar la brecha entre la confirmación retrasada y la intervención rápida.
Monitoreo Basado en Sensores
Indicadores clave como los niveles de oxígeno disuelto (DO) y pH pueden señalar contaminación temprana. Cuando las bacterias o los hongos infiltran un biorreactor, consumen rápidamente oxígeno, lo que hace que los niveles de DO caigan, y liberan ácidos metabólicos que reducen significativamente el pH [12]. Estos cambios pueden detectarse horas antes de que la contaminación se vuelva visualmente aparente. Mientras que las pruebas de esterilidad tradicionales confirman los resultados después del proceso, el monitoreo en tiempo real actúa como una salvaguarda, asegurando que el proceso se mantenga en curso y abordando los riesgos de contaminación más temprano.
Análisis de gases de escape, utilizando espectrometría de masas de sector magnético, mide continuamente los niveles de oxígeno y dióxido de carbono en el gas de escape de un biorreactor. En estudios de contaminación controlada, este método identificó el crecimiento microbiano dentro de 22.4 horas a través de cambios en el oxígeno, mientras que la detección basada en pH se retrasó a 25.8 horas [13]. Los sistemas de sector magnético ofrecen mediciones precisas de oxígeno con una exactitud de hasta 0.003% (v/v) durante siete días, superando a los detectores paramagnéticos tradicionales, que solo son precisos hasta ±0.2% (v/v) [13].
Sensores espectroscópicos proporcionan monitoreo no invasivo a través de las paredes de biorreactores de un solo uso, lo cual es vital para mantener la esterilidad.La espectroscopía UV-vis puede detectar daños en la membrana midiendo la absorción de luz a 350–400 nm, mientras que los materiales intracelulares filtrados aparecen a 800–900 nm [14]. Las sondas de capacitancia, los únicos sensores disponibles comercialmente diseñados para medir la densidad celular viable, logran esto detectando cambios en la polarización de la membrana [14]. Para instalaciones que gestionan múltiples biorreactores, herramientas como el Rapid Multi-Stream Sampler pueden monitorear hasta 16 corrientes de gas simultáneamente [13].
Estos sistemas basados en sensores, combinados con controles ambientales, como prevención de contaminación HVAC, crean una defensa robusta contra la contaminación.
Controles Ambientales y de Presión
Mantener una presión positiva entre las zonas de sala limpia es crucial para prevenir la entrada de contaminantes [3].Los sistemas de presión positiva, cuando se combinan con filtración HEPA, actúan como barreras físicas contra la intrusión microbiana. Las alarmas audibles o visuales en los filtros HEPA pueden notificar inmediatamente al personal si la presión cae por debajo de los niveles aceptables [3].
El conteo de partículas no viables es otra capa de defensa. Los contadores de partículas láser verifican continuamente que el entorno cumpla con los estándares de limpieza del aire ISO durante la operación. Al monitorear tanto partículas de 0.5 µm como de 5.0 µm, estos dispositivos aseguran que la calidad del aire se mantenga dentro de los límites requeridos [7]. Si ocurren desviaciones inesperadas, como una caída repentina en el DO o una fluctuación de pH, el aislamiento inmediato del biorreactor afectado y la detención de las adiciones de alimentación pueden prevenir que la contaminación se propague [12].
Para obtener sensores especializados y equipos adaptados a las operaciones de carne cultivada, empresas como
Nuevas Tecnologías en Pruebas de Esterilidad
Los métodos tradicionales de pruebas de esterilidad a menudo no cumplen debido a sus largos períodos de incubación de 14 días y su dependencia del muestreo manual, lo que puede dejar espacio para brechas en la detección. Las tecnologías más recientes están interviniendo para abordar estos desafíos, ofreciendo una detección de contaminación más rápida y precisa. Esto es especialmente crucial en la producción de carne cultivada, donde el alto costo de los medios de crecimiento y los tiempos de cultivo prolongados hacen que la contaminación en etapas avanzadas sea una pesadilla financiera.
Sistemas de Monitoreo Impulsados por IA
La inteligencia artificial está transformando la detección de contaminación al analizar datos en tiempo real para identificar intrusiones microbianas.Cuando las bacterias invaden un biorreactor, consumen oxígeno y producen ácidos metabólicos, lo que lleva a caídas notables en los niveles de oxígeno disuelto y pH. Los sistemas de IA pueden detectar estas desviaciones en el consumo de oxígeno y nutrientes, señalando una posible contaminación mucho antes de que las pruebas de carga biológica y los protocolos de esterilidad tradicionales puedan proporcionar resultados [12].
Estas plataformas de IA también incorporan modelos matemáticos para identificar el momento exacto en que ocurrió la contaminación y simular cómo crecen las poblaciones microbianas con el tiempo. Esto ayuda a los operadores a rastrear la contaminación hasta su origen, ya sea una fuente de alimentación defectuosa, un error operativo o un problema de equipo. Técnicas como el análisis de probabilidad de Poisson mejoran aún más la precisión de las pruebas de carga biológica, reduciendo la probabilidad de falsos negativos [12].
"Los modelos matemáticos ayudan a estimar el tiempo de introducción de la contaminación y la dinámica de crecimiento microbiano, mejorando la trazabilidad de la contaminación." - Naveenganesh Muralidharan, Gerente Senior, MSAT, AGC Biologics [12]
Cuando se detectan anomalías, una acción inmediata, como aislar el biorreactor y detener todas las adiciones de alimentación, puede evitar que el problema se propague [12]. Un enfoque sistemático que involucra pruebas de carga biológica, identificación molecular y análisis de la tasa de crecimiento es esencial para identificar la causa raíz e implementar medidas correctivas. Estas herramientas de IA cierran la brecha entre los métodos tradicionales y la gestión proactiva de la contaminación.
Esterilización por Plasma Frío
La tecnología de plasma frío ofrece una opción de esterilización no térmica que es particularmente adecuada para la producción de carne cultivada.Operando a temperatura ambiente o cerca de ella, es ideal para esterilizar componentes sensibles como partes de biorreactores, sensores y plásticos que no pueden soportar el calor de la autoclave tradicional [15][16][17]. Este método utiliza especies reactivas de oxígeno y nitrógeno, junto con luz UV, para interrumpir las membranas microbianas y el ADN. Es efectivo contra una amplia gama de contaminantes, incluidas esporas bacterianas (Bacillus, Clostridium), hongos, virus e incluso priones [15][17].
Una de las características destacadas del plasma frío es que deja sin residuos tóxicos. Una vez que se apaga la energía, las especies reactivas rápidamente se convierten en oxígeno, eliminando la necesidad de una fase de desorción [16][18].También es eficiente en energía, ya que solo requiere un enchufe eléctrico estándar en lugar de fuentes de calor basadas en combustibles fósiles [15][16]. Por ejemplo, los estudios muestran que el plasma frío puede lograr una >5 reducción logarítmica en esporas de Bacillus cereus en 25 minutos a 300W de potencia [15].
Sin embargo, la tecnología no está exenta de limitaciones. Sus efectos de esterilización son principalmente superficiales, lo que significa que tiene dificultades para penetrar en geometrías complejas donde los microbios pueden esconderse en grietas o ranuras [15][16]. Un alto contenido de proteínas o grasas en los entornos de biorreactores también puede proteger a los microbios al eliminar especies reactivas, reduciendo la eficiencia de la esterilización [15][18].
| Característica | Plasma Frío |
|---|---|
| Ventajas | No térmico, no tóxico, eficiente en energía, sin residuos, rápido [16] |
| Limitaciones | Penetración limitada, eficacia reducida en geometrías complejas [15][16] |
Sistemas Automatizados de Detección Basados en Imágenes
Agregando a la mezcla, los sistemas de imágenes automatizados proporcionan una herramienta poderosa para la detección de contaminación en tiempo real. Estos sistemas ofrecen información morfológica detallada sobre el crecimiento celular, lo cual es crucial para detectar patrones de contaminación a medida que ocurren [19]. A diferencia de la microscopía tradicional fuera de línea, que requiere muestreo y tinción manual, la imagen automatizada se integra perfectamente en configuraciones de monitoreo en línea o en el lugar. Esto permite a los operadores monitorear la biomasa y la salud celular sin comprometer la esterilidad [19].
Al reducir las intervenciones manuales, estos sistemas disminuyen el error humano y mejoran la reproducibilidad en los procesos de cultivo [19]. Los algoritmos avanzados de procesamiento de imágenes pueden rastrear el progreso de la fermentación, optimizar la producción de metabolitos y asegurar la consistencia, un factor crítico al escalar bioprocesos [19].
"La disponibilidad de técnicas de muestreo avanzadas junto con herramientas de medición automatizadas...puede reducir significativamente el tiempo requerido para la selección de cepas, el desarrollo de procesos y el control de procesos al disminuir el número de pasos en el proceso de producción/cultivo, especialmente los pasos manuales, y reducir la propagación de errores." - A.C. Veloso y E.C. Ferreira, Universidad de Minho [19]
A pesar de sus ventajas, integrar estos sistemas no siempre es sencillo. Los cultivos celulares son complejos, los materiales crudos varían y los sensores deben soportar métodos de esterilización rigurosos como el vapor o la irradiación gamma [19]. Para las empresas que buscan adoptar estas tecnologías, plataformas como
Conclusión
Asegurar la esterilidad del biorreactor en la producción de carne cultivada no es una tarea sencilla, pero una estrategia integrada de pruebas de esterilidad puede hacerlo alcanzable.Esta estrategia combina métodos tradicionales, como la filtración por membrana para volúmenes de muestra más grandes y la inoculación directa para volúmenes más pequeños, con herramientas moleculares modernas como PCR y qPCR para un rápido cribado de patógenos. Además, el monitoreo ambiental - a través de muestreo de aire y frotis de superficies - añade una salvaguarda adicional, abordando los riesgos de contaminación en los sistemas HVAC, detectando potenciales contaminaciones antes de que puedan afectar los recipientes de producción [11].
La elección del enfoque de prueba depende de factores como el tamaño de la muestra, la presencia de sustancias que puedan interferir con los resultados, y si el enfoque está en la validación completa de esterilidad o simplemente en el monitoreo de la carga biológica. El muestreo desde múltiples puntos en el biorreactor - superior, medio e inferior - ayuda a crear un perfil microbiano completo y reduce la posibilidad de pasar por alto una contaminación localizada [1].Esto es particularmente crítico dado que los riesgos de contaminación en la producción de carne cultivada son notablemente más altos que en la fabricación biofarmacéutica, destacando la necesidad de protocolos de esterilidad rigurosos [6].
Clave para mantener la esterilidad del medio en biorreactores es obtener el equipo adecuado. Herramientas como sistemas de muestreo aséptico con septos preesterilizados y filtros HEPA capaces de capturar el 99.97% de las partículas mayores de 0.3 μm son esenciales [4]. Plataformas como
A medida que la industria crece, los enfoques híbridos de esterilidad se están volviendo cada vez más importantes.Aplicar controles de grado farmacéutico durante las etapas tempranas de la cadena de semillas, mientras se adoptan estándares de grado alimenticio para la producción a gran escala, logra un equilibrio entre seguridad y rentabilidad [5][6]. Estas medidas integradas serán la piedra angular de la producción segura y eficiente de carne cultivada a medida que el campo continúe avanzando.
Preguntas Frecuentes
¿Cuáles son las principales causas de contaminación en los sistemas de biorreactores utilizados para la producción de carne cultivada?
La contaminación en los sistemas de biorreactores ocurre cuando se interrumpe el ambiente estéril o cuando los medios ricos en nutrientes proporcionan un entorno ideal para que prosperen los microbios. Esto puede ser causado por varios factores, como brechas durante el muestreo, mantenimiento o cosecha de células; filtros de gas dañados o bloqueados; contaminación ya presente en el medio de crecimiento; o aperturas temporales creadas al instalar o dar servicio a sensores.Además, el equipo desgastado puede desprender partículas de microplástico, que pueden servir como hogar para microorganismos.
En la producción de carne cultivada, incluso la contaminación más pequeña puede comprometer tanto la seguridad como el rendimiento de un lote. Para reducir estos riesgos, es crucial invertir en equipos de alta calidad como filtros estériles, biorreactores y kits de sensores que cumplan con estrictos estándares asépticos. Plataformas como
¿Cómo mejora la inteligencia artificial las pruebas de esterilidad en biorreactores?
Los sistemas impulsados por IA están transformando las pruebas de esterilidad en biorreactores de carne cultivada al ofrecer información en tiempo real a través de un monitoreo continuo. Usando biosensores avanzados, estos sistemas realizan un seguimiento de factores críticos como pH, oxígeno disuelto y metabolitos esenciales como glucosa y aminoácidos. Todo esto ocurre sin la necesidad de verificaciones manuales, lo que reduce drásticamente el riesgo de contaminación.
Lo que distingue a estos sistemas es su capacidad para analizar datos utilizando algoritmos que comparan las lecturas con estándares de esterilidad establecidos. Esto significa que pueden detectar incluso los signos más pequeños de crecimiento microbiano mucho antes que los métodos tradicionales. Más allá de la detección, el análisis predictivo entra en juego, identificando riesgos potenciales como problemas durante la instalación de sensores o entrada a través de puertos. Estos sistemas incluso sugieren medidas correctivas para ayudar a los productores a evitar pérdidas costosas de lotes.
La microscopía impulsada por IA añade otra capa de eficiencia al distinguir instantáneamente entre células saludables y contaminantes, acelerando los procesos de verificación de esterilidad.Para los productores, plataformas como
¿Qué desafíos limitan el uso de la esterilización por plasma frío en biorreactores para la producción de carne cultivada?
La esterilización por plasma frío es efectiva para neutralizar microbios, pero presenta una serie de desafíos cuando se aplica a biorreactores en la producción de carne cultivada. Un problema importante es la limitada profundidad de penetración de las especies reactivas producidas por el plasma. Esto dificulta la esterilización completa de grandes volúmenes o medios densamente empaquetados. Además, lograr una cobertura uniforme de plasma en todo un reactor se vuelve cada vez más difícil a medida que aumenta el tamaño del sistema.
Escalar los sistemas de plasma frío desde entornos de laboratorio a biorreactores a escala comercial introduce obstáculos adicionales.Los reactores más grandes demandan relaciones de potencia a volumen más altas, lo que puede resultar en tiempos de esterilización que están lejos de ser prácticos. Muchos sistemas de plasma frío también operan bajo condiciones de vacío o dependen de gases reactivos, añadiendo capas de complejidad en términos de seguridad, cumplimiento normativo y diseño de equipos. Estos factores hacen que el método sea menos ideal para los biorreactores a gran escala típicamente requeridos en la producción comercial de carne cultivada.
Otra preocupación es el potencial daño causado por especies reactivas de oxígeno y nitrógeno (RONS), que son clave para la inactivación microbiana. Estas especies reactivas pueden dañar células mamíferas sensibles o degradar componentes del medio, lo que requiere una optimización cuidadosa para mantener la viabilidad celular. Como resultado, el plasma frío a menudo se utiliza en combinación con otras técnicas de esterilización en lugar de como una solución independiente.











