Criopreservación es el proceso de congelar y almacenar células vivas a temperaturas ultra-bajas para mantener su viabilidad a lo largo del tiempo. Este método es crítico para la producción de carne cultivada, asegurando líneas celulares consistentes y estables y protegiendo contra pérdidas por contaminación o fallos en el equipo. Los pasos clave incluyen:
- Preparación: Cosechar células durante su fase de crecimiento, verificar la viabilidad (apuntar a ≥90%), y prepararlas en medios de congelación con crioprotectores como DMSO o glicerol.
- Congelación: Utilizar una tasa de enfriamiento controlada (-1°C a -3°C por minuto) para prevenir daños por cristales de hielo. Almacenar células en vapor de nitrógeno líquido (-135°C a -190°C) para preservación a largo plazo.
- Descongelación: Descongelar rápidamente las células en un baño de agua a 37°C para minimizar la toxicidad del crioprotector, luego transferirlas a medios de crecimiento para su recuperación.
- Control de Calidad: Etiquetar viales con precisión, monitorear las condiciones de almacenamiento y probar la viabilidad después de la descongelación para asegurar una preservación exitosa.
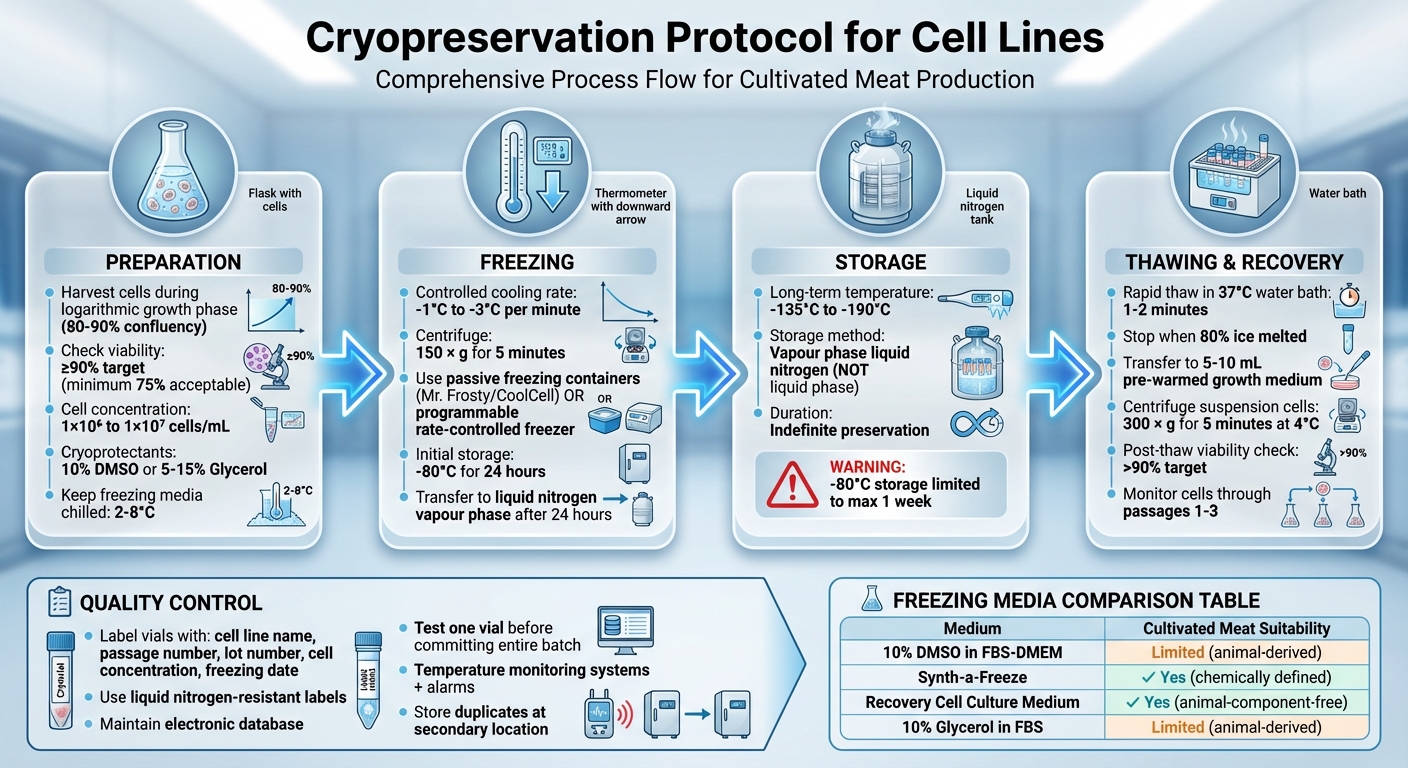
Protocolo Completo de Criopreservación para Líneas Celulares: Proceso de 4 Pasos desde la Preparación hasta el Almacenamiento
Preparación de Células para Criopreservación
Cosecha de Células y Comprobaciones de Viabilidad
Para asegurar la mejor recuperación después de la descongelación, coseche células durante su fase de crecimiento logarítmico (log). Para líneas celulares adherentes, esto es típicamente cuando alcanzan un 80–90% de confluencia [2][3][6].
Verifique la viabilidad de las células utilizando el método de exclusión de Azul de Trypan. Mezcle partes iguales (1:1) de 0.4% de Azul de Trypan con la suspensión celular, luego cuente las células utilizando un hemocitómetro.Las células viables excluirán el tinte y aparecerán brillantes bajo el microscopio, mientras que las células no viables se teñirán de azul [4]. Idealmente, apunte a una viabilidad de al menos el 90% para las mejores tasas de recuperación, aunque algunos protocolos pueden aceptar un mínimo del 75% [1][2][3][5].
Antes de la cosecha, use un microscopio para verificar la contaminación bacteriana o fúngica. Las células de suspensión saludables deben aparecer brillantes, redondas y refráctiles bajo un microscopio invertido de contraste de fase [2][3].
Una vez que las células cumplan con los estándares de viabilidad requeridos, pase a los pasos previos a la congelación.
Preparaciones Precongelación
Para células adherentes, utilice métodos de disociación suaves, como tripsina o TrypLE Express, y limite el tiempo de incubación para evitar dañar las membranas celulares [5]. Prepare las células a una concentración de 1 × 10⁶ a 1 × 10⁷ células/mL, dependiendo de la línea celular [1][6]. Al alícuotar, asegúrese de que la suspensión celular se mezcle con frecuencia para mantener una distribución uniforme en los crioviales [5].
Mantenga el medio de congelación refrigerado entre 2°C y 8°C durante la resuspensión para reducir la toxicidad del crioprotector antes de que comience el proceso de congelación [5]. Una vez que las células estén suspendidas en el medio de congelación, pase rápidamente al protocolo de congelación [1].Siempre criopreserve las células en el número de paso más bajo posible para reducir el riesgo de deriva genética o cambios morfológicos [5][7].
Selección de Crioprotectores y Medios de Congelación
Opciones de Crioprotectores y Sus Funciones
Dimetilsulfóxido (DMSO) se utiliza ampliamente como crioprotector, típicamente a una concentración del 10% [2]. Funciona penetrando las membranas celulares y reduciendo la formación de hielo durante la congelación. Sin embargo, el DMSO puede ser tóxico para las células a temperatura ambiente, por lo que el descongelamiento rápido es esencial para minimizar la exposición y diluirlo rápidamente [1].
Glicerol sirve como una alternativa útil para líneas celulares sensibles al DMSO, generalmente utilizado en concentraciones que oscilan entre el 5% y el 15% [8].Es particularmente efectivo para tipos de células donde el DMSO podría causar diferenciación no deseada [3], y tiende a tener menor toxicidad en comparación con el DMSO.
En aplicaciones de carne cultivada, los protocolos de congelación tradicionales a menudo utilizan una mezcla de 90% de suero bovino fetal (FBS) y 10% de DMSO [1]. Sin embargo, la dependencia de componentes de origen animal limita estos métodos en términos de escalabilidad y aprobación regulatoria [9]. Para abordar estos problemas, medios químicamente definidos - como Synth-a-Freeze o Recovery Cell Culture Medium - proporcionan una alternativa libre de componentes animales. Estos medios mantienen una alta viabilidad celular post-descongelación mientras superan los desafíos asociados con componentes de origen animal [9].
Comparación de Medios de Congelación
A continuación se presenta un desglose de las ventajas y limitaciones de varios medios de congelación utilizados en la producción de carne cultivada:
| Medio | Pros | Contras | Idoneidad para Carne Cultivada |
|---|---|---|---|
| 10% DMSO en FBS-DMEM | Protocolos establecidos [1] | Contiene componentes de origen animal; variabilidad por lote [9] | Escalabilidad limitada |
| Synth-a-Freeze | Químicamente definido; calidad consistente; libre de componentes animales [9] | Costo inicial más alto [9] | Sí |
| Medio de Cultivo Celular de Recuperación | Fácil de usar; diseñado para una recuperación rápida [9] | Puede necesitar optimización para líneas celulares específicas | Sí |
| 10% Glicerol en FBS | Alternativa para células sensibles al DMSO [1] | Se basa en suero de origen animal [9] | Escalabilidad limitada |
En febrero de 2023, investigadores de la Universidad Médica de Mujeres de Tokio, liderados por Hironobu Takahashi, demostraron la importancia de elegir el medio de congelación adecuado.Utilizando opciones comerciales como CELLBANKER 1 y 2, lograron criopreservar con éxito células miogénicas primarias bovinas a –80°C durante hasta un año. Notablemente, estas células retuvieron su capacidad para proliferar y diferenciarse en tejido muscular contráctil con estructuras de sarcómero intactas después de la descongelación [10].
Para la producción de carne cultivada, se favorecen cada vez más medios químicamente definidos y conformes a GMP. Como STEMCELL Technologies destaca:
En campos altamente regulados como la terapia celular y génica, se recomienda utilizar un medio de criopreservación totalmente definido y fabricado bajo GMP para garantizar que los productos se produzcan y controlen de manera consistente de acuerdo con los estándares de calidad [9].
Las plataformas como
Procedimiento de Criopreservación y Tasas de Enfriamiento
Protocolo de Congelación Paso a Paso
La clave para una criopreservación exitosa radica en mantener una tasa de enfriamiento constante de -1°C a -3°C por minuto[2]. Este proceso gradual permite que el agua salga de las células lentamente, previniendo la formación de cristales de hielo intracelular dañinos que podrían romper las membranas celulares[1].
Comience centrifugando las células a 150 x g durante 5 minutos[3]. Una vez centrifugadas, resuspenda el pellet celular en un medio de congelación frío que contenga 10% DMSO a una concentración de 2–4×10⁶ células/mL[3].Para reducir la exposición al DMSO, muévase rápidamente al siguiente paso: congelación.
Distribuya la suspensión celular en viales criogénicos preetiquetados. Cada vial debe indicar claramente detalles esenciales como el nombre de la línea celular, el número de paso, el número de lote, la concentración celular y la fecha de congelación[3]. Con los viales preparados, es hora de seleccionar y utilizar el equipo de enfriamiento adecuado.
Equipo y Técnicas de Enfriamiento
Coloque los viales inmediatamente en un dispositivo de enfriamiento de tasa controlada. Los contenedores de congelación pasiva, como el Nalgene "Mr Frosty" (que utiliza isopropanol) o el Corning "CoolCell", son opciones populares. Estas herramientas pueden lograr una tasa de enfriamiento de aproximadamente 1°C por minuto cuando se colocan en un congelador a -80°C[2].
Para operaciones a gran escala donde la consistencia es crítica, un congelador programable controlado por tasa es la mejor opción. Como afirma Sigma-Aldrich:
ECACC utiliza rutinariamente un congelador programable controlado por tasa. Esta es la forma más confiable y reproducible de congelar células[3].
Después de alrededor de 24 horas a -80°C, transfiera los viales a la fase de vapor de nitrógeno líquido, donde las temperaturas oscilan entre -135°C y -190°C, para almacenamiento a largo plazo[4]. Evite almacenar células a -80°C por más de una semana, ya que esto puede comprometer su viabilidad. Las temperaturas por debajo de -135°C son esenciales para la preservación indefinida[2]. Usar la fase de vapor en lugar de la fase líquida reduce el riesgo de contaminación cruzada mientras se mantienen temperaturas suficientemente bajas.
Protocolos de Descongelación y Recuperación
Proceso de Descongelación
Descongelar las células rápidamente es crucial para limitar la exposición a los crioprotectores tóxicos y prevenir que los cristales de hielo causen daños. Asegúrate de usar una visera completa y guantes aislantes por seguridad. Comienza retirando el criovial del nitrógeno líquido y aflojando ligeramente la tapa para liberar cualquier presión acumulada. Luego, vuelve a apretar la tapa.
Coloca el vial en un baño de agua a 37°C, asegurándote de que la tapa permanezca por encima de la línea de agua. Déjalo descongelar durante 1–2 minutos, o hasta que queden solo unos pocos cristales de hielo. Una vez descongelado, limpia el exterior del vial con alcohol al 70% para mantener la esterilidad.
Transfiere el contenido del vial a un tubo que contenga 5–10 mL de medio de cultivo precalentado. Agrega el medio lentamente para ayudar a reducir el choque osmótico. Si estás trabajando con líneas celulares en suspensión, centrifuga la suspensión celular inmediatamente a 300 × g durante 5 minutos a 4°C.Este paso ayuda a pelletizar las células y elimina el crioprotector. Después de la centrifugación, resuspenda las células en medio fresco. Para las células adherentes, la centrifugación generalmente no es necesaria. En su lugar, siembre directamente las células en un recipiente de cultivo adecuado y elimine cualquier DMSO residual durante el primer cambio de medio, típicamente después de 24 horas.
Evaluaciones Post-Congelación
Justo después de descongelar, verifique la viabilidad celular para asegurar que la recuperación ha sido exitosa. Utilice el método de exclusión de Trypan Blue para esta evaluación. Idealmente, la viabilidad celular debería superar el 90% [11], pero un mínimo del 75% es aceptable. Después de 24 horas, inspeccione las células bajo un microscopio de contraste de fase para confirmar la adherencia, evaluar la densidad celular y verificar cualquier signo de contaminación.
Siga monitoreando las células a través de los pasajes 1–3 para asegurar una proliferación normal y que retengan sus características esperadas. Para las líneas celulares que se recuperan más lentamente, puede mejorar la supervivencia aumentando la concentración inicial de suero bovino fetal a alrededor del 20% v/v.
sbb-itb-ffee270
Almacenamiento y Viabilidad a Largo Plazo
Condiciones y Duración de Almacenamiento
Para mantener la viabilidad de la línea celular a largo plazo, es esencial almacenarlas a temperaturas por debajo de -135°C [7][2]. Esto asegura que permanezcan preservadas indefinidamente.
El método preferido para almacenar líneas celulares de carne cultivada es el nitrógeno líquido en fase vapor. Esta técnica mantiene las temperaturas entre -135°C y -190°C, lo que la hace ideal para la preservación a largo plazo, ofreciendo una mayor seguridad en comparación con el almacenamiento en fase líquida.
Si necesita almacenar células a -80°C, limite esto a un período de 24 horas a una semana. Más allá de esto, la viabilidad celular puede disminuir.Para el almacenamiento temporal a esta temperatura, transfiera las células al almacenamiento en nitrógeno líquido lo antes posible.
Utilice viales criogénicos estériles estándar (1–2 mL) con roscado interno y un O-ring para un almacenamiento seguro [4][5]. Siempre coloque los crioviales sellados en la fase gaseosa en lugar de la fase líquida de nitrógeno para reducir el riesgo de explosiones de viales durante el descongelamiento [5]. Además, asegúrese de que los recipientes de nitrógeno líquido a granel se mantengan al menos a medio llenar para mantener un margen de seguridad.
Finalmente, las medidas rigurosas de control de calidad son críticas para asegurar la viabilidad a largo plazo de las células.
Controles de Calidad
Para asegurar la fiabilidad de las líneas celulares almacenadas, siga protocolos estrictos para el control de calidad. Comience etiquetando con precisión cada vial con etiquetas resistentes al nitrógeno líquido.Incluya detalles esenciales como la identidad de la línea celular, el número de lote, el número de paso y la fecha de congelación. Mantenga una base de datos electrónica para registrar la ubicación exacta de cada vial, lo que reduce el tiempo que los recipientes de almacenamiento necesitan permanecer abiertos [7][2].
Antes de comprometer lotes enteros a almacenamiento a largo plazo, pruebe la viabilidad de un vial después del almacenamiento a corto plazo en fase gaseosa. Este paso ayuda a confirmar que el proceso de congelación fue exitoso e identifica cualquier problema potencial [4][7][2]. Para stocks celulares de alto valor, es prudente almacenar duplicados en una ubicación secundaria para protegerse contra fallos de equipo o desastres locales [7][2].
Equipar todos los recipientes de almacenamiento con sistemas de monitoreo de temperatura y alarmas para detectar niveles bajos de nitrógeno líquido [7]. Además, instalar alarmas de oxígeno en las áreas de almacenamiento, configuradas para activarse al 18% de oxígeno (v/v), para minimizar los riesgos de asfixia para el personal que trabaja con nitrógeno líquido [7][2].
Protocolo de video de criopreservación de líneas celulares de mamíferos
Conclusión y Puntos Clave
A continuación, un resumen rápido de los pasos esenciales y recomendaciones para una criopreservación efectiva en la producción de carne cultivada:
- Cosecha de Células: Recoger células durante su fase de crecimiento logarítmico, asegurando que la viabilidad supere el 90%. Utilizar 10% de DMSO como crioprotector, aunque el glicerol puede ser una alternativa para líneas celulares más delicadas [11][1].
- Enfriamiento y Almacenamiento: Mantenga una tasa de enfriamiento controlada y transfiera rápidamente los viales al almacenamiento en nitrógeno líquido en fase vapor para salvaguardar la integridad celular [11]
Un estudio de Roka Kakehi et al. destaca la importancia de la precisión en la criopreservación [10]:
"Asegurar una fuente confiable y consistente de células mediante el uso de la criopreservación nos permitirá aumentar el suministro estable de células prometedoras para la producción de carne cultivada." - Roka Kakehi et al., Universidad Médica de Mujeres de Tokio
- Proceso de Descongelación: Descongele las células en un baño de agua a 37°C durante aproximadamente dos minutos, deteniéndose cuando el 80% del hielo se haya derretido. Esto reduce la toxicidad del DMSO y mejora la recuperación celular [1]. Realice controles de viabilidad post-descongelación para asegurar el éxito y ajustar los procedimientos futuros.
Estos métodos trabajan de la mano con prácticas estrictas de control de calidad. Siempre etiquete los viales con precisión, mantenga registros organizados e implemente verificaciones exhaustivas antes del almacenamiento a largo plazo [11]. Para necesidades especializadas de criopreservación, plataformas como
Preguntas frecuentes
¿Cuáles son las ventajas de usar medios químicamente definidos para la criopreservación de líneas celulares en la producción de carne cultivada?
Los medios químicamente definidos aportan múltiples beneficios cuando se trata de criopreservar líneas celulares para la producción de carne cultivada. Al eliminar componentes no definidos, como el suero de origen animal, garantizan resultados consistentes y predecibles - un factor crucial para mantener la fiabilidad a largo plazo de las líneas celulares.
Otra ventaja clave es el riesgo reducido de contaminación y variabilidad. Esto no solo apoya estándares de calidad y seguridad más altos, sino que también se alinea perfectamente con la precisión y escalabilidad requeridas para cumplir tanto con las demandas regulatorias como con las expectativas de los consumidores en la industria de la carne cultivada.
¿Cómo influye la elección de crioprotector en la supervivencia celular durante la congelación y descongelación?
La elección de crioprotector es un factor clave en la preservación de la salud celular durante la congelación y descongelación. Dos opciones ampliamente utilizadas son dimetilsulfóxido (DMSO) y glicerol, cada una con características distintas. El DMSO es conocido por su capacidad para penetrar rápidamente en las células y proporcionar una fuerte protección. Sin embargo, viene con una advertencia: a altas concentraciones o con exposición prolongada, puede volverse tóxico, lo que potencialmente reduce la viabilidad celular.
El glicerol, en contraste, es menos tóxico y se puede aplicar directamente.Su desventaja radica en su tasa más lenta de penetración celular, lo que puede resultar en una protección menos inmediata en comparación con el DMSO.
Lograr el equilibrio adecuado es crucial. Ajustar correctamente la concentración y el tiempo de exposición del crioprotector ayuda a proteger las células mientras se minimiza el riesgo de toxicidad. Además, adherirse a las mejores prácticas para las tasas de enfriamiento y las condiciones de almacenamiento es esencial para garantizar las tasas de recuperación más altas posibles después de la descongelación.
¿Por qué es importante controlar la tasa de enfriamiento durante la criopreservación?
Mantener una tasa de enfriamiento constante, generalmente entre –1°C y –3°C por minuto, es clave para mantener las células viables. Enfriar gradualmente permite que las células se deshidraten a un ritmo controlado, reduciendo la posibilidad de que se formen cristales de hielo dañinos, que pueden desgarrar o dañar las membranas celulares.
Este enfoque medido protege la estructura de las células, aumentando su supervivencia y funcionalidad una vez descongeladas.Seguir protocolos de enfriamiento precisos es esencial para garantizar el almacenamiento y la recuperación exitosos de líneas celulares.











