Validasi pembersihan memastikan peralatan produksi di fasilitas daging budidaya dibersihkan secara menyeluruh untuk menghilangkan residu seperti puing sel, media pertumbuhan, dan mikroba. Ini penting untuk mencegah kontaminasi silang, terutama dalam pengaturan multi-produk.
Poin-poin penting:
- Mengapa Ini Penting: Tanpa pembersihan yang tepat, residu dari satu batch dapat mencemari batch berikutnya. Peralatan bersama seperti bioreaktor dan alat adalah area berisiko tinggi.
- Standar Regulasi: Kepatuhan terhadap pedoman seperti HACCP, GMP, dan peraturan khusus Inggris adalah wajib.
-
Langkah-langkah untuk Memvalidasi Pembersihan:
- Pilih agen pembersih yang tepat (e.g. , alkali untuk protein, asam untuk mineral).
- Uji di bawah kondisi "terburuk" (e.g. , residu lengket atau tinggi protein).
- Gunakan pengambilan sampel swab dan tetapkan batas yang dapat diukur (e.g. , 10 ppm untuk residu kimia).
- Lakukan tiga siklus pembersihan berturut-turut untuk memastikan efektivitas.
- Alat Pemantauan: Swab ATP, analisis TOC, dan pelat mikrobiologi membantu memverifikasi kebersihan.
Validasi pembersihan bukan hanya tentang keamanan - ini tentang memastikan produksi yang konsisten, andal, dan mempertahankan kepercayaan pada produk daging yang dibudidayakan.
Persyaratan Regulasi dan Keamanan Hayati
Panduan Regulasi yang Relevan
Di Inggris, daging yang dibudidayakan berada di bawah pengawasan Food Standards Agency (FSA) dan Food Standards Scotland (FSS). Badan-badan ini mengevaluasi risiko dan menetapkan persyaratan untuk produk semacam itu dalam kerangka Novel Foods. Selain itu, produk tertentu mungkin perlu mematuhi peraturan GMO atau PBO.
Kepatuhan terhadap peraturan ini bergantung pada sistem jaminan kualitas yang sudah mapan:
- HACCP (Analisis Bahaya dan Titik Kendali Kritis): Berfokus pada identifikasi dan pengendalian bahaya mikroba.
- GMP (Good Manufacturing Practices): Memastikan produksi dan pengendalian kualitas yang konsisten.
- GCCP (Good Cell Culture Practices): Menangani penanganan garis sel untuk meminimalkan risiko kontaminasi.
- GHPs (Good Hygiene Practices): Mencakup standar operasional dan lingkungan umum.
Prinsip Codex Alimentarius membentuk dasar untuk menyusun pedoman industri spesifik dan rencana pengendalian kualitas, mengambil petunjuk dari sektor seperti industri klinis dan biofarmasi.
"Prinsip-prinsip Codex dan HACCP memberikan dasar yang kuat untuk membangun pedoman khusus dan rencana pengendalian kualitas untuk sektor ini, dan pembelajaran dapat diambil dari industri klinis/biopharmaceutical dan disesuaikan dengan persyaratan makanan baru."
– Penelitian dan Bukti FSA [1]
Untuk memastikan keandalan, validasi mikrobiologi dan pembersihan harus sesuai dengan standar UKAS. Pelajaran dari praktik klinis dan biopharmaceutical dapat disesuaikan untuk produksi makanan, mengatasi tantangan unik yang dihadapi fasilitas daging budidaya.
Risiko Biosafety di Pabrik Multi-Produk
Fasilitas yang memproduksi berbagai produk daging budidaya menghadapi kekhawatiran biosafety yang melampaui risiko khas dari manufaktur makanan. Ini termasuk:
- Patogen bawaan makanan tradisional: Seperti enterobacteria dan virus hewan.
- Kontaminan tersembunyi: Seperti mikoplasma dan mikobakteri, yang menghindari deteksi dalam media kultur karena tidak menyebabkan kekeruhan yang terlihat dan memerlukan pengujian khusus.
Risiko ini sangat meningkat dalam pengaturan peralatan bersama, di mana inspeksi visual saja tidak dapat menjamin kebersihan. Validasi pembersihan yang efektif sangat penting untuk menghilangkan zat berbahaya seperti endotoksin, eksotoksin, dan mikotoksin, bahkan dalam jumlah jejak.
Teknik pemantauan lanjutan dapat membantu mengurangi risiko ini. Misalnya, pemantauan in-line tingkat pH dan oksigen terlarut dapat menandakan pertumbuhan mikroba lebih awal, menunjukkan potensi kegagalan pembersihan atau sterilisasi. Selain itu, pemantauan lingkungan udara, permukaan, dan air di dalam fasilitas dapat mengidentifikasi ancaman kontaminasi sebelum mempengaruhi produksi.
"Seiring industri terus berkembang dan menyesuaikan peralatan serta proses untuk produksi CCP, pembersihan, sterilisasi, dan prosedur relevan lainnya akan memerlukan penilaian dan validasi, serta standar nasional/internasional harus dikembangkan."
– Penelitian dan Bukti FSA [1]
Tindakan ini menyoroti pentingnya protokol pembersihan dan validasi yang ketat untuk mencegah kontaminasi silang dan memastikan keamanan setiap batch produksi.
sbb-itb-ffee270
Validasi Pembersihan dalam 10 Langkah di Industri Farmasi | Panduan Lengkap Validasi Pembersihan
Membuat Protokol Validasi Pembersihan
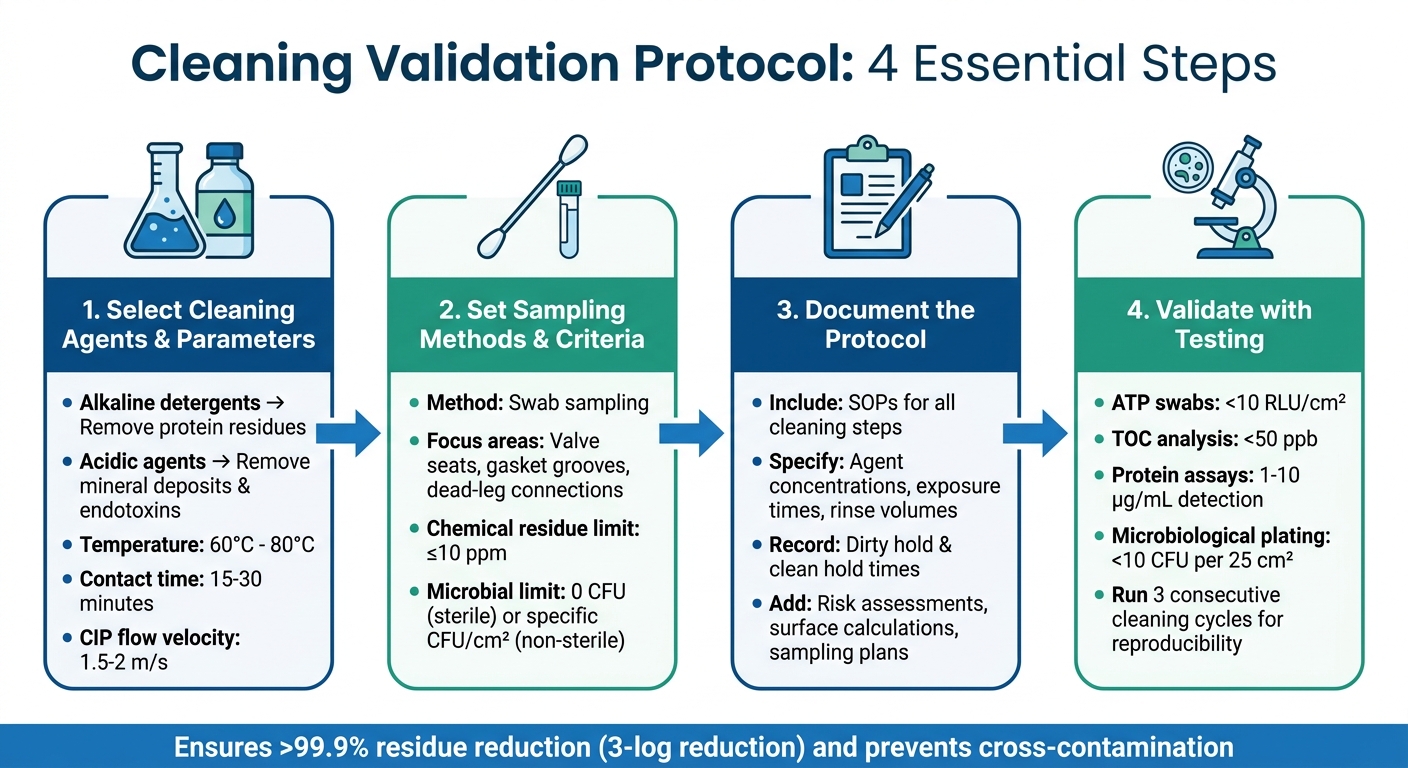
Protokol Validasi Pembersihan 4 Langkah untuk Fasilitas Daging Budidaya
Memilih Agen dan Parameter Pembersihan
Memilih agen pembersih yang tepat tergantung pada jenis residu dan bahan yang digunakan dalam peralatan Anda. Untuk fasilitas daging budidaya, bioreaktor stainless steel (biasanya grade 316L) adalah umum. Ini memerlukan deterjen alkali untuk menghilangkan residu protein, sementara agen asam ideal untuk mengatasi deposit mineral dan endotoksin. Untuk memaksimalkan efektivitas deterjen tanpa merusak segel atau gasket, pertahankan suhu pembersihan antara 60°C dan 80°C.
Biarkan agen pembersih tetap bersentuhan selama 15–30 menit, terutama di area yang sulit seperti bilah impeller dan port sensor . Untuk sistem clean-in-place (CIP), pastikan kecepatan aliran 1,5–2 m/s untuk secara efektif menghilangkan biofilm. Parameter ini harus didokumentasikan dengan cermat, karena mereka membentuk tulang punggung studi validasi Anda.
Menetapkan Metode Pengambilan Sampel dan Kriteria Penerimaan
Pengambilan sampel swab adalah metode utama untuk mendeteksi residu pada permukaan peralatan. Fokus pada area yang paling sulit dibersihkan, seperti tempat dudukan katup, alur gasket, dan sambungan dead-leg. Titik-titik ini memberikan uji yang kuat tentang seberapa efektif proses pembersihan Anda.
Kriteria penerimaan harus didasarkan pada bukti ilmiah. Untuk residu kimia, batas 10 ppm diakui secara luas, mewakili baik 1/1000 dari dosis terapeutik atau tingkat yang aman secara toksikologis.Untuk beban mikroba, produk steril menuntut ketiadaan total organisme yang dapat hidup, sementara produk non-steril dapat mengizinkan jumlah unit pembentuk koloni (CFU) tertentu per sentimeter persegi. Saat menetapkan batas residu, pertimbangkan total luas permukaan peralatan dan perhitungkan skenario produk yang paling menantang.
"Protokol validasi pembersihan adalah rencana rinci yang menggambarkan semua aktivitas validasi. Ini mencakup tujuan validasi spesifik dan pengelompokan produk serta peralatan untuk divalidasi." – Kazi, Ahli GMP [3]
Semua metode pengambilan sampel dan kriteria penerimaan harus dicatat secara menyeluruh dalam protokol.
Mendokumentasikan Protokol
Setelah parameter pembersihan dan metode pengambilan sampel ditetapkan, susun proses pembersihan lengkap ke dalam protokol yang terperinci. Dokumentasi ini harus mematuhi standar regulasi dan biosafety.Sertakan prosedur operasi standar (SOP) yang merinci setiap langkah dari proses pembersihan, mulai dari pra-bilas awal hingga inspeksi akhir. Tentukan konsentrasi agen pembersih, waktu paparan, volume bilasan, pemeriksaan verifikasi, dan durasi untuk "dirty hold" dan "clean hold" .
Juga, sertakan penilaian risiko, perhitungan luas permukaan, rencana pengambilan sampel, dan validasi untuk metode analitik. Laporan validasi akhir, setelah disetujui oleh manajemen, akan mengonfirmasi apakah proses pembersihan Anda memenuhi semua kriteria yang diperlukan dan mematuhi peraturan [3] .
Menjalankan Studi Validasi
Memilih Skenario Kasus Terburuk
Mengidentifikasi tantangan pembersihan terberat adalah kunci untuk membuktikan bahwa proses pembersihan Anda bekerja secara efektif.Di fasilitas daging budidaya, residu seperti media pertumbuhan berprotein tinggi atau scaffold daging budidaya yang lengket yang menempel pada dinding bioreaktor adalah salah satu yang paling sulit untuk dihilangkan.
Mulailah dengan merangking produk Anda berdasarkan faktor seperti kelarutan, viskositas, kandungan protein, dan berapa lama mereka tetap bersentuhan dengan permukaan. Misalnya, media pertumbuhan dengan konsentrasi protein 20% yang telah digunakan selama 72 jam meningkatkan risiko denaturasi dan pembentukan biofilm [4][5]. Perhatikan secara khusus peralatan dengan desain rumit - seperti bilah impeller, tempat duduk katup, dan port sensor - karena area ini terkenal sulit dibersihkan. Pengujian skenario seperti media tinggi lemak versus media tinggi gula juga dapat membantu mencakup spektrum produk yang Anda tangani [6][7].
Setelah Anda mendefinisikan skenario terburuk, fokuslah pada validasi proses dengan mengulangi siklus pembersihan.
Melakukan Siklus Pembersihan Berturut-turut
Melakukan tiga siklus pembersihan berturut-turut adalah cara efektif untuk mengonfirmasi baik reproduktibilitas maupun efisiensi. Pendekatan ini meniru pengaturan produksi aktual, memastikan tidak ada residu yang terbawa antara batch - terutama penting saat beralih dari media yang mengandung alergen.
Untuk memulai, kotori peralatan dengan produk skenario terburuk yang telah diidentifikasi (e.g. , 10% media pertumbuhan dalam bioreaktor). Kemudian, jalankan siklus pembersihan penuh sesuai dengan protokol Anda, dengan pengambilan sampel sebelum dan sesudah pembersihan. Ulangi proses ini dua kali lagi tanpa mengotori kembali peralatan. Data menunjukkan bahwa pada siklus ketiga, tingkat residu untuk tanah protein berkurang lebih dari 99,9% (pengurangan 3-log) [4][8]. Uji coba pabrik percontohan secara konsisten menunjukkan tingkat ATP turun di bawah 10 RLU/cm² setelah siklus berturut-turut [5][9].
Setelah Anda mengonfirmasi hasil pembersihan yang konsisten, gunakan berbagai metode deteksi residu untuk validasi menyeluruh.
Metode Pengujian untuk Deteksi Residu
Untuk memastikan biosafety dan memenuhi standar regulasi, gabungkan beberapa metode deteksi residu. Swab ATP adalah titik awal yang baik, menawarkan skrining cepat untuk residu organik dan mikroba, dengan batas deteksi serendah 100 RLU (setara dengan kurang dari 1.000 CFU/cm²). Analisis total karbon organik (TOC) adalah alat penting lainnya, mengukur residu organik dari media pertumbuhan dengan batas yang dapat diterima biasanya ditetapkan di bawah 50 bagian per miliar.Untuk deteksi spesifik protein - yang penting dalam produksi daging budidaya - uji seperti Bradford atau BCA dapat mengidentifikasi residu pada konsentrasi serendah 1–10 µg/mL [6][7].
Pelapisan mikrobiologis menambah lapisan presisi lain dengan mengidentifikasi sel-sel yang masih hidup setelah pembersihan. Gunakan pelat kontak atau swab pada permukaan yang telah dibersihkan, inkubasi sampel pada suhu 30–35°C selama 48–72 jam pada agar kedelai triptik. Produk steril umumnya memerlukan kurang dari 10 CFU per 25 cm². Penelitian yang dilakukan pada permukaan baja tahan karat telah menunjukkan kurang dari 1 CFU setelah tiga siklus pembersihan [8][10]. Untuk aplikasi daging budidaya, gabungkan swab ATP untuk pemeriksaan cepat dengan metode lanjutan seperti HPLC-MS untuk mendeteksi alergen jejak, seperti serum sapi janin, pada tingkat serendah 0.1 ppm [6][7].
Untuk panduan tentang peralatan pengujian yang sesuai dengan GMP, konsultasikan
Mendapatkan Peralatan Validasi Pembersihan melalui Cellbase
Setelah Anda menetapkan metode deteksi residu yang efektif, langkah selanjutnya adalah memastikan Anda memiliki peralatan yang tepat untuk mempertahankan proses validasi pembersihan Anda.
Peralatan dan Persediaan yang Sesuai dengan GMP untuk Validasi
Saat mendapatkan swab, mintalah data pemulihan dari pemasok untuk mengonfirmasi efektivitasnya.Pedoman Health Canada [2] menekankan bahwa proses pembersihan harus mematuhi prinsip-prinsip Manajemen Risiko Kualitas. Untuk memenuhi standar ini, pastikan alat pengambilan sampel Anda telah divalidasi melalui studi pemulihan. Selain itu, verifikasi bahwa sensitivitas alat deteksi residu Anda sesuai dengan Batas Paparan Berbasis Kesehatan (HBEL) yang telah Anda hitung.
Fokus pada pemasok di
Solusi untuk Fasilitas Daging Budidaya Multi-Produk
Fasilitas multi-produk menghadapi tantangan unik, terutama risiko kontaminasi silang saat beralih antara garis sel atau media yang mungkin mengandung alergen.
Jika Anda mengandalkan sistem CIP otomatis, carilah peralatan yang melacak parameter pembersihan kritis seperti suhu, tekanan, dan laju aliran. Health Canada menyoroti bahwa "HBEL, seperti PDE atau TTC, kemudian dapat digunakan dalam identifikasi risiko dan justifikasi batas maksimum carryover yang aman ke produk berikutnya" [2]. Peralatan CIP yang tersedia melalui
Kesimpulan
Validasi pembersihan memainkan peran penting dalam memastikan keamanan dan keandalan produksi daging budidaya multi-produk. Ini melampaui pemenuhan persyaratan regulasi - ini adalah investasi dalam mempertahankan standar keamanan, efisiensi operasional, dan kepercayaan konsumen. Dengan memvalidasi secara menyeluruh bahwa proses pembersihan menghilangkan kontaminasi silang produk dan risiko biosafety, fasilitas tidak hanya memenuhi kepatuhan tetapi juga meminimalkan kemungkinan penarikan kembali yang mahal atau gangguan operasional, sambil memperkuat kepercayaan pada produk daging budidaya.
Kunci untuk validasi pembersihan yang efektif terletak pada menetapkan tujuan yang jelas dan terukur yang selaras dengan harapan regulasi.Sebagai contoh, mengganti tujuan yang samar dengan target spesifik - seperti mendefinisikan tingkat penghapusan residu yang dapat diterima - memastikan akuntabilitas dan meningkatkan hasil produksi. Pendekatan ini tidak hanya memenuhi tuntutan regulasi tetapi juga menyediakan kerangka kerja yang solid untuk langkah-langkah praktis yang diuraikan sebelumnya.
Konsistensi sangat penting. Lakukan tinjauan triwulanan untuk mengevaluasi efektivitas protokol pembersihan dan lakukan penyesuaian berdasarkan data kinerja. Gunakan indikator utama dan tertinggal yang direkomendasikan untuk melacak kemajuan, dan perbarui dokumentasi secara teratur saat wawasan baru atau perubahan regulasi muncul [4].
FAQs
Bagaimana cara menetapkan batas residu untuk setiap pergantian produk?
Untuk menetapkan batas residu, mulailah dengan penilaian risiko menyeluruh untuk mengidentifikasi residu kritis yang dapat menimbulkan kekhawatiran. Gunakan teknik analisis lanjutan seperti HPLC (High-Performance Liquid Chromatography) atau analisis TOC (Total Organic Carbon) selama proses validasi untuk mengukur tingkat residu secara akurat.
Setelah Anda mengumpulkan data dari proses pembersihan, gunakan metode statistik - seperti menghitung rata-rata ditambah 2 atau 3 deviasi standar - untuk menentukan ambang batas yang dapat diterima. Perhitungan ini membantu mendefinisikan batas yang aman dan sesuai dengan standar industri.
Sangat penting untuk secara teratur meninjau kembali dan menyempurnakan batas-batas ini. Pemantauan dan validasi yang berkelanjutan memastikan bahwa ambang batas residu tetap efektif dan selaras dengan persyaratan keselamatan dalam bidang produksi daging budidaya yang terus berkembang.
Apa cara terbaik untuk memilih tanah "kasus terburuk" di pabrik multi-produk?
Saat memilih tanah "kasus terburuk" di fasilitas daging budidaya multi-produk, fokuslah pada residu yang paling sulit dibersihkan atau menimbulkan risiko terbesar untuk kontaminasi silang. Ini bisa termasuk protein tertentu, lemak, atau komponen media. Dengan menguji metode pembersihan pada residu yang menantang ini, Anda dapat memastikan bahwa prosesnya cukup menyeluruh untuk mengelola semua residu lainnya, memastikan dekontaminasi yang efektif di seluruh pabrik.
Kapan saya harus memvalidasi ulang pembersihan setelah perubahan proses atau resep?
Memvalidasi ulang pembersihan menjadi penting setiap kali ada perubahan pada proses, bahan, atau peralatan yang mungkin mempengaruhi efisiensi protokol pembersihan atau membawa residu baru. Langkah ini memastikan bahwa residu seperti protein, lemak, atau puing seluler dihilangkan secara efektif, mengurangi risiko kontaminasi.Selain itu, revalidasi rutin harus menjadi bagian dari prosedur rutin untuk menjaga kepatuhan dan standar biosafety dalam fasilitas produksi daging budidaya.











