ハイスループットCRISPRスクリーニングは、細胞株の性能を向上させるための正確な遺伝子改変を可能にし、培養肉セクターを変革しています。以下は知っておくべきことです:
- 主要な課題: 培養肉の生産には、効率的に成長し、老化に抵抗し、筋肉や脂肪組織に分化する細胞株が必要です。
- CRISPRの役割: 数千の遺伝子を同時にターゲットにすることで、これらのプラットフォームは成長を促進し、老化を遅らせ、分化をサポートする遺伝子編集を特定します。
- 注目すべき発見: TP53 やPTEN のような遺伝子をノックアウトすることで、ウシ間葉系幹細胞 の増殖が30日間で最大1,000倍に増加し、寿命が100日から200日に延びることが研究で示されています。
- アプリケーション: ノックアウトスクリーン、CRISPRi、CRISPRaなどのCRISPRツールは、細胞成長の最適化、遺伝子発現の調節、増殖と分化のバランスを取るために使用されています。
- 業界ツール: RMCE、RNA-seq、シングルセルプラットフォームのような高度な技術は、CRISPRの結果をマルチオミクスデータと統合し、正確でスケーラブルな改善を保証します。
バイオプロセスエンジニアやR&Dの専門家にとって、これらの革新は、細胞の品質と機能を維持しながら培養肉プロセスのスケーリングにおける重要なボトルネックに対処します。CRISPRと自動化システムおよび
ゲノムワイドノックアウトスクリーニングのためのCRISPR-Cas9の基礎
大規模な遺伝子編集におけるCRISPR-Cas9の働き
CRISPR-Cas9システムは、特定のDNA配列を標的とするために、単一ガイドRNA(sgRNA)とペアになったCas9ヌクレアーゼに依存しています。sgRNAがCas9を目的のゲノム位置に誘導すると、酵素はDNAに二本鎖切断を作成します。この切断は主に、エラーが発生しやすい非相同末端結合(NHEJ)によって修復され、しばしば小さな挿入または欠失(インデル)を導入します。これらのインデルはフレームシフト変異を引き起こし、標的遺伝子の機能を効果的に破壊することがあります。この正確なメカニズムは、細胞の行動の重要な調節因子を特定するためのゲノムワイドノックアウトスクリーニングを実施する基盤です。[1].
大規模スクリーニングでは、研究者は通常、レンチウイルス形質導入を通じて混合細胞集団に送達される多様なsgRNAライブラリーを使用します。各細胞が1つの遺伝的変化のみを受けるようにするため、低い感染率(MOI約0.3)が維持されます[1]. 時間が経つにつれて、有利な変異を持つ細胞は他の細胞よりも成功裏に増殖する傾向があり、この現象はさまざまな細胞タイプや実験条件で観察されています。
リコンビナーゼ媒介カセット交換(RMCE)などの代替送達方法は、特定のゲノム「ランディングパッド」を標的にすることで、統合部位の変動を減らし、追加の精度を提供します。例えば、CHO-K1細胞を使用した研究では、ウイルスを使用しないRMCE法を用いて21,585の遺伝子にわたる111,651のユニークなgRNAをスクリーニングしました。このアプローチにより、16日間および37日間の期間にわたって細胞の適合性に必須の遺伝子が特定されました[7].
ゲノム全体スクリーニングの利点
ゲノム全体のノックアウトスクリーニングは、CRISPR-Cas9の精度を活用して、数千の遺伝子を体系的に調査します。これにより、研究者は細胞の生存、成長、ストレスへの応答に影響を与える遺伝子を発見することができます。遺伝的要因を超えて、表面機能化の最適化は、これらのシステムにおける細胞の付着と成長を改善するために重要です。このような偏りのない探求は、培養肉生産 , に特に関連しており、間葉系幹細胞(細胞源の約25%を占める)は、限られた増殖や早期老化などの課題に直面することがよくあります[1].
sbb-itb-ffee270
プール型CRISPRライブラリスクリーニング方法
プール型CRISPRライブラリの構築
プール型CRISPRライブラリは、慎重に選択された単一ガイドRNA(sgRNA)のコレクションから始まります。培養肉研究の文脈では、転写因子や細胞増殖の調節因子など、特定の遺伝子ファミリーに焦点を当てたターゲットライブラリーが設計されることがよくあります。このアプローチは、コストとスケーラビリティのバランスを取りながら、望ましい表現型に関連する特性に焦点を当て続けるのに役立ちます。[1].
プロセスは、オリゴヌクレオチドをプールとして合成し、PCRで増幅し、デリバリーベクターにクローニングすることから始まります。例えば、2025年初頭に構築されたウシ特異的ライブラリーには、幹細胞の拡張に影響を与える因子を特定するために603の遺伝子を標的とする3,000のsgRNAが含まれていました。[1]. より大規模なスケールでは、ゲノム全体のスクリーニングははるかに高い複雑さに達することができます。一例として、中国ハムスター卵巣(CHO)細胞スクリーニングでは、21,585の遺伝子を標的とする111,651のユニークなgRNAが使用されました。[7].
レンチウイルス形質導入は、これらのライブラリーを低感染多重度(約0.3)で導入するために一般的に使用され、各細胞が単一の遺伝子修飾のみを受けることを保証します[1]. 代替として、ウイルスを使用しない方法としてリコンビナーゼ媒介カセット交換(RMCE)があり、gRNAライブラリーをマスター細胞株内の予め決められたゲノムの「ランディングパッド」に統合します。この技術は、最小限の偏りで99.9%のgRNAカバレッジを達成します[7].
統計的信頼性を維持するために、研究者は高いカバレッジを確保します - 通常、sgRNAあたり500から600の細胞です[1] [7] . いくつかのプラットフォームは、誘導性Cas9(iCas9)システムを使用し、遺伝子編集が行われるタイミングを正確に制御することを可能にします。例えば、編集は細胞が特定の状態、例えば高密度や老化の開始に達した後にトリガーされることがあります。この時間的制御は、一次細胞株と不死化細胞株の選択によって老化障壁を克服するために重要な非増殖期の研究に特に有用です。培養肉の生産を拡大するために[4] .
ライブラリが構築されると、研究者は遺伝子機能を評価するためのターゲットスクリーニングアッセイに進みます。
培養肉細胞株のスクリーニングアプローチ
ライブラリを構築した後、研究者は競争アッセイや機能的ソーティング技術を使用して細胞の性能を評価します。広く使用されている方法は、競争ベースの増殖アッセイであり、成長または老化抵抗性を付与する遺伝的変化を特定します。これは、培養肉用の細胞株を最適化するための重要な特性です。
短期スクリーニング(約30日間)は、細胞周期に即座に影響を与える遺伝子を特定し、長期スクリーニング(最大200日間)は、細胞が複製老化を克服するのを助ける遺伝子に焦点を当てます。これは、培養肉の生産を拡大する上での重要な課題です[1]. より複雑な特性、例えばタンパク質分泌の強化や特定のマーカーの発現などには、蛍光活性化セルソーティング(FACS)が使用されます。一例として、「コールドキャプチャー分泌アッセイ」があり、分泌されたタンパク質を細胞表面で捕捉してからソーティングすることで、生産性の高い細胞集団を分離します[7][5].
バリデーションは、スクリーニング結果を確認するための重要なステップです。例えば、Cellular Fitness(CelFi)アッセイは、時間の経過に伴うフレーム外変異とフレーム内変異の比率を追跡します。フレーム外変異を持つ細胞が集団から消失する場合、それは標的遺伝子が細胞の適応性にとって重要であることを示唆しています [2].
2025年6月、南京農業大学のShijie Ding率いる研究者たちは、CRISPR/Cas9を使用してCDKN2A–/– 豚衛星細胞株 . を作成しました。これらの改変された細胞は、無血清条件下で少なくとも15回の継代にわたって安定した増殖を維持し、幹細胞マーカーを保持しました。植物ベースの3D食用足場に播種されたとき、これらは改良された食感、特に噛みごたえと粘りを含む肉のような構造を形成しました [8].
"これらの発見は、ウシ幹細胞の特性を最適化するためのCRISPRスクリーニングの有用性を示し、将来的によりスケーラブルな培養肉生産への道を提供します。" – Communications Biology [1]
哺乳類細胞におけるプール型CRISPR-遺伝子スクリーニング | プロトコルプレビュー
可逆的遺伝子調節スクリーニングのためのCRISPRiとCRISPRa
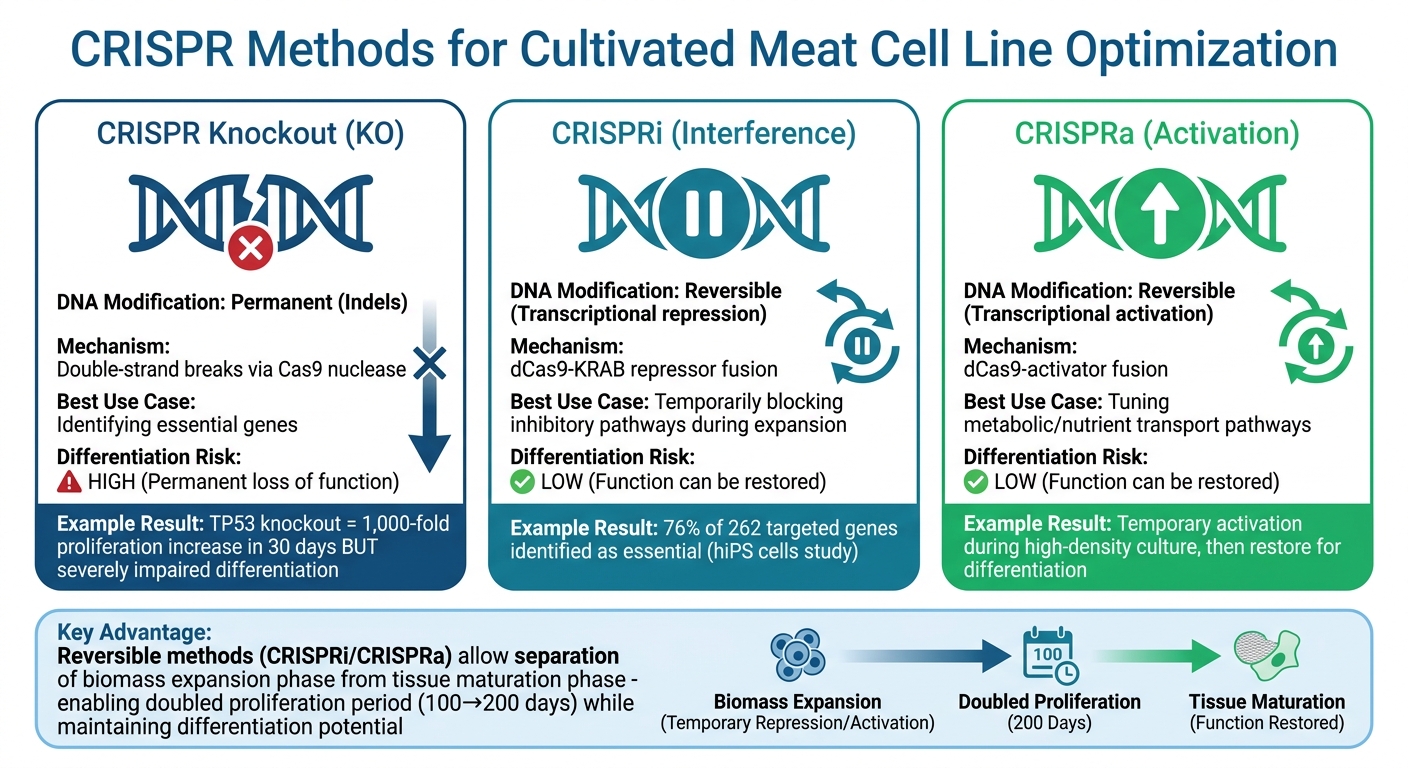
培養肉のためのCRISPR遺伝子編集方法: ノックアウト対CRISPRi/CRISPRaの比較
機能ゲノミクスにおけるCRISPRiとCRISPRaの使用
培養肉の生産を改善する際、CRISPR干渉(CRISPRi)とCRISPR活性化(CRISPRa)は強力なツールを提供します。これらの技術は、リプレッサーまたはアクティベーターと組み合わせた不活性化Cas9タンパク質を使用し、DNAに恒久的な変更を加えることなく、一時的に遺伝子発現を調整することを可能にします[10].
この可逆性は、主要な課題に取り組むために特に重要です。急速な細胞成長を促進する遺伝子は、しばしば筋肉や脂肪組織への分化の後期段階を妨げます。例えば、ウシ間葉系幹細胞でTP53遺伝子を永久にノックアウトすると、わずか30日で増殖が1,000倍以上に増加しますが、分化能力が著しく損なわれます。[1]. CRISPRiは、培養肉の バイオリアクターでのバイオマス拡大中に分化を阻害する経路を一時的にブロックすることで、より柔軟な解決策を提供します。
細胞が組織成熟の準備が整ったら、通常の遺伝子機能を回復させることができます。2025年10月、オランダがん研究所のGabriele Casagrande RaffiとRoderick L. Beijersbergenのような研究者が、誘導性CRISPRシステムを開発しました。このアプローチは、細胞が特定の状態(高密度や非増殖期など)に達するまで遺伝子編集を遅らせることで、細胞の生存率を維持するのに役立ちます。[4].
CRISPRiは、従来のRNA干渉(RNAi)と比較して、その精度で際立っています。RNAiはしばしば一貫性のない結果やオフターゲット効果を引き起こしますが、CRISPRiはより信頼性が高く、特定の遺伝子抑制を提供します。[2]. もう一つの利点は、CRISPRiがDNA損傷応答によって引き起こされることが多いp53関連の毒性を回避することです。2025年に孫逸仙大学がんセンター, のLiqin Wangが主導した研究では、研究者たちはドキシサイクリン誘導性KRAB–dCas9システムを使用してヒト誘導多能性幹細胞(hiPS細胞)で262の遺伝子をスクリーニングしました。彼らは、ターゲットとされた翻訳関連遺伝子の76%(262のうち200)が成長に不可欠であることを発見し、このシステムの有効性を示しました。[10].
この遺伝子発現の微調整能力により、CRISPRiとCRISPRaは、機能ゲノミクス研究において細胞の増殖と分化のバランスを取るための貴重なツールとなります。
培養肉アプリケーションへの可逆的スクリーンの適応
可逆的な遺伝子調節は、培養肉生産における重要な課題に対する解決策を提供します。例えば、CRISPRaは、高密度培養中に栄養輸送や代謝経路に関与する遺伝子を一時的に活性化することができます。細胞が望ましい密度に達したら、システムは遺伝子発現を通常のレベルに戻し、筋肉や脂肪組織への適切な分化をサポートします。
誘導性システムにより、バイオマス拡大フェーズと組織成熟を分離することも可能になります。CRISPRiは、スケールアッププロセス中に老化関連遺伝子を抑制し、ウシ細胞の増殖期間を約100日から200日以上に効果的に倍増させることができます[1]. 十分なバイオマスを達成した後、研究者は正常な遺伝子発現を回復させて分化を可能にすることができます。このアプローチは、培養中に早期に老化に入る傾向がある間葉系幹細胞に特に有用です[1].
「これらの二重プロセスの標的遺伝子編集は、MSCの拡張効率を最適化しながら、その重要な多能性と分化の可能性を維持し、最終的にはスケーラブルな培養肉システムを進化させることができます。" – コミュニケーションズ・バイオロジー [1]
以下の表は、可逆的および永久的な遺伝子調節方法の違いを示しています:
| 特徴 | CRISPRノックアウト (KO) | CRISPRi / CRISPRa |
|---|---|---|
| DNA修飾 | 永久的 (インデル) | 可逆的 (転写) |
| メカニズム | 二本鎖切断 | dCas9-エフェクターフュージョン |
| 最適な使用ケース | 必須遺伝子の特定 | 代謝/成長経路の調整 |
| 分化リスク | 高い (機能の永久的喪失) | 低い (機能が回復可能) |
この比較は、培養肉生産のための細胞株開発における特定の課題に対応するために、可逆的な遺伝子調節方法がどのように調整できるかを示しています。
CRISPRスクリーンと細胞パネルおよびジェノタイピング技術の組み合わせ
CRISPRスクリーンとマルチオミクス解析のリンク
マルチオミクスと自動ジェノタイピングをCRISPRスクリーンに統合することで、その有用性が向上し、特に培養肉の細胞株開発の進展に寄与します。
CRISPRスクリーンをRNAシーケンシングなどのマルチオミクスと組み合わせることで、研究者は特定の遺伝子ノックアウトが細胞経路に与える影響をマッピングできます。これは、細胞が増殖と分化のバランスをどのように取るかを理解することが重要な培養肉に特に関連しています。
例えば、ウシ脂肪由来間葉系幹細胞, を対象にした600遺伝子のプール型CRISPRノックアウトスクリーンとRNA-seqを組み合わせることで、TP53およびPTENのノックアウトが老化を遅らせることが明らかになりました。これらの細胞は、細胞周期遺伝子が上方制御された若々しい遺伝子発現プロファイルを維持し、トランスダクション後50日で倍加率が50%増加しました[1].
CROP-seqのようなシングルセルプラットフォームは、個々の細胞におけるsgRNAとトランスクリプトームの変化を同時に検出することで、これをさらに進めます [6]. このレベルの精度は、筋肉の分化やタンパク質合成を強化する遺伝子改変を特定するために非常に貴重です。これらは、培養肉における望ましい食感と栄養特性を達成するための重要な要素です。
もう一つの有望なアプローチは、CRISPRによる撹乱を様々なドナー、解剖学的部位、種からの多様な細胞株でテストする細胞パネルスクリーニングです。例えば、研究者たちは、7人のドナーからのヒト筋芽細胞株でMyoCRISPR-KOLibライブラリーを検証しました。分割毒素選択システムを使用して、筋芽細胞融合に必須な250の遺伝子を特定しました。これらのうち、41の遺伝子は医療データベースを通じて骨格筋形態に役割を果たすことが確認されました。[6]. この多段階の検証により、遺伝子ターゲットが生物学的変動にわたって堅牢であることが保証され、培養肉生産の拡大における重要な考慮事項となります。
これらの洞察は、遺伝子スクリーニングと詳細なジェノタイピングを組み合わせた自動化可能でスケーラブルなプラットフォームの道を開いています。
統合プラットフォームにおける自動化とスケーラビリティ
自動化は、統合CRISPRおよびジェノタイピングプラットフォームによって生成される膨大なデータセットとサンプルを処理するために不可欠です。ウイルスフリーで部位特異的なsgRNAライブラリーのデリバリーを可能にするRMCEシステムは、大きな前進です。これらのプラットフォームは、各細胞が単一で一貫したsgRNAコピーを受け取ることを保証し、変動性を低減します。RMCEは、チャイニーズハムスター卵巣(CHO)細胞において、最小限のバイアスで高いライブラリーカバレッジを既に実証しています[5].
「次世代のCHO工場の開発には、バイアスのないハイスループット遺伝子スクリーニングプラットフォームが不可欠です。」 - チャイニーズハムスター卵巣研究チーム[5]
スケーラビリティは、Cellular Fitness(CelFi)アッセイのような検証ツールによってさらに強化されます。このアッセイは、ターゲットを絞ったディープシーケンシングを使用して、時間の経過に伴うインデルプロファイルを監視し、インフレーム対アウトフレーム変異の比率を追跡します。これらの変異を成長の利点または不利と関連付けることにより、研究者は培養肉細胞株における遺伝子ターゲットを効率的に検証できます[2].
| テクノロジー | 統合方法 | 培養肉の主な利点 |
|---|---|---|
| RNA-seq / マルチオミクス | CRISPRヒットをトランスクリプトームプロファイルにリンクする | 遺伝子が成長と分化をどのように調節するかを理解する[1][6] |
| スプリットトキシンシステム | 細胞融合を生存選択にリンクする | 融合可能または欠陥のある細胞の定量的選択[6] |
| RMCEプラットフォーム | gRNAライブラリの部位特異的統合 | 一貫した遺伝子コピー数での高スループット、ウイルスフリーのスクリーニング[5] |
| CROP-seq | シングルセルCRISPR + RNA-seq | sgRNAとトランスクリプトーム変化の同時検出[6] |
| CelFiアッセイ | インデルのターゲットディープシーケンシング | アレル頻度の変化を追跡することで遺伝子ターゲットを迅速に検証[2] |
これらの先進的なプラットフォームは、遺伝子ターゲットの特定から細胞の適応度への影響の検証までのプロセスを合理化します。この効率性は、大規模な培養肉生産に十分な強度を持つ細胞株の開発をサポートします。
CRISPRスクリーンを使用して細胞株の成長と増殖を改善する
CRISPRスクリーニング法は、細胞株の性能を向上させる強力なツールとなり、培養肉生産に直接的な利益をもたらします。
CRISPRベースの細胞株改善の例
CRISPRスクリーンは、培養肉研究において細胞株の性能を向上させることに成功しています。例えば、ウシ脂肪由来間葉系幹細胞において600の遺伝子をターゲットにしたプール型ノックアウトスクリーンにより、TP53とPTENが成長の主要な阻害因子として特定されました。TP53をノックアウトすることで、30日以内に細胞の豊富さが大幅に増加しました[1]. さらに、編集されたウシ間葉系幹細胞は平均で12%高い倍加率を示しました [1] .
腫瘍抑制遺伝子を標的とすることで、研究者たちは細胞の増殖寿命を約100日から200日以上に延ばし、ハイフリック限界を効果的に回避しました。この老化の遅延により、産業的に関連する期間にわたってバイオマスの拡大が可能になります [1].
別の例では、南京農業大学のShijie Ding、Chunbao Li、Guanghong Zhouが率いる研究者たちが、CRISPR/Cas9を使用してCDKN2A−/−豚衛星細胞株を開発しました。これらのエンジニアリングされた細胞は、カスタム19成分無血清培地(A19)で少なくとも18回の継代にわたって安定した増殖を維持しました。また、食用足場, に成功裏に播種され、噛みごたえと粘りが改善された肉のような構造を作成しました[8]. 細胞は無血清条件で複数の継代にわたって90%以上の生存率を維持しました[8].
"CRISPRベースのCDKN2Aノックアウト細胞は、動物の生検を繰り返す必要性を減らし、筋肉前駆細胞の再生可能な供給源を提供します。"
これらの例は、CRISPRスクリーンが成長率を改善し、細胞の老化を遅らせ、血清フリーの培養を可能にする遺伝子改変を特定できることを示しています。これらは、培養肉の生産を拡大するための3つの重要な側面です。
CRISPR最適化細胞株のスケーリングの課題
CRISPR最適化細胞株は明確な利点を示しますが、産業用途に向けてスケーリングするには課題があります。増殖が強化されると、しばしば分化が犠牲になります。例えば、TP53ノックアウトを行ったウシ間葉系幹細胞では、筋分化遺伝子の発現が低下し、食用組織に成熟する能力が妨げられることが報告されています[1]. これに対処するためには、培地の補充や特定の転写因子の活性化など、拡張後の分化を回復させるための追加戦略が必要になる場合があります[1].
もう一つの重要な問題は、遺伝的安定性の維持です。CRISPR編集中の遺伝子コピー数の変動(異数性)やオフターゲット効果は、スクリーニング研究において一貫性のない結果や偽陽性を引き起こす可能性があります [2]. Cellular Fitness(CelFi)アッセイのようなツールは、時間の経過に伴うフレーム外インデルの比率を監視することで、観察された成長の利点が意図した編集に直接関連していることを保証し、これらのリスクを軽減するのに役立ちます[2].
経済的および技術的な障壁も依然として存在します。培養肉産業において細胞源の約25%を占める間葉系幹細胞は、成長因子の高コスト、最適化された無血清培地, の必要性、および大規模なバイオリアクター(10,000–50,000 Lの容量)の開発などの課題に直面しています[1][9][11]. さらに、3D足場に細胞を播種した際に望ましいテクスチャを確保することは依然として複雑な課題です[11].
「培養肉の現状は、高コスト、スケーラビリティの問題、さらなる技術的進歩の必要性を含む重大な課題に直面しています。"
- Communications Biology [1]
これらの課題を克服するには、遺伝子の最適化をメディアの配合、バイオリアクター技術、分化プロトコルの進歩と組み合わせた包括的なアプローチが必要です。CRISPRスクリーニングは重要な遺伝的洞察を提供しますが、これらの発見をスケーラブルなソリューションに変換するには、統合されたシステムと厳格な検証プロセスが求められます。これらの取り組みは、培養肉の生産を研究室から商業的な実現可能性へと移行させるために不可欠です。
どのようにCellbase が培養肉におけるCRISPR研究をサポートするか
CRISPRスクリーニングはその可能性をすでに示していますが、産業利用のためにスケールアップするには、専門的なツールとリソースへのアクセスが必要です。ここで
CRISPRリソースへのアクセスを通じて Cellbase
広範な製薬サプライヤーとは異なり、
培養肉開発における協力の促進
プラットフォームは、 Believer Meats やAleph Farms が手掛けるような大規模な商業プロジェクトの要求に対応するよう設計されています。. これらの事業には、50,000リットルのバイオリアクターと最適化された生産供給チェーン, のためのインフラが必要であり、
結論
ハイスループットCRISPRスクリーニングは、有望な概念から培養肉開発を進めるための重要なツールへと進化しました。この技術が細胞株の最適化に与える影響は否定できません。例えば、最近のブレークスルーでは、遺伝子改変によりウシ幹細胞の増殖寿命が100日から200日に倍増し、老化細胞の割合が60%からわずか10%に削減され、1か月で細胞の豊富さが1,000倍に達することが示されています[1]. これらの進展は、実験的研究から実用的な産業応用への明確なシフトを示しています。
コンパクトなプラットフォームとターゲットライブラリは、この分野で最も緊急の課題のいくつかに対処しています。デジタルマイクロ流体システムにより、条件ごとにわずか3,000個の細胞でスクリーニングが可能になり、市販されていない限られた一次動物細胞を扱うことが現実的になっています。一方で、MyoCRISPR-KOLibのような特化したライブラリは、ゲノムの3分の1をカバーしながら関連する転写物の90%を効率的にターゲットにします。このレベルの精度と効率は、リソースの制約を克服し、生産を拡大するために重要です。
「これらの発見は、ウシ幹細胞の特性を最適化するためのCRISPRスクリーニングの有用性を示しており、将来的によりスケーラブルな培養肉生産への道を提供します。」
これらの進歩にもかかわらず、成功は適切なインフラへのアクセスにかかっています。研究者は、種特異的なgRNAライブラリ、食品用途向けに設計された培地、培養肉生産に特化した分析ツールと互換性のあるバイオリアクターを必要としています。これらのニーズに対応して、
次世代の培養肉細胞株を設計するチームにとって、ツールと技術は準備が整っています。今の課題は、CRISPRスクリーニングを迅速かつ効果的に展開し、その可能性を最大限に引き出すことです。
よくある質問
スクリーニングのためにCRISPRノックアウト、CRISPRi、CRISPRaのどれを選ぶべきですか?
これらのシステムの選択は、特定の生物学的な質問と目指す結果に依存します:
- CRISPRノックアウト: この方法は遺伝子機能を完全に破壊するため、遺伝子の喪失や不活性化の影響を研究するのに理想的です。
- CRISPRi: DNAを切断せずに遺伝子発現を抑制することで、このアプローチは必須遺伝子の調査や可逆的な抑制が必要な場合に適しています。
- CRISPRa: 遺伝子発現を上方制御する必要がある場合、このシステムが最適です。細胞増殖や分化の促進など、過剰発現の影響を調べるのに特に有用です。
決定する際には、細胞モデル、ターゲットとする遺伝子、実験の全体的な目標を考慮してください。
筋肉や脂肪の分化を損なうことなく増殖を促進するにはどうすればよいですか?
培養肉の生産において、筋肉や脂肪細胞の増殖を促進しつつ、それらの分化能力を維持することは重要な課題です。有望なアプローチの一つは、 CRISPRベースの遺伝子編集, であり、成長を促進したり細胞の寿命を延ばすために遺伝子を正確に操作することができます。例えば、ミオスタチン (MSTN)を標的にすることで細胞の成長を促進し、CDKN2Aを編集することで細胞が老化を回避するのを助けます。
とはいえ、増殖と分化のバランスを取ることが重要です。P53 (TP53), のような特定のターゲットを誤って管理すると、分化が損なわれ、組織の質が低下する可能性があります。これらの複雑さを乗り越えるために、ハイスループットCRISPRスクリーニングが重要です。この技術は最も効果的な遺伝子調節因子を特定し、培養肉生産におけるスケーラブルで健康的な組織開発への道を開きます。
細胞株をスケールアップする前にCRISPRスクリーンヒットを検証するために必要なことは何ですか?
培養肉生産のためのCRISPRスクリーンヒットを検証するには、体系的なアプローチが必要です。まず、観察された効果が再現可能であることを確認するために、遺伝子ノックアウトなどの独立した実験を通じて遺伝子機能を確認する必要があります。次に、これらの遺伝子の生物学的関連性を評価し、細胞増殖、細胞生存率、寿命などの要因への影響を調べることが重要です。
プロセスを損なう可能性のあるオフターゲット効果や遺伝的不安定性を排除するための安全性評価も同様に重要です。バイオリアクターなどの産業環境を模倣した条件下での機能的検証は、もう一つの重要なステップです。これにより、大規模生産環境で遺伝子編集が期待通りに機能することが保証されます。スケールアップを検討する前に、各段階での徹底的なテストは不可欠です。











