Cryopreservatie is het proces van het invriezen en opslaan van levende cellen bij ultralage temperaturen om hun levensvatbaarheid in de loop van de tijd te behouden. Deze methode is cruciaal voor de productie van gekweekt vlees, omdat het zorgt voor consistente, stabiele cellijnen en bescherming biedt tegen verliezen door besmetting of uitval van apparatuur. Belangrijke stappen zijn:
- Voorbereiding: Oogst cellen tijdens hun groeifase, controleer de levensvatbaarheid (streef naar ≥90%) en bereid ze voor in invriesmedia met cryoprotectanten zoals DMSO of glycerol.
- Invriezen: Gebruik een gecontroleerde afkoelsnelheid (-1°C tot -3°C per minuut) om schade door ijskristallen te voorkomen. Sla cellen op in vloeibare stikstofdamp (-135°C tot -190°C) voor langdurige bewaring.
- Ontdooien: Ontdooi cellen snel in een waterbad van 37°C om cryoprotectant toxiciteit te minimaliseren, en breng ze vervolgens over naar groeimedia voor herstel.
- Kwaliteitscontrole: Label flacons nauwkeurig, bewaak opslagomstandigheden en test de levensvatbaarheid na ontdooiing om succesvolle conservering te garanderen.
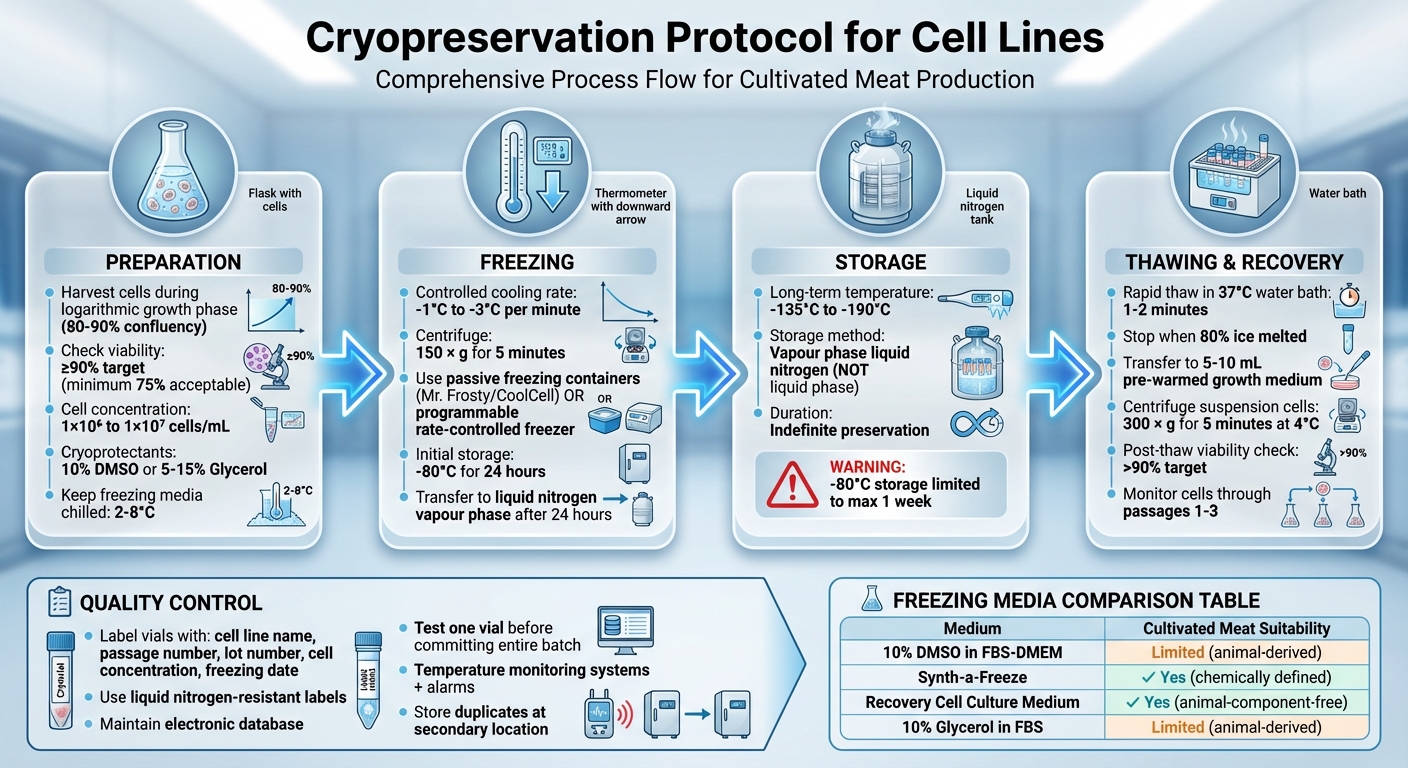
Volledig Cryopreservatieprotocol voor Cellijnen: 4-Stappenproces van Voorbereiding tot Opslag
Voorbereiding van Cellen voor Cryopreservatie
Cel Oogst en Levensvatbaarheid Controles
Om de beste herstel na ontdooiing te garanderen, oogst cellen tijdens hun logaritmische (log) groeifase. Voor adherente cellijnen is dit meestal wanneer ze 80–90% confluëntie bereiken [2][3][6].
Controleer de levensvatbaarheid van de cellen met behulp van de Trypan Blue uitsluitingsmethode. Meng gelijke delen (1:1) van 0,4% Trypan Blue met de celsuspensie en tel vervolgens de cellen met een hemocytometer.Levensvatbare cellen zullen de kleurstof uitsluiten en helder verschijnen onder de microscoop, terwijl niet-levensvatbare cellen blauw zullen kleuren [4]. Streef idealiter naar een levensvatbaarheid van ten minste 90% voor de beste herstelpercentages, hoewel sommige protocollen een minimum van 75% kunnen accepteren [1][2][3][5].
Controleer voor het oogsten met een microscoop op bacteriële of schimmelbesmetting. Gezonde suspensie cellen moeten helder, rond en brekend lijken onder een omgekeerde fasecontrastmicroscoop [2][3].
Zodra de cellen voldoen aan de vereiste levensvatbaarheidsnormen, ga verder met de stappen voor het invriezen.
Voorbereidingen voor invriezen
Voor adherente cellen, gebruik zachte dissociatiemethoden, zoals trypsine of TrypLE Express, en beperk de incubatietijd om beschadiging van de celmembranen te voorkomen [5]. Bereid de cellen voor op een concentratie van 1 × 10⁶ tot 1 × 10⁷ cellen/mL, afhankelijk van de cellijn [1][6]. Zorg ervoor dat de celsuspensie tijdens het aliquoteren regelmatig wordt gemengd om een gelijkmatige verdeling over de cryobuizen te behouden [5].
Houd het invriesmedium gekoeld tussen 2°C en 8°C tijdens de resuspensie om de toxiciteit van het cryoprotectant te verminderen voordat het invriesproces begint [5]. Zodra de cellen in het invriesmedium zijn gesuspendeerd, ga snel verder met het invriesprotocol [1].Bewaar cellen altijd bij het laagst mogelijke passagegetal om het risico op genetische drift of morfologische veranderingen te verminderen [5][7].
Selecteren van Cryoprotectanten en Invriesmedia
Cryoprotectant Opties en Hun Functies
Dimethylsulfoxide (DMSO) wordt veel gebruikt als cryoprotectant, meestal in een concentratie van 10% [2]. Het werkt door celmembranen te penetreren en de ijsvorming tijdens het invriezen te verminderen. Echter, DMSO kan toxisch zijn voor cellen bij kamertemperatuur, dus snel ontdooien is essentieel om blootstelling te minimaliseren en het snel te verdunnen [1].
Glycerol dient als een nuttig alternatief voor cellijnen die gevoelig zijn voor DMSO, en wordt over het algemeen gebruikt in concentraties variërend van 5% tot 15% [8].Het is bijzonder effectief voor celtypen waarbij DMSO ongewenste differentiatie kan veroorzaken [3], en het heeft de neiging om een lagere toxiciteit te hebben vergeleken met DMSO.
In toepassingen voor gekweekt vlees gebruiken traditionele vriesprotocollen vaak een mengsel van 90% Foetaal Kalfserum (FBS) en 10% DMSO [1]. Echter, de afhankelijkheid van dierlijke componenten beperkt deze methoden in termen van schaalbaarheid en goedkeuring door regelgevende instanties [9]. Om deze problemen aan te pakken, chemisch gedefinieerde media - zoals Synth-a-Freeze of Recovery Cell Culture Medium - bieden een alternatief zonder dierlijke componenten. Deze media behouden een hoge celviabiliteit na ontdooien en overwinnen de uitdagingen die gepaard gaan met componenten van dierlijke oorsprong [9].
Vergelijking van invriesmedia
Hier is een overzicht van de voordelen en beperkingen van verschillende invriesmedia die worden gebruikt in de productie van gekweekt vlees:
| Medium | Voordelen | Nadelen | Geschiktheid voor gekweekt vlees |
|---|---|---|---|
| 10% DMSO in FBS-DMEM | Vastgestelde protocollen [1] | Bevat componenten van dierlijke oorsprong; batchvariabiliteit [9] | Beperkte schaalbaarheid |
| Synth-a-Freeze | Chemisch gedefinieerd; consistente kwaliteit; vrij van dierlijke componenten [9] | Hogere initiële kosten [9] | Ja |
| Herstel Celkweekmedium | Eenvoudig te gebruiken; ontworpen voor snel herstel [9] | Kan optimalisatie vereisen voor specifieke cellijnen | Ja |
| 10% Glycerol in FBS | Alternatief voor DMSO-gevoelige cellen [1] | Afhankelijk van serum van dierlijke oorsprong [9] | Beperkte schaalbaarheid |
In februari 2023 toonden onderzoekers van Tokyo Women's Medical University, onder leiding van Hironobu Takahashi, het belang aan van het kiezen van het juiste invriesmedium. Using commercial options like CELLBANKER 1 and 2, they successfully cryopreserved primary bovine myogenic cells at –80°C for up to a year. Remarkably, these cells retained their ability to proliferate and differentiate into contractile muscle tissue with intact sarcomere structures after thawing [10] .
Voor de productie van gekweekt vlees worden chemisch gedefinieerde en GMP-conforme media steeds meer geprefereerd. Zoals STEMCELL Technologies benadrukt:
In sterk gereguleerde gebieden zoals cel- en gentherapie wordt aanbevolen om een GMP-geproduceerd, volledig gedefinieerd cryopreservatiemedia te gebruiken om ervoor te zorgen dat de producten consistent worden geproduceerd en gecontroleerd volgens kwaliteitsnormen [9].
Platforms zoals
Cryopreservatieprocedure en afkoelsnelheden
Stapsgewijs invriesprotocol
De sleutel tot succesvolle cryopreservatie ligt in het handhaven van een constante afkoelsnelheid van -1°C tot -3°C per minuut[2]. Dit geleidelijke proces zorgt ervoor dat water langzaam de cellen verlaat, waardoor de vorming van schadelijke intracellulaire ijskristallen die celmembranen kunnen scheuren, wordt voorkomen[1].
Begin met het centrifugeren van de cellen bij 150 x g gedurende 5 minuten[3]. Zodra ze gecentrifugeerd zijn, resuspendeer de celpellet in een koud invriesmedium dat 10% DMSO bevat bij een concentratie van 2–4×10⁶ cellen/mL [3].Om blootstelling aan DMSO te verminderen, ga snel door naar de volgende stap - invriezen.
Verdeel de celsuspensie in voorgeëtiketteerde cryogene vials. Elke vial moet duidelijk essentiële details aangeven, zoals de naam van de cellijn, passage nummer, lotnummer, celconcentratie en de datum van invriezen[3]. Met de vials voorbereid, is het tijd om de juiste koelingsapparatuur te selecteren en te gebruiken.
Koelingsapparatuur en -technieken
Plaats de vials onmiddellijk in een gecontroleerd koelingsapparaat. Passieve invriescontainers, zoals de Nalgene "Mr Frosty" (die isopropanol gebruikt) of de Corning "CoolCell", zijn populaire keuzes. Deze hulpmiddelen kunnen een koelsnelheid van ongeveer 1°C per minuut bereiken wanneer ze in een -80°C vriezer worden geplaatst[2] .
Voor grootschalige operaties waar consistentie cruciaal is, is een programmeerbare vriezer met snelheidsregeling de beste optie. Zoals vermeld door Sigma-Aldrich:
ECACC gebruikt routinematig een programmeerbare vriezer met snelheidsregeling. Dit is de meest betrouwbare en reproduceerbare manier om cellen in te vriezen[3].
Na ongeveer 24 uur bij -80°C, verplaats de buisjes naar de dampfase van vloeibare stikstof, waar de temperaturen variëren tussen -135°C en -190°C, voor langdurige opslag [4]. Vermijd het opslaan van cellen bij -80°C langer dan een week, omdat dit hun levensvatbaarheid kan aantasten. Temperaturen onder -135°C zijn essentieel voor onbeperkte conservering[2]. Het gebruik van de dampfase in plaats van de vloeibare fase vermindert het risico op kruisbesmetting terwijl voldoende lage temperaturen worden gehandhaafd.
Ontdooi- en Herstelprotocollen
Ontdooiingsproces
Het snel ontdooien van cellen is cruciaal om de blootstelling aan giftige cryoprotectanten te beperken en te voorkomen dat ijskristallen schade veroorzaken. Zorg ervoor dat u een gelaatsvizier en geïsoleerde handschoenen draagt voor de veiligheid. Begin met het verwijderen van de cryobuis uit vloeibare stikstof en draai de dop iets losser om eventuele opgebouwde druk vrij te geven. Draai vervolgens de dop weer vast.
Plaats de buis in een waterbad van 37°C, zorg ervoor dat de dop boven de waterlijn blijft. Laat het 1–2 minuten ontdooien, of totdat er slechts enkele ijskristallen overblijven. Zodra het ontdooid is, veeg de buitenkant van de buis af met 70% alcohol om steriliteit te behouden.
Breng de inhoud van de buis over in een tube met 5–10 mL voorverwarmd groeimedium. Voeg het medium langzaam toe om osmotische shock te helpen verminderen. Als u met suspensiecellijnen werkt, centrifugeer de celsuspensie onmiddellijk bij 300 × g gedurende 5 minuten bij 4°C. Deze stap helpt de cellen te pelletiseren en verwijdert het cryoprotectant. Na centrifugatie, resuspendeer de cellen in vers medium. Voor adherente cellen is centrifugatie meestal niet nodig. Zaai in plaats daarvan de cellen direct in een geschikt kweekvat en verwijder eventueel resterend DMSO tijdens de eerste mediumwisseling, meestal na 24 uur.
Beoordelingen na ontdooien
Direct na het ontdooien, controleer de levensvatbaarheid van de cellen om te verzekeren dat het herstel succesvol is geweest. Gebruik de Trypan Blue-exclusiemethode voor deze beoordeling. Idealiter zou de levensvatbaarheid van de cellen meer dan 90% moeten zijn [11], maar een minimum van 75% is acceptabel. Na 24 uur, inspecteer de cellen onder een fasecontrastmicroscoop om de hechting te bevestigen, de celdichtheid te evalueren en te controleren op tekenen van contaminatie.
Blijf de cellen monitoren door passages 1–3 om normale proliferatie te verzekeren en dat ze hun verwachte kenmerken behouden.Voor cellijnen die langzamer herstellen, kunt u de overleving verbeteren door de initiële concentratie foetaal kalfserum te verhogen tot ongeveer 20% v/v.
sbb-itb-ffee270
Opslag en Langdurige Levensvatbaarheid
Opslagcondities en Duur
Om de levensvatbaarheid van cellijnen op de lange termijn te behouden, is het essentieel om ze op te slaan bij temperaturen onder -135°C [7][2]. Dit zorgt ervoor dat ze voor onbepaalde tijd bewaard blijven.
De voorkeursmethode voor het opslaan van gekweekte vleescellijnen is dampfase vloeibare stikstof. Deze techniek houdt temperaturen tussen -135°C en -190°C, waardoor het ideaal is voor langdurige bewaring en verbeterde veiligheid biedt vergeleken met opslag in vloeibare fase.
Als u cellen bij -80°C moet opslaan, beperk dit dan tot een periode van 24 uur tot een week. Daarna kan de levensvatbaarheid van de cellen afnemen.Voor tijdelijke opslag bij deze temperatuur, verplaats de cellen zo snel mogelijk naar opslag in vloeibare stikstof.
Gebruik standaard steriele cryogene vials (1–2 mL) met interne schroefdraad en een O-ring voor veilige opslag [4][5]. Plaats altijd verzegelde cryovials in de gasfase in plaats van de vloeibare fase van stikstof om het risico op explosies van vials tijdens het ontdooien te verminderen [5]. Zorg er bovendien voor dat bulk vloeibare stikstofvaten ten minste halfvol zijn om een veiligheidsbuffer te behouden.
Ten slotte zijn rigoureuze kwaliteitscontrolemaatregelen cruciaal om de lange termijn levensvatbaarheid van de cellen te waarborgen.
Kwaliteitscontrolecontroles
Om de betrouwbaarheid van opgeslagen cellijnen te waarborgen, volg strikte protocollen voor kwaliteitscontrole. Begin met het nauwkeurig labelen van elke vial met vloeibare stikstofbestendige labels.Neem essentiële details op zoals de identiteit van de cellijn, het lotnummer, het passage-nummer en de invriesdatum. Houd een elektronische database bij om de exacte locatie van elke vial te registreren, wat de tijd vermindert dat opslagvaten open moeten blijven [7][2].
Voordat u hele batches aan langdurige opslag toewijst, test de levensvatbaarheid van één vial na kortdurende gasfase-opslag. Deze stap helpt te bevestigen dat het invriesproces succesvol was en identificeert eventuele potentiële problemen [4][7][2]. Voor zeer waardevolle celvoorraden is het verstandig om duplicaten op een secundaire locatie op te slaan om te beschermen tegen uitrustingsstoringen of lokale rampen [7][2].
Voorzie alle opslagvaten van temperatuurcontrolesystemen en alarmen om lage vloeibare stikstofniveaus te detecteren [7]. Installeer daarnaast zuurstofalarmen in opslagruimtes, ingesteld om te activeren bij 18% zuurstof (v/v), om verstikkingsrisico's voor personeel dat met vloeibare stikstof werkt te minimaliseren [7][2].
Cryopreservatie van zoogdiercellijnen video protocol
Conclusie en Belangrijke Inzichten
Hier is een kort overzicht van de essentiële stappen en aanbevelingen voor effectieve cryopreservatie in de productie van gekweekt vlees:
- Cel Oogsten: Verzamel cellen tijdens hun logaritmische groeifase, waarbij de levensvatbaarheid meer dan 90% moet bedragen. Gebruik 10% DMSO als cryoprotectant, hoewel glycerol een alternatief kan zijn voor meer delicate cellijnen [11][1].
- Koeling en Opslag: Handhaaf een gecontroleerde afkoelsnelheid en verplaats de vials snel naar opslag in dampfase vloeibare stikstof om de celintegriteit te waarborgen [11]
Een studie van Roka Kakehi et al. benadrukt het belang van precisie in cryopreservatie [10]:
"Het waarborgen van een betrouwbare en consistente bron van cellen door gebruik te maken van cryopreservatie stelt ons in staat om de stabiele levering van veelbelovende cellen voor de productie van gekweekt vlees te vergroten." - Roka Kakehi et al., Tokyo Women's Medical University
- Ontdooiingsproces: Ontdooi cellen in een waterbad van 37°C gedurende ongeveer twee minuten, en stop wanneer 80% van het ijs is gesmolten. Dit vermindert DMSO-toxiciteit en verbetert het herstel van cellen [1]. Volg op met levensvatbaarheidscontroles na het ontdooien om succes te garanderen en toekomstige procedures te verfijnen.
Deze methoden werken samen met strikte kwaliteitscontrolepraktijken. Label altijd de flesjes nauwkeurig, houd georganiseerde records bij en voer grondige controles uit voordat u ze voor lange termijn opslaat [11]. Voor gespecialiseerde cryopreservatiebehoeften verbinden platforms zoals
Veelgestelde vragen
Wat zijn de voordelen van het gebruik van chemisch gedefinieerd medium voor het cryopreserveren van cellijnen in de productie van gekweekt vlees?
Chemisch gedefinieerd medium biedt meerdere voordelen bij het cryopreserveren van cellijnen voor de productie van gekweekt vlees. Door ongedefinieerde componenten, zoals serum van dierlijke oorsprong, te verwijderen, zorgen ze voor consistente en voorspelbare resultaten - een cruciale factor voor het behouden van de langetermijnbetrouwbaarheid van cellijnen.
Een ander belangrijk voordeel is het verminderde risico op besmetting en variabiliteit. Dit ondersteunt niet alleen hogere kwaliteits- en veiligheidsnormen, maar sluit ook perfect aan bij de precisie en schaalbaarheid die nodig zijn om zowel aan de regelgevingseisen als aan de verwachtingen van consumenten in de gekweekte vleesindustrie te voldoen.
Hoe beïnvloedt de keuze van cryoprotectant de overleving van cellen tijdens bevriezing en ontdooiing?
De keuze van cryoprotectant is een cruciale factor bij het behoud van de gezondheid van cellen tijdens bevriezing en ontdooiing. Twee veelgebruikte opties zijn dimethylsulfoxide (DMSO) en glycerol, elk met onderscheidende eigenschappen. DMSO staat bekend om zijn vermogen om snel cellen binnen te dringen en sterke bescherming te bieden. Het heeft echter een keerzijde: bij hoge concentraties of bij langdurige blootstelling kan het toxisch worden, wat mogelijk de levensvatbaarheid van cellen verlaagt.
Glycerol daarentegen is minder toxisch en kan direct worden toegepast.Zijn nadeel ligt in de langzamere snelheid van celpenetratie, wat kan resulteren in minder onmiddellijke bescherming vergeleken met DMSO.
Het bereiken van de juiste balans is cruciaal. Het correct aanpassen van de concentratie en blootstellingstijd van het cryoprotectant helpt cellen te beschermen terwijl het risico op toxiciteit wordt geminimaliseerd. Bovendien is het naleven van best practices voor koelsnelheden en opslagomstandigheden essentieel om de hoogst mogelijke herstelpercentages na ontdooien te garanderen.
Waarom is het belangrijk om de koelsnelheid tijdens cryopreservatie te beheersen?
Het handhaven van een constante koelsnelheid, meestal tussen –1°C en –3°C per minuut, is essentieel om cellen levensvatbaar te houden. Geleidelijk koelen stelt cellen in staat om gecontroleerd te dehydrateren, waardoor de kans op schadelijke ijskristallen die celmembranen kunnen scheuren of beschadigen, wordt verminderd.
Deze gemeten aanpak beschermt de structuur van de cellen, waardoor hun overleving en functionaliteit na ontdooien worden verbeterd.Het volgen van precieze koelprotocollen is essentieel om succesvolle langdurige opslag en herstel van cellijnen te garanderen.











