Manter níveis precisos de pH é crítico para a produção de carne cultivada. Células de mamíferos prosperam em uma faixa estreita de pH (7,1–7,4), mas a acidificação metabólica, o acúmulo de CO₂ e os desafios de mistura tornam o controle de pH complexo, especialmente em biorreatores de grande escala. Estratégias eficazes incluem:
- Injeção de gás: Remove o excesso de CO₂ sem aumentar a osmolalidade ou causar picos de pH localizados.
- Sensores avançados: Sensores potenciométricos oferecem alta precisão para sistemas de aço inoxidável, enquanto sensores ópticos funcionam bem com biorreatores de uso único.
- Otimização de tampões: Adicionar tampões como HEPES melhora a estabilidade, mas requer equilíbrio cuidadoso para evitar a produção excessiva de lactato.
- Sistemas automatizados: Ajustes em tempo real usando loops de feedback garantem níveis de pH consistentes.
Essas abordagens ajudam a superar desafios como o acúmulo de ácido lático e o estresse de cisalhamento, melhorando a saúde celular e os rendimentos do produto.
Compreendendo as Medições de pH em Bioprocessos
Desafios Principais na Gestão de pH
Esta seção explora os principais fatores que contribuem para a instabilidade do pH, com base nos desafios discutidos anteriormente.
Acidificação Metabólica e Acúmulo de Ácido Lático
O ácido lático é um grande obstáculo no bioprocessamento de carne cultivada. À medida que as células metabolizam a glicose através da glicólise, elas produzem lactato e íons de hidrogênio em uma proporção de 1:1. Este processo cria uma carga ácida significativa, tornando o lactato o principal impulsionador da acidificação do meio [1].
A capacidade de tamponamento dos meios de cultura padrão - tipicamente entre 1,1 e 1,6 mM por unidade de pH [1] - é frequentemente insuficiente durante períodos de rápido crescimento celular.Conforme as células se multiplicam, a produção de resíduos metabólicos aumenta, sobrecarregando a capacidade do meio de manter um pH estável. A queda acentuada do pH durante esta fase pode ser diretamente atribuída à produção de ácido lático glicolítico [1], destacando o papel crucial do lactato na desestabilização do pH do meio.
As complicações não param por aí. O acúmulo de CO2 adiciona outra camada de complexidade.
Acúmulo de CO2 e Desvio de pH
A respiração celular introduz CO2 no meio, onde ele se dissolve para formar ácido carbônico. A questão chave é a pressão parcial do CO2 dissolvido (pCO2), que influencia se o CO2 pode escapar das células. Quando os níveis de pCO2 no meio sobem demais, o CO2 fica preso dentro das células, causando uma perigosa queda no pH intracelular e eventualmente levando à morte celular [2].
"Se o pCO2 estiver muito alto, o CO2 não pode sair das células, então o pH intracelular cairá e as células morrerão." - Alicat Scientific [2]
Esse problema se torna mais pronunciado em biorreatores de grande escala. Esses sistemas têm uma menor relação área superficial-volume, o que reduz a eficiência da desgaseificação de CO2 em comparação com vasos menores [3]. Mesmo operações rotineiras, como transferir meios para uma incubadora de CO2, podem causar flutuações de pH. Por exemplo, pequenos volumes de meio começam a alcalinizar quase imediatamente, com uma constante de tempo de 2–3 horas [1].
Além dos desafios químicos, processos físicos também desempenham um papel significativo na instabilidade do pH.
Impactos da Mistura e do Estresse de Cisalhamento na Estabilidade do pH
Ajustar o pH adicionando uma base introduz seus próprios riscos.Quando bicarbonato de sódio ou bases similares são bombeados em biorreatores, a má mistura pode criar zonas localizadas de alto pH que prejudicam as células próximas [2] [3]. Por outro lado, a agitação vigorosa necessária para distribuir a base uniformemente pode levar ao estresse de cisalhamento e formação de espuma, ambos prejudiciais para células mamíferas frágeis [2] [3].
Em experimentos controlados, a adição de base para estabilizar o pH frequentemente reduziu a viabilidade celular devido ao aumento da osmolalidade [3]. Isso cria um ato de equilíbrio difícil: mistura insuficiente resulta em pontos de alta concentração de pH, enquanto mistura excessiva previne esses pontos, mas aumenta o estresse mecânico. O problema se torna ainda mais desafiador durante a ampliação, onde tempos de mistura mais longos dificultam a manutenção do controle eficaz do pH sem comprometer a saúde celular.
Tecnologias para Monitoramento e Controle de pH
Manter o pH dentro da faixa estreita de 7,1–7,4 é crítico para culturas de células de mamíferos, exigindo ferramentas de monitoramento precisas e confiáveis [2]. Sensores potenciométricos, que atuam como eletrodos para medir íons de hidrogênio livres, são o padrão ouro para monitoramento contínuo de pH em biorreatores [1]. Esses sensores fornecem dados em tempo real, permitindo que sistemas automatizados façam ajustes imediatos para manter os níveis de pH necessários. Sua alta precisão os torna essenciais para operações em larga escala. Juntamente com estes, indicadores ópticos oferecem outra maneira eficaz de medir o pH.
Indicadores ópticos dependem da análise espectroscópica para fornecer medições quantitativas de pH.Embora o vermelho de fenol seja frequentemente usado como um indicador visual, leituras mais precisas são alcançadas através da análise ratiométrica da absorbância em dois comprimentos de onda específicos - 560 nm e 430 nm [1] . Este método compensa fatores como volume do meio ou concentração do corante, garantindo resultados consistentes e precisos.
"A concentração de íons H+ livres não é intuitiva de prever, mas, felizmente, é simples de medir (e.g. com eletrodos ou corantes indicadores)." - Johanna Michl et al., Universidade de Oxford [1]
Sistemas modernos de controle de pH vão além do monitoramento, integrando essas medições em loops de feedback automatizados que regulam dinamicamente os níveis de pH.
Sistemas de feedback automatizados aproveitam os dados dos sensores para fazer ajustes em tempo real, eliminando a necessidade de intervenção manual. Esses sistemas podem ajustar o pH adicionando uma base ou usando técnicas de dispersão de gás [2].Para biorreatores de grande escala, a dispersão de gás é particularmente eficaz. Usando controladores de fluxo de massa, os níveis de CO2 podem ser ajustados rápida e uniformemente, garantindo uma regulação uniforme do pH [2]. Em contraste, o bombeamento de base, embora eficaz para sistemas menores, pode criar desequilíbrios de pH localizados e aumentar a osmolaridade, tornando-o menos prático para vasos maiores [2]. No entanto, a dispersão de gás requer atenção cuidadosa ao design dos dispersores para evitar o estresse de cisalhamento que poderia prejudicar as células [2]. Para aqueles na produção de carne cultivada, investir em sistemas avançados de controle de gás pode levar a uma melhor saúde celular e maiores rendimentos, tornando-se um gasto que vale a pena.
sbb-itb-ffee270
Estratégias para Gestão de pH em Escala
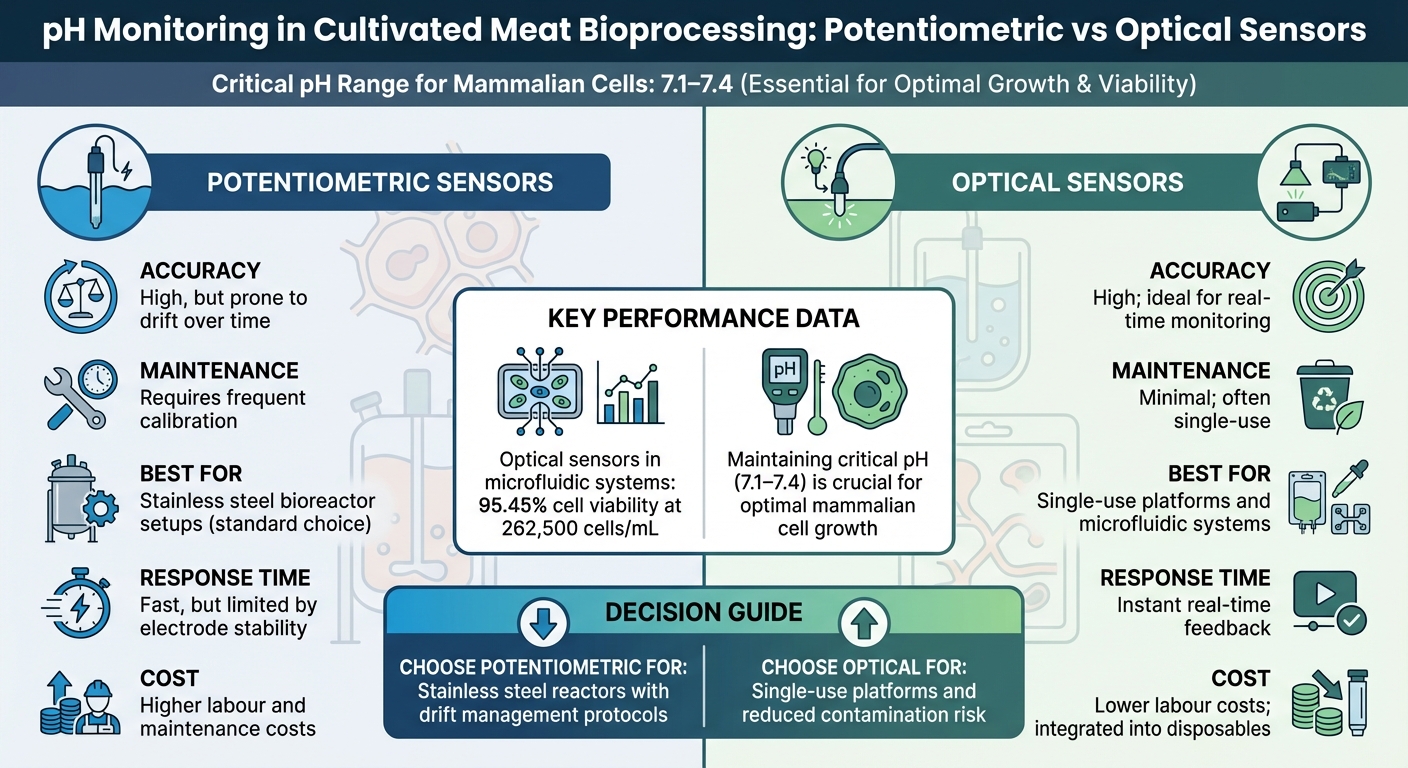
Sensores de pH Potenciométricos vs Ópticos para Biorreatores de Carne Cultivada
Sensores Potenciométricos vs Ópticos: Uma Comparação
Selecionar a tecnologia de sensor correta torna-se cada vez mais importante à medida que a produção de carne cultivada aumenta. Sensores potenciométricos são a escolha ideal para biorreatores de aço inoxidável devido à sua precisão e resposta rápida. No entanto, eles apresentam desafios como a necessidade de calibração regular e suscetibilidade a desvios durante processos prolongados. Jacob Crowe, Gerente de Suporte Técnico de Aplicações na
"Com o tempo, as medições de pH podem desviar, o que impactará a estabilidade e o desempenho do processo.É vital monitorar e mitigar a deriva de pH para prevenir efeitos prejudiciais tanto no metabolismo quanto no processo geral" [8].
Por outro lado, sensores ópticos surgem como uma opção prática, particularmente para sistemas de biorreatores de uso único. Esses sensores podem ser pré-instalados em sacos descartáveis, reduzindo os riscos de contaminação e eliminando a necessidade de esterilização entre os ciclos [7]. Em sistemas microfluídicos, sensores ópticos têm mostrado resultados e
| Recurso | Sensores Potenciométricos | Sensores Ópticos |
|---|---|---|
| Precisão | Alta, mas propensa a desvio | Alta; ideal para monitoramento em tempo real |
| Manutenção | Requer calibração frequente | Mínima; geralmente de uso único |
| Escalabilidade | Padrão para configurações de aço inoxidável | Ótimo para uso único e microfluídica |
| Tempo de Resposta | Rápido, limitado pela estabilidade do eletrodo | Feedback instantâneo em tempo real |
| Implicações de Custo | Custos mais altos de mão de obra e manutenção | Menor mão de obra; integrado em descartáveis |
A escolha do sensor depende em grande parte do tipo de reator.Bioreatores de aço inoxidável podem se beneficiar de sensores potenciométricos com medidas para gerenciar o desvio, enquanto plataformas de uso único podem capitalizar a facilidade de sensores ópticos integrados [7] [8]. Essas decisões afetam diretamente como a estabilidade do pH é mantida durante a otimização do meio.
Otimização do Meio e Melhorias no Tampão
Uma vez que os sensores apropriados estão no lugar, estabilizar o sistema tampão do meio de cultura torna-se essencial para manter o controle do pH durante a ampliação. Células de mamíferos dependem do sistema tampão CO₂/HCO₃⁻ (pKa 6,15 a 37°C), mas sua capacidade de tamponamento é frequentemente insuficiente. Por exemplo, DMEM padrão com 10% de FBS normalmente fornece apenas 1,1 a 1,6 mM de tamponamento [1].
Para resolver isso, adicionar tampões não voláteis (NVBs) como HEPES (pKa 7.3 a 37°C) pode fortalecer significativamente o tamponamento sem causar mudanças problemáticas na osmolalidade [1]. O método recomendado envolve titular o meio até o pH alvo primeiro, depois adicionar NaHCO₃ em uma concentração alinhada com o pCO₂ do incubador. Esta abordagem reduz o desvio inicial de pH quando o meio fresco é exposto ao CO₂, um processo que pode levar até duas horas com NVBs [1].
No entanto, sistemas de tamponamento mais fortes podem desencadear aumento da glicólise, levando a uma maior produção de lactato. Em algumas linhagens celulares, até 90% da glicose é diretamente convertida em lactato [1], e o tamponamento melhorado pode às vezes amplificar esse efeito, resultando em maior acúmulo de ácido láctico [10].
Técnicas de Sparging e Agitação
O sparging de gás oferece uma maneira prática de gerenciar o pH na produção de carne cultivada em larga escala.Alicat Scientific notes:
"As bolhas de gás dos spargers podem ser misturadas e distribuídas mais rapidamente do que a base, e com muito menos agitação" [2].
Ao distribuir uniformemente as bolhas de gás, o sparging oferece uma abordagem mais consistente do que as adições de base química. Por exemplo, um estudo de 2018 mostrou que manter taxas de sparge constantes enquanto aumentava a aeração do espaço de cabeça permitiu que os títulos permanecessem estáveis durante a ampliação de 30 L para 250 L [2].
Os macro spargers, que produzem bolhas de 1–4 mm de diâmetro, são particularmente eficazes na remoção do excesso de CO₂ da cultura. Isso eleva o pH naturalmente, evitando a necessidade de bases químicas que poderiam elevar a osmolalidade [2] [5]. Uma nova estratégia de controle de pH "apenas gás" usa loops de feedback de sparging de ar automatizados.Quando o pH cai, o fluxo de ar aumenta para remover mais CO₂. Este método foi escalado com sucesso de biorreatores ambr®250 para vasos de 200 L, mantendo níveis precisos de pH ao longo de culturas em batelada alimentada [6].
Equilibrar a transferência eficiente de gás com o mínimo de estresse de cisalhamento continua sendo um desafio crítico durante a ampliação. Biorreatores de airlift, que utilizam circulação impulsionada por gás, oferecem uma opção de mistura mais suave com estresse de cisalhamento reduzido. Simulações de dinâmica de fluidos computacional (CFD) também podem ajudar a identificar zonas de alto cisalhamento perto das lâminas do impulsor, permitindo que os designs de biorreatores sejam otimizados antes da ampliação [4]. Combinar essas abordagens com ferramentas avançadas de
Equipamentos de Controle de pH via Cellbase
Por que Escolher Cellbase para Aquisição?
O controle preciso de pH é essencial no bioprocessamento de carne cultivada, tornando crucial a obtenção do equipamento certo. Plataformas gerais de fornecimento de laboratório muitas vezes carecem do conhecimento especializado necessário para as faixas de pH restritas neste campo.
Ao usar
Encontrando Tecnologias de Controle de pH Através de Cellbase
Para escalonamento, a plataforma oferece acesso a controladores de fluxo de massa e dispersores especializados, que são críticos para um gerenciamento de pH eficiente baseado em gás. Como destaca a Alicat Scientific:
"Manter o pH em níveis biológicos saudáveis é potencialmente a ferramenta mais poderosa no bioprocessamento upstream para aumentar os títulos de produtos" [2].
Além disso,
Especialistas em compras também podem adquirir equipamentos para remoção de CO₂, incluindo sensores de CO₂ autoclaváveis e sondas de pH descartáveis. Essas ferramentas apoiam estratégias escaláveis para manter o controle preciso do pH, facilitando a integração de gerenciamento avançado de pH em produções em larga escala [11]. Ao oferecer soluções direcionadas,
Conclusão: Melhores Práticas para Controle de pH no Bioprocessamento de Carne Cultivada
Manter uma faixa de pH de 7,1 a 7,4 é crítico para a sobrevivência de células de mamíferos na produção de carne cultivada [2]. Manter o pH dentro dessa faixa desempenha um papel fundamental na melhoria dos rendimentos do produto durante o bioprocessamento upstream.
Para enfrentar os desafios do controle de pH, várias práticas eficazes surgiram. Um método de destaque é usar borbulhamento de gás em vez de adição de base durante a ampliação. O borbulhamento de gás remove efetivamente o excesso de CO₂ ao distribuí-lo uniformemente com agitação mínima, o que ajuda a evitar problemas como inconsistências de pH e flutuações de osmolalidade [2]. Um estudo de 2021 da Aryogen Pharmed demonstrou o sucesso desse método em uma escala de 250 litros, alcançando um aumento de 51% no rendimento final do produto [3].
Outra prática importante é o monitoramento direto de pH, que fornece uma compreensão mais abrangente da saúde da cultura em comparação com a dependência exclusiva de medições de pCO₂.Isso é particularmente vital porque os níveis de CO₂ dissolvido não levam em conta o acúmulo de ácido lático, que pode representar até 90% do metabolismo da glicose em certas linhagens celulares [1]. Monitorar o pH diretamente torna-se ainda mais crucial durante a fase de crescimento exponencial, quando a atividade metabólica atinge o pico.
Para tampões não voláteis como HEPES, é essencial considerar o equilíbrio do tampão. Os tampões HEPES podem levar até duas horas para estabilizar e devem ser cuidadosamente titulados com bicarbonato e CO₂ [1]. No entanto, aumentar a capacidade de tamponamento pode, inadvertidamente, aumentar a produção de lactato, o que pode contrariar o efeito estabilizador pretendido [1]. Quando combinadas com monitoramento baseado em sensores e técnicas de dispersão de gás, essas considerações de tampão ajudam a manter condições de processo estáveis e ideais.
Perguntas Frequentes
Como a injeção de gás apoia o controle de pH na produção de carne cultivada?
A injeção de gás desempenha um papel importante em manter os níveis de pH equilibrados durante a produção de carne cultivada. À medida que as células crescem, elas liberam dióxido de carbono (CO₂) como um subproduto da respiração. Este CO₂ pode diminuir o pH do meio de cultura, o que pode prejudicar a saúde das células. Ao introduzir gases como ar, oxigênio ou gases inertes no biorreator, a injeção ajuda a remover o excesso de CO₂. Isso evita que o meio se torne muito ácido e mantém o pH estável.
Manter o meio de cultura dentro da faixa de pH ideal de cerca de 7,1 a 7,4 é crucial para o crescimento saudável das células e produtividade. Quando combinado com sistemas de tamponamento e monitoramento em tempo real usando sensores de pH, a injeção de gás não apenas melhora a eficiência do processo, mas também aumenta a viabilidade celular. É um componente crítico para garantir o sucesso do bioprocessamento de carne cultivada.
O que torna os sensores potenciométricos uma escolha melhor do que os sensores ópticos para monitoramento de pH na produção de carne cultivada?
Os sensores potenciométricos desempenham um papel importante na produção de carne cultivada graças à sua capacidade de fornecer medições de pH em tempo real com alta precisão. Manter níveis adequados de pH é essencial para criar o ambiente certo para o crescimento celular, e esses sensores se destacam em fornecer os dados necessários para alcançar isso. Além disso, eles são relativamente acessíveis e se integram perfeitamente em biorreatores de grande escala, tornando-os ideais para monitoramento contínuo em ambientes industriais.
Além disso, esses sensores são construídos para lidar com os desafios de meios de cultura complexos, oferecendo desempenho confiável mesmo em condições exigentes. No entanto, eles exigem calibração periódica para manter sua precisão.Com sua combinação de precisão, confiabilidade e eficiência de custo, os sensores potenciométricos tornaram-se a escolha ideal para o controle eficaz de pH no bioprocessamento de carne cultivada.
Por que o acúmulo de ácido lático dificulta a manutenção de níveis estáveis de pH?
O acúmulo de ácido lático complica o controle de pH ao aumentar a acidez do ambiente de cultura, fazendo com que o pH caia. Isso pode prejudicar a viabilidade e a produtividade das células, já que a maioria das células precisa de uma faixa de pH cuidadosamente controlada para crescer e funcionar adequadamente.
Gerenciar os níveis de ácido lático é crucial no bioprocessamento de carne cultivada para apoiar o crescimento saudável das células e manter a qualidade do produto. Abordagens como monitoramento de pH em tempo real, o uso de tampões de pH ou ajuste de protocolos de alimentação podem ajudar a estabilizar o ambiente e evitar variações prejudiciais de pH.











