Att producera odlat kött är dyrt, där tillväxtmedier är den största kostnadsdrivaren. Metabolomik, en detaljerad analys av cellulär metabolism, ersätter gissningar med exakta data för att förfina mediesammansättningen. Denna metod identifierar näringsbrister, spårar hur celler använder resurser och belyser avfallsansamlingar som hindrar tillväxt.
Viktiga resultat:
- 40,72% ökning i celldensitet uppnåddes i en studie från 2019 genom att optimera medier för kycklingfibroblaster.
- Metabolomikverktyg identifierade kritiska näringsämnen som glukos, aminosyror och energirelaterade föreningar som behövs för effektiv celltillväxt.
- Justeringar i näringsnivåer (e.g. , kreatin, inosin-5'-monofosfat) förbättrade cellproliferationen samtidigt som avfallet minskades.
Analys av förbrukat medium för att underlätta optimering av odlat köttmedium - Ted O'Neill - ISCCM9
Inledande problem med tillväxtmedium
Forskarteamet stötte på stora hinder med den ursprungliga medieformuleringen för C2C12 muskelceller. Det standardiserade DMEM/F12 mediet kunde helt enkelt inte upprätthålla de celldensiteter eller utbyten som krävdes för storskalig produktion av odlat kött. Cellerna konsumerade näringsämnen mycket snabbare än mediet kunde fylla på, vilket ledde till tidig utarmning av kritiska komponenter och dålig biomassetillväxt. För att lösa dessa problem vände sig teamet till datadrivna strategier för optimering.
Näringsbrister i den ursprungliga formuleringen
En analys av det förbrukade mediet avslöjade några uppenbara näringsbrister. Glukos och specifika aminosyror användes upp i en ohållbar takt. För att producera bara 1 kg av C2C12 muskelceller, krävde cellerna mellan 1 100–1 500 g glukos och 250–275 g aminosyror[2]. Bland dessa var glutamin, glycin och cystin i särskilt hög efterfrågan, vilket begränsade celltillväxt och proliferation.
Den metaboliska profilen avslöjade också ineffektivitet i hur näringsämnen bearbetades. Till exempel var energirelaterade metaboliter som kreatin och inosin-5'-monofosfat nedreglerade, medan metaboliter involverade i membransyntes - såsom fosfoetanolamin och kolin - var uppreglerade[3]. Denna förändring indikerade att cellerna prioriterade omedelbar energikonsumtion över energilagring. Även när näringsämnen var tillgängliga, var deras proportioner långt ifrån optimala för effektiv biomassa produktion. Denna obalans gjorde det tydligt att en mer precis och analytisk metod behövdes.
Varför Metabolomik Valdes
Traditionella försök-och-misstag-metoder kunde ha tagit månader av testning för att identifiera dessa specifika problem. Istället valde teamet metabolomik, en teknik som identifierar och mäter metaboliter i förbrukat medium med anmärkningsvärd precision. Denna metod gav en detaljerad ögonblicksbild av cellulär metabolism i en enda analys[2].
"Tidigare data från metaboliska studier utförda med serum-innehållande media kanske inte direkt kan översättas till serumfria system." – ScienceDirect[2]
Metabolomik visade sig ovärderlig för att upptäcka subtila biokemiska förändringar, särskilt när teamet arbetade med att utveckla serumfria formuleringar. Medan standardbedömningar av tillväxt - som cellräkningar eller livskraftstester - bara kunde erbjuda ytliga insikter, avslöjade metabolomik cellernas djupare metaboliska behov.Detta gjorde det möjligt för teamet att förfina mediesammansättningen baserat på faktiska data snarare än antaganden, vilket banade väg för mer riktade och effektiva förbättringar.
Resultat från Metabolomisk Analys
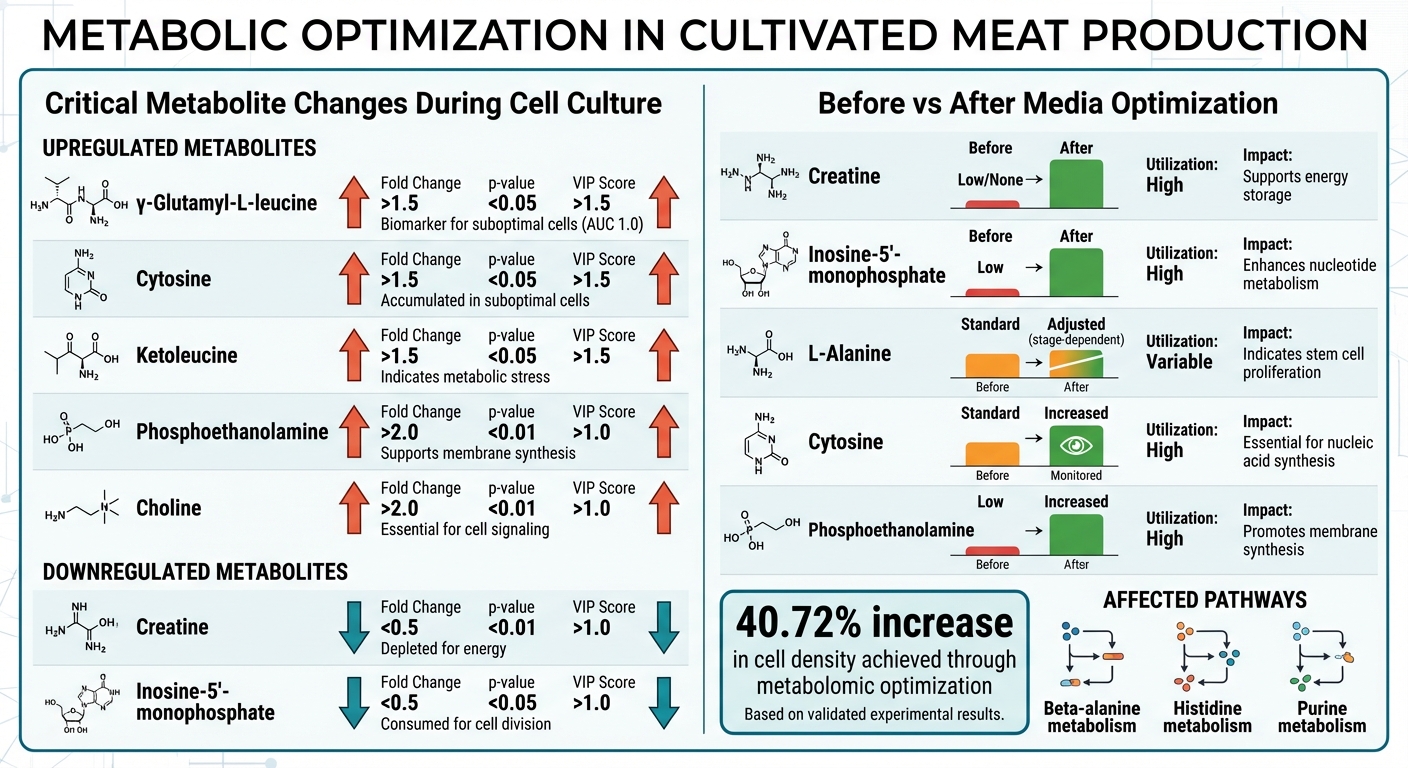
Metabolitförändringar och Näringsoptimering i Odlad Köttproduktion
Metabolitförändringar Under Cellkultur
En detaljerad metabolomisk analys identifierade sju kritiska metaboliter som visade betydande förändringar under odling av gris muskelstamceller. I april 2024 ledde ett team under Doo Yeon Jung vid Seoul National University identifierade γ‑glutamyl‑L‑leucin, cytosin och ketoleucin som viktiga biomarkörer för att känna igen suboptimala celltillstånd [5]. Dessa tre metaboliter uppnådde en AUC på 1,0, vilket visar perfekt noggrannhet i att förutsäga nedgångar i cellproliferation [5].
Studien avslöjade också förändringar i energihanteringen inom cellerna. Metaboliter som fosfoetanolamin och kolin var signifikant uppreglerade, vilket återspeglar den ökade efterfrågan på membransyntes under snabb celldelning [6]. Å andra sidan var kreatin och inosin-5′-monofosfat nedreglerade, vilket indikerar en förskjutning från energilagring mot omedelbar energiförbrukning [6]. Dessa fynd ger en stark grund för vidare undersökning av metaboliska vägar.
Metabolisk Väg Analys
Väganalysen avslöjade ökad aktivitet i tre nyckelsystem: beta-alaninmetabolism, histidinmetabolism och purinmetabolism [5][6]. Var och en av dessa vägar spelar en viktig roll - proteinsyntes, pH-buffring och DNA/RNA-produktion, respektive.Bland dessa utmärkte sig histidinvägen, som visade konsekvent aktivitet under både proliferations- och differentieringsstadierna. Detta tyder på att det kan vara en begränsande faktor i den ursprungliga medieformuleringen [6].
Purins metabolismväg erbjöd ytterligare insikter. En betydande utarmning av nukleotidrelaterade föreningar indikerade att cellerna använde dessa byggstenar snabbare än de kunde återfyllas av odlingsmediet. Detta stöddes ytterligare av ackumuleringen av avfallsmetaboliter som cytosin i senare passager, vilket sammanföll med minskad celltillväxt [5].
Metabolitjämförelsetabell
| Metabolitnamn | Förändringsfaktor | p-värde | VIP-poäng | Status |
|---|---|---|---|---|
| γ‑Glutamyl‑L‑leucine | > 1.5 | < 0.05 | > 1.5 | Uppreglerad (ackumulerad i suboptimala celler) [5] |
| Cytosin | > 1.5 | < 0.05 | > 1.5 | Uppreglerad (ackumulerad i suboptimala celler) [5] |
| Ketoleucin | > 1.5 | < 0.05 | > 1.5 | Uppreglerad (ackumulerad i suboptimala celler) [5] |
| Fosfoetanolamin | > 2.0 | < 0.01 | > 1.0 | Uppreglerad (stöder membransyntes) [6] |
| Kolin | > 2.0 | < 0.01 | > 1.0 | Uppreglerad (väsentlig för cellsignalering) [6] |
| Kreatin | < 0,5 | < 0,01 | > 1,0 | Nedreglerad (uttömd för energi) [6] |
| Inosin-5′-monofosfat | < 0,5 | < 0,05 | > 1,0 | Nedreglerad (konsumerad för celldelning) [6] |
Justeringar av tillväxtmedium
Ändringar av näringskoncentrationer
Forskare vid Seoul National University, ledda av Doo Yeon Jung, använde metabolomisk analys för att finjustera tillväxtmediet för odlad köttproduktion.Genom att undersöka förbrukade medier identifierade de vilka näringsämnen som var uttömda under odlingen och vilka avfallsprodukter som byggdes upp [5]. Detta gjorde det möjligt för dem att justera näringsnivåerna för att bättre matcha cellernas behov.
Teamet fokuserade på tre huvudfaktorer: näringsämnen som cellerna konsumerade snabbt, avfallsprodukter som indikerade metabolisk stress och kostnaden för ingredienser (med målet att ersätta dyra komponenter utan att offra prestanda) [7]. Till exempel modifierades L-alaninnivåerna beroende på celltillväxtens stadium, medan kreatin och inosin-5′-monofosfat ökades för att stödja en övergång från energilagring till direkt energianvändning.
"Övervakning av nivåerna av dessa nyckelmetaboliter i odlingsmedier kan fungera som en kvalitetskontrollåtgärd för produktion av odlat kött genom att möjliggöra indirekt detektion av suboptimala PSC:er." - Doo Yeon Jung, Forskare, Seoul National University [5]
Fosfoetanolamin-nivåerna ökades för att underlätta membransyntes under celldelning, medan cytosinkoncentrationerna noggrant övervakades för att undvika överdriven ansamling [5][6]. Dessa justeringar syftade till att skapa en metabolisk balans där näringsämnen effektivt omvandlades till biomassa, vilket minskade avfall och förbättrade foderomvandlingskvoten [7].
Tabellen nedan belyser de viktigaste förändringarna som gjorts i näringskoncentrationerna och deras inverkan på celltillväxt.
Före och efter jämförelse
| Näringsämne | Initial koncentration | Optimerad koncentration | Användningsgrad | Påverkan på celltillväxt |
|---|---|---|---|---|
| Kreatin | Låg/Ingen | Ökad | Hög | Stödjer energilagring; överensstämmer med konventionella köttegenskaper [6] |
| Inosin‑5′‑monofosfat | Låg | Ökad | Hög | Förbättrar nukleotidmetabolism och energiproduktion [6] |
| L-Alanin | Standard | Justerad (stegberoende) | Variabel | Indikerar stamcellers proliferationskapacitet [5] |
| Cytosin | Standard | Ökad/Övervakad | Hög | Väsentlig för nukleinsyrasyntes under snabb celldelning [5] |
| Fosfoetanolamin | Låg | Ökad | Hög | Främjar membransyntes och cellstrukturens integritet [6] |
Dessa förbättringar adresserade specifika metabola utmaningar, särskilt inom purin-, histidin- och sfingolipidmetabolism [6]. Genom att anpassa näringstillgängligheten för att matcha cellernas konsumtion, minskade teamet avfallet och uppnådde mer konsekvent cellproliferation över flera tillväxtcykler.
sbb-itb-ffee270
Resultat: Förbättrad odlingsprestanda
Celltillväxt och biomassa förbättringar
Den metabolomiska metoden gav tydliga vinster i cellprestanda. En studie från 2025 vid Texas A&M University belyste detta genom att testa två serumfria formuleringar: LM7 (kemiskt definierad) och LM8 (kemiskt odefinierad, innehållande mungbönsproteinisolat). Imponerande nog matchade LM8-formuleringen prestandan hos 20% FBS - en sällsynt prestation i muskelcellkultur [8] . Detta markerade ett stort framsteg, eftersom de flesta serumfria medier kämpar för att ens matcha 10% FBS-prestanda.
Ytterligare studier med C2C12-celler visade att optimering av näringsförhållanden inte bara minskade avfall utan också förbättrade biomassaomvandling [2] [7]. Liknande fördelar observerades i studier av lamm-, C2C12- och grismuskelceller, vilket visar hur allmänt tillämplig denna metabolomikdrivna medieoptimering kan vara.
Skalning av dessa resultat validerades i 3D-mikrobärarsystem, där LM8 visade överlägsen prestanda i skakflasksystem med CellBIND-mikrobärare [8]. Dessutom fann forskning om grismuskelstamceller i april 2024 att celler vid passage 2 (PSC2) hade de högsta tillväxthastigheterna. Däremot visade celler vid passage 3 (PSC3) en betydande förlust av myogena markörgener, vilket gör PSC2 till en pålitlig kvalitetskontrollreferens för skalning av produktion [5]. Dessa framsteg bekräftar inte bara effektiviteten av metabolomikmetoden utan öppnar också dörren för betydande kostnadsbesparingar.
Produktionsskala och kostnadsfördelar
Dessa förbättringar översattes till betydande kostnadsminskningar. Eftersom mediekostnader ofta står för över 60% av produktionskostnaderna, hade elimineringen av dyra animaliska komponenter och finjusteringen av näringstillförseln en meningsfull inverkan [8].
Utöver kostnaderna stärker dessa framsteg det miljölöfte som odlat kött innebär. Med den globala efterfrågan på kött som förväntas öka med cirka 70% till 2050 [8], erbjuder odlat kött ett sätt att minska mark- och vattenanvändning med upp till 90% jämfört med konventionell djuruppfödning [8]. Genom att säkerställa att näringsämnen riktas effektivt mot biomassa produktion, hjälper den metabolomiska metoden att bibehålla denna miljöfördel samtidigt som man undviker avfall orsakat av metaboliska ineffektiviteter.
Hur Cellbase Stödjer Mediaoptimering

Metabolomik-baserad mediaoptimering kräver specialiserade verktyg och material, vilket kan vara utmanande att skaffa.
Plattformen kategoriserar sina erbjudanden för att möta specifika behov:
- Tillväxtmedia & Tillskott: Erbjuder högkvalitativa, serumfria formuleringar.
- Labbutrustning & Instrumentering: Innehåller metabolomikverktyg och analytisk utrustning för analys av förbrukat medium.
- Sensorer & Övervakning: Erbjuder verktyg för att spåra näringsutnyttjandehastigheter, vilket är viktigt eftersom produktionen av 1 kg C2C12-celler förbrukar cirka 250–275 g aminosyror och 1 100–1 500 g glukos [2] .
Det som skiljer
Förutom att tillhandahålla utrustning erbjuder
Slutsats
Metabolomik spelar en nyckelroll i att förfina tillväxtmedier för odlad köttproduktion. Genom att identifiera metaboliska flaskhalsar och näringsluckor kan forskare göra riktade justeringar som avsevärt förbättrar cellprestanda. Till exempel visade en studie från East China University of Science and Technology hur jämförande metabolomisk analys ledde till betydande ökningar i celldensitet och virusproduktion [1].
Genom att använda insikter från metabolomik går analysen av förbrukat medium bortom gissningsarbete.Denna precision gör det möjligt för forskare att skapa medieformuleringar som maximerar cellproliferation samtidigt som de minskar avfall och kostnader.
Fördelarna sträcker sig över olika aspekter av produktionen. Metabolomik hjälper kvalitetskontroll genom biomarkörer som γ-glutamyl-L-leucin och ketoleucin [5]. Det underlättar också övergången från kostsamma, odefinierade serum-baserade formuleringar till prisvärda, serumfria alternativ - kritiskt för att skala upp produktionen. Som framhävs av Good Food Institute:
"Cellkulturmedia är för närvarande den största kostnads- och miljöpåverkansdrivaren för odlad köttproduktion" [7].
Dessa framsteg understryker potentialen hos datadriven medieoptimering att transformera området.
Vanliga frågor
Vad är metabolomik i optimering av tillväxtmedium?
Metabolomik spelar en nyckelroll i att optimera tillväxtmedium genom att analysera de metaboliska profilerna hos celler som används i odlad köttproduktion. Genom att förstå hur dessa celler utnyttjar näringsämnen och deras metaboliska vägar kan forskare utforma serumfria medier som är både mer effektiva och kostnadseffektiva, specifikt anpassade till behoven för odlad köttproduktion.
Vilka metaboliter är de bästa tidiga indikatorerna på dålig tillväxt?
Viktiga metaboliter associerade med dålig tillväxt i odlat kött inkluderar γ-glutamyl-L-leucine, cytosin, och ketoleucin. Dessa biomarkörer fungerar som indikatorer på underpresterande primärceller och belyser metaboliska förändringar som kan påverka cellproliferation.
Hur används data om förbrukat medium för att minska mediekostnader?
Analys av förbrukat medium spelar en nyckelroll i att minska kostnaderna vid produktion av odlat kött. Genom att identifiera näringsämnen som antingen är uttömda eller i överskott, hjälper det till att förfina medieformuleringar för bättre effektivitet. Verktyg som spektroskopi möjliggör övervakning i realtid, vilket minskar avfall och förhindrar överanvändning av kostsamma komponenter. Dessutom ger metabolomik värdefulla insikter som kan stödja återvinning eller återanvändning av medium, vilket ytterligare minskar kostnaderna. Detta riktade tillvägagångssätt säkerställer att resurser används klokt samtidigt som det fortfarande stöder robust, högkvalitativ celltillväxt.











