Skalering af cellelinjer til produktion af dyrket kød afhænger af valget af det rigtige bioreaktorsystem. Omkostningerne varierer betydeligt mellem omrørte-tank, bølge- og fastsengsbioreaktorer på grund af forskelle i kapitalinvestering, driftsudgifter og skalerbarhed. Her er hvad du behøver at vide:
- Omrørte-Tank Bioreaktorer: Bedst til storskalaproduktion med suspensionscellelinjer. De kræver typisk en høj startinvestering, men tilbyder dokumenteret skalerbarhed (op til 25.000 liter). Kontinuerlige perfusionsmetoder kan reducere omkostningerne pr. gram med 45%.
- Bølge Bioreaktorer: Overkommelig startmulighed (50–66% lavere startomkostninger end omrørte-tanksystemer). Ideel til små til mellemstore skalaer, men begrænset ud over 1.000 liter. Forbrugsomkostninger, såsom engangsposer, kan øge de langsigtede udgifter.
- Fastsengsbioreaktorer: Velegnet til adherente celler, der tilbyder stærk omkostningseffektivitet i skala.Høj initial investering, men effektiv til at reducere nedstrøms behandlingsomkostninger.
Hurtig Sammenligning
| Bioreaktortype | Kapitalomkostninger | Omkostning pr. enhed | Skalerbarhed | Bedst til | Begrænsninger |
|---|---|---|---|---|---|
| Omrørt Tank | Høj startinvestering | Højere omkostning pr. enhed | Op til 25.000 liter | Storskala suspension celler | Høje initiale og driftsomkostninger |
| Bølge | Lavere startinvestering end omrørte tanksystemer | Omkostning pr. enhed varierer efter opsætning og skala | Op til 1.000 liter | Pilot-skala, fleksible opsætninger | Høje forbrugsomkostninger, begrænset skala |
| Fast Bed | Højere startomkostninger | Stærk omkostningseffektivitet ved skala | Mindre enheder, høj tæthed | Adherente celler, omkostningseffektivitet | Lange procestider, høje startomkostninger |
Vigtig pointe: Omrørte tank-systemer dominerer storskalaproduktion, mens wave-bioreaktorer er ideelle til tidlige stadier.Faste sengesystemer udmærker sig ved omkostningseffektivitet for adherente cellelinjer. Valget afhænger af produktionsskala, cellelinjens egenskaber og budgetbegrænsninger.
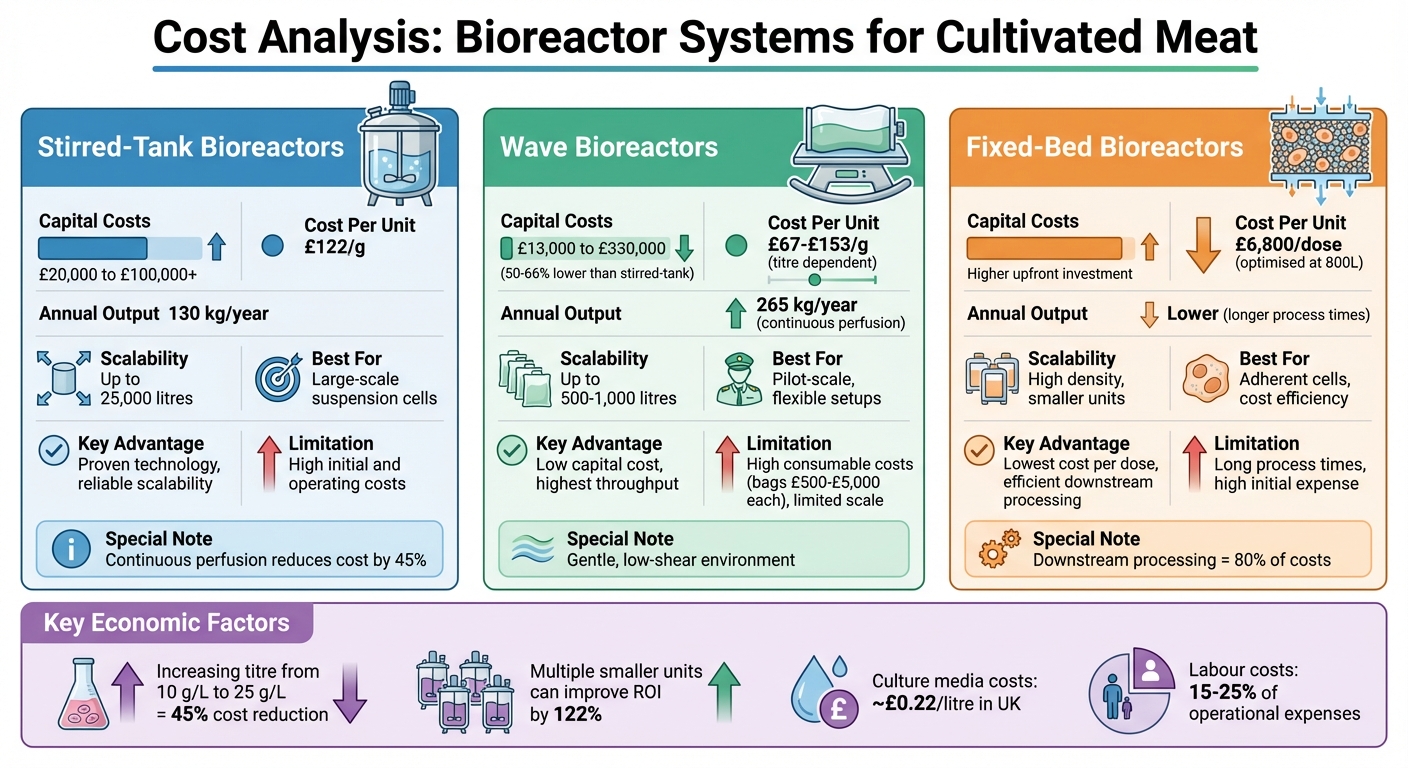
Bioreaktoromkostningssammenligning for dyrket kødproduktion: Kapital, driftsomkostninger og skalerbarhed
1. Omrørte tankbioreaktorer
Kapitalomkostninger
Investering i omrørte tankbioreaktorer er ingen lille bedrift, da omkostningerne stiger betydeligt, når systemerne skaleres op.[8] Valget af materiale spiller en stor rolle her. Rustfrit stål-systemer, som er genanvendelige, har en tendens til at koste 2–3 gange mere end engangsalternativer. Dette skyldes hovedsageligt de ekstra omkostninger ved stålfartøjer og de integrerede Clean-in-Place (CIP) og Sterilise-in-Place (SIP) systemer. [1] Men selve reaktoren er ikke den eneste store udgift.Facilitetsrelaterede omkostninger - såsom renrum, HVAC-systemer, vand til injektion og forsyninger - kan udgøre mere end halvdelen af det samlede projektbudget. [4] I Storbritannien tilføjer opfyldelse af Food Standards Agency krav til fødevaregodkendte faciliteter endnu et lag af omkostninger. Værktøjer som
Driftsomkostninger
Når den indledende investering er foretaget, bliver de daglige driftsomkostninger en nøglefaktor. For omrørte tanksystemer er de største tilbagevendende udgifter vækstmedier, forbrugsvarer og arbejdskraft. I Storbritannien forbliver kulturmedier en bemærkelsesværdig driftsomkostning for disse systemer.[6] Genanvendelige systemer tilbyder en omkostningsfordel her, med driftsomkostninger 20–40% lavere end engangsformater, da der ikke er behov for at blive ved med at købe engangsposer. [1] Omrørte tanksystemer drager også fordel af veletablerede protokoller, som kan reducere mængden af arbejdskraft, der kræves pr. batch sammenlignet med mindre automatiserede opsætninger. Procesintensivering, såsom kontinuerlige perfusionsteknikker, kan betydeligt reducere omkostningerne. For eksempel viser undersøgelser, at kontinuerlige perfusionsprocesser i omrørte tanke kan sænke omkostningen pr. gram med omkring 45% sammenlignet med traditionelle fed-batch metoder, takket være øget produktivitet og reduceret medieforbrug pr. biomasseenhed. [4]
Skalerbarhed
Når det kommer til skalerbarhed, er omrørte tankbioreaktorer guldstandarden. De er tilgængelige i størrelser fra små bænkskala-systemer (1–5 liter) til industrielle enheder, der overstiger 10.000–25.000 liter. [4][7] En omkostningsmodelleringsundersøgelse fandt, at ved 1.000 liter , kan omrørte tanksystemer være mere økonomiske end multi-bakke adherente systemer på en omkostning pr. dosis basis.[3] Intensiverede processer forbedrer yderligere skalerbarheden. For eksempel har kontinuerlige perfusionsprocesser vist sig næsten at fordoble den årlige produktionsudbytte (265 kg sammenlignet med 130 kg) sammenlignet med fed-batch forarbejdning, samtidig med at kapitalomkostningerne reduceres med 32% . [4]
Kompatibilitet med cellelinjer
Omrørte tankbioreaktorer udmærker sig med suspensionsadapterede cellelinjer, der kan håndtere hydrodynamisk skær og trives i godt blandede miljøer ved høje tætheder. [7] Til produktion af dyrket kød inkluderer dette suspensionsadapterede myoblaster, satellitceller eller pluripotente stamceller dyrket i serumfrit medium.Men shear-sensitive cellelinjer kræver mere skånsom omrøring, hvilket kan begrænse iltoverførsel og celletætheder, og i sidste ende øge mediekravene og driftsomkostningerne pr. kilogram biomasse. [7] Anchorage-afhængige cellelinjer kan også dyrkes i omrørte tanke ved hjælp af mikrobærere , men dette tilføjer kompleksitet og øger forbrugsomkostningerne, hvilket gør dem mindre omkostningseffektive sammenlignet med faste sengesystemer. Cellelinjer med hurtige fordoblingstider og høj specifik produktivitet kan reducere reaktorens opholdstider og medieforbrug, hvilket økonomiske modeller gentagne gange fremhæver som nøglefaktorer i at sænke produktionsomkostningerne.[4][7]
2. Wave Bioreactors
Kapitalomkostninger
Wave-bioreaktorer udgør et mere overkommeligt udgangspunkt for producenter af dyrket kød, med startomkostninger, der er cirka 50–66% lavere end dem for genanvendelige omrørte tank-systemer [1]. Denne omkostningsfordel skyldes i høj grad deres enklere mekaniske design - der er ikke behov for komplekse omrørere, drivmotorer eller integrerede rengøringssystemer. I Storbritannien varierer prisen på wave-bioreaktorer meget afhængigt af systemets størrelse og niveauet af automatisering [8]. En anden vigtig faktor, der driver disse besparelser, er brugen af engangsposer, hvilket eliminerer behovet for dyr rengørings- og steriliseringsinfrastruktur. For startups eller forskerhold, der arbejder med stramme budgetter, gør denne lavere indledende investering wave-bioreaktorer til et attraktivt valg for procesudvikling og pilotproduktion.Derudover tillader platforme som
Driftsomkostninger
Når det kommer til driftsomkostninger, fortæller wave-bioreaktorer en anden historie. Forbrugsudgifter, især engangsposer, bidrager til højere langsigtede omkostninger [5]. Det skal dog siges, at wave-systemer tilbyder nogle operationelle fordele. Deres blide vuggende bevægelse bruger mindre energi sammenlignet med den mekaniske omrøring af andre systemer, og de kræver generelt færre kvalificerede medarbejdere til overvågning. Dog betyder de højere omkostninger til forbrugsvarer pr. batch, at de langsigtede driftsomkostninger har tendens til at overstige dem for genanvendelige systemer.
Skalerbarhed
Skalerbarhed er et andet område, hvor wave bioreaktorer skiller sig ud - men med nogle begrænsninger. De fungerer exceptionelt godt i små til mellemstore skalaer, men har svært ved at håndtere mere end 500–1.000 liter, da den vuggende bevægelse bliver ineffektiv ved større volumener. Dette gør wave-systemer ideelle til procesudvikling, pilotproduktion og tidlig produktionsfase, snarere end storskala kommercielle operationer. En modulær "scale-out" tilgang - ved at bruge flere mindre enheder parallelt i stedet for én stor beholder - kan forbedre investeringsafkastet med op til 122% sammenlignet med traditionelle strategier med én stor bioreaktor [2]. Derudover, da downstream-behandling typisk udgør omkring 80% af de samlede produktionsomkostninger [2] , kan deling af downstream-udstyr på tværs af flere enheder føre til yderligere omkostningsreduktioner.Til produktion af dyrket kød understøtter denne skalerbarhedsprofil en distribueret produktionsmodel, hvor flere mindre faciliteter reducerer konstruktionsomkostningerne og forbedrer forsyningskædens modstandsdygtighed.
Kompatibilitet med cellelinjer
Wave-bioreaktorer er særligt velegnede til suspensionstilpassede cellelinjer og semi-adherente kulturer. Deres skånsomme, lav-shear miljø opretholder høj cellelevedygtighed for celletyper som immortaliserede muskelceller, fibroblaster og pluripotente stamceller [3]. Valget af cellelinje kan have en betydelig indvirkning på produktionsomkostningerne; for eksempel kan en stigning i produkttitre fra 10 gram pr. liter til 25 gram pr. liter reducere omkostningerne ved solgte varer med omkring 45% [4]. Den skånsomme blandingshandling af bølgesystemer er især fordelagtig for cellelinjer, der kræver længere kulturperioder, da det reducerer celledamage og begrænser behovet for hyppige medieændringer eller dyre vækstfaktortilskud. Selvom adherente cellelinjer også kan dyrkes i bølge-bioreaktorer ved brug af mikrobærerperler, er faste-seng systemer generelt en mere økonomisk mulighed for disse celletyper.
3. Faste-Seng Bioreaktorer
Kapitalomkostninger
Faste-seng bioreaktorer kræver en betydelig forudgående investering på grund af udgifterne til specialiseret udstyr og engangskar. Et godt eksempel på dette er iCELLis ® systemet, en velkendt faste-seng teknologi. På en klinisk skala på 200 liter var den indledende omkostning pr. dosis høj. Denne faldt ved 800 liter og blev yderligere forbedret efter optimering af produktionsprotokollen [3]. Selvom disse kapitalomkostninger kan virke høje, bliver de mere håndterbare ved større produktionsskalaer, takket være systemets effektivitet i behandlingsgennemstrømning. For producenter af dyrket kød tilbyder platforme som
Driftsomkostninger
På trods af deres højere indledende pris, leverer fixed-bed bioreaktorer den laveste omkostning pr. dosis sammenlignet med andre systemer. For eksempel, ved en 800-liters skala, leverede iCELLis® systemet en lavere omkostning pr. dosis end suspensionsbioreaktorer [3] . Denne omkostningsfordel kommer fra bedre materialeanvendelse og reducerede downstream-behandlingsbehov.I proteinproduktion viste faste senge-systemer lavere omkostninger pr. gram, hvor kontinuerlige faste senge-processer yderligere forbedrede omkostningseffektiviteten [4]. Dog er omkostningerne stærkt afhængige af produktets titer. For eksempel, når titeren steg til 25 gram pr. liter, faldt omkostningerne med omkring 45%. Omvendt, et fald til 10 gram pr. liter øgede omkostningerne pr. gram [4]. Arbejdsomkostninger, som typisk udgør 15–25% af driftsudgifterne i produktion af dyrket kød, reduceres også på grund af de lavere håndteringskrav i faste senge-systemer [1].
Skalerbarhed
Skalerbarhed er et andet område, hvor faste senge-systemer udmærker sig, og tilbyder økonomiske fordele gennem produktivitetsgevinster frem for blot at øge beholderens størrelse.Selvom iCELLis®-systemet producerer færre doser årligt sammenlignet med suspensionsbioreaktorer - på grund af længere procestider og immobilisering efter såning - fremstår det stadig som den mest omkostningseffektive løsning, når det måles på omkostning pr. dosis [3] . Dens høje overfladetæthed muliggør effektiv storskala dyrkning uden behov for enorme beholdere. Derudover kan brugen af flere mindre fastsengsenheder, der deler downstream-udstyr, øge investeringsafkastet med 122% sammenlignet med brugen af en enkelt stor bioreaktor [2]. Denne skalerbarhed understøtter distribuerede produktionsopsætninger, som ikke kun sænker konstruktionsomkostningerne, men også forbedrer forsyningskædens fleksibilitet.
Kompatibilitet med cellelinjer
Fastsengsbioreaktorer er særligt velegnede til adhærente cellelinjer, der kræver en overflade til vækst.Deres packed-bed design skaber et høj-densitetsmiljø, der er ideelt til pattedyrsceller, inklusive primære vs immortaliserede cellelinjer og stamcellelinjer, som er bredt anvendt i dyrket kødproduktion [3] . Det lav-shear miljø inden for bed matrix beskytter celler mod mekanisk skade, hvilket gør disse systemer til et e
sbb-itb-ffee270
Omkostningsdrivere for produktion af dyrket kød
Fordele og Ulemper
Valg af det rigtige bioreaktorsystem indebærer en balance mellem den indledende investering, operationel effektivitet og produktionsomkostninger. Her er et nærmere kig på styrkerne og svaghederne ved forskellige systemer for at hjælpe med beslutningstagning.
Omrørte tankbioreaktorer er en veletableret mulighed med dokumenteret skalerbarhed, hvilket gør dem til et pålideligt valg for mange industrier. Dog er der betydelige udfordringer ved skalering af dyrket kød, der skal adresseres. De kommer dog med de højeste startomkostninger og den stejleste omkostning pr. gram blandt de sammenlignede systemer [4] . Mens deres kontrolparametre er vel forstået, kræver de længere frøfermenteringstog og har en lavere årlig produktionskapacitet (130 kg om året) [4].
Fastbed bioreaktorer skiller sig ud for deres omkostningseffektivitet pr. dosis efter optimering [3] . De udmærker sig i downstream-behandling, en kritisk faktor, da downstream-omkostninger kan udgøre cirka 80% af de samlede produktionsudgifter for højværdiprodukter [2]. På den negative side begrænser deres længere behandlingstider antallet af producerede partier årligt [3].
Wave-bioreaktorer og kontinuerlige perfusionssystemer opnår en balance med et lavere kapitalbehov end nogle alternativer og stærk omkostningseffektivitet pr. gram, samtidig med at de opnår den højeste gennemstrømning (265 kg/år) [4] . Men deres operationelle kompleksitet og følsomhed over for produkttitre kan udgøre udfordringer. For eksempel kan et fald i titre fra 25 g/L til 10 g/L øge omkostningerne pr. gram betydeligt [4].
Valget af bioreaktor afhænger i sidste ende af faktorer som produktionsskala, egenskaberne ved cellelinjen og den opnåelige titre.
Her er en hurtig sammenligning af de vigtigste målepunkter:
| Bioreaktortype | Kapitaludgifter | Omkostning pr. enhed | Årlig gennemstrømning | Primær fordel | Hovedbegrænsning |
|---|---|---|---|---|---|
| Omrørt tank | Højeste kapitalbehov blandt de sammenlignede muligheder | Højere omkostning pr. enhed | 130 kg/år | Pålidelig og skalerbar med gennemprøvet teknologi | Høje kapital- og driftsomkostninger |
| Fast seng | Højere CAPEX | Lave omkostninger pr. dosis efter optimering | Lavere (på grund af længere proces) | Effektiv downstream-behandling, lave dosisomkostninger | Lang processtid, høj initial investering |
| Kontinuerlig perfusion | Lavere kapitalbehov end omrørte tankopsætninger | Lav pris pr. gram | 265 kg/år | Lav pris pr. gram, højeste gennemløb | Kompleks at betjene, følsom over for titerændringer |
Konklusion
Omkostningseffektiviteten af bioreaktorer afhænger i høj grad af produktionsskalaen.Til storskala kommerciel produktion skiller kontinuerlige vs fed-batch systemer sig ud, hvor kontinuerlige perfusionsomrørte tankopsætninger tilbyder lavere produktionsomkostninger pr. gram end fed-batch systemer, sammen med en imponerende årlig produktion på 265 kg [4].
For tidlige stadier af R&D og pilot-skala faciliteter tilbyder wave bioreaktorer en praktisk løsning. Deres lavere startomkostninger og hurtige opsætning gør dem ideelle for start-ups i Storbritannien, der arbejder med begrænsede budgetter. Ligeledes kan optimerede faste sengesystemer reducere omkostninger pr. enhed ved at understøtte høje celletætheder og strømline downstream-behandling [3]. Disse tilgange giver mindre virksomheder mulighed for at minimere finansielle risici, mens de perfektionerer deres cellelinjer og processer.
Ved opskalering kan brugen af flere mindre bioreaktorer betydeligt forbedre afkastet.For eksempel stiger ROI med 122%, når downstream-omkostninger udgør så meget som 80% af de samlede produktionsudgifter [2]. Denne strategi hjælper også med at reducere kapitaludgifter og det samlede anlægsaftryk.
På tværs af alle systemer spiller fremskridt som højere celletætheder, forbedrede titre og kortere procestider en kritisk rolle i at reducere omkostningerne. For eksempel kan en stigning i titren fra 10 g/L til 25 g/L effektivt halvere produktionsomkostningerne [4]. Disse økonomiske overvejelser er vigtige for producenter, der ønsker at vælge det mest passende system til deres behov.
Ofte stillede spørgsmål
Hvad skal jeg overveje, når jeg vælger en bioreaktor til produktion af dyrket kød?
Når du vælger en bioreaktor til produktion af dyrket kød, er der flere nøglefaktorer at overveje.Disse omfatter de specifikke behov for din cellelinje, den tilsigtede produktionsskala, og de tilknyttede omkostninger. Hver type bioreaktor tilbyder varierende niveauer af effektivitet, skalerbarhed og kompatibilitet, så det er essentielt at matche udstyret til dit projekts unikke krav.
Lige så vigtigt er det at skaffe pålideligt udstyr.
Hvad er forskellene i driftsomkostninger mellem omrørte tank-, bølge- og fastsengsbioreaktorer?
Driftsomkostningerne varierer meget mellem omrørte tank-, bølge- og fastsengsbioreaktorer på grund af forskelle i deres design, skalerbarhed og hvordan de bruger ressourcer.Omrørte tankbioreaktorer er almindeligt anvendte og er typisk økonomiske til storskalaproduktion. Dog kræver de ofte højere energiforbrug til omrøring og temperaturvedligeholdelse. Bølgebioreaktorer er derimod lettere at betjene og har tendens til at bruge mindre energi, hvilket gør dem til et godt valg til mindre skala opsætninger eller tidlige udviklingsstadier. Fastbedbioreaktorer, selvom de har højere startomkostninger på grund af specialiserede materialer, kan give effektiv ressourceudnyttelse og lavere vedligeholdelse over tid.
Når man opsætter dyrkningsprocesser, er det afgørende at afveje disse omkostningsovervejelser mod de unikke krav til din cellelinje og produktionsmål. Værktøjer som
Hvad er skalerbarhedsudfordringerne ved bølge-bioreaktorer sammenlignet med andre systemer?
Bølge-bioreaktorer er populære for deres enkle design og overkommelige pris, især i mindre skala operationer. Når det er sagt, kan de støde på forhindringer ved opskalering. Når volumen øges, kan problemer som reduceret blandingseffektivitet og begrænset iltoverførsel opstå. Disse udfordringer kan påvirke cellevækst og den samlede produktivitet, når man overgår til større bioreaktorsystemer.
I tilfælde af produktion af dyrket kød handler valget af det ideelle bioreaktorsystem om at finde den rette balance mellem skalerbarhed, omkostninger og de unikke behov for dine cellelinjer. En grundig evaluering af disse elementer er afgørende for at opnå pålidelig ydeevne ved større produktionsskalaer.











