La estabilidad genética es crítica para la producción de carne cultivada. Sin ella, las líneas celulares pueden mutar, lo que lleva a una calidad inconsistente, riesgos de seguridad y fallos en la producción. Escalar de miles a billones de células amplifica estos riesgos, haciendo que los sistemas de control de calidad robustos sean esenciales. Los reguladores como la FDA y la EMA requieren pruebas de estabilidad antes de aprobar productos, ya que incluso cambios genéticos menores pueden desencadenar resultados alérgicos o perjudiciales.
Los desafíos clave incluyen la deriva genética, la acumulación de mutaciones y la activación de oncogenes. Estos problemas surgen del pasaje celular extendido, las presiones selectivas y los factores de estrés ambiental durante la producción. Métodos avanzados de prueba, como el cariotipado, los arrays de SNP y la secuenciación de nueva generación (NGS), ayudan a detectar y abordar estos riesgos. Estrategias preventivas como la banca estructurada de células y la ingeniería genética dirigida protegen aún más contra la inestabilidad.
Los productores deben integrar el control de calidad en cada etapa de la producción, desde el banco de células hasta los biorreactores a gran escala. Herramientas como el perfilado STR, las pruebas de contaminación y los ensayos funcionales aseguran la consistencia y la seguridad. Plataformas como
Acelerando el Desarrollo de Líneas Celulares desde el ADN hasta el Banco Maestro de Células - AGC Biologics
Desafíos Comunes en el Mantenimiento de la Estabilidad Genética
Asegurar la estabilidad genética a lo largo del ciclo de producción de carne cultivada no es tarea fácil. La magnitud de la producción introduce muchas oportunidades para que se desarrollen y propaguen cambios genéticos. Reconocer estos desafíos es clave para implementar sistemas efectivos de control de calidad.
Deriva genética y acumulación de mutaciones
El paso extendido de células es una fuente importante de inestabilidad genómica en la producción de carne cultivada. Las líneas celulares inmortalizadas, por su naturaleza, son propensas a cambios genómicos, lo que puede llevar a mutaciones espontáneas durante el cultivo a largo plazo [6][5]. A medida que las células pasan por múltiples duplicaciones de población, los errores en la replicación del ADN se acumulan, resultando en poblaciones celulares diversas y, potencialmente, en una pérdida de función. Christopher Frye y Luhong He de BioPharm International destacan este problema:
Se ha observado a menudo que las líneas celulares CHO derivadas clonalmente divergen, convirtiéndose en una población heterogénea durante largos períodos de subcultivo [6].
En entornos industriales, alrededor del 20% de las líneas celulares de producción muestran una considerable heterogeneidad de transgenes a lo largo de generaciones sucesivas [6]. Estas mutaciones pueden ocurrir temprano, durante la replicación del ADN después de la transfección, o debido a errores cuando los genes extranjeros se integran en el genoma del huésped [5].
Las presiones selectivas añaden otra capa de complejidad. Agentes como antibióticos y marcadores metabólicos (e.g. , MTX) utilizados para estabilizar líneas celulares pueden en realidad aumentar las tasas de mutación [6][5]. En algunos casos, cuanto mayor es la concentración de estos agentes, mayor es la tasa de mutación [6]. Los factores de estrés ambiental - como la escasez de nutrientes, condiciones de cultivo subóptimas durante la ampliación y el estrés físico por la expansión - pueden desestabilizar aún más la integridad genética [6][5].
Shuai Wang, Director de Desarrollo de Líneas Celulares en WuXi Biologics, nota:
Es probable que los niveles de mutación cambien durante el pasaje celular debido a la plasticidad genómica de las células de ovario de hámster chino (CHO) [5].
Los cambios epigenéticos también juegan un papel. Los transgenes pueden perderse parcial o completamente o silenciarse durante el proceso de cultivo, afectando la estabilidad a largo plazo. Estas mutaciones acumuladas no solo dañan la función celular, sino que también aumentan el riesgo de activar oncogenes.
Riesgos de Activación de Oncogenes
La activación de oncogenes representa una preocupación crítica de seguridad para los productores de carne cultivada, ya que puede comprometer lotes de producción enteros. La inestabilidad genética puede llevar a la activación de oncogenes a través de mecanismos como la hipermetilación, lo que puede resultar en perfiles similares a tumores [3][1]. La rápida expansión requerida en la producción aumenta aún más la probabilidad de acumular estas mutaciones dañinas [5][6].
Este es un desafío bien reconocido. Según el Consorcio Internacional para la Innovación & Calidad en el Desarrollo Farmacéutico (IQ), el 67% de los encuestados cree que las mutaciones genéticas representan una amenaza mayor que la incorporación errónea de aminoácidos durante la producción [5] . Un caso de mayo de 2024 ilustra la gravedad de este problema: WuXi Biologics descubrió que el 43% de los clones de un programa de desarrollo de líneas celulares portaban la misma mutación puntual genética. ¿La causa raíz? Un nivel de variante del 2.1%–2.2% en el ADN plasmídico utilizado durante la transfección, que no fue detectado por la secuenciación tradicional de Sanger. Para abordar esto, la empresa incorporó la Secuenciación de Nueva Generación (NGS) en sus procesos de control de calidad para detectar tales variantes temprano [5].
La detección temprana de anomalías genéticas es crucial, ya que los cambios oncogénicos pueden comprometer lotes enteros. El cariotipado estándar de bandas G puede identificar subpoblaciones anormales con tan solo un 14% de mosaicismo en veinte metafases celulares [1]. Técnicas más avanzadas como NGS pueden detectar mutaciones genéticas en células clonales con una sensibilidad del 0.5% [5].
El análisis de metilación del ADN es otra herramienta valiosa para evaluar el potencial tumorígeno:
Debido a que los niveles de metilación del ADN y la hipermetilación de ciertos genes ocurren en la iniciación y progresión del cáncer, el análisis de los perfiles de metilación del ADN podría proporcionar información complementaria sobre el potencial tumorígeno de las células [3].
El verdadero desafío radica en implementar sistemas de monitoreo robustos capaces de identificar estos cambios antes de que comprometan la seguridad. Para los productores de carne cultivada, mantener la estabilidad genética durante la rápida expansión celular exige medidas avanzadas de control de calidad. Plataformas especializadas como
Métodos de Pruebas de Control de Calidad
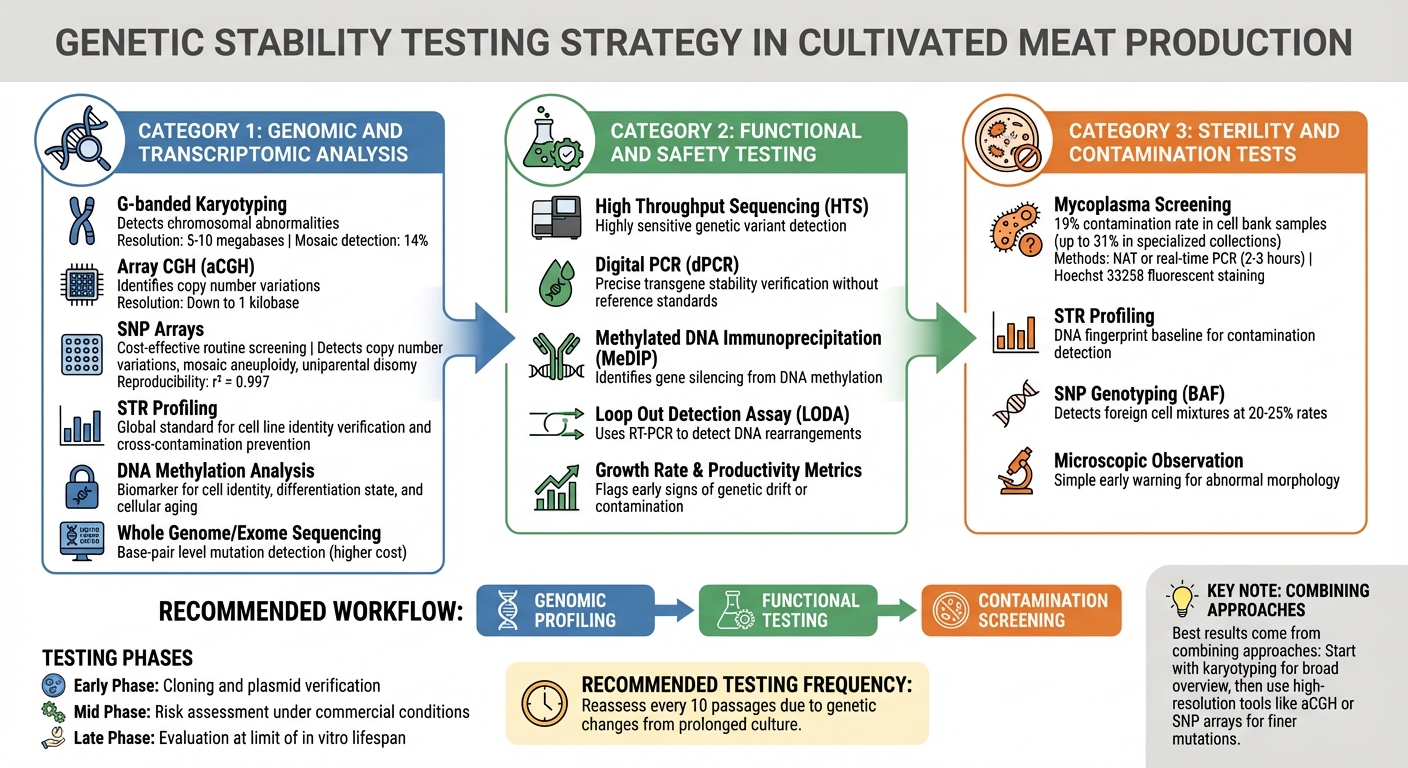
Métodos de Pruebas de Control de Calidad para la Estabilidad Genética en Líneas Celulares de Carne Cultivada
Identificar la inestabilidad genética antes de que impacte la producción requiere una estrategia de pruebas en múltiples capas. Los productores de carne cultivada confían en métodos que detectan desde grandes cambios cromosómicos hasta mutaciones de una sola base. La elección de técnicas depende de los riesgos presentes en cada etapa de producción. Estas herramientas genómicas actúan como el primer punto de control, seguido de evaluaciones funcionales y de contaminación detalladas.
Análisis Genómico y Transcriptómico
El cariotipado en bandas G es una herramienta clave para identificar problemas cromosómicos importantes como anomalías numéricas y grandes reordenamientos estructurales, como translocaciones. Aunque puede detectar niveles de mosaico de alrededor del 14%, su resolución está limitada a cambios de 5–10 megabases, lo que significa que alteraciones más pequeñas podrían pasar desapercibidas [1].
La Hibridación Genómica Comparativa en Array (aCGH) ofrece una mayor resolución, identificando variaciones en el número de copias hasta 1 kilobase. De manera similar, los arrays de Polimorfismo de Nucleótido Único (SNP) proporcionan una opción rentable para el cribado rutinario, detectando variaciones en el número de copias, aneuploidía en mosaico y disomía uniparental. Los estudios de validación han demostrado que los arrays SNP son altamente reproducibles, con mediciones de Frecuencia del Alelo B (BAF) logrando un impresionante r² = 0.997 [8] [1].
Rocío Aguilar-Quesada del Biobanco del Sistema Sanitario Público de Andalucía destaca el valor de combinar métodos:
El cariotipo sigue siendo un ensayo versátil, especialmente cuando se complementa con pruebas de alta resolución [1].
El perfil de Repeticiones Cortas en Tándem (STR) es el estándar global para verificar la identidad de las líneas celulares y prevenir la contaminación cruzada [1] [9]. Mientras tanto, el análisis de metilación del ADN sirve como biomarcador para la identidad celular, el estado de diferenciación y el envejecimiento celular [1]. Para la detección de mutaciones a nivel de pares de bases, la secuenciación del genoma completo o del exoma es una opción, aunque conlleva costos más altos en comparación con los métodos basados en arrays [1].
Los mejores resultados provienen de combinar estos enfoques. Comience con el cariotipado para obtener una visión general amplia, luego use herramientas de alta resolución como aCGH o matrices de SNP para capturar mutaciones más finas. La reevaluación regular, idealmente cada 10 pasajes, es crítica, ya que el cultivo prolongado puede llevar a cambios genéticos [10]. Estos conocimientos genómicos se complementan luego con ensayos funcionales para asegurar un comportamiento celular consistente durante toda la producción.
Pruebas Funcionales y de Seguridad
El perfilado genómico por sí solo no es suficiente. Las pruebas funcionales confirman que las células mantienen sus características previstas durante la expansión. Métricas como las tasas de crecimiento y la productividad pueden señalar signos tempranos de deriva genética o contaminación [9].
La Secuenciación de Alto Rendimiento (HTS) es altamente sensible para detectar variantes genéticas, mientras que la PCR digital (dPCR) verifica con precisión la estabilidad del transgén sin necesidad de estándares de referencia [11] . Christopher Frye y Luhong He de BioPharm International enfatizan la importancia de este paso:
La línea celular de producción es la base de cualquier bioproceso, y por lo tanto, la caracterización genética adecuada de la línea celular de producción es absolutamente crucial para el éxito del desarrollo del proceso [6].
La estabilidad epigenética también es crítica. La Inmunoprecipitación de ADN Metilado (MeDIP) ayuda a identificar la silenciamiento de genes causado por la metilación del ADN, una razón común para la disminución de la productividad [7]. Herramientas como el Ensayo de Detección de Salida de Bucle (LODA) utilizan RT-PCR para detectar reordenamientos de ADN, como cuando un gen de interés es eliminado mientras el marcador seleccionable permanece [7].
Las pruebas deben alinearse con la fase de producción: las pruebas de fase temprana se centran en la clonación y verificación de plásmidos, las pruebas de fase intermedia evalúan riesgos bajo condiciones comerciales, y las pruebas de fase tardía evalúan células al límite de su vida útil in vitro [6]. Comenzar experimentos con células frescas y de bajo pasaje de un banco maestro de células reduce el riesgo de deriva genética [9].
Pruebas de Esterilidad y Contaminación
Las pruebas de contaminación son esenciales para evitar factores que podrían desestabilizar la genética. Mycoplasma es particularmente preocupante, ya que altera el metabolismo y comportamiento celular sin causar cambios visibles en el cultivo [1]. Los estudios revelan contaminación por micoplasma en el 19% de las muestras de bancos de células, con algunas colecciones especializadas mostrando tasas de hasta el 31% [1].
El cribado regular de micoplasma utilizando técnicas sensibles de amplificación de ácidos nucleicos (NAT) o PCR en tiempo real puede proporcionar resultados semicuantitativos en 2–3 horas [1]. La tinción fluorescente Hoechst 33258 es otro método, revelando patrones de fluorescencia extracelular característicos [9].
El perfilado STR establece una huella digital de ADN para las líneas celulares, actuando como una línea base para detectar la contaminación cruzada [9]. Además, la genotipificación SNP utilizando distribuciones de frecuencia de alelo B (BAF) puede identificar la contaminación de otras líneas celulares, detectando mezclas de células extranjeras a tasas del 20–25% [8].
La observación microscópica es una herramienta de advertencia temprana simple pero efectiva, ya que la morfología celular anormal a menudo indica problemas en el cultivo [9]. Implementar un Sistema de Gestión de Calidad, como ISO 9001:2015, junto con Buenas Prácticas de Métodos In Vitro (GIVIMP), ayuda a mantener condiciones de cultivo estandarizadas y reproducibles, reduciendo el riesgo de inestabilidad genómica [10].
Para los productores de carne cultivada que necesitan acceso a equipos y materiales de prueba especializados, plataformas como
sbb-itb-ffee270
Estrategias de Prevención para la Inestabilidad Genética
Detectar la inestabilidad genética es una cosa; prevenirla es otro desafío completamente diferente.Para mantener la estabilidad genética intacta, los productores de carne cultivada necesitan sistemas bien pensados que eviten que las líneas celulares se desvíen antes de que surjan problemas. Dos estrategias clave lideran el camino aquí: banco de células estructurado y ingeniería genética dirigida. Juntas, estas enfoques abordan directamente los riesgos de la deriva genética y la activación de oncogenes.
Banco de Células y Criopreservación
La acumulación de mutaciones es una preocupación real, por lo que un sistema de banco de células confiable es imprescindible. El estándar de la industria implica un sistema de dos niveles: un Banco Maestro de Células (MCB) y un Banco de Células de Trabajo (WCB). Esta configuración asegura un punto de partida consistente para la producción. Limitar el número de pasajes es crucial, ya que cada pasaje aumenta la posibilidad de mutaciones. Al almacenar células en nitrógeno líquido, la actividad biológica se pausa efectivamente, reduciendo el riesgo de cambios genéticos durante el almacenamiento.
En lugar de rastrear el tiempo, la edad celular se mide por duplicaciones de población . Por ejemplo, un biorreactor de producción típico de 5,000 litros implica alrededor de 30 duplicaciones de población[6]. Para mantener la consistencia genética, la fabricación comercial limita este número a entre 45 y 60 duplicaciones[6].
Métodos de detección como RT-PCR y qPCR de célula única pueden detectar problemas temprano, como empalme inusual de ARNm o variabilidad de transgenes. Las líneas celulares que muestran una amplia variabilidad en el número de copias deben ser descartadas para evitar problemas futuros.
El control de calidad es innegociable. Alarmantemente, estudios han encontrado que hasta el 31% de las líneas celulares en algunos bancos estaban contaminadas con micoplasma [3]. Para prevenir esto, se utiliza la tipificación STR para confirmar la autenticidad de las líneas celulares a lo largo del proceso de bancarización.Como destacado por la Investigación y Evidencia de la FSA:
Debido a que las células almacenadas son el material de partida para el producto final, los reguladores podrían requerir altos estándares en el futuro para garantizar un producto cárnico seguro y de alta calidad [2].
Ingeniería Genética para la Estabilidad
La ingeniería genética proporciona otra capa de defensa al mejorar directamente la estabilidad de la línea celular. Técnicas como integración dirigida (TI), particularmente Intercambio de Casete Mediado por Recombinasa (RMCE), permiten la inserción precisa de transgenes en ubicaciones genómicas específicas. Este enfoque evita la imprevisibilidad de la integración aleatoria, donde los efectos de posición y la inestabilidad del número de copias pueden causar estragos. Aunque RMCE en células CHO tiene tasas de eficiencia por debajo del 0.1%[12], los clones resultantes son más predecibles y estables.
La elección del sistema de expresión también importa. Por ejemplo, el sistema de Glutamina Sintetasa (GS) típicamente resulta en alrededor de cinco copias de transgenes por célula, mientras que el sistema de Reductasa de Dihidrofolato (DHFR) puede amplificar el número de copias hasta 1,000[6]. Aunque un mayor número de copias pueda parecer atractivo, aumenta la probabilidad de alteraciones en el ADN, haciendo que los sistemas basados en GS sean una elección más inteligente para la estabilidad a largo plazo.
Para minimizar aún más los riesgos, la mutagénesis específica del sitio y el cribado NGS previo a la transfección son cruciales. Dado que la secuenciación de Sanger tiene un límite de detección más alto, NGS puede detectar mutaciones de plásmidos por debajo del 0.5%, mejorando el éxito del cribado de clones a más del 90%[5].
Shuai Wang y colegas de WuXi Biologics enfatizan la importancia de esta vigilancia:
Dado que la optimización de procesos no puede rectificar mutaciones a nivel genético, monitoree rigurosamente los niveles de mutación en clones estables[5].
Para productores que necesitan herramientas especializadas - ya sea para criopreservación, ingeniería genética o caracterización de líneas celulares -
Integración del Control de Calidad en la Producción
Incorporar el control de calidad en cada fase de producción es crucial. Sin un sistema estructurado, incluso las líneas celulares bien mantenidas pueden experimentar cambios durante la expansión y el aumento de escala. El control de calidad no debe ser una ocurrencia tardía, debe ser una parte central de la producción. Esto comienza en la etapa de escalado, donde los sistemas de gestión estrictos y los entornos controlados juegan un papel clave.
Control de Calidad Durante la Expansión y el Escalado
Como se discutió anteriormente, las pruebas genómicas y de contaminación son vitales, especialmente durante el escalado. Pasar de pequeños volúmenes a miles de litros introduce nuevos riesgos, con cada paso celular aumentando la posibilidad de mutaciones. Un Sistema de Gestión de Calidad (SGC) ayuda a gestionar estos riesgos de manera efectiva. Por ejemplo, entre 2017 y 2022, Josep M. Canals y su equipo en la Universidad de Barcelona implementaron el SGC ISO 9001:2015 para estandarizar los cultivos de células madre pluripotentes humanas. Su análisis retrospectivo de datos de bandeo G y aCGH reveló una reducción significativa en las aberraciones cromosómicas en comparación con las condiciones previas a la adaptación[10][13] . Canals destacó la importancia del monitoreo continuo:
La inestabilidad genética mostrada por las hPSCs en cultivo hace que la reevaluación frecuente de la integridad genómica sea un requisito esencial al planificar su uso para experimentos[10].
El cribado genómico de rutina es imprescindible. Técnicas como el cariotipado por bandas G y aCGH detectan cambios estructurales, mientras que la Secuenciación de Nueva Generación (NGS) identifica mutaciones a niveles por debajo del 0.5%[5]. El análisis de la curva de crecimiento también puede señalar problemas tempranos, como contaminación o deriva genética[9]. El monitoreo ambiental añade otra capa de seguridad, con prácticas como la prueba de placas de sedimentación y controles semestrales de filtros HEPA que aseguran que el entorno de producción permanezca estable y libre de estrés para las líneas celulares [4].
La consistencia en medios y reactivos es igualmente importante. Usar medios definidos sin suero como mTeSR1, junto con reactivos con un Certificado de Análisis, ayuda a reducir la variación entre lotes y limita el riesgo de contaminación viral[10][4]. Las verificaciones regulares de morfología - simples observaciones microscópicas a diferentes densidades de cultivo - pueden detectar signos tempranos de diferenciación o estrés[9]. Para la adquisición de equipos o reactivos especializados, plataformas como
Ensayos Funcionales para la Consistencia del Producto
Mientras que el monitoreo genómico protege el proceso, los ensayos funcionales aseguran que las células funcionen como se espera.La estabilidad genética por sí sola no es suficiente; las células también deben mantener su capacidad de funcionar correctamente a lo largo de los lotes de producción. En la carne cultivada, esto significa confirmar que las células madre, como las células satélite musculares, aún pueden diferenciarse en tejido muscular o adiposo maduro después de la expansión[2] . Los ensayos de diferenciación son esenciales para verificar esto.
Los ensayos metabólicos como MTT, LDH y Resazurina proporcionan información sobre la salud y viabilidad celular[4][9]. Estos, combinados con el perfil de Repeticiones Cortas en Tándem (STR), ayudan a confirmar que las líneas celulares permanecen auténticas y libres de contaminación cruzada durante todo el proceso de producción[1][9].
El análisis transcripcional es otro paso crítico.Xiaoyue Chen y Sam Zhang recomiendan:
Se recomienda la secuenciación de cDNA en lugar de la secuenciación de ADN genómico para la detección de mutaciones y evaluar riesgos a nivel de transcripción[5].
Este método ofrece una imagen más precisa del producto final, ya que refleja cómo se expresan los genes en lugar de solo sus ubicaciones genómicas. Al combinar el cribado genómico con ensayos funcionales, los productores pueden garantizar que cada lote cumpla con estrictos estándares de seguridad, calidad y rendimiento en cada etapa de producción.
Conclusión
Mantener la estabilidad genética es fundamental para producir carne cultivada de manera segura y consistente. Francisco J. Molina-Ruiz y sus colegas del Laboratorio de Células Madre y Medicina Regenerativa destacan los riesgos:
Los cambios genéticos en las hPSCs podrían comprometer no solo la seguridad de los productos celulares basados en hPSC...pero también conducen a una propensión de diferenciación heterogénea del material de partida, perfiles de expresión génica alterados e ineficiencia del producto celular final [10].
Las apuestas son significativas: se han registrado más de 531 líneas celulares mal identificadas por el Comité Internacional de Autenticación de Líneas Celulares [1].
Abordar estos problemas requiere un marco de control de calidad robusto. Esto implica combinar métodos como el perfilado STR, el cariotipado G-banding, aCGH y NGS avanzado [5] , junto con sistemas como ISO 9001:2015 para estandarizar procesos y minimizar anomalías cromosómicas [13].
Factores económicos también impulsan la necesidad de estas medidas.La deriva genética puede resultar en células mutadas que ganan una ventaja de crecimiento, potencialmente arruinando lotes enteros de producción [10][11]. Con el creciente enfoque en las células madre pluripotentes humanas, la demanda de líneas celulares estables nunca ha sido mayor. Como explica el Profesor David L. Kaplan de Tufts University:
Las líneas celulares inmortalizadas generalmente se consideran un requisito para la generación de grandes cantidades de tejido comestible a partir de un bioproceso estable y robusto [14].
Para los productores de carne cultivada, el control de calidad debe estar integrado en cada paso, desde la selección de plásmidos hasta el monitoreo de la producción a gran escala. Al combinar pruebas exhaustivas con estrategias preventivas, los productores pueden asegurar resultados consistentes y confiables.
Preguntas Frecuentes
¿Con qué frecuencia se debe realizar la prueba de estabilidad genética durante la ampliación?
La prueba de estabilidad genética es un paso crucial durante la ampliación y debe realizarse de manera regular. La frecuencia de estas pruebas depende en gran medida de la línea celular específica y del proceso en cuestión. Para reducir las posibilidades de mutaciones y mantener la pluripotencia de las células, es prudente establecer un límite de pasaje informado por el análisis genético.
¿Qué pruebas detectan mejor las pequeñas mutaciones y los cambios cromosómicos grandes?
Pruebas como análisis de matriz SNP y genotipado SNP a nivel del genoma son e
¿Cuál es la forma más sencilla de prevenir la deriva genética en lotes de producción?
Para minimizar la deriva genética, es crucial realizar análisis genéticos y funcionales regulares de las líneas celulares y restringir el número de pasajes que experimentan. Implementar prácticas como establecer bancos de células maestros y verificar rutinariamente la estabilidad genética, como se recomienda en los protocolos de control de calidad. Estas medidas son clave para mantener la consistencia y asegurar resultados confiables en diferentes lotes de producción.











