- Propósito: Asegura que los biorreactores cumplan con los estándares regulatorios y de producción, manteniendo la esterilidad, el control ambiental preciso y la seguridad alimentaria.
- Características Clave: Se eligieron biorreactores de tanque agitado por su idoneidad para células musculares bovinas, ofreciendo fuerzas de cizallamiento controladas y escalabilidad.
- Desafíos: Escalar biorreactores para altas densidades celulares y reducir costos requirió replantear materiales, métodos de esterilización y diseño de procesos.
- Soluciones: Cambiar a materiales de grado alimenticio, usar métodos de esterilización rentables e integrar el aprendizaje automático para la optimización de procesos redujo significativamente los costos.
- Resultados: Los costos de producción se redujeron de £437,000/kg a £1.95/kg, con un aumento de 15 veces en la productividad y hasta un 92% de reducción en las emisiones de gases de efecto invernadero cuando se utiliza energía renovable.
Este estudio describe cómo los protocolos de validación y las elecciones de diseño inteligente están acercando la carne cultivada a la paridad de precios con la carne convencional.
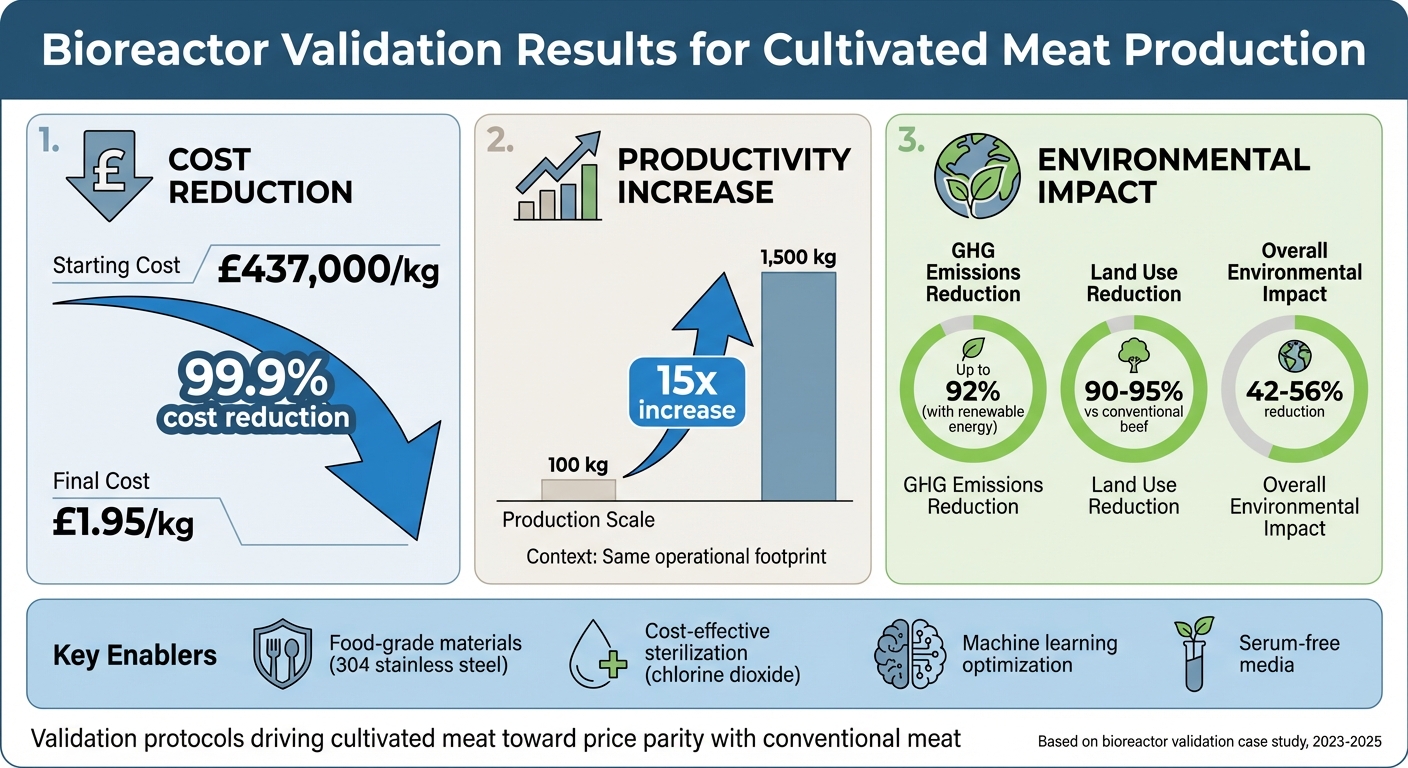
Impacto de la Validación de Biorreactores: Reducción de Costos y Beneficios Ambientales en la Producción de Carne Cultivada
Requisitos Regulatorios para la Validación de Biorreactores
Normas Regulatorias Aplicables
En la industria de la carne cultivada, cumplir con estrictas normas regulatorias es una parte crítica del proceso de validación de biorreactores. En el Reino Unido, la Agencia de Normas Alimentarias (FSA) y Food Standards Scotland (FSS) categorizan la carne cultivada bajo "productos de origen animal" (POAO). Esta clasificación asegura que las regulaciones de seguridad alimentaria e higiene se apliquen en todas las etapas de producción, incluidas las operaciones de biorreactores.Sin embargo, según la guía del Reino Unido (diciembre de 2025), aunque estos productos caen bajo la categoría POAO, no califican legalmente como "carne". Esta distinción significa que ciertos requisitos convencionales de bienestar animal y microbiológicos están excluidos, dando forma a los protocolos específicos de validación necesarios en el Reino Unido.
A nivel mundial, las evaluaciones de seguridad varían en duración. Singapur y los Estados Unidos típicamente completan revisiones dentro de 12 meses, mientras que la Unión Europea promedia alrededor de 18 meses. El Reino Unido ha trazado su propio camino con el Programa Sandbox CCP, financiado hasta febrero de 2027. Esta iniciativa permite a los reguladores colaborar directamente con empresas como Gourmey, Hoxton Farms, y Mosa Meat, simplificando los requisitos de datos y acelerando las evaluaciones de seguridad.
"El programa sandbox nos está permitiendo acelerar el conocimiento regulatorio para reducir las barreras para las tecnologías alimentarias emergentes sin comprometer los estándares de seguridad."
– Dr. Thomas Vincent, Subdirector de Innovación, FSA [3]
Independientemente de la jurisdicción, las empresas deben presentar expedientes de seguridad detallados antes de ingresar al mercado. Estos expedientes describen los procesos de producción, la composición del producto y los datos de seguridad. También deben confirmar que la carne cultivada es nutricionalmente comparable a la carne convencional, incluyendo análisis de macronutrientes y micronutrientes, así como perfiles de aminoácidos y ácidos grasos.
Requisitos del Protocolo de Validación
Los estándares regulatorios exigen protocolos de validación de biorreactores rigurosos para garantizar operaciones seguras y controladas. Un componente clave es la implementación de un plan de Análisis de Peligros y Puntos Críticos de Control (HACCP).Este marco identifica y mitiga riesgos en cada etapa de la producción, desde la biopsia celular inicial hasta la cosecha final de la masa celular. Dada la novedad de la producción de carne cultivada, las evaluaciones de seguridad deben abordar los peligros potenciales a lo largo del proceso.
Los protocolos de validación deben demostrar que los sistemas de biorreactores mantienen condiciones estériles durante los ciclos de producción, previniendo efectivamente la contaminación microbiana. Además, estos protocolos necesitan evaluar si las proteínas en la carne cultivada podrían desencadenar reacciones alérgicas en los consumidores.
"Nuestra nueva guía proporciona claridad para las empresas, ayudándolas a entender y demostrar correctamente a los reguladores de alimentos del Reino Unido cómo sus productos son seguros. Específicamente, esta guía asegura que las empresas hayan evaluado los riesgos alérgicos potenciales y que sean nutricionalmente apropiados antes de que puedan ser autorizados para la venta."
– Dr. Thomas Vincent, Subdirector de Innovación, FSA [2]
En el Reino Unido, la validación se centra en proporcionar suficientes datos para una evaluación científica de riesgos en lugar de otorgar autorización de mercado. Nicolas Morin-Forest, Cofundador & CEO de GOURMEY, destacó esta distinción:
"La validación de Gran Bretaña marca un paso crítico en nuestro viaje regulatorio de nuevos alimentos y confirma que ahora estamos avanzando hacia una evaluación completa de riesgos, acercándonos un paso más a hacer que nuestros productos estén disponibles para los consumidores." [4]
Selección de Biorreactor y Especificaciones del Sistema
Tecnología de Biorreactor Seleccionada
La instalación optó por un biorreactor de tanque agitado, una elección impulsada por su rendimiento confiable con células progenitoras de músculo bovino. Factores clave que influyeron en esta decisión incluyeron las necesidades específicas de las células, la escala de producción deseada y las consideraciones generales de costo.
Las células musculares bovinas, al ser dependientes de anclaje, requieren fuerzas de cizallamiento bajas - por debajo de 0.1 N/m² - para evitar daños durante el cultivo. El diseño de tanque agitado cumplió con este requisito mientras demostraba ser adaptable tanto para experimentos a escala piloto como para producción comercial. El costo fue otro factor importante, con unidades a escala piloto con precios entre £50,000 y £100,000, haciéndolas accesibles para presupuestos típicos en el sector de carne cultivada en lugar de la industria farmacéutica[5][7].
La escala de producción apuntaba a volúmenes entre 100 y 1,000 litros para asegurar la viabilidad comercial.Los sistemas modulares de tanque agitado fueron elegidos sobre las alternativas de lecho empacado debido a su capacidad para escalar por un factor de 10 sin superar los límites de transferencia de masa, manteniendo valores de kLa por encima de 50 h⁻¹. Estos sistemas tienen como objetivo producir 1–10 kg de carne cultivada por lote, equilibrando la inversión de capital en aproximadamente £200 por litro de capacidad [7][8].
Características del Diseño del Sistema
Una vez seleccionado el biorreactor de tanque agitado, su diseño incorporó características avanzadas para fomentar un crecimiento celular óptimo. El sistema de intercambio de gases emplea tecnología de micro-difusores, entregando burbujas entre 20–100 µm. Esta configuración logra valores de kLa de 100–200 h⁻¹ a 37°C, manteniendo niveles de oxígeno disuelto al 30–50% de saturación. Para gestionar la eliminación de CO₂, la aireación del espacio de cabeza se combina con contactores de membrana y sensores antiespumantes[5][6].
Para una mezcla eficiente, el biorreactor utiliza impulsores Rushton duales, operando a velocidades de 50–150 rpm. Esto asegura una mezcla uniforme con tasas de cizallamiento por debajo de 5,000 s⁻¹, protegiendo las células de daños mientras mantiene gradientes de nutrientes por debajo del 10%. La agitación está controlada por PID, con retroalimentación en tiempo real sobre los niveles de pH y oxígeno disuelto, apoyando tasas de perfusión de 1–5 volúmenes de recipiente por día[5][7].
La escalabilidad fue un enfoque clave del diseño. El biorreactor mantiene similitud geométrica a través de diferentes escalas, adhiriéndose a una relación altura-diámetro de 2:1. Impulsores optimizados por CFD aseguran una ampliación lineal, y las pruebas piloto mostraron un 95% de retención en la viabilidad celular al escalar de 10 litros a 200 litros.El diseño modular permite la integración en sistemas de producción más grandes mientras cumple con los estándares de cumplimiento GxP[7] [8].
La tecnología analítica de procesos también está integrada, con espectroscopía Raman para el monitoreo en tiempo real de parámetros críticos como el pH (6.8–7.2) y el lactato (mantenido por debajo de 2 g/L). Modelos predictivos, adaptados de la producción de anticuerpos monoclonales, rastrean los niveles de glucosa con valores de R² superiores a 0.95, asegurando un control preciso del proceso[5] [6][7].
Estas características no solo mejoran el cultivo celular, sino que también cumplen con los rigurosos estándares de validación requeridos por los organismos reguladores del Reino Unido.
Ejecución del Protocolo de Validación
Procedimientos de Validación Principal
Para asegurar la integridad operativa, se llevó a cabo un protocolo de validación exhaustivo, incorporando características de diseño avanzadas. El monitoreo en tiempo real desempeñó un papel clave, con tecnología analítica de procesos (PAT) sensores que rastrean continuamente parámetros críticos como oxígeno disuelto, pH y niveles de CO₂ durante cada ejecución de cultivo[6] . El proceso comenzó con células sembradas a una densidad de 1×10⁵ células/mL, cultivadas durante una semana en un medio que contiene 3 g/L de glucosa. Se empleó espectroscopía Raman para monitorear los niveles de lactato y glucosa a lo largo del proceso[5].
El análisis de esfuerzo cortante confirmó que las fuerzas de agitación se mantuvieron por debajo de 0.1 Pa, que es el límite crítico para las células musculares bovinas. Las pruebas posteriores al estrés demostraron que la viabilidad celular se mantuvo por encima del 90%[6].
Pruebas de esterilidad extendidas a todas las materias primas, con especial atención a los medios de cultivo. Se requirió que los proveedores proporcionaran certificados de análisis, verificados a través de pruebas de terceros, de acuerdo con los estándares de las instalaciones del Reino Unido. El protocolo incluyó inmunoensayos ELISA para detectar endotoxinas de bacterias gramnegativas, junto con citometría de flujo para identificar contaminantes basados en el tamaño, forma y propiedades de fluorescencia de las células[9] .
Métodos de Optimización de Procesos
Una vez confirmada la estabilidad del sistema, los esfuerzos se centraron en refinar el proceso utilizando análisis avanzados. Los algoritmos de aprendizaje automático ajustaron dinámicamente las tasas de flujo de medios y las velocidades de agitación basándose en datos continuos de PAT.Estos modelos, entrenados en conjuntos de datos de diseño de experimentos (DoE), identificaron estrategias de alimentación rentables al correlacionar las mediciones de permitividad con la calidad de la biomasa[6]. Este enfoque fue particularmente efectivo durante la fase de proliferación, donde las tasas de crecimiento consistentes son cruciales para la producción comercial.
La espectroscopía Raman, desarrollada inicialmente para la producción de anticuerpos monoclonales, se adaptó con éxito para aplicaciones de carne cultivada. Su especificidad de analito permitió a la instalación adoptar protocolos de validación establecidos mientras mantenía la precisión necesaria para el monitoreo en tiempo real a lo largo del ciclo de cultivo[5].
Desafíos Técnicos y Soluciones
Problemas de Escalado y Productividad
Escalar biorreactores desde entornos de laboratorio hasta la producción comercial no fue una hazaña menor.La instalación tenía como objetivo producir 10–100 kg de carne cultivada, requiriendo un enorme 10¹²–10¹³ células para lograr este objetivo [11]. Sin embargo, alcanzar altas densidades celulares resultó ser un obstáculo significativo. Aunque los biorreactores de fibra hueca pueden teóricamente alcanzar densidades de 10⁸ a 10⁹ células/mL [13], los diseños de biorreactores convencionales no cumplieron con la producción de carne cultivada.
Matt McNulty, un investigador de GFI, explicó la raíz del problema: "Los biorreactores utilizados en la carne cultivada todavía están en gran medida adaptados de diseños convencionales de alimentos y farmacéuticos. Estos diseños no están específicamente adaptados a las necesidades de producción de carne cultivada y, por lo tanto, generan costos más altos debido a ineficiencias en esta falta de ajuste" [12]. Esta discrepancia entre diseño y propósito requirió un replanteamiento completo del equipo y los procesos.
Soluciones Implementadas y Datos de Rendimiento
Para abordar estos desafíos, la instalación reformuló su equipo y protocolos para alinearse más estrechamente con las demandas específicas de la producción de carne cultivada. Uno de los cambios clave involucró la transición de estándares de grado farmacéutico a grado alimenticio. Por ejemplo, el equipo reemplazó los recipientes de acero inoxidable 316 con alternativas de acero inoxidable 304, que cumplían con los requisitos de seguridad alimentaria mientras reducían significativamente los costos de capital [12]. Además, el proceso tradicional de esterilización en sitio con vapor fue reemplazado por el tratamiento con gas de dióxido de cloro. Este ajuste permitió el uso de recipientes de paredes más delgadas hechos de materiales alternativos, reduciendo aún más los costos [12].
Otra medida de ahorro de costos involucró cambiar de agua de grado farmacéutico a agua de grado alimenticio clasificada como "Generalmente Reconocida como Segura" (GRAS) para la preparación de medios [12]. El equipo también introdujo microportadores y andamios comestibles, que no solo resolvieron problemas de desprendimiento celular, sino que también cumplieron con las regulaciones de seguridad alimentaria [11].
Para optimizar aún más las operaciones, la instalación implementó sistemas de sensores multiplexados. Estos sensores proporcionaron datos de rendimiento en tiempo real, que podrían ser utilizados en aplicaciones de aprendizaje automático para afinar los procesos [12]. Colectivamente, estos cambios tuvieron un impacto dramático en los costos de producción, reduciéndolos de £437,000/kg a solo £1.95/kg [10]. Esta notable reducción de costos destaca cómo alinear los protocolos de producción con los estándares regulatorios puede lograr una escalabilidad comercial sin sacrificar la seguridad o la calidad.
sbb-itb-ffee270
Resultados de Validación e Impacto en la Industria
Resultados de Desempeño Medidos
A través de pruebas rigurosas, el sistema demostró un impresionante salto en productividad. Usando tecnología de biorreactor continuo sin burbujas, la productividad del crecimiento celular aumentó 15 veces, impulsando la producción de 100 kg a 1,500 kg - todo dentro del mismo espacio operativo[16]. Durante la etapa de diferenciación, los ajustes para optimizar la biomasa celular llevaron a un aumento del 128%, lo que redujo significativamente el impacto ambiental general en un 42–56%. La transición del metabolismo de células C2C12 a CHO también jugó un papel importante en la reducción de los impactos ambientales, logrando reducciones de hasta 67% cuando se alimenta con fuentes de energía renovable[14]. Aún más sorprendente, el uso de energía renovable redujo las emisiones de gases de efecto invernadero hasta en un 92% y disminuyó el uso de suelo en un 90–95% en comparación con los métodos tradicionales de producción de carne de res[15] [16] . Estos resultados allanan el camino para una adopción más amplia en toda la industria.
Contribuciones a las Prácticas de la Industria
Los resultados de validación han redefinido los estándares para el diseño de biorreactores y el cumplimiento normativo en la producción de carne cultivada. Al demostrar que los estándares de grado alimenticio pueden reemplazar efectivamente a los de grado farmacéutico sin comprometer la seguridad, el proceso ha introducido una hoja de ruta de ahorro de costos para la industria.Por ejemplo, cambiar de acero inoxidable 316 a 304, combinado con la esterilización con dióxido de cloro y el uso de agua clasificada como GRAS, redujo significativamente los costos de capital mientras se mantenía el cumplimiento.
Más allá de demostrar la viabilidad técnica, estos avances están cambiando los puntos de referencia de la industria. Los modelos económicos sugieren que el procesamiento continuo integrado podría ofrecer un ahorro del 55% en costos de capital y operativos durante una década[1]. Para los equipos de adquisiciones, plataformas como
Conclusión
Principales Hallazgos
Este análisis destaca cómo la producción de carne cultivada puede avanzar hacia el éxito comercial mediante la elección inteligente de equipos y el perfeccionamiento de los protocolos operativos. Optar por materiales de grado alimenticio como el acero inoxidable 304 en lugar del más caro acero inoxidable 316 garantiza seguridad y cumplimiento mientras se reducen costos. El cambio a medios sin suero, como lo validó la Agencia de Alimentos de Singapur con la aprobación de las formulaciones de GOOD Meat a principios de 2023, elimina los desafíos éticos y financieros relacionados con insumos derivados de animales[15].
Escalar la producción con reactores de elevación por aire, particularmente a 260,000 L, ha mostrado potencial para reducir los costos a aproximadamente £10.50/kg. Esto es una mejora significativa en comparación con el costo de £24.50/kg asociado con reactores de tanque agitado más pequeños de 42,000 L[17]. Sin embargo, lograr altas densidades celulares - hasta 2 × 10⁸ células/mL - requiere sistemas de perfusión avanzados para manejar desechos metabólicos como amoníaco y lactato. La optimización de procesos ha demostrado ser esencial para abordar estos desafíos[11]. Para los equipos de adquisiciones, plataformas como
Desarrollos Futuros
Con la eficiencia de costos y el control de procesos validados, el enfoque ahora se desplaza hacia biorreactores de mega escala, que prometen redefinir la economía de producción.El anuncio de GOOD Meat en mayo de 2022 de una instalación con diez biorreactores de 250,000 L, capaces de producir 13,700 toneladas métricas de pollo y carne cultivados anualmente, marca un movimiento significativo de proyectos piloto a producción a escala industrial [11][15]. Esto se alinea con el punto de referencia económico establecido por Patrick G. Negulescu et al. de la Universidad de California, Davis:
"Para ser directamente competitivos con la carne de res, los productos CM, o al menos el costo de producción, deben bajar a un nivel por debajo de $9/kg de carne"[17]
Las proyecciones indican que este objetivo está al alcance, especialmente a medida que los costos de los medios continúan disminuyendo, con objetivos establecidos en menos de £0.20 por litro.
Innovaciones como los microportadores comestibles y los sistemas híbridos, que combinan la expansión y diferenciación celular en un solo recipiente, se espera que simplifiquen los procesos de validación y reduzcan los riesgos de contaminación. Los protocolos descritos en este estudio de caso ofrecen un modelo replicable para las empresas que están ampliando sus operaciones, demostrando que las pruebas rigurosas pueden coexistir con la reducción de costos. A medida que más instalaciones adopten estos métodos validados, la industria de la carne cultivada se acerca a la paridad de precios con la carne tradicional. Junto a esto, el sector ofrece notables beneficios ambientales, incluyendo hasta un 92% de reducción en las emisiones de gases de efecto invernadero cuando se alimenta con fuentes de energía renovable[15].
Resumen de biorreactores: sensores, modelado, escalado y diseño alternativo de reactores
Preguntas Frecuentes
¿Qué evidencia esperan los reguladores en un expediente de validación de biorreactores para carne cultivada?
Los organismos reguladores exigen expedientes de validación de biorreactores para confirmar que los sistemas funcionan dentro de parámetros definidos. Esto implica asegurar un rendimiento de proceso consistente y monitoreo en tiempo real de factores clave como niveles de pH, oxígeno disuelto, y temperatura. Además, las pruebas de esterilidad juegan un papel crucial en la prevención de la contaminación. La adherencia a estándares como ISO 14644-1 y EU GMP Anexo 1 es obligatoria para mantener el control microbiano y sostener prácticas de fabricación estériles.
¿Cómo puede escalarse un biorreactor de tanque agitado sin dañar las células musculares bovinas?
Escalar un biorreactor de tanque agitado para la producción de carne cultivada implica gestionar el estrés de cizallamiento, que puede dañar las células musculares bovinas. Para abordar esto, se utilizan herramientas como la dinámica de fluidos computacional (CFD) y modelos de escala reducida para predecir patrones de flujo. Estos conocimientos guían los ajustes en el diseño del impulsor y las velocidades de agitación, ayudando a reducir el daño celular.
Igualmente importante es asegurar una distribución uniforme de nutrientes y oxígeno. Los sistemas de monitoreo avanzados, combinados con técnicas de mezcla efectivas, son clave para crear condiciones consistentes. Este enfoque ayuda a minimizar el estrés localizado y apoya la salud celular durante la producción a gran escala.
¿Qué cambios de validación para la reducción de costos tienen el mayor impacto en £/kg?
La adopción de biorreactores de un solo uso tiene un efecto notable en la reducción de costos medidos en £/kg. Si bien estos sistemas reducen las inversiones de capital iniciales y los gastos de mano de obra, vienen con costos más altos de consumibles. Además, la introducción de monitoreo en tiempo real y tecnologías de reciclaje de medios mejora la eficiencia operativa. Estos avances no solo optimizan los procesos, sino que también conducen a ahorros de costos a largo plazo.











