Escalar biorreatores para a produção de carne cultivada é complexo, especialmente ao gerenciar tensão de cisalhamento, uma força mecânica que pode danificar células de mamíferos durante a ampliação. Ao contrário das células microbianas, as células de mamíferos são frágeis e sensíveis a forças de turbulência e aeração. Quando a tensão de cisalhamento excede 3 Pa, as células podem se romper, reduzindo a viabilidade e a produtividade.
Para enfrentar esses desafios, os engenheiros confiam em Dinâmica de Fluidos Computacional (CFD) e modelos de escala reduzida para prever e gerenciar a tensão de cisalhamento antes da produção em escala total. A CFD analisa padrões de fluxo, zonas de cisalhamento e eficiência de mistura em biorreatores, enquanto os modelos de escala reduzida validam essas previsões experimentalmente, minimizando riscos durante a ampliação.
Pontos Principais:
- Limites de Tensão de Cisalhamento: Células de mamíferos toleram até 3 Pa; exceder isso danifica as células.
- Ferramentas CFD: Métodos avançados como Simulações de Grandes Vórtices (LES) e simulações de Lattice-Boltzmann (LB-LES) permitem modelagem precisa de fluxo e turbulência.
- Modelos de Escala Reduzida: Estes replicam condições de grandes biorreatores em configurações menores para validar previsões de CFD.
-
Considerações de Design:
- Use impelidores de lâmina inclinada para menor cisalhamento.
- Mantenha comprimentos de vórtices de Kolmogorov acima de 20 μm para evitar danos celulares.
- Mantenha velocidades de ponta do impelidor abaixo de 1,5 m/s.
Ao combinar insights de CFD com validação experimental, as equipes podem otimizar designs de biorreatores para a produção de carne cultivada, garantindo a sobrevivência celular e escalonamento eficiente.
CFD Compass | Melhores Práticas para CFD em Biorreatores
Usando Dinâmica de Fluidos Computacional (CFD) para Modelar o Estresse de Cisalhamento
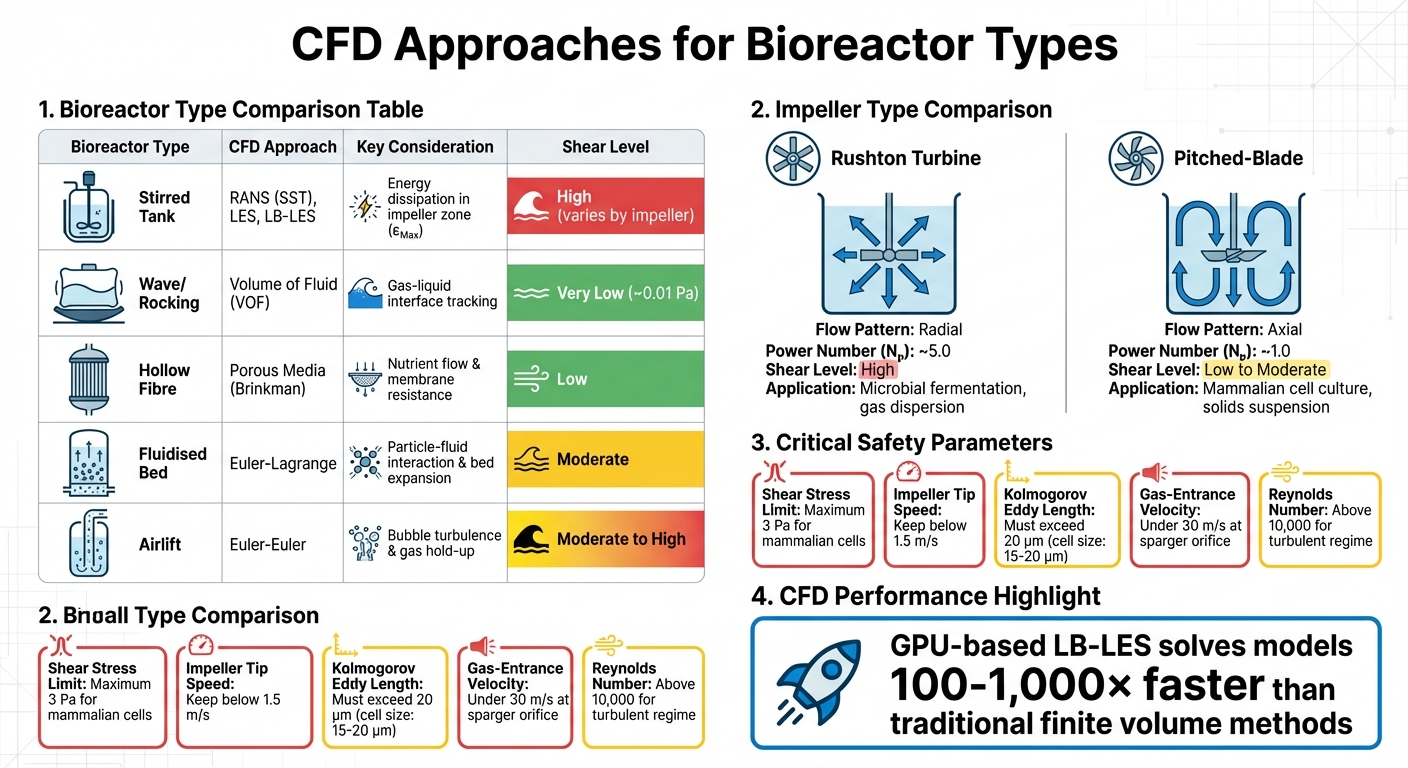
Abordagens de CFD e Parâmetros Chave para Diferentes Tipos de Biorreatores na Produção de Carne Cultivada
Simulações de CFD fornecem aos engenheiros as ferramentas para mapear a dinâmica dos fluidos e as forças de cisalhamento dentro dos biorreatores antes de serem fisicamente construídos. Em vez de depender de métodos de tentativa e erro em escala de produção, o CFD ajuda a prever fatores críticos como zonas de alto cisalhamento, redemoinhos turbulentos e viabilidade celular em partes específicas do vaso. Isso é especialmente importante na produção de carne cultivada, onde as escalas dos biorreatores podem eventualmente atingir 200.000 litros - muito maiores do que os vasos biofarmacêuticos tradicionais [8]. Esses insights preditivos orientam experimentos de escala reduzida e influenciam a seleção de equipamentos.
A evolução das técnicas computacionais tem sido notável. Enquanto os modelos de Reynolds-Averaged Navier-Stokes (RANS), como k-ε, continuam amplamente utilizados na indústria, métodos avançados como Simulações de Grandes Vórtices (LES) e simulações Lattice-Boltzmann com GPU (LB-LES) estão ultrapassando limites. De acordo com o Professor Miroslav Soos da Universidade de Química e Tecnologia de Praga, o LB-LES baseado em GPU pode resolver modelos “100 a 1.000 vezes mais rápido do que os solucionadores de método de volume finito comumente usados” [2]. Essa vantagem de velocidade permite que engenheiros simulem vasos massivos com a precisão necessária para detectar redemoinhos que danificam células.
Um exemplo prático das capacidades do CFD vem de pesquisadores da Regeneron Ireland DAC e Thermo Fisher Scientific. Eles escalaram com sucesso um processo de cultura celular de um biorreator de 2.000 litros para um biorreator descartável de 5.000 litros geometricamente diferente.Em vez de depender de heurísticas empíricas, eles usaram CFD para analisar parâmetros como taxas de transferência de massa, tempos de mistura e taxas de cisalhamento. Essa abordagem permitiu uma ampliação bem-sucedida na primeira tentativa, evitando as falhas custosas frequentemente associadas à escala baseada na razão potência-por-volume [5].
Configurando CFD para Biorreatores de Tanque Agitado
Para configurar CFD para biorreatores de tanque agitado, comece definindo a geometria do vaso - isso inclui as dimensões do tanque, o design do impulsor (e.g., Rushton ou lâmina inclinada) e a colocação dos defletores. Escolher o modelo de turbulência correto é crucial: o modelo k-ε realizável funciona bem para sistemas gás-líquido, enquanto o LB-LES oferece maior resolução para identificar picos de estresse que podem prejudicar as células. Um estudo de convergência de grade garante que os resultados não dependam do tamanho da malha.
As condições de contorno devem refletir os parâmetros operacionais do mundo real, como velocidade do impulsor, taxas de aeração de gás, densidade do fluido e viscosidade. Para aplicações de carne cultivada, modelos conservadores de arrasto de bolhas são frequentemente usados para estimar o estresse de cisalhamento [8]. O sistema deve operar em um regime totalmente turbulento, com números de Reynolds superiores a 10.000 para garantir que o número de potência permaneça consistente, independentemente da velocidade do impulsor [1].
As previsões de CFD para transferência de oxigênio, tempos de mistura e estresse hidrodinâmico devem estar alinhadas com os dados experimentais coletados usando micro-sondas sensíveis ao cisalhamento ou agregados de nanopartículas [2]. Por exemplo, um modelo matemático de transferência de massa guiou a ampliação direta de um processo de cultura de células CHO de uma unidade de bancada de 2 litros para um biorreator industrial de 1.500 litros na Sartorius.Ao usar CFD para prever a demanda de oxigênio e a remoção de CO₂, a equipe manteve atributos consistentes de qualidade do produto - como N-glicanos e variantes de carga - em diferentes escalas [6].
CFD para Outros Tipos de Biorreatores
Enquanto tanques agitados dominam a cultura celular industrial, outros designs de biorreatores requerem abordagens CFD personalizadas. Por exemplo, biorreatores de balanço ou onda dependem do método Volume de Fluido (VOF) para simular a interface gás-líquido, já que o movimento das ondas gera tensão de cisalhamento nesses sistemas. Esses designs criam ambientes de cisalhamento muito mais suaves - a tensão máxima é de cerca de 0,01 Pa em comparação com tanques agitados - mas sua escalabilidade é limitada para a produção de carne cultivada em larga escala [4].
Biorreatores de fibra oca, por outro lado, usam modelos de mídia porosa baseados em equações de Brinkman para simular a difusão de nutrientes e a resistência ao fluxo através de membranas.Sistemas de leito fluidizado requerem modelos de Euler-Lagrange para capturar interações partícula-fluido e expansão do leito, enquanto biorreatores airlift utilizam métodos de Euler-Euler para analisar a turbulência induzida por bolhas e retenção de gás [4]. Cada design apresenta desafios únicos: leitos fluidizados devem equilibrar a distribuição de microcarregadores contra a exposição ao cisalhamento, enquanto sistemas airlift precisam gerenciar tensões causadas por bolhas estourando, uma das principais causas de morte celular em biorreatores com aeração [1] [7].
Compreender essas abordagens de CFD é essencial para controlar o estresse de cisalhamento em diferentes designs de biorreatores usados na produção de carne cultivada.
| Tipo de Biorreator | Abordagem CFD | Consideração Chave |
|---|---|---|
| Tanque Agitado | RANS (SST), LES, LB-LES | Dissipação de energia na zona do impulsor (εMax) |
| Onda/Balanço | Volume de Fluido (VOF) | Rastreamento da interface gás-líquido |
| Fibra Oca | Mídia Porosa (Brinkman) | Fluxo de nutrientes e resistência da membrana |
| Leito Fluidizado | Euler-Lagrange | Interação entre partículas e fluido, expansão do leito |
| Airlift | Euler-Euler | Turbulência de bolhas e retenção de gás |
Esses variados métodos de CFD destacam a necessidade de estratégias personalizadas, que desempenham um papel crítico na seleção de equipamentos e no gerenciamento de tensão de cisalhamento.
Modelos de Redução de Escala e Validação Experimental
Embora a Dinâmica dos Fluidos Computacional (CFD) forneça previsões valiosas, ela não pode substituir a necessidade de testes no mundo real ao aumentar a escala de processos. A validação experimental desempenha um papel crucial em garantir que os modelos computacionais representem com precisão as condições reais de tensão de cisalhamento. É aqui que os modelos de redução de escala entram em ação, imitando o ambiente hidrodinâmico de grandes biorreatores de produção em sistemas menores e mais fáceis de gerenciar. Ao fazer isso, eles reduzem o risco de erros dispendiosos ao passar de operações em pequena escala para escala industrial. Esta etapa não só confirma as previsões do CFD, mas também garante um processo de aumento de escala mais confiável e eficaz.
Criando Modelos de Redução de Escala
O design de um modelo de redução de escala começa com a manutenção da semelhança geométrica.Isso significa manter as mesmas proporções entre componentes-chave, como a altura do vaso em relação ao diâmetro e o diâmetro do impulsor em relação ao diâmetro do tanque [11]. Uma vez que a geometria está alinhada, os engenheiros selecionam um critério de escala. As escolhas comuns incluem potência por volume (P/V), velocidade da ponta do impulsor ou taxa de dissipação de energia (EDR). No entanto, focar na EDR localizada em vez da P/V média proporciona uma melhor compreensão da heterogeneidade de cisalhamento, o que é crítico para uma modelagem precisa.
Uma abordagem mais avançada envolve simuladores de múltiplos compartimentos. Por exemplo, em fevereiro de 2021, Emmanuel Anane e sua equipe desenvolveram um simulador de escala reduzida de dois compartimentos combinando um reator de tanque agitado (STR) e um reator de fluxo pistão (PFR). Este modelo foi usado para estudar como as células CHO respondem aos gradientes de oxigênio dissolvido. Sua pesquisa revelou um limite crítico de tempo de residência de 90 segundos.Além deste ponto, as células CHO mostraram uma queda de 15% na densidade celular viável e um aumento no acúmulo de lactato [10]. Esta descoberta oferece um ponto de referência claro para projetar biorreatores industriais que mantenham a viabilidade celular.
Para proteger o crescimento celular, os engenheiros frequentemente visam manter as velocidades das pontas dos impelidores abaixo de 1,5 m/s [1]. Além disso, o comprimento da microturbulência de Kolmogorov - uma medida de turbulência - deve exceder o tamanho das células, tipicamente 20 μm ou mais para células de mamíferos, para evitar danos hidrodinâmicos [1][3]. Por exemplo, com uma entrada de energia de 0,1 W/kg em culturas de células animais, os menores redemoinhos têm cerca de 60 μm, proporcionando uma margem de segurança [3].
Validação de Previsões de CFD Através de Experimentos
Uma vez que um modelo em escala reduzida está em vigor, métodos experimentais são essenciais para validar os parâmetros derivados de CFD. A Velocimetria por Imagem de Partículas (PIV) é uma técnica amplamente utilizada para esse propósito. Ao rastrear partículas no fluido, a PIV ajuda a confirmar se os padrões de fluxo e os campos de velocidade no modelo em escala reduzida estão alinhados com as previsões de CFD [12][4].
Métodos de injeção de traçadores e descoloração também são usados para validar tempos de mistura. Nesse processo, traçadores como ácidos, bases ou soluções salinas são introduzidos perto do impulsor, e sua distribuição é monitorada até que 95% de homogeneidade seja alcançada [12][3]. Para biorreatores de células de mamíferos em grande escala (5.000 L a 20.000 L), os tempos de mistura geralmente variam de 80 a 180 segundos [10].
Em março de 2020, James Scully e sua equipe na Regeneron Ireland DAC escalaram com sucesso um processo de cultura celular de um biorreator de 2.000 L para um biorreator descartável de 5.000 L com uma geometria diferente. Eles confiaram em CFD para prever parâmetros chave como taxas de transferência de massa, tempos de mistura e taxas de cisalhamento. Essas previsões foram então validadas através de experimentos de fase única e multifásica, permitindo uma primeira tentativa bem-sucedida de escalonamento sem a necessidade de testes piloto em grande escala [5].
"Simulações de CFD estão sendo cada vez mais utilizadas para complementar investigações clássicas de engenharia de processos no laboratório com resultados espacial e temporalmente resolvidos, ou até mesmo substituí-las quando investigações laboratoriais não são possíveis." - Stefan Seidel, Escola de Ciências da Vida, ZHAW [12]
Técnicas adicionais de validação incluem medição de torque para confirmar a entrada de potência específica (P/V) e números de potência adimensionais em velocidades específicas do agitador [12][3]. As taxas de transferência de oxigênio são verificadas usando métodos como as técnicas de desgaseificação ou sulfito, que determinam o coeficiente de transferência de massa de oxigênio volumétrico (kLa) [12][7]. Para sistemas que utilizam microcarregadores, métodos de atenuação de luz ou baseados em câmera são empregados para encontrar a velocidade mínima necessária para suspender todas as partículas, garantindo que as previsões de CFD da distribuição da fase sólida sejam precisas [12][4].
sbb-itb-ffee270
Fatores que Afetam o Estresse de Cisalhamento em Biorreatores
Para proteger a viabilidade celular durante a ampliação, é fundamental entender os fatores físicos que impulsionam o estresse de cisalhamento. As previsões de Dinâmica de Fluidos Computacional (CFD) e as validações em escala reduzida revelam que a taxa de dissipação de energia (EDR) desempenha um papel fundamental. A EDR mede como a energia cinética do impulsor se converte em calor, levando a uma distribuição desigual de energia. Por exemplo, em impulsores de lâminas inclinadas, a energia tende a se concentrar ao redor do impulsor, criando zonas de alto cisalhamento que podem danificar as células se não forem geridas adequadamente.
Design do Impulsor e Entrada de Potência
O tipo de impulsor utilizado influencia significativamente os padrões de fluxo e a intensidade do cisalhamento. As turbinas Rushton, por exemplo, geram fluxo radial e alto cisalhamento, tornando-as ideais para fermentação microbiana, mas menos adequadas para células de mamíferos sensíveis ao cisalhamento.Por outro lado, os impelidores de lâmina inclinada criam fluxo axial com menor cisalhamento e melhor eficiência de bombeamento com a mesma entrada de energia. Isso os torna a escolha preferida para aplicações como a produção de carne cultivada, onde a viabilidade celular é uma prioridade.
| Tipo de Impelidor | Padrão de Fluxo | Número de Potência (Nₚ) | Nível de Cisalhamento | Aplicação Primária |
|---|---|---|---|---|
| Turbina Rushton | Radial | ~5.0 | Alto | Fermantação microbiana; dispersão de gás[3] |
| Lâmina Inclinada | Axial | ~1.0 | Baixo a Moderado | Cultura de células de mamíferos; suspensão de sólidos [3] |
As estratégias de escalonamento muitas vezes dependem de manter uma entrada de potência constante por volume (P/V). No entanto, à medida que o tamanho do reator aumenta, isso pode levar a velocidades de ponta do impelidor mais altas. Para células de mamíferos, as velocidades de ponta devem permanecer abaixo de 1,5 m/s para evitar problemas de crescimento [1]. Em reatores de grande escala, a aeração pode introduzir ainda mais estresse hidrodinâmico do que os impelidores, especialmente em recipientes que excedem 20 m³ [9]. Esses fatores estão intimamente ligados à turbulência, que é explorada mais detalhadamente na discussão sobre a escala de Kolmogorov.
Escala de Kolmogorov e Modelagem de Turbulência
A escala de Kolmogorov (λ) define o tamanho dos menores redemoinhos turbulentos onde a energia se dissipa como calor.Se esses redemoinhos forem menores que o diâmetro da célula, danos mecânicos se tornam uma preocupação. Para células de mamíferos, que são tipicamente de 15–20 μm de tamanho, o comprimento do redemoinho deve exceder 20 μm para evitar danos [1][3]. Por exemplo, com uma entrada de energia de 0,1 W/kg, o diâmetro do redemoinho de Kolmogorov é de cerca de 60 μm, proporcionando uma margem de segurança [3].
"Se entidades biológicas (e.g., células de mamíferos) forem menores que λ [escala de Kolmogorov] em um biorreator, então danos por cisalhamento a tais entidades não ocorrerão." - Muhammad Arshad Chaudhry [3]
Em agosto de 2024, pesquisadores da Boehringer Ingelheim Pharma e da Universidade de Química e Tecnologia de Praga usaram Simulações de Grandes Redemoinhos de Lattice-Boltzmann (LB-LES) para validar previsões de CFD em um biorreator industrial de 12.500 L.Ao usar agregados de nanopartículas sensíveis ao cisalhamento, eles mediram o estresse hidrodinâmico máximo e demonstraram que o LB-LES poderia resolver escalas turbulentas 100–1.000 vezes mais rápido do que os métodos tradicionais [2]. Essas descobertas são fundamentais para desenvolver estratégias para minimizar o estresse de cisalhamento.
Reduzindo o Estresse de Cisalhamento Usando Dados de Modelagem
A modelagem CFD permite que os engenheiros identifiquem zonas de alto cisalhamento e ajustem as condições de operação de acordo. Uma abordagem eficaz é introduzir substratos, bases de pH ou antiespumantes perto da zona do impulsor em vez de na superfície do líquido. Isso garante uma distribuição rápida e minimiza gradientes de concentração localizados [3]. Na produção de carne cultivada, o cisalhamento excessivo pode desprender células dos microcarregadores, enquanto a agitação insuficiente leva ao assentamento dos microcarregadores e desequilíbrios nutricionais [9].
Aditivos protetores como Pluronic F-68 (Poloxamer 188) são comumente usados para proteger as células de forças de cisalhamento, particularmente aquelas causadas pela explosão de bolhas na superfície do líquido - um dos principais contribuintes para a morte celular em biorreatores [1]. Com esses surfactantes, entradas de energia de até 100.000 W/m³ foram relatadas sem efeitos letais [1]. Além disso, manter a velocidade de entrada de gás no orifício do dispersor abaixo de 30 m/s ajuda a reduzir perdas de produtividade e mortalidade celular [1].
Encontrando Equipamentos para Escalonamento de Biorreatores
Como Cellbase Suporta a Aquisição de Biorreatores
Escalonar biorreatores para a produção de carne cultivada traz seus próprios desafios. É aqui que
Ao usar
O dimensionamento bem-sucedido dos biorreatores utilizados na indústria biofarmacêutica desempenha um papel importante na qualidade e no tempo de lançamento desses produtos no mercado [5].
Ao aproveitar os dados respaldados por CFD, as equipes podem otimizar a seleção de equipamentos e minimizar a necessidade de execuções de teste repetidas [5]. Esses insights são cruciais para escolher biorreatores projetados com o gerenciamento ideal de tensão de cisalhamento em mente.
Escolhendo Equipamentos para Controle de Tensão de Cisalhamento
Para controlar a tensão de cisalhamento de forma eficaz, certas especificações de equipamentos são particularmente importantes. A geometria do impulsor é um fator chave. Por exemplo, impulsores de lâmina inclinada geram fluxo axial com um número de potência (Np) de aproximadamente 1,0, enquanto as turbinas Rushton têm um Np muito mais alto, de cerca de 5,0.Isso significa que os designs de lâminas inclinadas produzem significativamente menos potência e, portanto, menos cisalhamento na mesma velocidade de rotação [3]. Para aplicações envolvendo células de mamíferos usadas em carne cultivada, manter a velocidade da ponta do impulsor abaixo de 1,5 m/s é essencial para evitar danos às células [1].
A configuração do sparger é outra consideração crítica. Para evitar cisalhamento excessivo, o equipamento deve garantir que a velocidade de entrada de gás no orifício do sparger permaneça abaixo de 30 m/s, e o número de Reynolds do orifício permaneça abaixo de 2.000. Ultrapassar esses limites pode levar ao "regime de jato", onde as bolhas se dispersam de forma desigual e criam zonas de cisalhamento localizadas [1]. Spargers de furos perfurados ou de tubo aberto são mais adequados para células sensíveis ao cisalhamento em comparação com microspargers. Além disso, o equipamento deve suportar compatibilidade de escala reduzida. Fornecedores que oferecem modelos de bancada (e.g., 3 L systems) que são geometricamente semelhantes a sistemas em larga escala (2.000 L ou mais) permitem que as equipes validem previsões de CFD em uma escala menor antes de passar para a produção em escala total [1][2].
Conclusão
Escalar biorreatores para a produção de carne cultivada requer o abandono dos métodos tradicionais de tentativa e erro e a adoção de estratégias baseadas em modelos para lidar com diferenças de cisalhamento localizadas. A Dinâmica dos Fluidos Computacional (CFD) tornou-se uma ferramenta chave nesse processo, permitindo que engenheiros prevejam ambientes hidrodinâmicos e visualizem zonas de cisalhamento além de simples razões de potência por volume [1]. Ao aderir a parâmetros críticos - como manter comprimentos de vórtices de Kolmogorov acima de 20 μm e velocidades de ponta de impulsor abaixo de 1,5 m/s - os engenheiros podem proteger células de mamíferos de danos por cisalhamento enquanto garantem a mistura adequada e a transferência de oxigênio [1].
Métodos computacionais avançados, como Simulação de Grandes Vórtices (LES) e técnicas de Lattice-Boltzmann, demonstraram sua eficácia na ampliação de processos. Por exemplo, em março de 2020, a Regeneron Ireland DAC escalou com sucesso um processo de cultura celular de um biorreator de 2.000 L para um sistema de uso único de 5.000 L geometricamente distinto na primeira tentativa. Isso foi alcançado usando previsões de CFD multiparâmetro, eliminando a necessidade de extensos testes físicos [5]. Essa estratégia de "acerto na primeira vez" não só reduz os riscos de contaminação, mas também encurta o tempo de lançamento no mercado - crítico para o setor de carne cultivada.
Métodos de validação experimental, como Velocimetria por Imagem de Partículas (PIV), confirmam ainda mais a precisão dos modelos de CFD [2]. Esses modelos validados agora desempenham um papel crucial nas decisões de aquisição.Empresas como
Perguntas Frequentes
Como a Dinâmica de Fluidos Computacional (CFD) apoia a ampliação de biorreatores para a produção de carne cultivada?
A Dinâmica de Fluidos Computacional (CFD) é uma mudança de paradigma quando se trata de ampliar biorreatores para carne cultivada. Ela fornece uma compreensão profunda de dinâmicas de fluxo, tensão de cisalhamento, eficiência de mistura e taxas de transferência de massa - todos fatores críticos para criar o ambiente ideal para o crescimento celular.
Com CFD, os engenheiros podem otimizar elementos essenciais como o design do impulsor, a velocidade de agitação e a dispersão de gás. Isso garante que os biorreatores operem nas melhores condições possíveis, protegendo tanto a saúde celular quanto a produtividade.
Além disso, o CFD possibilita a transição de pequenos setups laboratoriais para grandes biorreatores em escala industrial sem comprometer a eficiência ou a consistência. Isso significa que a produção de carne cultivada pode aumentar de forma suave enquanto mantém altos padrões.
O que torna as Simulações de Grandes Vórtices (LES) melhores do que os métodos tradicionais para modelagem de biorreatores?
As Simulações de Grandes Vórtices (LES) oferecem uma visão mais profunda e precisa do fluxo turbulento dentro dos biorreatores em comparação com métodos tradicionais como Reynolds-averaged Navier-Stokes (RANS).Ao focar em grandes redemoinhos e modelar apenas os menores movimentos dissipativos, o LES pode identificar pontos críticos de tensão de cisalhamento, como zonas de alto cisalhamento induzidas por vórtices, que de outra forma poderiam ser negligenciadas. Este nível de detalhe desempenha um papel fundamental na redução de danos celulares e garante maior confiabilidade ao aumentar a produção de carne cultivada.
Ao contrário de métodos que dependem fortemente de correlações empíricas, o LES oferece capacidades preditivas mais fortes ao passar de biorreatores em escala de laboratório para escala industrial. Avanços em técnicas computacionais também tornaram o LES mais acessível, permitindo simulações detalhadas sem a necessidade de recursos computacionais proibitivos. Para empresas que buscam integrar designs orientados por LES,
Por que é importante manter os comprimentos de vórtices de Kolmogorov acima de 20 µm para a viabilidade de células de mamíferos?
Manter os comprimentos de vórtices de Kolmogorov acima de aproximadamente 20 µm é crucial para proteger as células de mamíferos durante as operações de biorreatores. Quando esses vórtices turbulentos diminuem para um tamanho menor que o das células, podem expor as células a um estresse de cisalhamento excessivo, o que pode danificar suas membranas e reduzir a viabilidade celular.
Manter as menores estruturas turbulentas maiores que as células ajuda a reduzir as chances de danos mecânicos. Isso não apenas promove culturas celulares mais saudáveis, mas também melhora o desempenho geral do biorreator. Essa consideração torna-se ainda mais importante durante a ampliação do biorreator, onde garantir condições consistentes de estresse de cisalhamento é notavelmente mais difícil.











