Genetisk stabilitet är avgörande för produktion av odlat kött. Utan den kan cellinjer mutera, vilket leder till inkonsekvent kvalitet, säkerhetsrisker och produktionsmisslyckanden. Att skala från tusentals till biljoner celler förstärker dessa risker, vilket gör robusta kvalitetskontrollsystem nödvändiga. Regulatorer som FDA och EMA kräver bevis på stabilitet innan produkter godkänns, eftersom även små genetiska förändringar kan utlösa allergiska eller skadliga effekter.
Viktiga utmaningar inkluderar genetisk drift, ackumulering av mutationer och aktivering av onkogener. Dessa problem uppstår från förlängd cellpassage, selektionstryck och miljöstressorer under produktionen. Avancerade testmetoder, såsom karyotypering, SNP-arrayer och nästa generations sekvensering (NGS), hjälper till att upptäcka och hantera dessa risker. Förebyggande strategier som strukturerad cellbankning och riktad genetisk ingenjörskonst skyddar ytterligare mot instabilitet.
Producenter måste integrera kvalitetskontroll i varje steg av produktionen - från cellbankning till storskaliga bioreaktorer. Verktyg som STR-profilering, kontamineringstester och funktionella tester säkerställer konsekvens och säkerhet. Plattformar som
Påskynda cellinjeutveckling från DNA till Master Cell Bank - AGC Biologics
Vanliga utmaningar i att upprätthålla genetisk stabilitet
Att säkerställa genetisk stabilitet genom hela produktionscykeln av odlat kött är ingen liten bedrift. Den stora produktionsskalan introducerar många möjligheter för genetiska förändringar att utvecklas och spridas. Att känna igen dessa utmaningar är nyckeln till att införa effektiva kvalitetskontrollsystem.
Genetisk drift och mutationsackumulering
Förlängd cellpassage är en stor källa till genomisk instabilitet i produktionen av odlat kött. Immortaliserade cellinjer är av sin natur benägna till genomiska förändringar, vilket kan leda till spontana mutationer under långvarig odling [6][5]. När celler genomgår flera populationer av fördubblingar, byggs fel i DNA-replikation upp, vilket resulterar i olika cellpopulationer och, potentiellt, en förlust av funktion. Christopher Frye och Luhong He från BioPharm International belyser detta problem:
Klonalt härledda CHO-cellinjer har ofta observerats divergera och bli en heterogen population över långa perioder av subkultivering [6].
I industriella miljöer visar cirka 20% av produktionscellinjer betydande transgen heterogenitet över successiva generationer [6]. Dessa mutationer kan uppstå tidigt, under DNA-replikation efter transfektion, eller på grund av fel när främmande gener integreras i värdgenomet [5].
Selektiva tryck lägger till ytterligare ett lager av komplexitet. Medel som antibiotika och metaboliska markörer (e.g. , MTX) som används för att stabilisera cellinjer kan faktiskt öka mutationsfrekvenser [6][5]. I vissa fall, ju högre koncentration av dessa medel, desto högre mutationsfrekvens [6]. Miljöbelastningar - såsom näringsbrist, suboptimala odlingsförhållanden under uppskalning och fysisk stress från expansion - kan ytterligare destabilisera genetisk integritet [6][5].
Shuai Wang, chef för cellinjeutveckling på WuXi Biologics, noterar:
Mutationsnivåer kan förändras över cellpassagering på grund av kinesiska hamsteräggstockscellers (CHO) genomiska plasticitet [5].
Epigenetiska förändringar spelar också en roll. Transgener kan delvis eller helt förloras eller tystas under odlingsprocessen, vilket påverkar långsiktig stabilitet. Dessa ackumulerade mutationer skadar inte bara cellfunktionen utan ökar också risken för att aktivera onkogener.
Risker för onkogenaktivering
Onkogenaktivering utgör en kritisk säkerhetsfråga för odlade köttproducenter, eftersom det kan äventyra hela produktionssatser. Genetisk instabilitet kan leda till onkogenaktivering genom mekanismer som hypermetylering, vilket kan resultera i tumörliknande profiler [3][1]. Den snabba expansionen som krävs i produktionen ökar ytterligare sannolikheten för att ackumulera dessa skadliga mutationer [5][6].
Detta är en välkänd utmaning. Enligt International Consortium for Innovation & Quality in Pharmaceutical Development (IQ) anser 67% av de tillfrågade att genetiska mutationer utgör ett större hot än felinkorporering av aminosyror under produktionen [5] . Ett fall från maj 2024 illustrerar allvaret i denna fråga: WuXi Biologics upptäckte att 43% av klonerna från ett cellinjeutvecklingsprogram bar på samma genetiska punktmutation. Grundorsaken? En variantnivå på 2,1%–2,2% i plasmid-DNA:t som användes under transfektion, vilket inte upptäcktes av traditionell Sanger-sekvensering. För att åtgärda detta inkluderade företaget Next-Generation Sequencing (NGS) i sina kvalitetskontrollprocesser för att fånga sådana varianter tidigt [5].
Tidig upptäckt av genetiska avvikelser är avgörande, eftersom onkogeniska förändringar kan kompromettera hela partier. Standard G-band karyotypering kan identifiera onormala subpopulationer med så lite som 14% mosaikism i tjugo cellmetafaser [1]. Mer avancerade tekniker som NGS kan upptäcka genetiska mutationer i klonala celler med en känslighet på 0,5% [5].
DNA-metyleringsanalys är ett annat värdefullt verktyg för att bedöma tumörigen potential:
Eftersom DNA-metyleringsnivåer och hypermetylering av vissa gener förekommer vid cancerinitiering och progression, kan analysen av DNA-metyleringsprofiler ge kompletterande information om cellernas tumörigen potential [3].
Den verkliga utmaningen ligger i att implementera robusta övervakningssystem som kan identifiera dessa förändringar innan de komprometterar säkerheten. För odlade köttproducenter kräver upprätthållande av genetisk stabilitet under snabb cellexpansion avancerade kvalitetskontrollåtgärder. Specialiserade plattformar som
Kvalitetskontrolltestmetoder
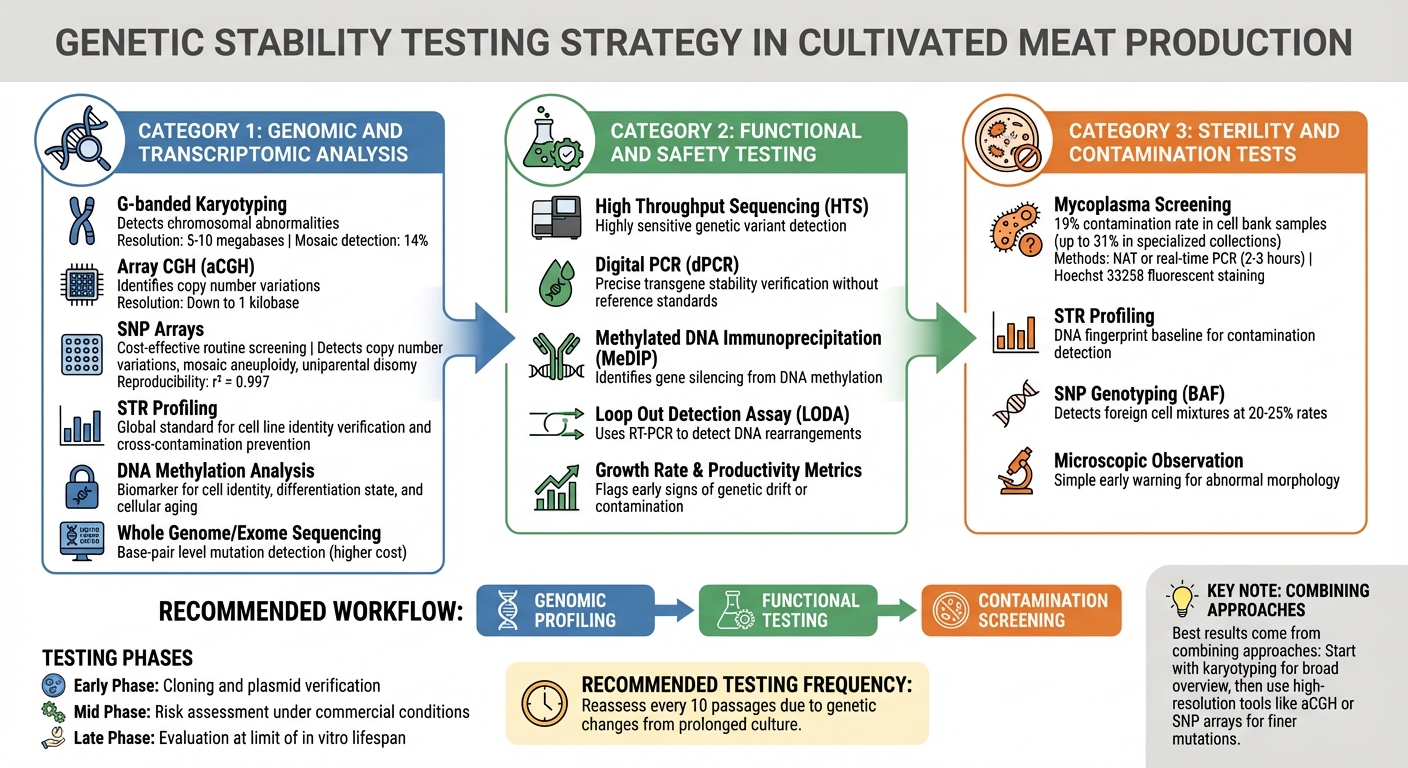
Kvalitetskontrolltestmetoder för genetisk stabilitet i odlade köttcellinjer
Att identifiera genetisk instabilitet innan det påverkar produktionen kräver en flerskikts teststrategi. Odlade köttproducenter förlitar sig på metoder som upptäcker allt från stora kromosomförändringar till enskilda basmutationer. Valet av tekniker beror på de risker som finns i varje produktionsstadium. Dessa genomiska verktyg fungerar som den första kontrollpunkten, följt av detaljerade funktionella och kontaminationsbedömningar.
Genomisk och transkriptomisk analys
G-bandskaryotypering är ett viktigt verktyg för att identifiera större kromosomproblem som numeriska avvikelser och stora strukturella omarrangemang, såsom translokationer. Även om det kan upptäcka mosaiknivåer på omkring 14%, är dess upplösning begränsad till förändringar på 5–10 megabaser, vilket innebär att mindre förändringar kan gå obemärkta förbi [1].
Array-komparativ genomisk hybridisering (aCGH) erbjuder högre upplösning och identifierar kopietalsvariationer ner till 1 kilobas. På liknande sätt ger Single Nucleotide Polymorphism (SNP) arrays ett kostnadseffektivt alternativ för rutinmässig screening, som upptäcker kopietalsvariationer, mosaikaneuploidy och uniparental disomi. Valideringsstudier har visat att SNP-arrayer är mycket reproducerbara, med B Allele Frequency (BAF)-mätningar som uppnår ett imponerande r² = 0.997 [8] [1].
Rocio Aguilar-Quesada från Andalusian Public Health System Biobank betonar värdet av att kombinera metoder:
Karyotypering förblir en mångsidig analys, särskilt när den kompletteras med högupplöst testning [1].
Short Tandem Repeat (STR) profilering är den globala standarden för att verifiera cellinjeidentitet och förhindra korskontaminering [1] [9]. Samtidigt fungerar DNA-metyleringsanalys som en biomarkör för cellidentitet, differentieringsstatus och cellulärt åldrande [1]. För detektion av mutationer på basparsnivå är helgenom- eller exomsekvensering ett alternativ, även om det medför högre kostnader jämfört med array-baserade metoder [1].
De bästa resultaten uppnås genom att kombinera dessa metoder. Börja med karyotypering för en bred översikt, använd sedan högupplösta verktyg som aCGH eller SNP-arrayer för att fånga finare mutationer. Regelbunden omvärdering - helst var 10:e passage - är kritisk, eftersom långvarig odling kan leda till genetiska förändringar [10]. Dessa genomiska insikter kompletteras sedan med funktionella tester för att säkerställa konsekvent cellbeteende under hela produktionen.
Funktionell och säkerhetstestning
Genomisk profilering är inte tillräcklig. Funktionella tester bekräftar att cellerna behåller sina avsedda egenskaper under expansion. Mätvärden som tillväxthastigheter och produktivitet kan flagga tidiga tecken på genetisk drift eller kontaminering [9].
Hög genomströmning sekvensering (HTS) är mycket känslig för att upptäcka genetiska varianter, medan digital PCR (dPCR) exakt verifierar transgen stabilitet utan att behöva referensstandarder [11] . Christopher Frye och Luhong He från BioPharm International betonar vikten av detta steg:
Produktionscellinjen är grunden för varje bioprocess, och därför är lämplig genetisk karakterisering av produktionscellinjen absolut avgörande för framgången med processutveckling [6].
Epigenetisk stabilitet är också kritisk. Metylerad DNA-immunoprecipitation (MeDIP) hjälper till att identifiera gensilencing orsakad av DNA-metylering, en vanlig orsak till produktivitetsminskning [7]. Verktyg som Loop Out Detection Assay (LODA) använder RT-PCR för att upptäcka DNA-omarrangemang, såsom när en intressant gen raderas medan den selekterbara markören förblir [7].
Testning bör anpassas till produktionsfasen: tidiga fas-tester fokuserar på kloning och plasmidverifiering, mellanfas-tester bedömer risker under kommersiella förhållanden, och sena fas-tester utvärderar celler vid gränsen för deras in vitro-livslängd [6]. Att starta experiment med färska, lågt passageceller från en huvudcellbank minskar risken för genetisk drift [9].
Sterilitets- och Kontamineringstester
Kontamineringstestning är avgörande för att undvika faktorer som kan destabilisera genetiken. Mykoplasma är särskilt oroande, eftersom det förändrar cellmetabolism och beteende utan att orsaka synliga förändringar i kulturen [1]. Studier visar att mykoplasmakontaminering förekommer i 19% av cellbankproverna, med vissa specialiserade samlingar som visar frekvenser så höga som 31% [1].
Regelbunden mykoplasmascreening med känsliga Nukleinsyraamplifikationstekniker (NAT) eller realtids-PCR kan ge semikvantitativa resultat inom 2–3 timmar [1]. Hoechst 33258 fluorescerande färgning är en annan metod, som avslöjar karakteristiska extracellulära fluorescensmönster [9].
STR-profilering etablerar ett DNA-fingeravtryck för cellinjer, vilket fungerar som en baslinje för att upptäcka korskontaminering [9]. Dessutom kan SNP-genotypning med B Allele Frequency (BAF)-fördelningar identifiera kontaminering från andra cellinjer, och upptäcka främmande cellblandningar vid frekvenser på 20–25% [8].
Mikroskopisk observation är ett enkelt men effektivt tidigt varningsverktyg, eftersom onormal cellmorfologi ofta signalerar kulturproblem [9]. Implementering av ett kvalitetsledningssystem, såsom ISO 9001:2015, tillsammans med Good In Vitro Method Practices (GIVIMP), hjälper till att upprätthålla standardiserade och reproducerbara kulturförhållanden, vilket minskar risken för genomisk instabilitet [10].
För odlade köttproducenter som behöver tillgång till specialiserad testutrustning och material, erbjuder plattformar som
sbb-itb-ffee270
Förebyggande strategier för genetisk instabilitet
Att upptäcka genetisk instabilitet är en sak; att förebygga det är en helt annan utmaning.För att hålla genetisk stabilitet intakt behöver producenter av odlat kött väl genomtänkta system som förhindrar att cellinjer driver innan problem uppstår. Två nyckelstrategier leder vägen här: strukturerad cellbankning och riktad genetisk ingenjörskonst. Tillsammans hanterar dessa metoder direkt riskerna med genetisk drift och aktivering av onkogener.
Cellbankning och kryokonservering
Mutation ackumulering är en verklig oro, så ett pålitligt cellbankningssystem är ett måste. Branschstandarden involverar ett tvånivåsystem: en Master Cell Bank (MCB) och en Working Cell Bank (WCB). Denna uppsättning säkerställer en konsekvent startpunkt för produktion. Att begränsa antalet passager är avgörande, eftersom varje passage ökar risken för mutationer. Genom att lagra celler i flytande kväve pausas biologisk aktivitet effektivt, vilket minskar risken för genetiska förändringar under lagring.
Istället för att spåra tid mäts cellålder genom populationens fördubblingar . Till exempel involverar en typisk 5 000-liters produktionsbioreaktor omkring 30 populationens fördubblingar[6]. För att bibehålla genetisk konsistens begränsar kommersiell tillverkning detta antal till mellan 45 och 60 fördubblingar[6].
Screeningsmetoder som RT-PCR och single-cell qPCR kan upptäcka problem tidigt, såsom ovanlig mRNA-splitsning eller transgenvariabilitet. Cellinjer som visar stor variabilitet i kopieantal bör kasseras för att undvika framtida problem.
Kvalitetskontroll är icke-förhandlingsbart. Alarmerande nog har studier funnit att upp till 31% av cellinjer i vissa banker var kontaminerade med mykoplasma [3]. För att förhindra detta används STR-profilering för att bekräfta äktheten av cellinjer genom hela bankprocessen.Som framhävs av FSA Research and Evidence:
Eftersom de bankade cellerna är utgångsmaterialet för den slutliga produkten, kan höga standarder krävas av tillsynsmyndigheter i framtiden för att säkerställa en säker köttprodukt av hög kvalitet [2].
Genetisk Ingenjörskonst för Stabilitet
Genetisk ingenjörskonst ger ett ytterligare försvarslager genom att direkt förbättra cellinjestabiliteten. Tekniker som riktad integration (TI), särskilt Rekombinas-Medierad Kassettutbyte (RMCE), tillåter exakt insättning av transgener i specifika genomiska platser. Denna metod undviker oförutsägbarheten hos slumpmässig integration, där positionseffekter och kopienummerinstabilitet kan orsaka kaos. Även om RMCE i CHO-celler har effektivitetsgrader under 0,1%[12], är de resulterande klonerna mer förutsägbara och stabila.
Valet av uttryckssystem är också viktigt. Till exempel resulterar Glutamin Syntetas (GS)-systemet vanligtvis i cirka fem transgenkopior per cell, medan Dihydrofolat Reduktas (DHFR)-systemet kan förstärka kopieantalet upp till 1 000[6]. Även om högre kopieantal kan låta lockande, ökar de sannolikheten för DNA-förändringar, vilket gör GS-baserade system till ett smartare val för långsiktig stabilitet.
För att ytterligare minimera riskerna är plats-specifik mutagenes och pre-transfektion NGS-screening avgörande. Eftersom Sanger-sekvensering har en högre detektionsgräns kan NGS upptäcka plasmidmutationer under 0,5 %, vilket förbättrar klonscreeningsframgången till över 90 %[5].
Shuai Wang och kollegor från WuXi Biologics betonar vikten av denna vaksamhet:
Eftersom processoptimering inte kan rätta till gen-nivå mutationer, övervaka mutationsnivåer i stabila kloner noggrant[5].
För producenter i behov av specialiserade verktyg - oavsett om det gäller kryokonservering, genetisk ingenjörskonst eller cellinje-karakterisering -
Integrera kvalitetskontroll i produktionen
Att integrera kvalitetskontroll i varje produktionsfas är avgörande. Utan ett strukturerat system kan även väl underhållna cellinjer uppleva förändringar under expansion och uppskalning. Kvalitetskontroll bör inte vara en eftertanke - det måste vara en central del av produktionen. Detta börjar vid uppskalningsstadiet, där strikta ledningssystem och kontrollerade miljöer spelar en nyckelroll.
Kvalitetskontroll under expansion och uppskalning
Som diskuterats tidigare är genomiska och kontamineringstester avgörande, särskilt under uppskalning. Att gå från små volymer till tusentals liter introducerar nya risker, där varje cellpassage ökar risken för mutationer. Ett Quality Management System (QMS) hjälper till att hantera dessa risker effektivt. Till exempel, mellan 2017 och 2022, implementerade Josep M. Canals och hans team vid Universitetet i Barcelona ISO 9001:2015 QMS för att standardisera kulturer av humana pluripotenta stamceller. Deras retrospektiva analys av G-banding och aCGH-data visade en betydande minskning av kromosomavvikelser jämfört med förhållandena före anpassning[10][13] . Kanaler betonade vikten av kontinuerlig övervakning:
Den genetiska instabiliteten som hPSCs visar i kultur gör den frekventa omvärderingen av genomisk integritet till ett väsentligt krav när man planerar att använda dem för experiment[10].
Rutinmässig genomisk screening är ett måste. Tekniker som G-bandskaryotypering och aCGH upptäcker strukturella förändringar, medan Next-Generation Sequencing (NGS) identifierar mutationer på nivåer under 0,5%[5]. Tillväxtkurvanalys kan också flagga problem tidigt, såsom kontaminering eller genetisk drift[9]. Miljöövervakning lägger till ett ytterligare säkerhetslager, med metoder som sedimentplattestestning och halvårsvisa HEPA-filterkontroller som säkerställer att produktionsmiljön förblir stabil och stressfri för cellinjer [4].
Konsekvens i media och reagenser är lika viktigt. Användning av serumfria, definierade medier som mTeSR1, tillsammans med reagenser med ett analyscertifikat, hjälper till att minska variationen mellan batcher och begränsar risken för viruskontaminering[10][4]. Regelbundna morfologikontroller - enkla mikroskopiska observationer vid olika kulturtätheter - kan fånga tidiga tecken på differentiering eller stress[9]. För att skaffa specialiserad utrustning eller reagenser, plattformar som
Funktionella tester för produktkonsekvens
Medan genomisk övervakning skyddar processen, säkerställer funktionella tester att cellerna fungerar som avsett.Genetisk stabilitet är inte tillräckligt; celler måste också bibehålla sin förmåga att fungera korrekt över produktionssatser. Inom odlat kött innebär detta att bekräfta att stamceller, såsom muskel-satellitceller, fortfarande kan differentiera till mogen muskel- eller fettvävnad efter expansion[2] . Differentiation assays är nödvändiga för att verifiera detta.
Metaboliska tester som MTT, LDH och Resazurin ger insikt i cellhälsa och livskraft[4][9]. Dessa, kombinerade med Short Tandem Repeat (STR) profilering, hjälper till att bekräfta att cellinjer förblir autentiska och fria från korskontaminering under hela produktionsprocessen[1][9].
Transkriptionell analys är ett annat kritiskt steg.Xiaoyue Chen och Sam Zhang rekommenderar:
cDNA snarare än genomisk-DNA-sekvensering rekommenderas för mutationsdetektion för att utvärdera risker på transkriptionsnivå[5].
Denna metod erbjuder en mer exakt bild av slutprodukten, eftersom den återspeglar hur gener uttrycks snarare än bara deras genomiska platser. Genom att kombinera genomisk screening med funktionella tester kan producenter säkerställa att varje batch uppfyller strikta standarder för säkerhet, kvalitet och prestanda i varje produktionssteg.
Slutsats
Att upprätthålla genetisk stabilitet är avgörande för att producera odlat kött säkert och konsekvent. Francisco J. Molina-Ruiz och hans kollegor från Laboratoriet för stamceller och regenerativ medicin belyser riskerna:
Genetiska förändringar i hPSCs kan äventyra inte bara säkerheten för hPSC-baserade cellprodukter... men också leda till heterogen differentieringsbenägenhet hos utgångsmaterialet, förändrade genuttrycksprofiler och ineffektivitet hos den slutliga cellprodukten [10].
Insatserna är betydande - över 531 felidentifierade cellinjer har registrerats av International Cell Line Authentication Committee [1].
Att hantera dessa problem kräver en robust kvalitetskontrollram. Detta innebär att kombinera metoder som STR-profilering, G-bandskaryotypering, aCGH och avancerad NGS [5] , tillsammans med system som ISO 9001:2015 för att standardisera processer och minimera kromosomavvikelser [13].
Ekonomiska faktorer driver också behovet av dessa åtgärder.Genetisk drift kan resultera i att muterade celler får en tillväxtfördel, vilket potentiellt kan förstöra hela produktionssatser [10][11]. Med det växande fokuset på humana pluripotenta stamceller har efterfrågan på stabila cellinjer aldrig varit större. Som professor David L. Kaplan från Tufts University förklarar:
Immortaliserade cellinjer anses generellt vara ett krav för att generera stora mängder ätbar vävnad från en stabil, robust bioprocess [14].
För odlade köttproducenter måste kvalitetskontroll vara inbäddad i varje steg - från plasmidscreening till storskalig produktionsövervakning. Genom att kombinera noggranna tester med förebyggande strategier kan producenter säkerställa konsekventa och tillförlitliga resultat.
Vanliga frågor
Hur ofta bör genetisk stabilitetstestning utföras under uppskalning?
Genetisk stabilitetstestning är ett avgörande steg under uppskalning och bör utföras regelbundet. Hur ofta denna testning sker beror till stor del på den specifika cellinjen och den aktuella processen. För att minska risken för mutationer och bibehålla cellernas stamcellsegenskaper är det klokt att fastställa en passagegräns baserad på genetisk analys.
Vilka tester upptäcker bäst små mutationer och stora kromosomförändringar?
Tester som SNP-arrayanalys och genomomfattande SNP-genotypning är e
Vad är det enklaste sättet att förhindra genetisk drift över produktionssatser?
För att minimera genetisk drift är det viktigt att regelbundet utföra genetiska och funktionella analyser av cellinjer och begränsa antalet passager de genomgår. Implementera praxis som att etablera huvudcellbanker och rutinmässigt kontrollera genetisk stabilitet, som rekommenderas i kvalitetskontrollprotokoll. Dessa åtgärder är nyckeln till att upprätthålla konsekvens och säkerställa pålitliga resultat över olika produktionssatser.











